망막은 고도로 전문화된 기능 때문에 사람의 신체 조직 중 가장 높은 대사 요구량을 가지고 있으며 높은 밀도로 혈관이 분포하고 있다[
1]. 황반부 망막혈관계는 망막신경섬유층과 신경절세포층의 혈관으로 구성된 표층모세혈관총과 내망상층과 외망상층 사이의 접합부에 위치한 혈관으로 구성된 심부모세혈관총의 2개의 주요 혈관총으로 구성되어 있다[
2-
4].
빛간섭단층혈관조영술은 같은 지점에서 고속의 연속적인 단면촬영을 통해 적혈구 움직임을 감지 및 분석하여 망막에 분포하는 미세혈관구조를 분석하는 비침습적 영상 기술이다[
5]. 빛간섭단층혈관조영술은 기존의 형광안저촬영과는 다르게 조영제를 사용하지 않아 조영제에 의한 부작용이 없고[
6], 누출 없는 깨끗한 영상을 통해 망막중심오목무혈관부위의 면적을 보다 정확하게 측정할 수 있으며[
7], 망막을 표층 및 심부모세혈관총으로 나누어 각 층의 혈관밀도와 관류밀도 등을 정량적으로 측정할 수 있는 장점이 있다[
8].
빛간섭단층혈관조영술을 다양한 안과적 질환의 진단 및 예후 판정 등에 활용하기 위한 연구들이 시행되었다. 당뇨망막병증에서 진행될수록 황반 혈관밀도가 감소하고 망막중심오목무혈관부위 면적이 커진다는 연구가 있으며[
9], 신생혈관성 나이관련황반변성 환자에서 혈류 면적, 혈관밀도를 분석하여 신생혈관 활동성을 평가한 연구도 있다[
10]. 소아에서는 근시인 눈에서 정시인 눈에 비해 표층모세혈관총의 혈관밀도가 낮고 망막중심오목무혈관부위 면적이 크다는 연구가 있으며[
11], 약시가 있는 눈의 표층 및 심부모세혈관총의 혈관밀도는 같은 나이대의 정상 대조군과 비교했을 때 더 낮다는 연구도 있다[
12]. 이러한 빛간섭단층혈관조영술을 이용한 연구를 하기 위해서는 인종, 성별, 나이 등에 따른 정상 수치에 대한 자료가 필요한데, 국내에서는 정상 성인을 대상으로 한 연구는 있지만[
13-
15], 한국 정상 소아를 대상으로 시행한 표층 및 심부모세혈관총의 혈관밀도와 망막중심오목무혈관부위 넓이에 관한 연구는 없는 실정이다. 따라서 본 연구에서는 정상안을 가진 한국 소아를 대상으로 빛간섭단층혈관조영술을 이용하여 표층모세혈관총과 심부모세혈관총의 혈관밀도와 망막중심오목무혈관부위 면적을 측정하여 나이에 따른 표준 자료를 얻고, 이들과 나이, 성별, 안축장, 구면렌즈대응치와의 상관관계를 분석하고자 하였다.
대상과 방법
2018년 3월부터 2021년 6월까지 건강검진을 목적으로 방문한 만 3세 이상 만 15세 이하의 한국 소아 중 양안 최대교정시력이 0.8 이상, 안압 21 mmHg 미만이고, 굴절값이 구면렌즈도수 ± 6 diopters (D), 난시도수 3 D 이내이며 사시 및 약시가 없으며 세극등현미경검사 및 안저검사에서 양안 모두 이상 소견이 발견되지 않고, 전신질환이 없는 환자 68명 126안을 대상으로 후향적으로 의무기록을 분석하였다. 본 연구는 헬싱키선언을 준수하여 시행하였으며 본원 의학연구윤리심의위원회(Institutional Review Board, IRB)의 승인을 받아(승인 번호: DFE21ORIO104) 진행되었다.
약시, 사시, 미숙아망막증 같은 안과적 병력이 있는 경우, ± 6 D 이상의 굴절이상이 있는 경우, 안축장이 22 mm 이하거나 26 mm 이상인 경우, 망막미세혈관계에 영향을 줄 수 있는 당뇨, 고혈압을 포함한 심혈관계 등의 전신질환을 가진 경우, 빛간섭단층혈관조영술에서 주시 장애로 움직임 허상(motion artifact)이 심하거나, 화질이 낮아(scan quality <6/10 or presence of significant artifact) 정확한 검사 결과 판독이 어려운 경우는 대상에서 제외하였다.
모든 대상군에서 세극등현미경검사 및 안저검사를 시행하였으며, 최대교정시력을 측정하였다. 조절마비굴절검사는 1% cyclopentolate (Ocucyclo®, Samil Co., Ltd., Seoul, Korea)와 0.5% phenylephrine과 0.5% tropicamide 혼합제(Midrin P, Santen Pharmaceutical Co., Ltd., Osaka, Japan)를 양안에 10분 간격으로 3회 점안한 후 1시간 뒤 동공확대 및 빛 반사가 없는 것을 확인한 후 자동굴절검사기(HRK-8000A auto kerato-refractometer, Huvitz, Anyang, Korea)로 3회 이상 검사하여 표기되는 대표값을 이용하여 측정하였다. 또한 IOL Master® (IOL Master®, Carl Zeiss Meditec AG, Jena, Germany)를 이용한 안축장 측정을 시행하였다. 빛간섭단층혈관조영술은 숙련된 한 명의 검사자에 의해 시행되었으며 840 nm의 파장을 광원으로 이용하여 초당 70,000개의 A-scan을 조사하는 RTVue XR Avanti (Optovue Inc., Fremont, CA, USA)를 이용하여 황반을 중심으로 한 3 × 3 mm2 영역을 촬영하였다.
촬영된 이미지는 내장된 프로그램(Angio Analytics, version 2018.1.0.33; Optovue, Inc., Fremont, CA, USA)을 이용하여 분석하였으며, 내경계막(internal limiting membrane)의 3.0 µm 아래에서 내망상층(inner plexiform layer) 경계부의 15.0 µm의 아래까지로 정의한 표층모세혈관총과 내망상층과 내핵층(inner nuclear layer) 경계부의 15.0 µm 아래에서 70.0 µm 아래까지로 정의한 심부모세혈관총으로 자동적으로 구분된 후, 각 층에서 황반부에 1 mm, 3 mm 직경의 2개의 동심원을 적용하여 1 mm 동심원 안의 영역인 중심오목과 1 mm, 3 mm 직경의 두 동심원 사이 영역인 중심오목부근 영역으로 구획되었다. 각 층의 구획된 영역의 혈관 밀도는 측정 영역 중 혈관이 차지하는 면적의 백분율로 계산되었으며 망막중심오목무혈관부위 면적은 무혈관부위 경계가 자동으로 감지된 후 정량적으로 계산되었다(
Fig. 1).
통계 분석은 SPSS version 20.0 (IBM Corp., Armonk, NY, USA)을 사용하였다. 전체 대상자의 나이, 성별, 구면렌즈 대응치, 안축장, 표층모세혈관총과 심부모세혈관총의 혈관밀도, 망막중심오목무혈관부위 면적 등에 대한 기술통계를 실시하였다. 성별에 따라 표층모세혈관총과 심부모세혈관총의 평균 혈관밀도 및 망막중심오목무혈관부위 평균 면적을 비교하기 위하여 independent t-test를 사용하였고, 나이군에 따른 비교를 위하여 Kruskal Wallis test와 Mann-Whitney U-test를 사용하였다. 표층모세혈관총과 심부모세혈관총의 혈관밀도 및 망막중심오목무혈관부위 면적과 나이, 성별, 구면렌즈대응치 및 안축장과의 상관관계를 분석하기 위하여 단변량 및 다변량선형회귀분석을 사용하였다. Pearson correlation coefficient를 이용하여 회귀분석에서 유의한 결과를 보인 안축장, 표층모세혈관총과 심부모세혈관총의 혈관밀도 및 망막중심오목무혈관부위 면적과의 상관관계를 분석하였다. 통계적 유의수준은 p값이 0.05 미만인 경우를 통계적으로 유의하다고 판정하였다.
결 과
대상자는 총 68명 126안이었고, 대상자의 분포는 3-5세 26안, 6-8세 32안, 9-11세 50안, 12-15세 18안이었다. 대상자의 평균 나이는 8.33 ± 2.93세(범위: 3-15세)였으며, 성별은 남성 64안, 여성 62안이었고, 평균 구면렌즈대응치는 -0.79 ± 1.57 D (범위: -5.32 to +2.35)였으며, 평균 안축장은 23.70 ± 1.01 mm (범위: 22.05-25.94 mm)였다. 전체 대상안의 표층모세혈관총의 중심오목과 중심오목부근 평균 혈관밀도는 각각 20.69 ± 5.48%와 49.42 ± 3.13%이고, 심부모세혈관총의 중심오목과 중심오목부근 평균 혈관밀도는 각각 34.51 ± 6.72%와 53.47 ± 3.31%이며, 표층모세혈관총의 망막중심오목무혈관부위 평균 면적은 0.27 ± 0.09 mm
2였다(
Table 1).
대상안을 나이군별로 나누어 비교하였을 때, 각 군 간 성비는 의미 있는 차이를 보이지 않았으나(
p=0.362), 안축장과 구면렌즈대응치는 의미 있는 차이가 있었는데, 3-5세와 6-8세, 3-5세와 9-11세, 3-5세와 12-15세, 6-8세와 12-15세, 9-11세와 12-15세 사이의 안축장 사후 분석에서 유의한 차이가 있었으며(
p<0.001,
p<0.001,
p<0.001,
p<0.001,
p=0.006), 구면렌즈대응치 차이를 사후 분석했을 때 3-5세와 12-15세에서 유의한 차이가 있었다(
p<0.001) (
Fig. 2).
표층모세혈관총 및 심부모세혈관총의 중심오목혈관밀도는 나이군에 따라 비교하였을 때 의미 있는 차이를 보였는데, 나이군에 따른 표층모세혈관총의 중심오목혈관밀도는 3-5세에서 17.41 ± 5.41%, 6-8세에서 20.53 ± 4.76%, 9-11세에서 21.78 ± 5.73%, 12-15세에서 22.95 ± 3.91%였으며, 심부모세혈관총의 중심오목혈관밀도는 3-5세에서 30.20 ± 6.59%, 6-8세에서 34.54 ± 7.16%, 9-11세에서 35.81 ± 6.02%, 12-15세에서 37.38 ± 5.16%였다. 나이군에 따라 사후 분석했을 때 표층모세혈관총의 중심오목혈관밀도는 3-5세와 9-11세, 3-5세와 12-15세에서 의미 있는 차이가 있었으며(
p=0.002,
p<0.001), 심부모세혈관총의 중심오목혈관밀도 또한 3-5세와 9-11세, 3-5세와 12-15세에서 의미 있는 차이가 있었다(
p<0.001,
p<0.001) (
Fig. 2). 표층모세혈관총 및 심부모세혈관총의 중심오목혈관밀도는 나이군 간 유의한 차이를 보이지 않았다(
p=0.481,
p=0.143) (
Table 1).
성별에 따라 혈관밀도를 비교하였을 때 표층모세혈관총의 중심오목 평균 혈관밀도, 심부모세혈관총의 중심오목 평균 혈관밀도 및 중심오목부근 평균 혈관밀도, 망막중심오목무혈관부위 평균 면적은 통계적으로 유의한 차이를 보였으며(
p=0.004,
p=0.006,
p<0.001,
p=0.016), 표층모세혈관총의 중심오목부근 혈관밀도는 유의한 차이를 보이지 않았다(
p=0.116) (
Table 2).
표층모세혈관총과 심부모세혈관총의 혈관밀도와 망막중심오목무혈관부위 면적에 영향을 미치는 인자를 알아보기 위하여 시행한 단변량선형회귀분석에서 나이, 성별, 안축장이 표층모세혈관총 중심오목부근 혈관밀도를 제외한 나머지 영역에 영향을 미치는 인자로 나타났고 모든 영역에서 구면렌즈대응치는 영향을 미치지 않는 것으로 나타났다(
Table 3). 다변량선형회귀분석에서는 다중공선성을 확인하기 위해 공차한계(tolerance)와 분산팽창요인(variance inflation factor)을 파악하였고, 안축장이 표층모세혈관총과 심부모세혈관총 중심오목혈관밀도와 망막중심오목무혈관부위 면적에 영향을 미치는 인자로 나타났다(
p=0.032,
p=0.041,
p=0.043) (
Table 3).
피어슨 상관 계수(Pearson correlation coefficient)를 이용하여 분석하였을 때 안축장과 표층모세혈관총과 심부모세혈관총의 중심오목혈관밀도는 양의 상관관계가 있었고(R
2=0.153,
p<0.001; R
2=0.158,
p<0.001), 망막중심오목무혈관부위 면적과는 음의 상관관계를 보였다(R
2=0.085,
p<0.001) (
Fig. 3).
고 찰
본 연구는 빛간섭단층혈관조영술을 이용하여 만 3세 이상 만 15세 이하의 정상안을 가진 소아를 대상으로 나이군별로 나누어 표층모세혈관총과 심부모세혈관총의 중심오목 및 중심오목부근 혈관밀도, 망막중심오목무혈관부위 면적에 대한 표준 자료를 구하고자 하였으며, 이는 국내 최초라는 의미가 있다.
본 연구에서 전체 대상안의 표층모세혈관총 중심오목 및 중심오목부근 평균 혈관밀도는 각각 20.69 ± 5.48%, 49.42 ± 3.13%, 심부모세혈관총 중심오목 및 중심오목부근 평균 혈관밀도는 34.51 ± 6.72%, 53.47 ± 3.31%, 망막중심오목무혈관부위 평균 면적은 0.27 ± 0.09 mm
2로, 표층모세혈관총과 심부모세혈관총의 평균 혈관밀도가 20.10-44.20%와 27.21-50.74%, 망막중심오목무혈관부위 면적이 0.22-0.32 mm
2라고 보고한 기존의 정상 소아를 대상으로 한 연구 결과와 큰 차이를 보이지 않았다[
11,
16-
20]. Zhang et al [
17]은 75명의 평균 나이 11.51 ± 1.91세(범위: 8-16세)의 중국 소아 정상안을 대상으로 한 연구에서 표층모세혈관총 중심오목 및 중심오목부근 혈관밀도는 각각 31.24 ± 5.82%, 56.61 ± 2.60%, 심부모세혈관총 중심오목 및 중심오목부근 혈관밀도는 각각 27.21 ± 6.32%, 63.66 ± 1.72%, 망막중심오목무혈관부위 면적은 0.29 ± 0.10 mm
2로 보고하였다. 이는 본 연구에 비해 상대적으로 혈관밀도가 높았는데, 평균 나이가 8.33 ± 2.93세인 본 연구보다 상대적으로 높은 나이를 대상으로 하였고 인종이 다르기 때문에 차이를 보일 수 있을 것으로 생각한다. 그러나 Zhang et al [
18]은 71명의 평균 나이 10.59 ± 1.96세(범위: 5-18세)의 중국 소아 정상안을 대상으로 한 다른 연구에서는 표층모세혈관총 중심오목 및 중심오목부근 혈관밀도는 20.10 ± 7.13%, 50.25 ± 4.41%, 심부모세혈관총 중심오목 및 중심오목부근 혈관밀도는 36.19 ± 7.68%, 53.86 ± 4.71%, 망막중심오목무혈관부위 면적은 0.28 ± 0.10 mm
2로 본 연구 결과와 큰 차이를 보이지 않았다. 표층모세혈관총은 모세혈관이 세정맥과 세동맥을 연결하는가로 형태의 모세혈관으로 구성되어 있지만 심부모세혈관총은 모세혈관이 방사상 형태의 다각형 구조를 이루는 와류모세혈관을 이루기 때문에 심부모세혈관총의 혈관밀도가 더 높게 나타난 것이라고 추정되며[
21], 표층모세혈관총 모세혈관의 투사 효과(projection artifact)로 인해 표층 모세혈관총의 모세혈관이 심부모세혈관총에도 나타나 혈관밀도가 높게 나타날 가능성도 있다[
22].
본 연구에서 표층모세혈관총 및 심부모세혈관총의 중심오목 혈관밀도는 나이군에 따라 유의한 차이를 보였다(
p=0.002,
p<0.001) (
Table 1). 43명의 평균 나이 46.40 ± 16.05세(범위: 20-78세)의 국내 정상 성인을 대상으로 표층모세혈관총 및 심부모세혈관총 혈관밀도를 분석한 연구에서는 나이에 따른 유의한 차이를 보이지 않았으나[
13], 소아에서는 나이의 증가에 따른 성장발육으로 인해 안축장 증가와 구면렌즈대응치 감소에 영향을 받아 차이를 보인 것으로 생각된다[
23,
24]. 하지만 아직까지 표층모세혈관총과 심부모세혈관총의 혈관밀도와 망막중심오목무혈관부위 면적에 나이가 직접적으로 영향을 미치는지 아니면 나이의 증가에 따른 안축장의 변화에 영향을 받은 것인지에 대해 명확하게 밝혀진 것이 없기 때문에 향후 추가 연구가 필요할 것으로 생각된다.
본 연구에서 결과는 성별에 따른 차이를 보였는데, 표층모세혈관총 및 심부모세혈관총의 중심오목 평균 혈관밀도는 남성에서 유의하게 컸으며(
p=0.004,
p=0.006), 망막중심오목무혈관부위 평균 면적은 여성에서 유의하게 더 컸다(
p=0.016). Yu et al [
25]와 Hashmani et al [
26]은 모세혈관이 없는 영역이 여성에서 더 크기 때문에 표층모세혈관총의 중심오목 평균 혈관밀도가 남성에서 더 크다고 하였으며, He et al [
27]은 사춘기 여성에서는 여성 호르몬에 의한 망막 순환의 보호 효과를 가지는 데에 비해 사춘기 남성에서는 상대적으로 높은 혈압을 가지며 이에 따라 망막혈관이 더 넓다고 하였다. Samara et al [
28]은 표층모세혈관총의 망막중심오목무혈관부위 면적을 분석하였을 때 여성에서 더 크지만 통계학적으로 유의한 차이를 보이지 않았다고 보고하였다. 이렇듯 황반혈관밀도와 망막중심오목무혈관부위 면적과 성별과의 상관관계에 대해서 명확하게 결론 지어진 것은 없어 향후 추가 연구가 필요할 것으로 생각된다.
본 연구에서 안축장은 표층모세혈관총 및 심부모세혈관총의 중심오목혈관밀도와 망막중심오목무혈관부위 면적과 유의한 상관관계가 있었다(R
2=0.153,
p<0.001; R
2=0.158,
p<0.001; R
2=0.085,
p<0.001). Hsu et al [
19]은 89명 135안의 평균 나이 8.5 ± 5.3세(범위: 9주-17세)의 정상안을 대상으로 한 연구에서 안축장이 표층모세혈관총과 심부모세혈총의 혈관밀도와 연관성이 있다고 하였고, Gołębiewska et al [
11]은 89명 174안의 평균 나이 13.9 ± 2.3세의 근시군과 54명 101안의 평균 나이 13.1 ± 2.4세의 정시군을 대상으로 한 연구에서 안축장과 표층모세혈관총 중심오목혈관밀도는 양의 상관관계, 안축장과 망막중심오목무혈관부위 면적과는 음의 상관관계를 보인다고 보고하였다. Yang et al [
29]은 고도근시안에서 안축장이 길어짐에 따라 공막, 맥락막 및 망막이 늘어나게 되고, 그로 인해 망막과 맥락막이 얇아지게 되면 혈류량이 감소할 수 있다고 하였다. 본 연구에서는 안축장이 길어짐에 따라 표층 및 심부모세혈관총의 중심오목혈관밀도가 증가하였는데, 고도근시에서 발생할 수 있는 병적 변성이 없는 정상안의 경우에는 안축장이 길어짐에 따라 발생할 수 있는 줄어든 혈류량을 보상하기 위해서 중심오목혈관밀도가 증가한 것이 아닌가 생각된다. 이러한 안축장과 망막혈관밀도의 관계에 대해서는 추가적인 연구가 필요할 것으로 생각된다.
구면렌즈대응치는 표층모세혈관총 중심오목과 중심오목부근 혈관밀도(
p=0.063,
p=0.320), 심부모세혈관총 중심오목과 중심오목부근 혈관밀도(
p=0.052,
p=0.062), 망막중심오목무혈관부위 면적과 유의한 상관관계를 나타내지 않았는데(
p=0.148), 이는 기존의 연구들과 비슷하였다[
17,
20]. Mo et al [
30]은 병적 변성이 있는 근시안에서 정상안 또는 병적 변성이 없는 근시안과는 다르게 구면렌즈대응치가 혈관밀도에 영향을 미친다고 보고하였는데, 본 연구에서는 병적 변성이 없는 근시안만을 포함하였기에 구면렌즈대응치와 혈관밀도는 상관관계를 나타내지 않은 것으로 생각된다.
본 연구는 몇 가지 한계점이 있다. 첫 번째로 3-5세, 6-8세 및 12-15세 군에서 대상안 수가 상대적으로 적었는데, 이러한 각 군 별 대상안 수의 차이가 결과에 영향을 미쳤을 가능성이 있다. 두 번째로 후향적 단면 연구이기 때문에 같은 대상에서 나이 및 안축장이 증가함에 따라 어떤 변화가 일어나는지 분석하지 못한 한계가 있다. 세 번째로 상대적으로 화질이 높은 검사값만을 사용하였으나, 화질의 차이가 결과에 영향을 미쳤을 가능성이 있다. 따라서 균등하게 분포된 더 많은 수의 국내 정상안을 가진 소아를 대상으로 한 전향적 종축 연구가 필요할 것으로 생각된다. 결론적으로, 국내 정상안을 가진 소아에서 나이군에 따라 표층모세혈관총 및 심부모세혈관총 중심오목혈관밀도는 유의한 차이를 보였으며, 안축장이 길어짐에 따라 표층모세혈관총 및 심부모세혈관총의 중심오목혈관밀도는 증가하고 망막중심오목무혈관부위 면적은 감소하는 경향을 보였다.
Figure 1.
Optical coherence tomography angiography (OCTA) results of the representative case. (A) The OCTA 3 × 3 mm scan of the macula at deep capillary plexus showing the vascular plexus. (B) The OCTA 3 × 3 mm scan of the macula at deep capillary plexus showing the vascular plexus. (C) The foveal avascular zone (FAZ) area are automatically drawn (yellow inner line) and obtained.
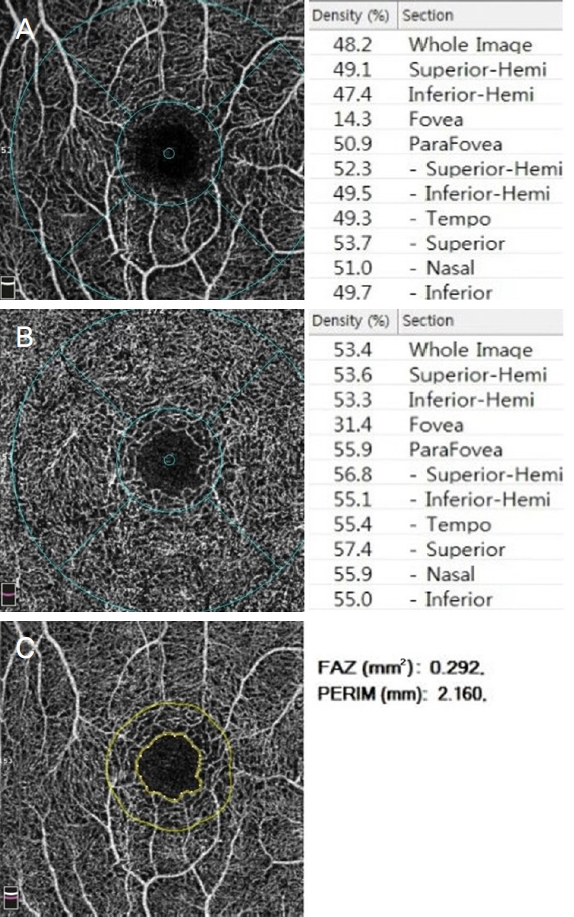
Figure 2.
Comparison between the age groups in axial length (AL) (A). Spherical equivalent (SE) after cycloplegic refraction (CR) (B). Superficial retinal fovea vessel density (SRFVD) (C). Deep retinal fovea vessel density (DRFVD) (D), and foveal avascular zone (FAZ) (E). *p-value was obtained by the Mann-Whitney U-test, p < 0.0125 was considered statistically significant.

Figure 3.
Scatter plots showing the correlation between axial length and vessel density (VD) of the macula. Superficial retinal fovea VD (A) and deep retinal fovea VD (B) show significant positive correlation with axial length (R2 = 0.152, p < 0.001, R2 = 0.157, p < 0.001). (C) Foveal avascular zone (FAZ) area show significant negative correlation with axial length (R2 = 0.084, p < 0.001).

Table 1.
Baseline characteristics and microvascular structures using optical coherence tomography angiography in age-stratified healthy subjects
|
3-5 years (n = 26) |
6-8 years (n = 32) |
9-11 years (n = 50) |
12-15 years (n = 18) |
Total (n = 126) |
p-value |
|
Age (years) |
4.42 ± 0.64 |
6.90 ± 0.77 |
9.66 ± 0.82 |
13.43 ± 1.36 |
8.33 ± 2.93 |
|
|
Sex (M:F) |
10:16 |
16:16 |
28:22 |
10:8 |
64:62 |
0.362*
|
|
AL (mm) |
22.76 ± 0.68 |
23.66 ± 0.81 |
23.99 ± 0.93 |
24.82 ± 0.85 |
23.76 ± 1.03 |
<0.001†
|
|
SE CR (D) |
-0.12 ± 1.30 |
-0.72 ± 1.36 |
-0.73 ± 1.28 |
-2.24 ± 2.24 |
-0.79 ± 1.57 |
0.001†
|
|
SRFVD (%) |
17.41 ± 5.41 |
20.53 ± 4.76 |
21.78 ± 5.73 |
22.95 ± 3.91 |
20.69 ± 5.48 |
0.002†
|
|
SRPFVD (%) |
49.65 ± 2.24 |
49.91 ± 3.30 |
48.97 ± 3.38 |
49.44 ± 3.32 |
49.42 ± 3.13 |
0.481†
|
|
DRFVD (%) |
30.20 ± 6.59 |
34.54 ± 7.16 |
35.81 ± 6.02 |
37.38 ± 5.16 |
34.51 ± 6.72 |
<0.001†
|
|
DRPFVD (%) |
54.50 ± 3.05 |
53.57 ± 3.27 |
53.30 ± 3.46 |
52.12 ± 3.06 |
53.47 ± 3.31 |
0.143†
|
|
FAZ (mm2) |
0.32 ± 0.10 |
0.28 ± 0.11 |
0.26 ± 0.08 |
0.25 ± 0.06 |
0.27 ± 0.09 |
0.024†
|
Table 2.
The difference of vascular density between sex
|
Male |
Female |
p-value |
|
SRFVD (%) |
22.07 ± 5.25 |
19.27 ± 5.39 |
0.004*
|
|
SRPFVD (%) |
48.98 ± 3.56 |
49.87 ± 2.57 |
0.116 |
|
DRFVD (%) |
36.13 ± 6.79 |
32.83 ± 6.26 |
0.006*
|
|
DRPFVD (%) |
52.43 ± 3.12 |
54.55 ± 3.18 |
<0.001*
|
|
FAZ area (mm2) |
0.25 ± 0.09 |
0.30 ± 0.09 |
0.016*
|
Table 3.
Linear regression analysis of factors affecting OCTA parameters
|
Univariate linear regression analysis
|
Multiple linear regression analysis
|
|
Coefficient |
R2
|
p-value |
Coefficient |
Tolerance |
VIF |
p-value |
|
SRFVD (%) |
|
|
|
|
|
|
|
|
|
Age (years) |
0.298 |
0.089 |
<0.001*
|
0.097 |
0.603 |
1.658 |
0.369 |
|
Sex (M:F) |
-0.256 |
0.066 |
0.004*
|
-0.131 |
0.795 |
1.258 |
0.162 |
|
AL (mm) |
0.391 |
0.153 |
<0.001*
|
0.309 |
0.341 |
2.937 |
0.032*
|
|
SE CR (D) |
0.194 |
0.038 |
0.063 |
0.039 |
0.541 |
1.847 |
0.731 |
|
SRPFVD (%) |
|
|
|
|
|
|
|
|
Age (years) |
-0.103 |
0.011 |
0.255 |
-0.074 |
0.603 |
1.658 |
0.551 |
|
Sex (M:F) |
0.141 |
0.020 |
0.117 |
0.872 |
0.795 |
1.258 |
0.170 |
|
AL (mm) |
-0.114 |
0.013 |
0.208 |
0.096 |
0.341 |
2.937 |
0.837 |
|
SE CR (D) |
0.090 |
0.008 |
0.320 |
0.167 |
0.541 |
1.847 |
0.498 |
|
DRFVD (%) |
|
|
|
|
|
|
|
|
Age (years) |
0.311 |
0.097 |
<0.001*
|
0.266 |
0.603 |
1.658 |
0.281 |
|
Sex (M:F) |
-0.246 |
0.061 |
0.006*
|
-1.778 |
0.795 |
1.258 |
0.157 |
|
AL (mm) |
0.397 |
0.158 |
<0.001*
|
1.707 |
0.341 |
2.937 |
0.041*
|
|
SE CR (D) |
-0.128 |
0.054 |
0.052 |
-0.095 |
0.541 |
1.847 |
0.844 |
|
DRPFVD (%) |
|
|
|
|
|
|
|
|
Age (years) |
-0.203 |
0.041 |
0.024*
|
0.037 |
0.603 |
1.658 |
0.759 |
|
Sex (M:F) |
0.322 |
0.103 |
<0.001*
|
1.553 |
0.795 |
1.258 |
0.012*
|
|
AL (mm) |
-0.383 |
0.147 |
<0.001*
|
-0.817 |
0.341 |
2.937 |
0.072 |
|
SE CR (D) |
0.256 |
0.058 |
0.062 |
0.215 |
0.541 |
1.847 |
0.366 |
|
FAZ (mm2) |
|
|
|
|
|
|
|
|
Age (years) |
-0.240 |
0.058 |
0.007*
|
-0.114 |
0.603 |
1.658 |
0.350 |
|
Sex (M:F) |
0.215 |
0.046 |
0.016*
|
0.135 |
0.795 |
1.258 |
0.200 |
|
AL (mm) |
-0.291 |
0.085 |
<0.001*
|
-0.217 |
0.341 |
2.937 |
0.043*
|
|
SE CR (D) |
0.131 |
0.017 |
0.148 |
0.173 |
0.541 |
1.847 |
0.737 |
REFERENCES
1) Buttery RG, Hinrichsen CF, Weller WL, Haight JR. How thick should a retina be? A comparative study of mammalian species with and without intraretinal vasculature. Vision Res 1991;31:169-87.


2) Gariano RF, Iruela-Arispe ML, Hendrickson AE. Vascular development in primate retina: comparison of laminar plexus formation in monkey and human. Invest Ophthalmol Vis Sci 1994;35:3442-55.

3) Hughes S, Yang H, Chan-Ling T. Vascularization of the human fetal retina: roles of vasculogenesis and angiogenesis. Invest Ophthalmol Vis Sci 2000;41:1217-28.

4) Tan PE, Yu PK, Balaratnasingam C, et al. Quantitative confocal imaging of the retinal microvasculature in the human retina. Invest Ophthalmol Vis Sci 2012;53:5728-36.


5) Spaide RF, Klancnik JM Jr, Cooney MJ. Retinal vascular layers imaged by fluorescein angiography and optical coherence tomography angiography. JAMA Ophthalmol 2015;133:45-50.


6) Paques M, Tadayoni R, Sercombe R, et al. Structural and hemodynamic analysis of the mouse retinal microcirculation. Invest Ophthalmol Vis Sci 2003;44:4960-7.


7) Novotny HR, Alvis DL. A method of photographing fluorescence in circulating blood in the human retina. Circulation 1961;24:82-6.


8) Yannuzzi LA, Rohrer KT, Tindel LJ, et al. Fluorescein angiography complication survey. Ophthalmology 1986;93:611-7.


9) Takase N, Nozaki M, Kato A, et al. Enlargement of foveal avascular zone in diabetic eyes evaluated by en face optical coherence tomography angiography. Retina 2015;35:2377-83.


10) Savastano MC, Lumbroso B, Rispoli M. In vivo characterization of retinal vascularization morphology using optical coherence tomography angiography. Retina 2015;35:2196-203.


12) Yilmaz I, Ocak OB, Yilmaz BS, et al. Comparison of quantitative measurement of foveal avascular zone and macular vessel density in eyes of children with amblyopia and healthy controls: an optical coherence tomography angiography study. J AAPOS 2017;21:224-8.


13) Noh D, Ryu G, Saong M. Analysis of foveal microvascular structures using optical coherence tomography angiography in age-stratified healthy Koreans. J Korean Ophthalmol Soc 2017;58:1058-65.

14) Park HJ, Lim HB, Lee MW, et al. Interocular symmetry of optical coherence tomography angiography parameters in normal eyes of Korean adults. J Korean Ophthalmol Soc 2019;60:676-84.

15) Im JC. Measurement of vessel density using optical coherence tomography angiography in normal subjects: difference by analysis area. J Korean Ophthalmol Soc 2019;60:355-61.

16) Yang Y, Zhang G, Zhang S, et al. Quantitiative analysis of the macular and peripapillary capillary network with optical coherence tomography angiography in chineese adolescents: the tuyou county pediatric eye (type) study. Int J Gen Med 2021;5:371-9.
18) Zhang Y, Zhang B, Fan M, et al. The vascular densities of the macula and optic disc in normal eyes from children by optical coherence tomography angiography. Graefes Arch Clin Exp Ophthalmol 2020;258:437-44.


19) Hsu ST, Ngo HT, Stinnett SS, et al. Assessment of macular microvasculature in healthy eyes of infants and children using OCT angiography. Ophthalmology 2019;126:1703-11.


21) Bonnin S, Mané V, Couturier A, et al. New insight into the macular deep vascular plexus imaged by optical coherence tomography angiography. Retina 2015;35:2347-52.


22) Spaide RF, Fujimoto JG, Waheed NK. Image artifacts in optical coherence angiography. Retina 2015;35:2163-80.


24) Kim SY, Min BW. Myopic progression according to the age of onset in childhoods. J Korean Ophthalmol Soc 1998;39:721-7.
26) Hashmani N, Hashmani S, Murad A, Baig N. Macular vascular density at the superficial capillary plexus using the optical coherence tomography angiography. Clin Ophthalmol 2019;13:295-302.


28) Samara WA, Say EA, Khoo CT, et al. Correlation of foveal avascular zone size with foveal morphology in normal eyes using optical coherence tomography angiography. Retina 2015;35:2188-95.


29) Yang Y, Wang J, Jiang H, et al. Retinal microvasculature alteration in high myopia. Invest Ophthalmol Vis Sci 2016;57:6020-30.


Biography
전태하 / Tae Ha Jun
대구파티마병원 안과
Department of Ophthalmology, Daegu Fatima Hospital









 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




