 |
 |
| J Korean Ophthalmol Soc > Volume 63(8); 2022 > Article |
|
국문초록
대상과 방법
망막 수술 환자 40명의 의무기록을 후향적으로 분석했다. 수술 전후 빛간섭단층혈관조영술과 안과적 검사를 시행한 환자들을 대상으로 했다. 전신마취 중 활력징후 값을 확인하였고, 수술 중 저혈압(평균동맥압 <70 mmHg)이 발생한 경우를 분석하였다. 망막 표층모세혈관총 및 심부모세혈관총의 혈관밀도, 맥락막모세혈관층 관류 공극, 맥락막 및 망막 두께 변화에 대한 정량적 분석을 했으며, 마취 변수 및 만성질환 유무에 따른 연관성을 분석하였다.
결과
심부모세혈관총의 밀도는 전신마취 후 유의하게 증가됐다(p<0.05). 수술 중 저혈압 및 만성질환 유무에 따른 환자군의 비교분석에서 수술 전후로 통계적인 차이가 없었다(p>0.05). 마취 시간 및 맥락막모세혈관 관류 공극의 평균 크기는 낮은 음의 상관관계(p<0.05, r=-0.32)를 보였다. 수술 중 혈압 변동폭은 심부모세혈관총 혈관밀도 및 맥락막 공극 계수와 낮은 음의 상관관계(p<0.05, r=-0.38; p<0.05, r=-0.37)를, 평균 크기 및 신호 공극(p<0.01, r=0.41; p<0.01, r=0.44)과는 각각 낮은 양의 상관관계를 나타냈다.
ABSTRACT
Purpose
To investigate chorioretinal vascular changes in the non-surgical eyes of patients who underwent vitreoretinal surgery under general anesthesia using optical coherence tomography angiography (OCTA).
Methods
Data from 40 patients who underwent retinal surgery were retrospectively analyzed. Ophthalmologic examinations (including OCTA) were performed in the morning before and after surgery. The presence of intraoperative hypotension (IOH; mean arterial pressure <70 mmHg) was determined based on medical records. The vessel density of superficial and deep retinal capillary plexus layers, choriocapillaris void features, and thickness of the choroid and retina were quantified after image processing. Associations between retinal OCTA parameters and anesthesia profiles were also assessed.
Results
DCP vessel density was increased after general anesthesia (p < 0.05). Among the patients who experienced IOH, there was no statistical difference in chorioretinal vessel parameters before and after general anesthesia. Also, we did not observe a difference in chorioretinal vessel parameters after general anesthesia between healthy patients and patients with chronic disease, including hypertension and diabetes (p > 0.05). The duration of anesthesia and average size of the choriocapillaris void (p < 0.05, r = -0.32), and the intraoperative mean arterial pressure (MAP) fluctuation and DCP, showed statistically significant negative linear correlations (p < 0.05, r = -0.38). The choriocapillaris void size and intraoperative MAP fluctuation also displayed a significant negative correlation (p < 0.05, r = -0.37), while the average size signal void showed a weak positive linear correlation (p < 0.01, r = 0.41; and p < 0.01, r = 0.44, respectively).
Conclusions
This is the first study to assess the effects of general anesthesia on chorioretinal vessels using OCTA. The Vessel density of the DCP was significantly increased in the non-surgical eye after total vitrectomy under general anesthesia. Furthermore, we found a correlation between MAP fluctuation and choriocapillaris void features. More studies are needed to confirm and expand on these observations.
전신마취는 다양한 기전을 통하여 심혈관 기능에 영향을 주며, 전신혈관의 저항을 변화시킴으로써 혈역학적 변화를 일으키며 전신마취의 가장 흔한 부작용은 수술 중 저혈압(intraoperative hypotension, IOH; 평균 동맥압[mean arterial pressure, MAP] <70 mmHg)이다[1]. 수술 중 저혈압이 급성 신장 손상(acute kidney injury, AKI)이나 심근 손상(myocardial injury)과 관련 있다는 보고들이 있으나[2,3], 허혈성 뇌졸중(ischemic stroke)이나 망상(delirium)의 경우 연관성에 대한 가능성은 있지만 뚜렷한 증거를 찾기 어려운 등, 아직도 수술 중 저혈압이 장기 관류(organ perfusion)를 저해하고 파괴(disruption)하여 장기 손상이 일어나는지 여부는 논란과 연구의 대상이 되고 있다[1]. 전신마취는 주요 장기 뿐만 아니라 안구에도 영향을 미친다. 안구 혈류의 변화[4] 및 안압의 변화[5,6] 그리고 망막 혈관신생[7]에도 변화를 초래할 수 있다는 연구들이 있다.
망막의 미세혈관은 100-300 µm정도 크기의 세동맥이나 세정맥으로 뇌나 심장에 존재하는 작은 혈관들과 유사한 구조와 생리적 특성을 지니고 있으며, 안구는 우리 몸에서 미세혈관계를 비침습적, 시각적으로 직접 관찰할 수 있는 유일한 부위로, 안구를 통해 여러 망막 미세혈관 매개변수들의 정량적 평가와 더불어 미세순환의 변화를 관찰할 수 있다[8]. 특정 망막 미세혈관의 변화는 노화 과정을 포함한 심혈관계 위험 요소, 염증, 혈관 내피 기능 이상 및 유전적 요인 등 다양한 혈관 상태와 관련이 있는 것으로 알려져 있다[9]. 또한 망막 혈관의 미세한 변화는 전신의 미세혈관계의 손상을 반영할 수 있어, 고혈압, 뇌졸중, 당뇨병 및 신부전을 포함한 전신 미세혈관 질환의 임상증세가 아직 드러나지 않은 잠복기의 표지(marker)로서의 역할을 할 수 있다[10].
빛간섭단층혈관조영술(optical coherence tomography angiography, OCTA)은 맥락막 및 망막 미세순환의 3차원적 시각화를 위해 빛간섭단층촬영(optical coherence tomography, OCT)을 사용하는 비침습적 영상화 기술이다. 기존의 형광안저촬영과 달리 조영제를 사용하지 않기 때문에, 조영제를 사용하기 어렵거나 자주 검사를 받아야하는 경우 유용한 장점이 있다. 빛간섭단층혈관조영술은 적혈구의 움직임을 감지하고 빛간섭단층촬영 B-스캔을 사용하여 연속적인 단면 촬영으로 혈류를 시각화하여 망막 및 맥락막의 미세순환계의 자세한 정보를 제공한다. 망막을 표층모세혈관총(superficial capillary plexus)과 심부모세혈관총(deep capillary plexus)으로 나누어 혈관밀도(vessel density, VD) 등을 정량적으로 측정할 수 있으며, 황반의 관류 상태를 평가하는 데 유용하게 사용되고 있다[11,12].
본 연구는 망막 수술 환자에게 시행되는 빛간섭단층혈관조영술 검사 결과를 활용하여, 수술안이 아닌 비수술안의 검사 결과를 분석하여 전신마취가 망막 혈관에 미치는 영향을 알아보고자 고안되었으며, 수술 중 저혈압과 맥락망막 매개변수의 변화와의 관계를 조사하였다.
2020년 6월부터 2021년 6월까지 한양대학교 구리병원에서 전신마취 하에 망막수술을 받은 만 19세 이상의 성인 환자 중, 수술 전후로 빛간섭단층혈관조영술을 양안 모두에서 시행한 환자 40명의 비수술안 40안을 대상으로 후향적으로 의무기록 자료를 분석하였다. 의무기록 중 마취기록지, 기본 입원 요약지, 영상 자료를 분석하였다. 본 연구는 헬싱키선언을 준수하였으며, 한양대학교 구리병원 임상연구윤리위원회(institutional review board, IRB)의 승인을 받아 진행하였다(IRB 승인 번호: 2021-11-015-001).
수술 전후 하루 이내에 빛간섭단층혈관조영술을 촬영하지 않은 환자, 비수술안에 고도근시(6디옵터 이상)가 있는 경우, 또는 망막 혈관질환, 황반질환이 있는 경우에는 본 연구에서 제외하였다. 또한 낮은 해상도의 빛간섭단층혈관조영술을 피하기 위하여 환자들 중 이전에 안구 내 수술이나 다른 안질환의 이력 또는 상당한 수정체혼탁이 있는 경우, 눈의 움직임이나 안구 매체혼탁으로 인해 낮은 해상도의 빛간섭단층혈관조영술(60 미만의 낮은 화질)도 제외되었다.
전신마취 유도에는 Thiopental Sodium (Pentotal Sodium Inj®; JW Pharmaceutical, Seoul, Korea) 또는 Propofol (Anepol®; Hana Pharm Co., Seoul, Korea)과 근이완제인 Rocuronium Bromide (Rocuron Inj®; Myungmoon Pharm. Co., Seoul, Korea)가 사용되었고, 흡입마취의 경우 흡입마취제인 Sevoflurane (Sourjon solution®; Kyongbo Pharm. Co., Asan, Korea)이나 Desflurane (Suprane solution®; BAXTER INCORPORATED Co., Seoul, Korea)을 이용해 마취 유지를 하였고, 전정맥마취(total intravenous anesthesia, TIVA)의 경우 Propofol (FRESOFOL MCT Inj®; Fresenius Kabi Korea, Seoul, Korea)과 Remifentanil Hydrochloride (Kabi Remifentanil Inj®; Fresenius Kabi Korea)를 이용해 마취 유지를 하였다. 마취 중 활력징후 Life Scope G9 CSM-1901 (Nihon Kohden Co., Tokyo, Japan)로 3-5분 간격으로 기록된 수축기 혈압, 이완기 혈압, 평균 동맥압, 심박수 및 맥압 등을 분석하고, 수술 중 저혈압의 유지 시간 등을 추가로 분석하였다.
수술 중 저혈압은 대부분의 마취 및 수술에 관련된 연구에서 다양하게 정의되고 있다[13]. 수술 중 저혈압을 정의하는 역치(threshold)는 수술 중 저혈압 모델의 선택에 따라 수술 예후와의 관계에 영향을 미친다. 단독의 최선의 동맥혈압 역치나 저혈압의 정의는 밝혀지지 않았다[14]. 본 연구에서는 여러 문헌[15,16]을 참고하여, 절대적 역치(absolute threshold)는 MAP <70 mmHg로, 상대적 역치(relative threshold)는 마취 유도 전 기준 MAP 대비 20% 아래(20% below baseline MAP)로 설정하여 분석하였다.
빛간섭단층혈관촬영(OCT)과 빛간섭단층혈관조영술을 포함한 안과 검사는 수술 당일 아침과 수술 다음날 아침에 시행한 결과를 이용하였다. 빛간섭단층혈관조영술 영상은 4.5×4.5 mm 이미지로 DRI OCT (Topcon Corporation, Tokyo, Japan) 기기를 사용하여 얻었다. 표층모세혈관총과 심부모세혈관총, 맥락막 모세혈관층의 혈관밀도(VD)를 영상처리 후 정량적으로 분석하였다. 황반의 맥락막 두께(choroidal thickness, CT)와 망막 두께(retinal thickness, RT) 또한 모든 피험자에서 측정되었다. 관류 혈관밀도(perfused VD)를 측정하는데 사용된 것과 동일한 DRI OCT 기기를 사용하여 ETDRS grid의 9개 부영역에서 내장된 소프트웨어의 황반 3D 스캔(512×256A 스캔/0.8초)을 사용하여 맥락막 두께 및 망막 두께를 측정하였다.
맥락망막 매개변수와 마취 관련 변수(수술 중 혈역학적 변화 관련 변수 및 마취 시간, 종류) 간의 연관성을 평가하였으며, 맥락망막 매개변수에는 표층모세혈관총의 혈관밀도 및 심부모세혈관총의 혈관밀도, 맥락막 두께 및 망막 두께, 그리고 맥락막 모세혈관층(choriocapillaris)의 혈류 공극 변수(flow void features)인 계수(count), 평균 크기(average size) 및 신호 공극(signal void)이 포함된다. 표층모세혈관총은 내경계막의 2.6 µm 아래에서 내망상층과 내핵층 경계부(Inner plexiform layer/inner nuclear layer, IPL/INL)의 15.6 µm 아래까지로 정의하였다. 심부모세혈관총은 IPL/INL의 15.6 µm 아래에서 70.2 µm 아래까지로, 맥락막 모세혈관은 망막세포상피에서 10-40 µm 아래까지로 정의하였다. Image J 소프트웨어(version 1.53f51; National Institutes of Health, Bethesda, MD, USA)를 사용하여 각 매개변수를 측정하였다. 빛간섭단층촬영의 표층모세혈관총과 심부모세혈관총의 en-face 영상을 “Phansalkar local thresholding” 방법을 통해 변환하여 혈관밀도를 계산하였다. 맥락막 모세혈관은 표층모세혈관총의 큰 혈관(Threshold 220 이상)은 마스킹한 후 “Otsu method”을 이용하여 변환하였고, 혈관관류는 하얀색으로, 배경은 검은색으로 한 후 분석하였다. 여기서 나오는 혈류 공극변수의 계수는 검은색 입자의 숫자이며, 평균 크기는 각 입자들의 평균 크기, 신호 공극은 입자들이 차지하는 비율로 맥락막 모세혈관의 비관류 영역이다[17].
모든 통계 분석에는 SPSS ver. 23.0 (SPSS, Inc., Chicago, IL, USA)이 사용되었다. 전신마취 이후의 맥락망막 매개변수의 분석에는 Wilcoxon signed-rank 검정법이 사용되었다. 수술 중 저혈압 발생 및 기저질환 유무에 따른 환자군의 혈역학적 변수와 맥락망막 매개변수 영향 분석에는 Mann-Whitney U 검정법을 이용하였다. 모든 변수 값 간의 상관관계는 Pearson의 상관관계 검정으로 분석하였다. 0.05 미만의 p값은 통계적으로 유의한 것으로 간주되었다.
연구 기준을 충족한 40명의 환자의 40안이 연구에 포함되었다. 남성이 21명, 여성이 19명이었으며, 평균 연령은 64.35 ± 8.72세(범위 40-82세)였다. 28명의 환자가 만성 질환을 가졌으며, 이 중에는 당뇨 환자가 16명, 고혈압 환자가 24명, 만성 신부전 환자가 3명이 포함 되어있었다. 전신마취는 흡입마취(38예)와 전정맥마취(2예)가 사용되었다. 수술 중 평균 마취 시간은 104.6 ± 19.6분이었다(Table 1).
전신마취 이후 망막 혈관의 변화를 보면, 표층모세혈관총의 혈관밀도(VD)는 대부분의 하위 영역에서 크게 변하지 않았다. 그러나 심부모세혈관총의 혈관밀도는 전신마취 후 58.83 ± 2.0에서 59.47 ± 2.54로 유의하게 증가되었다(p<0.05) (Table 2). 전신마취 후 평균 망막 두께(RT) 및 맥락막 두께(CT)는 모든 하위영역에서 유의한 변화가 없었다(Table 3).
수술 중 저혈압(IOH, MAP <70 mmHg)은 24명의 환자에서 발생하였으며, 수술 중 저혈압의 평균 지속시간은 21.04 ± 16.1분이었다. 환자들은 수술 중 저혈압의 유무에 따라 두 그룹으로 나뉘었으며, 마취시간 및 혈역학적 특성에 관한 변수들은 두 그룹 간에 유의미한 차이는 없었다(p>0.05) (Table 4). 전신마취 중 수술 중 저혈압이 발생한 환자들에서 맥락망막 매개변수들은 수술 전후로 통계적인 차이가 없었다(p>0.05) (Table 5).
또한 전체 환자 40명 중 11명의 환자에서는 평균 10.8 ± 20.4분의 상대적인 MAP 감소(마취 유도 전 기준 MAP에서 20% 이상의 감소)를 보였다. 상대적인 수술 중 저혈압을 보인 환자와 보이지 않은 환자를 두 그룹으로 나누어, 역시 마취 시간 및 혈역학적 특성에 관한 비교를 하였으며, 두 그룹 간에 유의미한 차이는 없었다(p>0.05) (Table 6). 상대적인 수술 중 저혈압 환자들에서 맥락망막 매개변수들은 수술 전후로 통계적인 차이가 없었다(p>0.05) (Table 7).
대상 환자들을 추가적으로 만성 질환 유무에 따라 두 그룹(만성 질환이 있는 28안과 없는 12안)으로 나누어 분석을 진행하였다. 전신마취 및 맥락망막 매개변수를 포함한 모든 매개변수는 두 그룹 간에 유의한 차이가 없었다(Mann-Whitney U test, 모두 p>0.05) (Table 8, 9).
마취 시간과 맥락막 모세혈관층의 평균 크기(average size)는 통계적으로 유의미한 선형상관관계(Pearson correlation, p=0.045)를 보였으며 낮은 음의 선형 상관관계(r=-0.319)를 보였다. 연령과 표층모세혈관총 혈관밀도 변화량 사이에서도 유의미하게 낮은 음의 선형 상관관계(p=0.014, r=-0.386)를 보였다. 수술 중 혈압 변동의 폭(intraoperative MAP fluctuation)과 심부모세혈관총 혈관밀도 변화량 또한 통계적으로 유의한 낮은 음의 선형 상관관계(p=0.017, r=-0.377)를 보였다. 혈압 변동의 폭은 또한 맥락막 모세혈관층(choriocapillaris)의 혈류 공극 변수 중 계수(count)와는 유의한 낮은 음의 선형 상관관계(p=0.017, r=-0.374)를 보였으며, 다른 변수인 평균 크기(average size) (p<0.01, r=0.409) 및 신호 공극(signal void) (p<0.01, r=0.438)은 각각 유의미하게 낮은 양의 선형 상관관계를 나타냈다. 다른 매개변수 간에는 유의한 상관관계가 없었다. 자세한 값은 Table 10과 Fig. 1에 기술하였다.
본 연구에서는 전신마취 전후에 수술 환자의 망막 혈관에 생기는 변화를 관찰하고자 빛간섭단층혈관조영술(OCTA)을 이용하였다. 지금까지 전신마취와 빛간섭단층혈관조영술을 연관시킨 연구는 많지 않았다.
Alnawaiseh et al [18]과 Zhang et al [19]은 실험용 쥐를 전신마취하여 빛간섭단층혈관조영술로 비침습적으로 혈관 변화를 관찰할 수 있음을 보고 했고, Ripolles-Garcia et al [20]은 망막 이형성증으로 진단된 개를 전신마취하여 빛간섭단층 혈관조영술로 망막 미세혈관 이상이 있음을 밝혀냈다. Iezzi and Dalvin [21]은 소아나 인지장애 환자를 전신마취 하에 옆으로 눕혀 빛간섭단층혈관조영술을 시행하여, 3세 망막아 세포종 환아의 정상안 빛간섭단층혈관조영술 영상을 얻었다. Nakao et al [22]은 망막병증이 동반된 색소 실조증 영아에서, 전신마취 하에 빛간섭단층혈관조영술 검사를 통해 조기 광응고술을 시행한 환아 3명의 예후를 통해 조기 발견 및 치료의 중요성을 언급했고, Kothari et al [23]은 7명의 초저체중 미숙아의 미숙아 망막병증 검진을 위해 전신마취하 빛간섭단층혈관조영술 시행을 위한 기구를 보고하였다. 따라서 본 연구는 성인 환자를 대상으로 전신마취에 따른 망막 혈관의 변화를 빛간섭단층혈관조영술을 이용해 밝히고자 하는 최초의 연구로서 의미가 있다.
전신마취는 다양한 기전을 통해 혈역학적 변화를 일으키는데, 그중 수술 중 저혈압이 가장 흔한 부작용이며, 관련 연구도 많이 진행되어 왔다. 수술 중 저혈압의 정의를 내리는 것은 매우 어려운 일로, Bijker et al [13]은 체계적 문헌 고찰에서 130개의 논문에서 140가지 다른 수술 중 저혈압의 정의를 사용하였다고 보고하였다. Wesselink et al [1]은 비심장 수술 중 저혈압의 정의와 수술 후 합병증과의 관계에 대한 42개의 논문을 체계적 문헌 고찰을 하였는데, 비심장 수술 후의 어떤 장기라도 MAP <80 mmHg에서 10분 이상 노출되기 시작하면 손상이 시작되는 것으로 보고되고 있고, MAP <70 mmHg인 경우엔 더 짧은 시간에도 위험도가 올라가는 것으로 보인다고 하였다. 신체 장기가 입는 손상 위험도 측정시에 MAP를 기준으로 컷오프의 개념으로 분석한 경우가 42개 연구 중 69%라고 하였다. 반면 Vernooij et al [14]은 하나로 통일된 최선의 동맥혈압 역치(threshold)나 저혈압의 정의는 정해지지 않았으며, 여러가지 저혈압을 정의하는 역치와 수술 중 저혈압 모델의 선택 방법에 대해 언급했다. 절대적인(absolute) 역치와 상대적인(relative) 역치가 함께 수술 후 합병증에 영향을 미친다고 보았으며, 저혈압 모델을 12가지를 제시하였다.
본 연구에서는 수술 중 저혈압이 주요 장기인 심장이나 신장 및 뇌에 영향을 미칠 수 있다는 기존 연구들[1-3]을 바탕으로 망막 혈관에도 변화가 나타날 것이라는 가설 하에 저혈압의 적절한 기준을 정하기 위해 앞서 언급한 논문들을 참고하였으며, 절대적 역치는 MAP <70 mmHg, 상대적 역치는 마취유도 전 혈압을 기준으로 그 20% 아래의 MAP로 설정했으며, 12가지 모델 중 ‘저혈압 총 유지 시간’을 차용하여 적용하여 의무기록을 분석하였다.
망막의 미세혈관은 우리 몸에서 미세혈관계를 직접적으로 관찰할 수 있는 유일한 부위이다. Blindbæk et al [24]은 당뇨 망막증에 있어 망막 혈관은 비침습적인 표지(marker)로서, 장기간 지속될 미세혈관질환의 예측인자이자 치료 예후의 표지라고 했으며, Sabanayagam et al [10]은 만성 신장 질환에 대해 논하면서, 망막 혈관의 변화가 전신 미세혈관질환의 잠복기의 표지로서의 역할을 할 수 있다고 언급하였다.
망막은 간뇌 유래 조직으로 중추신경계의 연장으로 간주되며, 망막과 뇌의 혈관계는 동일하다고 보고 있다[25,26]. 본 연구에서는 전신마취가 뇌에 미치는 영향을 빛간섭단층혈관조영술을 이용하여 망막 혈관의 정보를 얻음으로써 간접적으로 밝혀낼 가능성에 대해서도 살펴보려 하였다.
전신마취로 진행된 수술 이후 발생하는 수술 후 인지장애에 대한 많은 연구들이 있다. 수술 후 인지장애는 치매의 초기 단계로 여겨져 노인 환자가 늘고 있는 최근 관심의 대상이 되고 있다. Evered and Silbert [27]는 비심장 수술 후 3개월까지 수술 후 인지장애의 발생률은 12-21%라고 언급했다. Gao et al [28]은 1,031명의 환자를 다룬 7개의 논문을 바탕으로 한 체계적 문헌 고찰에서 전신마취와 국소마취를 비교했으며, 전신마취가 수술 후 3일내의 수술 후 인지장애의 발생률을 높인다고 언급하였다.
이에 더불어 빛간섭단층혈관조영술을 이용한 경증 인지장애(mild cognitive impairment)에 관한 연구가 많이 진행되고 있는데, Hui et al [25]은 빛간섭단층혈관조영술을 이용한 8개의 연구에서 경증 인지장애 환자 195명, 알츠하이머 치매(Alzheimer’s disease) 환자 150명, 인지적 건강군(cognitively healthy controls, HCS) 226명에 대한 체계적 문헌 고찰을 하였다. 경증 인지장애 환자는 표층모세혈관총과 심부모세혈관총의 혈관밀도가 의미있게 감소하였으며, 망막중심오목무혈관부위(fovea avascular zone, FAZ)의 면적이 늘어났다. 반면 알츠하이머 치매 환자에서는 표층모세혈관총의 혈관밀도는 의미있게 감소하였으나 심부모세혈관총의 혈관밀도나 FAZ의 면적에는 변화가 없었다. 이는 망막 미세혈관 변화가 심부모세혈관총보다는 표층모세혈관총에서 지속된다는 근거이며, 빛간섭단층혈관조영술로 감지되는 표층모세혈관총의 혈관밀도 감소는 경증 인지장애의 유용한 생물학적 표지라고 언급하고 있다. 망막 미세혈관의 변화를 빛간섭단층혈관조영술로 감지하여 경증 인지장애 환자를 선별(screen)할 수 있으면, 알츠하이머 치매로 진행하기 전에 경계징후(warning sign)를 제공하여 치료나 예후 향상에 도움을 줄 수 있고, 알츠하이머 치매로 가기 전단계인 경증 인지장애에서는 심각한 증상이 없어 확실하게 발견하기가 어려워, 비가역적인 과정으로 접어들기 전에 조기 진단이 중요한데, 임상 진단인 신경생리학적 검사(neuropsychological test)는 번거롭고, 뇌 촬영이나 척수액 검사는 비용 부담과 침습적 술기의 이유로, 빛간섭단층혈관조영술이 새로운 비침습적인 경제적인 선별 도구가 될 가능성이 있다고 기술하였다. 이에 따라 전신마취 수술 후 발생하는 수술 후 인지장애에 대해서도 빛간섭단층혈관조영술을 이용하면 같은 장점이 있지 않을지 기대되는 바이다.
전신마취와 미세순환과의 관계를 다룬 연구들은 비교적 최근에 이루어지고 있다[29,30]. 본 연구에서 빛간섭단층혈관조영술을 사용하듯 다른 여타의 장비들로 여러 사실들을 증명하고자 노력하는 시도들이 있다. Cho et al [30]은 미세 혈류 반응성(microvascular reactivity)과 조직 산소 포화도(tissue oxygen saturation)에 전신마취가 끼치는 영향에 대해 60명의 건강한 환자를 대상으로 전향적 연구를 하였으며, 근적외선 분광분석기(near-infrared spectroscopy, INVOSTM 5100C Cerebral/Somatic Oximeter; Medtronic, Minneapolis, MN, USA)를 이용하였고, 혈관 폐색 검사(vascular occlusion test)를 같이 시행하였다. 전신마취로 인한 모세혈관의 회복(capillary recruitment)을 동반한 미세혈류 반응성의 향상이 관찰되었지만 이는 건강한 젊은 층(65세 미만)에 국한되어 나타났다. 휴식기에는 모세혈관의 30%만이 관류가 이뤄지며, 나머지 70%는 스트레스 조건에서 모세혈관 조임근(capillary sphincter)의 이완과 소동맥의 혈관확장에 의해 열리는데, 하지만 나이든 환자에서는 기저질환이 없다 해도 조임근의 조절이 잘 이루어지지 않고, 혈관확장 장애, 혈관강직성 증가, 혈관밀도 감소 등의 이유로 모세혈관 혈류 회복이 거의 이뤄지지 않는다고 설명되고 있다. 또한, 혈관확장(vasodilation)은 혈관내피 의존적 확장(endothelium dependent vasodilation)과 혈관벽의 평활근(smooth muscle)에 의해 좌우되는 혈관내피 비의존적 확장(endothelium independent vasodilation)에 의해 이루어지는데, 혈관내피 의존적 확장은 나이듦에 따라 감소하지만, 혈관내피 비의존적 확장은 나이와 상관없이 이루어지며, 흡입마취제는 혈관내피 의존적 확장은 억제, 혈관내피 비의존적 확장은 세포 내 Ca2+의 조절을 통해 촉진시켜 혈관확장을 유발하고, 프로포폴과 아편유사제는 전신혈관 저항을 감소시킴으로써 혈관내피 비의존적 확장에 작용하여 혈관확장을 일으킨다고 기술하고 있다. 미세순환을 조절하는데 있어서 수많은 임상적 여건이 존재하기 때문에 단정적으로 결과를 예측하는 데 한계를 보인다.
마취약제 혹은 마취방식에 따른 안압의 변화 및 안와구조의 영향에 대해 다양한 연구가 있었다. Chang et al [6]은 16개의 연구에서 정맥마취와 흡입마취가 안압(intraocular pressure)에 미치는 영향에 대한 체계적 논문 고찰을 하였다. 기술된 바에 따르면, 모든 흡입마취제 및 정맥마취제는 안압을 감소시키며 그 기전으로는 혈압의 감소에 따른 맥락막 혈류 감소, 안와근육의 이완으로 인한 안와벽 긴장 감소 등이 거론되고 있다. 펜타닐, 알펜타닐, 레미펜타닐과 같은 속효성 아편유사제 역시 안압을 감소시키는데, 중추신경계의 안구 중추가 억제됨으로써 이루어지는 것으로 추측되고 있다. 비탈분극성 근이완제 또한 안압을 감소시킨다. 이 연구에 따르면 흡입마취제보다 정맥마취제가 안압을 더 많이 감소시켰다고 하였다. Geeraerts et al [4]은 전신마취를 받는 13명의 어린이들을 대상으로 Color Doppler imaging using a Sonoline AntaresTM ultrasound system (Siemens Medical System Inc., Issaquah, WA, USA)를 이용하여 안구 뒤(retrobulbar) 동맥들의 혈류 속도를 측정하였다. 대표적인 흡입마취제인 Sevoflurane은 뇌혈관을 직접적으로 확장시키기는 하지만, 뇌의 자동 조절 기능(cerebral autoregulation) 덕분에 뇌혈류량은 일정하게 유지된다. 안동맥(ophthalmic artery)은 내경동맥(internal carotid artery)의 첫 번째 분지로 중뇌동맥(middle cerebral artery)과 같은 뇌혈관과는 다른 자가조절 기전을 가지고 있으며, 고농도의 Sevoflurane 마취에 의해 혈류 속도가 감소하는데 이는 MAP의 감소와 관련이 있는 듯하다고 기술되어 있다. 반면 안동맥의 분지인 중심망막동맥(central retinal artery)은 망막 산소 공급의 40%를 차지하는데, 내피유래 물질들에 의해 혈관의 긴장도를 잘 유지하는 자동조절기능이 있어, 고농도의 Sevoflurane 마취에도 망막 혈류를 일정하게 유지시킨다는 결과를 보였다.
본 연구는 유리체망막 수술을 받는 환자의 수술받지 않는 반대안을 대상으로 시행되었다. 비수술안의 경우 망막 혈관질환, 황반질환이 있는 경우나 다른 안질환의 과거력이 있는 경우를 배제했기 때문에 사실상 건강한 환자를 대상으로 한 것이나 마찬가지이다. 고혈압, 당뇨, 신장질환을 가진 환자들이 포함되었지만, 임상적으로 문제가 되는 혈관의 변화가 없는 상태에서 연구 대상이 되었기 때문이다. 그래서인지 만성 질환 유무에 따라 나뉘어진 그룹에서는 전신마취 전후로 모든 맥락망막 매개변수에서 유의한 차이를 보이지 않았다.
본 연구의 결과를 보면 기대했던 수술 중 저혈압(절대적 기준과 상대적 기준 모두)에 따른 맥락망막 매개변수의 변화는 거의 보이지 않았다. 앞서 망막 혈액 순환에서도 잠시 언급했지만, 망막은 자율조절 기능이 있어서, 어느 정도의 관류압 변동에는 영향받지 않고 망막 혈류를 유지할 수 있다. 반면에, 맥락막 순환은 관류압 변동에 영향을 받기 때문에 혈압 변동에 민감하다[5,22]. 우리 결과에서는 수술 중 저혈압 상황에서 망막과 맥락막 모두에서 영향을 받지 않았다. 저혈압의 컷오프 포인트를 보다 낮게 설정했다면 유의한 결과를 얻을 가능성이 있었겠지만, 수술 중 과도한 저혈압을 피하는 조치들이 대부분 취해지기 때문에 장시간 수술 중 저혈압과 관련된 후향적 데이터는 수집하기가 매우 어렵다. 또한 체액 변동이 거의 없는 안과 수술이었던 것도 변동이 보이지 않은 또 다른 원인이 되었다. 따라서 전신마취의 지속시간과 방법, 수술의 종류, 전신마취에 대한 누적된 노출력, 수술 중 저혈압의 지속 기간 등과 관련하여 보다 적절한 사례가 필요해 보인다.
본 연구에서 흥미로운 점은 수술 중 MAP의 변동폭에 따른 통계적으로 유의한 선형상관관계 결과이다. 수술 중 어느 시점이건 가장 높은 MAP와 가장 낮은 MAP와의 차이가 클수록 심부모세혈관총과 맥락막 모세혈관의 계수(count)는 감소하는 경향을 보이고, 맥락막 모세혈관의 크기(size)와 신호 공극(signal void)은 증가하는 경향을 보였다. MAP의 변동폭은 개인차가 있는 것으로, 본 연구에서는 절대적이거나 상대적인 저혈압보다 의미 있는 결과를 보였다. 이 결과의 의의는 저혈압이 없었다 하더라도 혈압의 변동폭이 컸다면 충분히 망막 혈관의 변화를 초래할 수도 있다는 것이다. 의미를 연장하면 뇌혈관의 변화 가능성까지 추론해 볼 수도 있다. 빛간섭단층혈관조영술을 이용한 경도 인지장애 연구에서도 표층모세혈관총과 심부모세혈관총의 혈관밀도가 감소하고 망막중심오목무혈관부위의 면적이 늘어나는 등, 본 연구값과 비슷한 양상을 보였다[25]. 맥락막 모세혈관층 혈관밀도의 감소가 투석 환자의 투석 후 혈압 감소와 상관관계가 있었다는 빛간섭단층혈관조영술을 활용한 투석 환자에 대한 연구도 있었다[12]. 환자 개별 맞춤형 혈압 관리의 중요성을 보여주는 결과로, 좀 더 많은 대상에 대해 전향적이거나 후향적인 연구가 필요하다.
또한 본 연구에서 전신마취 후에 심부모세혈관총의 혈관밀도가 유의하게 증가되었다. 수술 중 저혈압 여부로 나누지 않은 전체 환자에서 얻어진 결과이다. 혈압의 변동보다는 전신마취가 미세혈관에 미치는 다른 영향 때문이 아닌가 생각된다. 전체 환자 중 대부분의 환자에서 흡입마취를 시행하였고(38명/40명), 흡입마취제는 뇌혈관이나 망막 혈관을 직접적으로 혈관을 확장시키는 성질이 있는데[5], 자율 조절에 의해서 혈류는 일정하게 유지되지만 심부모세혈관총에서만 잔류 효과가 남은 것으로 보인다. 또 다른 추론은 전신마취로 인해 안구 관류압이 일시적으로 떨어지면서 혈관확장 메커니즘이 일시적으로 작용하는 피드백 자율조절이 실행되어 그 효과가 심부모세혈관총에 남아 있는 것일 수도 있다[31]. Zhang et al [32]은 뇌혈관 질환과 빛간섭단층혈관조영술을 다룬 논문 14편에 대한 체계적 문헌 고찰에서 심부모세혈관총의 혈관밀도가 증가하는 것이 표층모세혈관총의 혈관밀도 감소에 대한 보상적 메커니즘이라는 관점을 언급했다. 추후 대규모의 전향적 연구 등을 통해 정확한 메커니즘에 대한 추후 연구가 필요할 것으로 사료된다.
본 연구의 또 다른 결과는 마취 시간과 맥락막 모세혈관층의 평균 크기(average size)와의 유의한 약한 음의 선형 상관관계와, 연령과 표층모세혈관총의 혈관밀도와의 유의미한 약한 음의 선형 상관관계이다. 맥락막 모세혈관층은 자율신경계의 지배를 받고 있으며, 지속적인 마취로 인한 스트레스로 교감신경 말단에서 노르아드레날린이 분비되며 맥락막 혈류가 줄어드는 영향이 아닌가 생각되며[31], 연령이 증가함에 따른 표층모세혈관총의 혈관밀도의 감소는 정확한 메커니즘은 알 수 없어도 자율신경계의 지배를 받지 않는 망막의 혈관이 연령이 증가함에 따라 혈관 내피 기능의 장애가 생기면서 전신마취 후 제자리로 돌아오는 복귀 기능이 저하됨에 따른 현상으로 보인다[30,31].
본 연구의 강점은 전신마취와 망막 혈관과의 관계를 최초로 빛간섭단층혈관조영술을 이용하여 규명하려 했다는 것이다. 망막 혈관에 관심을 가지며 자연스럽게 뇌혈관에도 관심을 갖게 되었는데, 전신마취와 뇌혈관장애와의 관계에 대한 수많은 연구가 있고, 빛간섭단층혈관조영술과 뇌혈관장애 판정과의 관계에 대한 수많은 연구가 있었지만, 전신마취와 빛간섭단층혈관조영술과의 접점을 찾는 연구는 드물었으며, 이에 우리는 전신마취에 따른 망막 혈관의 변화를 빛간섭단층혈관조영술을 이용하여 분석해보고자 연구를 진행하게 되었다. 앞서 전신마취 중 혈압 변동폭이 클 때의 맥락망막 혈관의 변화가 경증 인지장애 환자의 빛간섭단층혈관조영술 결과와 비슷하다고 언급하였었다. 또한 전신마취 후 심부모세혈관총의 혈관밀도가 유의하게 높아지는 결과에 대한 해석 중 Zhang et al [32]의 표층모세혈관총의 혈관밀도 감소에 대한 보상적 메커니즘이라는 관점에서 보면 우리 연구에서 표층모세혈관총의 혈관밀도가 감소하는 시기를 관찰 못하고 지나쳤을 가능성이 있으며, 이는 경증 인지장애의 유용한 생물학적 지표를 놓친 것이라고 가정할 수 있다. 수술 환자에서 생기는 경증 인지장애가 수술 후 인지장애인데, 비심장 수술 후 12-21% 발생하고 국소마취에서보다 전신마취 후 더 잘 생기며, 특히 수술 직후 3일간 발생률이 높다고 했다[27,28]. 따라서 대표적인 비심장 수술인 안과 수술의 경우 꼭 필요한 경우가 아니라면 전신마취보다는 국소마취를 권하는 게 수술 후 인지장애의 위험을 피할 수 있는 방법이라는 가설을 세울 수 있다. 연령이 증가함에 따라 표층모세혈관총의 혈관밀도가 감소하는 결과로 볼 때, 특히 노인의 경우 전신마취를 더 주의해야하는 것으로 보인다.
본 연구의 제한점으로 적은 대상자의 수, 단일 기관이라는 점, 수술이 안과에 국한되었다는 것, 후향적 연구의 한계로 대상자에 대한 변수의 통제가 잘 안되었다는 점, 마취제의 종류가 달랐지만 그것을 비교할 정도의 개체수가 못되었다는 점, 그리고 무엇보다도 최초의 시도이기에 기준을 삼을 만한 연구 결과의 부재로 결과의 해석 및 분석이 어렵다는 점이다. 맥락망막 혈관 변화가 유의하지 않은 것이 아니라 초기에 변화를 보인 후 회복 가능성도 배제할 수 없어, 추후 적절한 변수를 설정한 대규모의 연구를 통해 전신마취와 망막 혈관의 관계에 대한 추가 연구가 필요하다. 추가적으로 전신마취 영향을 분석하려면 실제 시간에 따른 연속 데이터가 필요하나, 본 연구에서는 후향적 연구의 특성상 술 후 다음 날 한차례 결과 측정을 시행하였다. 이에 종단 연구를 통해 본 연구의 한계를 보완할 수 있다.
결론적으로 전신마취하에 유리체망막 수술을 받은 환자에서 마취 전후의 비수술안의 망막 혈관의 변화를 빛간섭단층혈관조영술을 이용하여 분석하였고, 수술 중 저혈압에 따른 망막 관류 양상의 유의한 차이는 없었다. 반면 전신마취 후 심부모세혈관총의 혈관밀도는 유의한 증가를 보였고, 수술 중 혈압 변동폭이 증가될수록 심부모세혈관총 혈관밀도와 맥락막 모세혈관층의 계수(count)는 감소되었으나, 맥락막 모세혈관층의 평균 크기(average size)와 신호 공극(signal void)은 증가되었다. 그리고 마취시간 증가에 따른 맥락막 모세혈관의 평균 크기의 감소 및 연령 증가에 따른 표층모세혈관총의 혈관밀도의 감소라는 결과를 얻었다. 전신마취 후 수술 후 인지장애 및 나아가 치매로의 발전 가능성 등에 대한 빛간섭단층혈관조영술을 이용한 대규모의 전향적 추가 연구가 필요하다.
Figure 1.
Scatter plots between clinical and tomographic parameters and anesthesia parameters. (A) Duration of anesthesia and difference in average size of choroidal capillary layer showed a weak negative linear correlation (p < 0.05, r = -0.319). (B) Negative linear correlation (p < 0.05, r = -0.386) was observed between age and SCP vessel density. (C-F) Intraoperative MAP fluctuation appeared to have linear correlation with change of DCP vessel density, and of flow void features of choriocapillaris (count, average size, signal void). (C) DCP & (D) count showed a weak negative correlation with MAP fluctuation, however, (E) average size (p < 0.01, r = 0.409) and (F) signal void of choriocapillaris (p < 0.01, r = 0.438) showed a weak positive correlation. SCP = superficial capillary plexus; DCP = deep capillary plexus; MAP = mean arterial pressure.
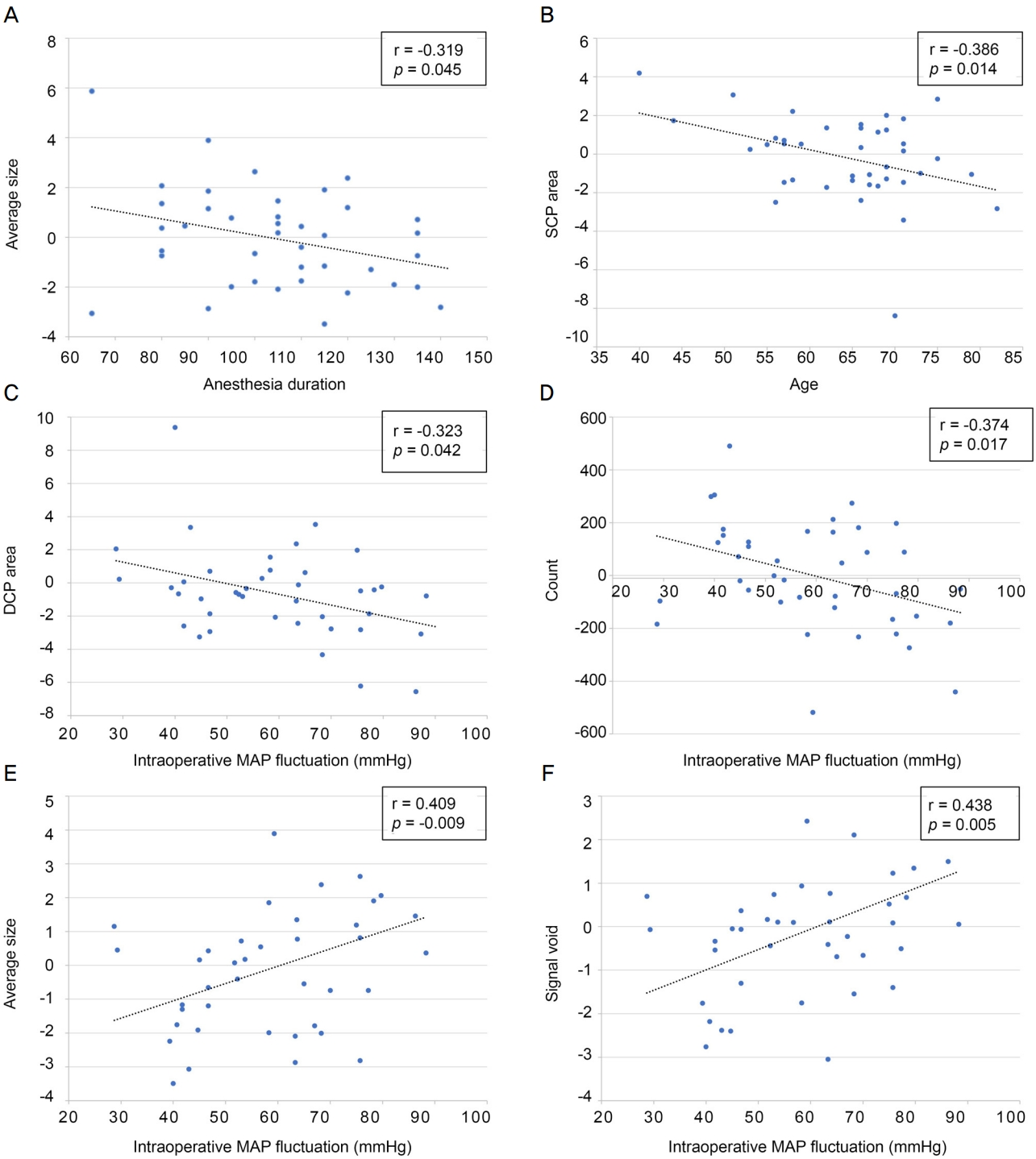
Table 1.
Baseline characteristics of patients
Table 2.
Comparisons of structural and angiographic microvascular parameters before and after general anesthesia
| Before GA | After GA | p-value* | |
|---|---|---|---|
| BCVA | 0.78 ± 0.22 | 0.81 ± 0.19 | 0.340 |
| LogMAR | 0.13 ± 0.14 | 0.11 ± 0.12 | 0.235 |
| RT | 277.80 ± 18.85 | 276.88 ± 18.71 | 0.452 |
| CT | 193.84 ± 83.27 | 192.39 ± 83.51 | 0.662 |
| SCP (VD) | 65.49 ± 2.70 | 65.68 ± 2.41 | 0.767 |
| DCP (VD) | 58.83 ± 2.00 | 59.47 ± 2.54 | 0.037† |
| Choriocapillaris flow void parameters | |||
| Count | 2,434.95 ± 274.35 | 2,433.8 ± 277.27 | 0.877 |
| Average size | 16.18 ± 2.53 | 16.25 ± 2.63 | 0.648 |
| Signal void | 38.85 ± 1.87 | 38.95 ± 1.89 | 0.545 |
Table 3.
Changes in choroidal thickness and retinal thickness associated with general anesthesia
|
Choroidal thickness |
Retinal thickness |
|||||
|---|---|---|---|---|---|---|
| Before GA | After GA | p-value* | Before GA | After GA | p-value* | |
| Total | 193.8 ± 83.3 | 192.4 ± 83.5 | 0.662 | 277.8 ± 18.8 | 276.9 ± 18.7 | 0.452 |
| C | 202.0 ± 91.8 | 199.8 ± 92.1 | 0.731 | 233.0 ± 30.8 | 231.2 ± 33.2 | 0.542 |
| OS | 199.4 ± 81.4 | 199.9 ± 82.2 | 0.950 | 272.0 ± 16.7 | 271.0 ± 15.8 | 0.552 |
| ON | 160.2 ± 86.9 | 161.4 ± 88.8 | 0.656 | 286.0 ± 15.1 | 284.3 ± 15.2 | 0.563 |
| OI | 190.7 ± 89.9 | 190.4 ± 91.9 | 0.602 | 254.4 ± 19.1 | 254.8 ± 18.5 | 0.685 |
| OT | 185.4 ± 75.8 | 185.2 ± 76.1 | 0.935 | 254.4 ± 22.4 | 255.0 ± 18.5 | 0.606 |
| IS | 207.8 ± 90.5 | 201.6 ± 90.0 | 0.101 | 305.1 ± 22.0 | 304.2 ± 21.6 | 0.425 |
| IN | 197.5 ± 94.5 | 197.5 ± 94.4 | 0.364 | 305.9 ± 24.3 | 304.0 ± 25.1 | 0.463 |
| II | 203.8 ± 96.7 | 200.8 ± 92.8 | 0.388 | 300.9 ± 22.2 | 299.6 ± 22.9 | 0.635 |
| IT | 196.8 ± 87.4 | 194.8 ± 86.8 | 0.994 | 295.0 ± 26.5 | 295.3 ± 23.4 | 0.978 |
Table 4.
Anesthesia and intraoperative hemodynamic characteristics between patients with and without IOH
| Without IOH (n = 16) | With IOH (n = 24) | p-value* | |
|---|---|---|---|
| Age | 62.8 ± 8.8 | 65.3 ± 8.9 | 0.872 |
| Anesthesia duration (minutes) | 105.3 ± 19.6 | 104.1 ± 19.9 | 0.671 |
| Intraoperative MAP fluctuation (mmHg) | 54.5 ± 14.1 | 62.4 ± 16.6 | 0.842 |
| Baseline and intraoperative MAP difference (mmHg) | 0.9 ± 11.3 | -4.4 ± 8.4 | 0.473 |
| Intraoperative MAP <baseline MAP time (minutes) | 21.3 ± 41.5 | 29.4 ± 38.8 | 0.874 |
| Intraoperative MAP <80% of baseline MAP time (minutes) | 6.6 ± 19.0 | 13.8 ± 21.1 | 0.927 |
| IOH time (minutes) | 0.0 | 21.0 ± 16.1 | - |
Table 5.
Comparisons of structural and angiographic vessel parameters between patients with and without IOH
| Without IOH (n = 16) | With IOH (n = 24) | p-value* | |
|---|---|---|---|
| Difference in SCP area | 0.34 ± 1.89 | -0.55 ± 2.32 | 0.204 |
| Difference in DCP area | -0.89 ± 1.98 | -0.47 ± 3.17 | 0.641 |
| Difference in count | -24.94 ± 184.40 | 18.54 ± 222.02 | 0.521 |
| Difference in average size | 0.02 ± 1.64 | -0.12 ± 2.22 | 0.829 |
| Difference in signal void | -0.04 ± 1.00 | -0.13 ± 2.07 | 0.885 |
| Difference in BCVA | 0.00 ± 0.17 | -0.43 ± 0.16 | 0.421 |
| Difference in logMAR | 0.01 ± 0.11 | 0.03 ± 0.09 | 0.701 |
| Difference in retinal thickness | 0.85 ± 3.22 | 0.97 ± 5.52 | 0.938 |
| Difference in choroidal thickness | -0.34 ± 7.61 | 2.64 ± 22.72 | 0.616 |
Table 6.
Anesthesia and intraoperative hemodynamic characteristics between patients with and without relative IOH
| Without relative IOH (n = 29) | With relative IOH (n = 11) | p-value* | |
|---|---|---|---|
| Age | 64.0 ± 8.5 | 65.2 ± 10.2 | 0.719 |
| Anesthesia duration (minutes) | 102.8 ± 18.7 | 109.6 ± 21.8 | 0.334 |
| Intraoperative MAP fluctuation (mmHg) | 58.9 ± 16.0 | 60.2 ± 16.3 | 0.815 |
| Baseline and intraoperative MAP difference (mmHg) | -0.1 ± 9.9 | -8.1 ± 7.7 | 0.020† |
| Intraoperative MAP <baseline MAP time (minutes) | 4.7 ± 13.9 | 82.7 ± 26.6 | 0.000† |
| Intraoperative MAP <80% of baseline MAP time (minutes) | 0.0 | 39.6 ± 19.3 | - |
Table 7.
Comparisons of structural and angiographic parameters between patients with and without relative IOH
| Without relative IOH (n = 29) | With relative IOH (n = 11) | p-value* | |
|---|---|---|---|
| Difference in SCP area | -0.16 ± 1.62 | -0.28 ± 3.34 | 0.873 |
| Difference in DCP area | -0.80 ± 2.24 | -0.22 ± 3.85 | 0.556 |
| Difference in count | -6.55 ± 193.86 | 21.45 ± 245.65 | 0.707 |
| Difference in average size | -0.07 ± 1.76 | -0.02 ± 2.60 | 0.941 |
| Difference in signal void | -0.27 ± 1.31 | 0.39 ± 2.48 | 0.279 |
| Difference in BCVA | -0.02 ± 0.18 | -0.05 ± 0.12 | 0.605 |
| Difference in logMAR | 0.02 ± 0.11 | 0.03 ± 0.08 | 0.782 |
| Difference in retinal thickness | 0.51 ± 5.27 | 2.00 ± 2.46 | 0.376 |
| Difference in choroidal thickness | -0.60 ± 11.93 | 6.85 ± 28.99 | 0.251 |
Table 8.
Anesthesia and intraoperative hemodynamic characteristics between patients with and without underlying chronic disease
| With chronic diseases (n = 28) | Without chronic diseases (n = 12) | p-value* | |
|---|---|---|---|
| Age | 64.5 ± 8.17 | 62.8 ± 10.6 | 0.886 |
| Anesthesia duration (minutes) | 103.7 ± 19.2 | 106.7 ± 21.1 | 0.686 |
| Intraoperative MAP fluctuation (mmHg) | 59.6 ± 15.3 | 58.5 ± 18.0 | 0.842 |
| Baseline and intraoperative MAP difference (mmHg) | -1.5 ± 10.7 | -4.0 ± 8.0 | 0.473 |
| Intraoperative MAP <baseline MAP time (minutes) | 26.8 ± 39.7 | 24.6 ± 41.0 | 0.874 |
| Intraoperative MAP <80% baseline MAP time (minutes) | 11.1 ± 20.2 | 10.4 ± 21.6 | 0.927 |
Table 9.
Comparisons of structural and angiographic parameters between patients with and without underlying chronic disease
| Without chronic diseases (n = 12) | With chronic diseases (n = 28) | p-value* | |
|---|---|---|---|
| Difference in SCP area | -0.73 ± 3.03 | -0.04 ± 1.71 | 0.310 |
| Difference in DCP area | -1.26 ± 2.15 | -0.37 ± 2.95 | 0.350 |
| Difference in count | -35.25 ± 192.07 | 16.64 ± 213.77 | 0.476 |
| Difference in average size | 0.35 ± 2.16 | -0.24 ± 1.93 | 0.395 |
| Difference in signal void | -0.04 ± 0.20 | -0.02 ± 0.15 | 0.136 |
| Difference in BCVA | 0.04 ± 0.12 | 0.01 ± 0.09 | 0.684 |
| Difference in logMAR | 1.27 ± 1.58 | 0.77 ± 5.54 | 0.539 |
| Difference in retinal thickness | -1.27 ± 1.58 | -0.77 ± 5.54 | 0.762 |
| Difference in choroidal thickness | -2.40 ± 10.40 | 3.10 ± 20.54 | 0.387 |
Table 10.
Correlation between anesthetic parameters and clinical and tomographic parameters
| BCVA | LogMAR | SCP | DCP | Count | Average size | Signal void | RT | CT | |
|---|---|---|---|---|---|---|---|---|---|
| Anesthesia duration | |||||||||
| r* | 0.061 | -0.028 | -0.001 | -0.111 | 0.208 | -0.319 | -0.291 | 0.139 | 0.252 |
| p-value | 0.708 | 0.862 | 0.996 | 0.494 | 0.198 | 0.045† | 0.068 | 0.391 | 0.117 |
| Intraoperative MAP fluctuation | |||||||||
| r | -0.228 | 0.226 | -0.144 | -0.377 | -0.374 | 0.409 | 0.438 | -0.139 | 0.033 |
| p-value | 0.157 | 0.160 | 0.376 | 0.017† | 0.017† | 0.009† | 0.005† | 0.393 | 0.838 |
| Baseline - intraoperative MAP gap | |||||||||
| r | 0.080 | -0.073 | -0.033 | 0.123 | -0.184 | 0.122 | -0.005 | -0.171 | 0.034 |
| p-value | 0.622 | 0.656 | 0.838 | 0.449 | 0.254 | 0.453 | 0.977 | 0.291 | 0.833 |
| Intraoperative hypotension | |||||||||
| r | 0.291 | -0.304 | -0.342 | -0.120 | -0.128 | 0.051 | -0.011 | -0.214 | 0.001 |
| p-value | 0.167 | 0.148 | 0.102 | 0.576 | 0.551 | 0.812 | 0.960 | 0.314 | 0.997 |
| Intraoperative MAP <baseline MAP time | |||||||||
| r | -0.011 | -0.022 | 0.062 | 0.248 | 0.122 | -0.096 | 0.023 | 0.133 | 0.106 |
| p-value | 0.944 | 0.892 | 0.704 | 0.123 | 0.454 | 0.557 | 0.889 | 0.413 | 0.514 |
| Intraoperative MAP <80% baseline MAP time | |||||||||
| r | -0.042 | 0.001 | 0.097 | 0.243 | 0.081 | -0.048 | 0.076 | 0.141 | -0.037 |
| p-value | 0.796 | 0.994 | 0.552 | 0.131 | 0.617 | 0.768 | 0.640 | 0.387 | 0.821 |
| Age | |||||||||
| r | -0.045 | 0.047 | -0.386 | -0.081 | 0.131 | -0.167 | -0.137 | -0.304 | 0.299 |
| p-value | 0.784 | 0.772 | 0.014† | 0.621 | 0.420 | 0.302 | 0.401 | 0.056 | 0.061 |
REFERENCES
1) Wesselink EM, Kappen TH, Torn HM, et al. Intraoperative hypotension and the risk of postoperative adverse outcomes: a systematic review. Br J Anaesth 2018;121:706-21.


3) van Waes JA, van Klei WA, Wijeysundera DN, et al. Association between intraoperative hypotension and myocardial injury after vascular surgery. Anesthesiology 2016;124:35-44.


4) Geeraerts T, Devys JM, Berges O, et al. Sevoflurane effects on retrobulbar arteries blood flow in children. Br J Anaesth 2005;94:636-41.

5) Samy E, El Sayed Y, Awadein A, Gamil M. Effect of general inhalational anesthesia on intraocular pressure measurements in normal and glaucomatous children. Int Ophthalmol 2021;41:2455-63.


6) Chang CY, Chien YJ, Wu MY. Attenuation of increased intraocular pressure with propofol anesthesia: a systematic review with meta-analysis and trial sequential analysis. J Adv Res 2020;24:223-38.



7) Kim HY, Baek SH, Baik SW, et al. The effect of sevoflurane on retinal angiogenesis in a mouse model of oxygen-induced retinopathy. J Anesth 2018;32:204-10.


8) Sabanayagam C, Lye WK, Klein R, et al. Retinal microvascular calibre and risk of diabetes mellitus: a systematic review and participant-level meta-analysis. Diabetologia 2015;58:2476-85.



9) Daien V, Kawasaki R, Villain M, et al. Retinal vascular caliber is associated with renal function in apparently healthy subjects. Acta Ophthalmol 2013;91:e283-8.


10) Sabanayagam C, Shankar A, Koh D, et al. Retinal microvascular caliber and chronic kidney disease in an Asian population. Am J Epidemiol 2009;169:625-32.


11) de Carlo TE, Romano A, Waheed NK, Duker JS. A review of optical coherence tomography angiography (OCTA). Int J Retina Vitreous 2015;1:5.


12) Shin YU, Lee DE, Kang MH, et al. Optical coherence tomography angiography analysis of changes in the retina and the choroid after haemodialysis. Sci Rep 2018;8:17184.



13) Bijker JB, van Klei WA, Kappen TH, et al. Incidence of intraoperative hypotension as a function of the chosen definition: literature definitions applied to a retrospective cohort using automated data collection. Anesthesiology 2007;107:213-20.

14) Vernooij LM, van Klei WA, Machina M, et al. Different methods of modelling intraoperative hypotension and their association with postoperative complications in patients undergoing non-cardiac surgery. Br J Anaesth 2018;120:1080-9.


15) Kluger MT, Collier JMK, Borotkanics R, et al. The effect of intra-operative hypotension on acute kidney injury, postoperative mortality and length of stay following emergency hip fracture surgery. Anaesthesia 2022;77:164-74.


16) Sessler DI, Bloomstone JA, Aronson S, et al. Perioperative Quality Initiative consensus statement on intraoperative blood pressure, risk and outcomes for elective surgery. Br J Anaesth 2019;122:563-74.


17) Noh D, Ryu G, Sagong M. Analysis of foveal microvascular structures using optical coherence tomography angiography in age-stratified healthy Koreans. J Korean Ophthalmol Soc 2017;58:1058-65.

18) Alnawaiseh M, Brand C, Bormann E, et al. Quantitative analysis of retinal perfusion in mice using optical coherence tomography angiography. Exp Eye Res 2017;164:151-6.


19) Zhang P, Miller EB, Manna SK, et al. Temporal speckle-averaging of optical coherence tomography volumes for in-vivo cellular resolution neuronal and vascular retinal imaging. Neurophotonics 2019;6:041105.



20) Ripolles-Garcia A, Holle DM, Cohen JA, et al. Retinal structural and microvascular abnormalities in retinal dysplasia imaged by OCT and OCT angiography. Vet Ophthalmol 2021 Nov 22 doi:10.1111/vop.12952. [Epub ahead of print].
21) Iezzi LA, Dalvin LA. Optical path redirection device for optical coherence tomography angiography of recumbent patients under general anesthesia. Transl Vis Sci Technol 2020;9:45.



22) Nakao S, Nishina S, Tanaka S, et al. Early laser photocoagulation for extensive retinal avascularity in infants with incontinentia pigmenti. Jpn J Ophthalmol 2020;64:613-20.


23) Kothari N, Chu A, Huang JM, et al. Arm-mounted optical coherence tomography angiography in extremely low birth weight neonates with retinopathy of prematurity. Am J Ophthalmol Case Rep 2020;18:100624.



24) Blindbæk SL, Torp TL, Lundberg K, et al. Noninvasive retinal markers in diabetic retinopathy: advancing from bench towards bedside. J Diabetes Res 2017;2017:2562759.


25) Hui J, Zhao Y, Yu S, et al. Detection of retinal changes with optical coherence tomography angiography in mild cognitive impairment and Alzheimer's disease patients: A meta-analysis. PLoS One 2021;16:e0255362.



26) van de Kreeke JA, Nguyen HT, Konijnenberg E, et al. Optical coherence tomography angiography in preclinical Alzheimer's disease. Br J Ophthalmol 2020;104:157-61.



27) Evered LA, Silbert BS. Postoperative cognitive dysfunction and noncardiac surgery. Anesth Analg 2018;127:496-505.


28) Gao Y, Liu L, Zhao B, et al. Effect of general and non-general anesthesia on postoperative cognitive dysfunction. J Coll Physicians Surg Pak 2020;30:407-11.


29) Brettner F, Heitzer M, Thiele F, et al. Non-invasive evaluation of macro- and microhemodynamic changes during induction of general anesthesia - a prospective observational single-blinded trial. Clin Hemorheol Microcirc 2021;77:1-16.


30) Cho AR, Lee HJ, Kim HJ, et al. Microvascular reactivity measured by dynamic near-infrared spectroscopy following induction of general anesthesia in healthy patients: observation of age-related change. Int J Med Sci 2021;18:1096-103.







 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




