 |
 |
| J Korean Ophthalmol Soc > Volume 65(2); 2024 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ņä¼ņ£ĀņŻ╝ņäĖĒżņŚÉņä£ ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒģÉ ļČĆļģĖļō£(latanoprostene bunod, LBN)Ļ░Ć ņØ╝ņé░ĒÖöņ¦łņåī(nitric oxide, NO)ņØś ņāØņä▒Ļ│╝ ņä¼ņ£ĀņŻ╝ņØś Ēł¼Ļ│╝ļÅäņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢśņśĆļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
ņä¼ņ£ĀņŻ╝ņäĖĒżņŚÉ 50, 100 ╬╝M LBNĻ│╝ ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖ ņ£Āļ”¼ņé░(latanoprost free acid, LAT)ņØä 30ļČäĻ░ä ļģĖņČ£ņŗ£ņ╝░ņ£╝ļ®░, 0.5 mM L-NAME (N-Nitroarginine methyl ester)ņŚÉļÅä ĒĢ©Ļ╗ś ļģĖņČ£ņŗ£ņ╝░ļŗż. ņäĖĒż ņāØņĪ┤Ļ│╝ NO ņāØņä▒ņØĆ MTT (3-[4, 5-dimethylthiazol-2-yl]-2, 5-diphenyltetrazolium bromide) assayņÖĆ Griess assayļĪ£ ņĖĪņĀĢĒĢśņśĆļŗż. ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅäņÖĆ ņĀĆĒĢŁļÅäļŖö carboxyfluorescein permeabilityņÖĆ trans-endothelial electrical resistance (TEER)ļĪ£ Ļ░üĻ░ü ņĖĪņĀĢĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
100 ╬╝M LBNņØĆ NOņØś ņāØņä▒ņØä ņ”ØĻ░Ćņŗ£ņ╝░ņ£╝ļ®░, L-NAMEņŚÉ ĒĢ©Ļ╗ś ļģĖņČ£ņŗ£Ēé© Ļ▓ĮņÜ░ņŚÉļŖö NO ņāØņä▒ņØ┤ ņ¢ĄņĀ£ļÉśņŚłļŗż. 100 ╬╝M LBNņØĆ ņä¼ņ£ĀņŻ╝ ļŗ©ņĖĄņäĖĒżņĖĄņØś TEERņØä ņĀĆĒĢśņŗ£ņ╝░ļŗż. ļśÉĒĢ£ carboxyfluorescein permeability testņŚÉņä£ LBNņØĆ Ēł¼Ļ│╝ļÅäļź╝ ņ”ØĻ░Ćņŗ£ņ╝░ņ£╝ļ®░, 100 ╬╝M LBNņŚÉ L-NAMEļź╝ ĒĢ©Ļ╗ś ļģĖņČ£ņŗ£Ēé© Ļ▓ĮņÜ░ Ēł¼Ļ│╝ļÅäĻ░Ć Ļ░ÉņåīĒĢśņśĆļŗż. LATļŖö NOņØś ņāØņä▒Ļ│╝ ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅäņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śņ¦Ć ņĢŖņĢśļŗż.
ABSTRACT
Purpose
To investigate the effects of latanoprostene bunod (LBN) on nitric oxide (NO) production and permeability in human trabecular meshwork cells (HTMC).
Methods
HTMC were treated with 50 and 100 ┬ĄM LBN and latanoprost free acid (LAT) for 30 minutes. Additionally, 100 ┬ĄM LBN was co-exposed to 0.5 mM L-NAME (N-Nitroarginine methyl ester). Cellular viability and NO production were measured using MTT (3-[4, 5-dimethylthiazol-2-yl]-2, 5-diphenyltetrazolium bromide) and Griess assays. The permeability and resistance of the HTMC monolayer were evaluated by trans-endothelial electrical resistance (TEER) and carboxyfluorescein permeability.
Results
Exposure to 100 ┬ĄM LBN led to increased NO production, whereas co-exposure to L-NAME reduced NO production. Treatment with 100 ┬ĄM LBN decreased the TEER of the HTMC monolayer. LBN exposure heightened carboxyfluorescein permeability, but co-exposure to 100 ┬ĄM LBN and L-NAME reduced permeability. LAT treatment did not affect NO production or permeability.
ņä¼ņ£ĀņŻ╝ļŖö ļģ╣ļé┤ņןņŚÉņä£ ļ░®ņłśņ£ĀņČ£ņØś ņĪ░ņĀłņŚÉ ņżæņÜöĒĢ£ ņŚŁĒĢĀņØä ĒĢśļŖöļŹ░, ņä¼ņ£ĀņŻ╝ņØś ļ│Ćņä▒ņØ┤ļéś ņä¼ņ£ĀņŻ╝ņäĖĒżņØś Ļ░ÉņåīļĪ£ ņØĖĒĢ┤ ņä¼ņ£ĀņŻ╝ņØś ĻĖ░ļŖźņØ┤ ņĀĆĒĢśļÉśļ®┤ ļ░®ņłśņ£ĀņČ£ļĪ£ņØś ņĀĆĒĢŁņØ┤ ņ”ØĻ░ĆļÉśņ¢┤ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņןņØ┤ ņ£Āļ░£ļÉ£ļŗż.1,2 ļīĆļČĆļČäņØś ņĢłņĢĢĒĢśĻ░ĢņĀ£ļŖö ļ░®ņłś ņāØņä▒ņØä Ļ░Éņåīņŗ£ņ╝£ ņĢłņĢĢĒĢśĻ░Ģ ņ×æņÜ®ņØä ļéśĒāĆļé┤ņ¦Ćļ¦ī ĒöäļĪ£ņŖżĒāĆĻĖĆļ×Ćļöś ņĀ£ņĀ£ļŖö ĒżļÅäļ¦ēĻ│Ąļ¦ēņØä ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£ņ╝£ Ļ░ĢļĀźĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ņ×æņÜ®ņØä ļéśĒāĆļé┤ņ¢┤ ļģ╣ļé┤ņןņØś ņØ╝ņ░© ņ╣śļŻīņĀ£ļĪ£ ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż.3,4 ņØ┤ņÖĆ ĒĢ©Ļ╗ś ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö ņĢĮņĀ£ņŚÉ ļīĆĒĢ┤ņä£ļÅä ļŗżņ¢æĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ņŗ£Ē¢ēļÉśņ¢┤ ņÖöļŖöļŹ░5 ĻĘĖņżæ ņØ╝ņé░ĒÖöņ¦łņåī(nitric oxide, NO)Ļ░Ć ņä¼ņ£ĀņŻ╝ļź╝ ņØ┤ņÖäņŗ£ņ╝£ ļ░®ņłśņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£Ēéżļ®┤ņä£ ņĢłņĢĢĒĢśĻ░Ģ ņ×æņÜ®ņØä ļéśĒāĆļé┤ļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ņ¢┤6,7 ņØ┤ļź╝ ņØ┤ņÜ®ĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ņĢĮņĀ£Ļ░Ć ņŚ░ĻĄ¼ļÉśņ¢┤ ņÖöļŗż.8-10
ņĄ£ĻĘ╝ Ļ░£ļ░£ļÉ£ ņĢłņĢĢĒĢśĻ░ĢņĀ£ņØĖ ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒģÉ ļČĆļģĖļō£(latanoprostene bunod, LBN)ļŖö ĻĖ░ņĪ┤ņŚÉ ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖö ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖ(latanoprost) ņĀ£ņĀ£ņŚÉ NOļź╝ Ļ▓░ĒĢ®ņŗ£Ēé© ņĢĮņĀ£ļĪ£ņä£, LBNņØĆ ņĢłĻĄ¼ ļé┤ņŚÉņä£ Ļ░ĆņłśļČäĒĢ┤ļÉśņ¢┤ ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖ ņ£Āļ”¼ņé░(latanoprost free acid, LAT)Ļ│╝ butanediolļĪ£ ĒÖśņøÉļÉśņ¢┤ NO Ļ│ĄņŚ¼ņ×ÉļĪ£ņä£ņØś ņ×æņÜ®ņØä ĒĢ©Ļ╗ś ļéśĒāĆļé┤ņ¢┤,11 LBNņØĆ ĻĖ░ņĪ┤ ņĢĮņĀ£ļōżņŚÉ ļ╣äĒĢ┤ ņÜ░ņłśĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļź╝ ļéśĒāĆļéĖļŗżļŖö ņŚ¼ļ¤¼ ņ×äņāü ņŚ░ĻĄ¼Ļ░Ć ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŗż.12-20
NOļŖö cyclic guanosine monophosphate (cGMP)ļź╝ ĒÖ£ņä▒ĒÖöņŗ£ņ╝£ ņä¼ņ£ĀņŻ╝ļź╝ ņØ┤ņÖäņŗ£ĒéżļŖö ņ×æņÜ®ņØä ļéśĒāĆļé┤ļŖöļŹ░21-23 LBNņØĆ ĻĖ░ņĪ┤ņØś ĒżļÅäļ¦ēĻ│Ąļ¦ēņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö LATņŚÉ ņä¼ņ£ĀņŻ╝ļź╝ ņØ┤ņÖäņŗ£ņ╝£ ļ░®ņłśņ£ĀņČ£ņØä ņ┤ēņ¦äĒĢśļŖö NOņØś ņ×æņÜ®ņØä ņČöĻ░ĆĒĢśņŚ¼ ņØ┤ņżæ ņ×æņÜ®ņØä ļéśĒāĆļéĖļŗżĻ│Ā ĒĢ£ļŗż.24,25 ļö░ļØ╝ņä£ LBNņØ┤ ņä¼ņ£ĀņŻ╝ņŚÉņä£ NOļź╝ ņ”ØĻ░Ćņŗ£ņ╝£ cGMPļź╝ ĒÖ£ņä▒ĒÖöņŗ£Ēé┤ņ£╝ļĪ£ņŹ© ļ░®ņłśņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö ņ×æņÜ®ņØä ļéśĒāĆļé╝ Ļ░ĆļŖźņä▒ņØ┤ ņ׳ņ£╝ļéś ņĢäņ¦ü ņŗżĒŚśņŗż ļé┤ņŚÉņä£ ņä¼ņ£ĀņŻ╝ņØś Ēł¼Ļ│╝ļÅäņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØĆ ņ×ÉņäĖĒ׳ ņŚ░ĻĄ¼ļÉśņ¦Ć ņĢŖņĢśļŗż. ņØ┤ņŚÉ ļö░ļØ╝ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņØĖņ▓┤ņØś ņä¼ņ£ĀņŻ╝ņäĖĒżņŚÉņä£ LBNņØ┤ NOņØś ņāØņä▒ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źĻ│╝ ņä¼ņ£ĀņŻ╝ņØś Ēł¼Ļ│╝ļÅäņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä LATņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ ņŗżĒŚśņĀüņ£╝ļĪ£ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢśņśĆļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ļīĆĻĄ¼Ļ░ĆĒå©ļ”ŁļīĆĒĢÖĻĄÉļ│æņøÉ ņØśĒĢÖņ£żļ”¼ņŗ¼ņØśņ£äņøÉĒÜī(IRB)ņØś ņŖ╣ņØĖņØä ļ░øņĢśĻ│Ā(CR-22-115-L) ĒŚ¼ņŗ▒ĒéżņäĀņ¢ĖņØä ļö░ļØ╝ ņŗ£Ē¢ēļÉśņŚłļŗż. ņāüņÜ®ņØś ņé¼ļ×ī ņØ╝ņ░© ņä¼ņ£ĀņŻ╝ņäĖĒż(Cat. No. 6590, ScienCell, San Diego, CA, USA)ļź╝ ĒĢ┤ļÅÖĒĢśņŚ¼ ĒĢŁņāØņĀ£ņÖĆ 10% ņÜ░Ēā£ņĢäĒśłņ▓ŁņØ┤ ĒżĒĢ©ļÉ£ DulbeccoŌĆÖs modified EagleŌĆÖs medium ļ░░ņ¦Ćļź╝ ņé¼ņÜ®ĒĢśņŚ¼ 5% CO2ļ░░ņ¢æĻĖ░ņŚÉņä£ ļ░░ņ¢æĒĢ£ Ēøä ņČ®ļ¦īĒĢ┤ņ¦Ćļ®┤ 1:3ņØś ļ╣äņ£©ļĪ£ ĒŖĖļ”ĮņŗĀ ņ▓śļ”¼ĒĢśņŚ¼ Ļ│äļīĆļ░░ņ¢æĒĢśņśĆļŗż. ļ░░ņ¢æļÉ£ ņé¼ļ×īņØś ņä¼ņ£ĀņŻ╝ņäĖĒżņŚÉ 50, 100 ╬╝M LBN (Cayman Chemical, Ann Arbor, MI, USA)Ļ│╝ 50, 100 ╬╝M LAT (Cayman Chemical)ņŚÉ Ļ░üĻ░ü 30ļČäĻ░ä ļģĖņČ£ņŗ£ņ╝░ļŗż. ņØ┤ļĢī NOĻ░Ć ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅäņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä ņĢīņĢäļ│┤ĻĖ░ ņ£äĒĢśņŚ¼ 100 ╬╝M LBNņŚÉ cGMP ņĀĆĒĢ┤ņĀ£ņØĖ 0.5 mM N-Nitroarginine methyl ester (L-NAME, Sigma-Aldrich, St. Louis, MO, USA)ņŚÉ ĒĢ©Ļ╗ś ļģĖņČ£ņŗ£ņ╝£ ņŗżĒŚśņØä ņŗ£Ē¢ēĒĢśņśĆļŗż.
ņäĖĒżņØś ņāØņĪ┤ņŚÉ ļīĆĒĢ£ ĒÜ©Ļ│╝ļź╝ ņĢīņĢäļ│┤ĻĖ░ ņ£äĒĢ┤ ņäĖĒżņØś ņāØņĪ┤Ļ│╝ ĒÖ£ņä▒ļÅä Ļ▓Ćņé¼ļĪ£ ņØ┤ņÜ®ļÉśĻ│Ā ņ׳ļŖö ļ░£ņāēĻ▓Ćņé¼ņØś ņØ╝ņóģņØĖ MTT (3-[4, 5-dimethylthiazol-2-yl]-2, 5-diphenyltetrazolium bromide, Sigma-Aldrich) assayļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż.26,27 Ļ░ü ļåŹļÅäņØś ņĢĮļ¼╝ļĪ£ 30ļČäĻ░ä ņ▓śļ”¼ĒĢ£ ņäĖĒżņØś ļ░░ņ¦ĆņŚÉ MTTļź╝ Ļ░ü wellļŗ╣ 100 ╬╝Lņö® Ēł¼ņŚ¼ĒĢ£ Ēøä 4ņŗ£Ļ░ä ļÅÖņĢł ņĀĢņ╣śļ░░ņ¢æĒĢ£ ļŗżņØī ņŚ╝ļźśņÜ®ņĢĪ(phosphated buffered saline [PBS]; Gibco, Invitrogen, Carlsbad, CA, USA)ņ£╝ļĪ£ ņö╗ņ¢┤ļéĖ Ēøä dimethylsulfoxideļź╝ Ļ░ü well ļŗ╣ 0.5 mLņö® ļäŻņ¢┤ 10ļČä ņØ┤ņāü ĒØöļōĀ ļŗżņØī 96-well ļ░░ņ¢æņĀæņŗ£ņŚÉ 200 ╬╝Lņö® ņś«Ļ▓© ļČäĻ┤æĻ┤æļÅäĻ│ä(FLUOstar OPTIMA, BMG labtech, Ortenberg, Germany)ļĪ£ 570 nmņŚÉņä£ ĒØĪĻ┤æļÅäļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. ņØ┤ļĢī ņäĖĒżņØś ņāØņĪ┤ ņĀĢļÅäļŖö ņŗżĒŚśĻĄ░ņØś Ļ░ÆņØä ņĢĮļ¼╝ņ▓śļ”¼ļź╝ ĒĢśņ¦Ć ņĢŖņØĆ ļīĆņĪ░ĻĄ░ņØś Ļ░Æņ£╝ļĪ£ ļéśļłäņ¢┤ ļ░▒ļČäņ£©ļĪ£ ļéśĒāĆļé┤ņŚłļŗż.
ņä¼ņ£ĀņŻ╝ņäĖĒżņŚÉņä£ ņØ╝ņé░ĒÖöņ¦łņåīņØś ņāØņä▒ņØĆ Griess assayļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļ░░ņ¦ĆņŚÉņä£ņØś nitrite ņāØņä▒ļ¤ēņØä ņĖĪņĀĢĒĢśņśĆļŗż.28 Ļ░üĻ░üņØś ņĢĮļ¼╝ņŚÉ ļģĖņČ£ņŗ£Ēé© ņäĖĒżņØś ļ░░ņ¦ĆņŚÉ ļÅÖļ¤ēņØś Griess ļ░śņØæņĢĪ(Sigma-Aldrich)ļź╝ ņä×ņØĆ Ēøä 96-well plateņŚÉ ņś«Ļ▓© spectrophotometerļĪ£ 540 nmņŚÉņä£ ĒØĪĻ┤æļÅäļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. ņØ┤ļĢī Ēæ£ņżĆņ╣śļź╝ ĻĄ¼ĒĢśĻĖ░ ņ£äĒĢ┤ sodium nitrite (Sigma-Aldrich)ļź╝ ļŗ©Ļ│äņĀüņ£╝ļĪ£ ĒؼņäØĒĢśņŚ¼ ņé¼ņÜ®ĒĢśņśĆļŗż.
ņä¼ņ£ĀņŻ╝ņäĖĒżļź╝ ĒŖĖļ”ĮņŗĀ ņ▓śļ”¼ĒĢ£ Ēøä 12-wellņØś Transwell (Corning, No.3460, Tewksbury, MA, USA)ņØś ļé┤ņĖĪ chamber (insert diameter 12 mm, pore size 0.4 mm)ņŚÉ 2├Ś104 cells/mLņØś ļåŹļÅäļĪ£ Ļ░ü wellņŚÉ Ļ│Āļź┤Ļ▓ī ņäĖĒżļź╝ ļČäņŻ╝ĒĢśņŚ¼ 10% ņÜ░Ēā£ņĢäĒśłņ▓ŁņØä ĒżĒĢ©ĒĢ£ ļ░░ņ¦ĆļĪ£ ļ░░ņ¢æĒĢśņśĆļŗż.29-32 ņŚŁņ£äņāüņ░©Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ ņä¼ņ£ĀņŻ╝ņäĖĒżĻ░Ć ļŗ©ņĖĄņ£╝ļĪ£ ņČ®ļ¦īĒĢśĻ▓ī ņ×Éļ×Ć Ļ▓āņØä ĒÖĢņØĖĒĢ£ Ēøä Ēśłņ▓ŁņŚÉ ĒżĒĢ©ļÉ£ ļŗ©ļ░▒ņ¦ł ļō▒ņØś ņśüĒ¢źņØä ļ░░ņĀ£ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ 1% ņÜ░Ēā£ņĢäĒśłņ▓ŁņØä ĒżĒĢ©ĒĢ£ ļ░░ņ¦ĆļĪ£ ĻĄÉĒÖśĒĢ£ ļŗżņØī Ļ░ü ņĢĮļ¼╝ņŚÉ 30ļČäĻ░ä Ļ░üĻ░ü ļģĖņČ£ņŗ£Ēé© Ēøä Ēł¼Ļ│╝ļÅä Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ļé┤ņĖĪ chamberņŚÉ ņ×ÉļØ╝Ļ│Ā ņ׳ļŖö ņäĖĒżļź╝ PBSļĪ£ 3ĒÜī ņäĖņ▓ÖĒĢ£ ļŗżņØī 50 mM carboxyfluorescein (Sigma-Aldrich)ņŚÉ ļģĖņČ£ņŗ£ņ╝░ļŗż. ļģĖņČ£ 2ņŗ£Ļ░ä Ēøä TranswellņØä ĒåĄĒĢśņŚ¼ ņÖĖņĖĪ chamberļĪ£ Ēł¼Ļ│╝ļÉ£ carboxyfluoresceinņØś ļåŹļÅäļź╝ 532 nmņŚÉņä£ spectrofluorometer (Fluostar Optima, BMG Labtech, Offenburg, Germany)ļĪ£ ņĖĪņĀĢĒĢśņŚ¼ ļ░▒ļČäņ£©ļĪ£ ļéśĒāĆļé┤ņŚłļŗż.
ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅäļź╝ ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ£ ļśÉ ļŗżļźĖ ļ░®ļ▓Ģņ£╝ļĪ£ trans-endothelial electrical resistance (TEER)ļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. ņä¼ņ£ĀņŻ╝ņäĖĒżļź╝ 12 wellņØś Transwell insertņŚÉ Ļ░üĻ░ü 2├Ś104 cells/mL ļåŹļÅäļĪ£ ļČäņŻ╝ĒĢ£ ļŗżņØī ņäĖĒżĻ░Ć ņČ®ļ¦īĒĢśĻ▓ī ļ░░ņ¢æļÉ£ Ļ▓āņØä ĒÖĢņØĖĒĢ£ Ēøä, Ļ░üĻ░üņØś ņĢĮļ¼╝ņŚÉ 30ļČäĻ░ä ļģĖņČ£ņŗ£Ēé© Ēøä epithelial voltohmmeter (EVOM2, World Precision Instruments, Sarasota, FL, USA)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ TEER Ļ░ÆņØä ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░ĻĘĖ Ļ▓░Ļ│╝ļź╝ net value (Ōä” cm2)ļĪ£ ĻĖ░ļĪØĒĢśņśĆļŗż.33,34
30ļČäĻ░ä ņĢĮļ¼╝ņŚÉ ļģĖņČ£ņŗ£Ēé© Ēøä ņäĖĒżņØś ņāØņĪ┤ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ ņŗ£Ē¢ēĒĢ£ MTT assayņŚÉņä£ ņĢĮļ¼╝ņŚÉ ļģĖņČ£ņŗ£Ēéżņ¦Ć ņĢŖņØĆ ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢ┤ LBNĻ│╝ LATļŖö Ļ░üĻ░ü ņäĖĒżņØś ņāØņĪ┤ņŚÉ ņ£ĀņØśĒĢ£ ņśüĒ¢źņØä ļ»Ėņ╣śņ¦Ć ņĢŖņĢśļŗż(all p>0.005) (Fig. 1). ļö░ļØ╝ņä£ ņĢäļלņØś Ēł¼Ļ│╝ļÅä ņŗżĒŚśņØś Ļ▓░Ļ│╝ļŖö ņäĖĒż ņłśņØś ļ│ĆĒÖöņŚÉ ņØśĒĢ£ Ļ▓āņØ┤ ņĢäļŗśņØä ņĢī ņłś ņ׳ņŚłļŗż.
ņĢĮļ¼╝ņŚÉ ļģĖņČ£ņŗ£Ēéżņ¦Ć ņĢŖņØĆ ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢśņŚ¼ 100 ╬╝M LBNņØĆ ļ░░ņ¦ĆņŚÉņä£ņØś nitrite ļåŹļÅäļź╝ ņ£ĀņØśĒĢśĻ▓ī ņ”ØĻ░Ćņŗ£ņ╝░ļŗż(p=0.029) (Fig. 2). 100 ╬╝M LBNņŚÉ L-NAMEļź╝ ĒĢ©Ļ╗ś ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ LBN ļŗ©ļÅģņ£╝ļĪ£ ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ņŚÉ ļ╣äĒĢ┤ nitriteņØś ļåŹļÅäĻ░Ć ņ£ĀņØśĒĢśĻ▓ī Ļ░ÉņåīĒĢśņśĆļŗż(p=0.041). LBNĻ│╝ LATļź╝ 50 ╬╝Mņö® ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ļź╝ ļ╣äĻĄÉĒĢ┤ļ│┤ļ®┤ NO ņāØņä▒ņŚÉņä£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśņ£╝ļéś(p=0.191), LBNĻ│╝ LATļź╝ 100 ╬╝Mņö® ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ļź╝ ļ╣äĻĄÉĒĢ┤ļ│┤ļ®┤ LBNņØ┤ LATņŚÉ ļ╣äĒĢ┤ ņ£ĀņØśĒĢśĻ▓ī nitriteņØś ļåŹļÅäļź╝ ņ”ØĻ░Ćņŗ£ņ╝░ļŗż(p=0.040).
ņĢĮļ¼╝ņŚÉ ļģĖņČ£ņŗ£Ēéżņ¦Ć ņĢŖņØĆ ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢśņŚ¼ 50, 100 ╬╝M LBNņØĆ carboxyfluoresceinņØś ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅäļź╝ 106.1%, 111.4%ļĪ£ Ļ░üĻ░ü ņ£ĀņØśĒĢśĻ▓ī ņ”ØĻ░Ćņŗ£ņ╝░ņ£╝ļéś(p=0.010, 0.001) LATļŖö ņ£ĀņØśĒĢ£ ņśüĒ¢źņØä ļ»Ėņ╣śņ¦Ć ņĢŖņĢśļŗż(Fig. 3). 100 ╬╝M LBNņŚÉ L-NAMEļź╝ ĒĢ©Ļ╗ś ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ 100 ╬╝M LBN ļŗ©ļÅģņ£╝ļĪ£ ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ņŚÉ ļ╣äĒĢ┤ Ēł¼Ļ│╝ļÅäĻ░Ć 7.8% Ļ░ÉņåīĒĢśņśĆļŗż(p=0.001). LBNĻ│╝ LATļź╝ ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ Ēł¼Ļ│╝ļÅäļź╝ ļ╣äĻĄÉĒĢ┤ļ│┤ļ®┤ 50, 100 ╬╝M ļåŹļÅä ļ¬©ļæÉņŚÉņä£ LATņŚÉ ļ╣äĒĢ┤ LBNņØ┤ ņ£ĀņØśĒĢśĻ▓ī Ēł¼Ļ│╝ļÅäļź╝ ņ”ØĻ░Ćņŗ£ņ╝░ļŗż(p=0.018, 0.001).
ņĢĮļ¼╝ņŚÉ ļģĖņČ£ņŗ£Ēéżņ¦Ć ņĢŖņØĆ ļīĆņĪ░ĻĄ░ņØś ņĀĆĒĢŁļÅäļŖö 63.02 Ōä” cm2ņśĆņ£╝ļ®░ ņØ┤ņŚÉ ļ╣äĒĢśņŚ¼ 100 ╬╝M LBNņØä ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ņØś ņĀĆĒĢŁļÅäļŖö 53.01 Ōä” cm2ļĪ£ 15.89% Ļ░ÉņåīĒĢśņśĆļŗż(p=0.047) (Fig. 4). 50 ╬╝M LBNņØä ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ ņĀĆĒĢŁļÅäļŖö 58.48 Ōä” cm2ļĪ£ 7.21% Ļ░ÉņåīĒĢśņśĆņ£╝ļéś ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśņ¦ĆļŖö ņĢŖņĢśņ£╝ļ®░(p=0.235), 50 ļśÉļŖö 100 ╬╝M LATļŖö ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢśņŚ¼ ņĀĆĒĢŁļÅäņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż.
100 ╬╝M LBNņŚÉ L-NAMEļź╝ ĒĢ©Ļ╗ś ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ 100 ╬╝M LBN ļŗ©ļÅģņ£╝ļĪ£ ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ņŚÉ ļ╣äĒĢ┤ ņĀĆĒĢŁļÅäļŖö 10.58% Ļ░ÉņåīĒĢśņśĆņ£╝ļéś ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśņ£╝ļ®░(p=0.162), LBNĻ│╝ LATļź╝ ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░ņØś Ēł¼Ļ│╝ļÅäļź╝ Ļ░üĻ░ü ļ╣äĻĄÉĒĢ┤ļ│┤ļ®┤ 50, 100 ╬╝M ļåŹļÅä ļ¬©ļæÉņŚÉņä£ LATņŚÉ ļ╣äĒĢ┤ LBNņØ┤ ļåŹļÅäĻ░Ć ņ”ØĻ░ĆĒĢĀņłśļĪØ ņĀĆĒĢŁļÅäļź╝ Ļ░Éņåīņŗ£ĒéżļŖö Ļ▓ĮĒ¢źņØä ļéśĒāĆļé┤ņŚłņ£╝ļéś ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśņ¦ĆļŖö ņĢŖņĢśļŗż(p=0.444, 0.073).
ĻĖ░ņĪ┤ņØś ļÅÖļ¼╝ņŗżĒŚśņŚÉņä£ ĒöäļĪ£ņŖżĒāĆĻĖĆļ×ĆļöśņŚÉ NOļź╝ Ļ▓░ĒĢ®ņŗ£Ēé© ņĢĮņĀ£ņØś ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝Ļ░Ć ļ│┤Ļ│ĀļÉ£ ņØ┤Ēøä11,35 ņĄ£ĻĘ╝ Ļ░£ļ░£ļÉ£ LBNņØĆ ĻĖ░ņĪ┤ņØś ļģ╣ļé┤ņן ņĢłņĢĢĒĢśĻ░ĢņĀ£ļōżņŚÉ ļ╣äĒĢ┤ ņÜ░ņłśĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļź╝ ļéśĒāĆļé┤ņŚłļŗżļŖö ņŚ¼ļ¤¼ ņ×äņāü ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļōżņØ┤ ļ│┤Ļ│ĀļÉśņ¢┤ ņÖöļŗż.12-20 ņØ┤ļ¤¼ĒĢ£ LBNņØś ņÜ░ņłśĒĢ£ ĒÜ©Ļ│╝ļŖö ļÅÖļ¼╝ņŗżĒŚśņØä ĒåĄĒĢ┤ņä£ļŖö LATņŚÉ ņØśĒĢ£ ĒżļÅäļ¦ēĻ│Ąļ¦ēņ£ĀņČ£ņØä ņ┤ēņ¦äĒĢśļŖö ņ×æņÜ®Ļ│╝ ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö NOņØś ņØ┤ņżæ ņ×æņÜ®ņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņŚ¼Ļ▓©ņĀĖ ņÖöņ¦Ćļ¦ī,11 LBNņØ┤ ņØĖņ▓┤ ļé┤ņŚÉņä£ ņä¼ņ£ĀņŻ╝ņØś ļ░®ņłśņ£ĀņČ£ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØĆ ņä¼ņ£ĀņŻ╝ņäĖĒżļź╝ ņØ┤ņÜ®ĒĢ£ ņŗżĒŚśņŗż ļé┤ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĢäņ¦ü ņ×ÉņäĖĒ׳ ļ░ØĒśĆņ¦Ćņ¦Ć ņĢŖņĢśļŗż. ņØ┤ņŚÉ ļö░ļØ╝ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ░░ņ¢æĒĢ£ ņØĖņ▓┤ ņä¼ņ£ĀņŻ╝ņäĖĒżļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗżĒŚśņŗż ļé┤ņŚÉņä£ LBNņØ┤ ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä LATņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ ņĢīņĢäļ│┤ņĢśļŗż.
ļ│Ė ņŚ░ĻĄ¼ņØś Ļ▓░Ļ│╝ņŚÉņä£ LBNņØĆ ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅäļź╝ ļåŹļÅäņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ņ”ØĻ░Ćņŗ£ņ╝░ņ£╝ļ®░ ņĀĆĒĢŁļÅäļź╝ Ļ░Éņåīņŗ£ņ╝░ņ£╝ļ»ĆļĪ£ LBNņØ┤ ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö ņ×æņÜ®ņØä ļéśĒāĆļāäņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. ņØ┤ņŚÉ ļ╣äĒĢ┤ LATļŖö Ēł¼Ļ│╝ļÅäņŚÉ ņ£ĀņØśĒĢ£ ņśüĒ¢źņØä ļ»Ėņ╣śņ¦Ć ņĢŖņĢśļŖöļŹ░ ĻĖ░ņĪ┤ņØś ļ¬ćļ¬ć ņŚ░ĻĄ¼ņŚÉņä£ ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖĻ░Ć ņä¼ņ£ĀņŻ╝ņŚÉņä£ ņäĖĒżņÖĖĻĖ░ņ¦łņØä Ļ░Éņåīņŗ£ĒéżĻ▒░ļéś ĻĖ░ņ¦łĻĖłņåŹļŗ©ļ░▒ņ¦łļČäĒĢ┤ĒÜ©ņåīļź╝ ņ”ØĻ░Ćņŗ£ņ╝£ ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņØä ņ┤ēņ¦äņŗ£Ēé©ļŗżļŖö ļ│┤Ļ│ĀļÅä ņ׳ņŚłņ£╝ļéś4,36 ņØ┤ņŚÉ ļīĆĒĢ┤ņä£ļŖö ņĢäņ¦ü ļģ╝ļ×ĆņØś ņŚ¼ņ¦ĆĻ░Ć ļ¦ÄļŗżĻ│Ā ļ│╝ ņłś ņ׳ņ£╝ļ®░ ļ│Ė ņŚ░ĻĄ¼ņØś Ļ▓░Ļ│╝ņŚÉ ļö░ļź┤ļ®┤ LATļŖö ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņŚÉļŖö ņ£ĀņØśĒĢ£ ņśüĒ¢źņØä ļ»Ėņ╣śņ¦Ć ņĢŖņĢśņ£╝ļ»ĆļĪ£ LATĻ░Ć ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØĆ ņĀüņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ļö░ļØ╝ņä£ LBNņØĆ LATņŚÉ ļ╣äĒĢ┤ ņä¼ņ£ĀņŻ╝ļź╝ ĒåĄĒĢ£ ļ░®ņłśņ£ĀņČ£ņØś ņ”ØĻ░Ćļź╝ ņČöĻ░ĆņĀüņ£╝ļĪ£ ļéśĒāĆļé╝ ņłś ņ׳ņ£╝ļ»ĆļĪ£ ņĪ░ĻĖł ļŹö ņÜ░ņłśĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļź╝ ļéśĒāĆļé╝ Ļ▓āņ£╝ļĪ£ ņŚ¼Ļ▓©ņ¦äļŗż.
ņØ┤ļ¤¼ĒĢ£ LBNņØś ņČöĻ░ĆņĀüņØĖ ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļŖö ņä¼ņ£ĀņŻ╝ņŚÉ ņ×æņÜ®ĒĢśļŖö NOņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņŚ¼Ļ▓©ņ¦Ćļ®░37 ļ│Ė ņŚ░ĻĄ¼ņä£ļÅä LBNņØ┤ NOņØś ņāØņä▒ņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż. NOļŖö cGMPļź╝ ĒåĄĒĢśņŚ¼ ņ×æņÜ®ņØä ļéśĒāĆļé┤ļŖöļŹ░21-23 ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ cGMP ņĀ£ĒĢ┤ņĀ£ļĪ£ ņ×æņÜ®ĒĢśļŖö L-NAMEļź╝38,39 ĒĢ©Ļ╗ś ļģĖņČ£ņŗ£Ēé© Ļ▓░Ļ│╝ LBNņŚÉ ņØśĒĢ£ ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØś Ēł¼Ļ│╝ļÅä ņ”ØĻ░ĆņÖĆ ņĀĆĒĢŁļÅä Ļ░ÉņåīĻ░Ć ņāüņćäļÉśņŚłļŗż. ļö░ļØ╝ņä£ LBNņØĆ ņä¼ņ£ĀņŻ╝ņŚÉņä£ NOņØś ņāØņä▒ņØä ņ”ØĻ░Ćņŗ£ņ╝£ cGMPļź╝ ĒåĄĒĢ┤ ņä¼ņ£ĀņŻ╝ļź╝ ņØ┤ņÖäņŗ£ņ╝£ ļ░®ņłśņ£ĀņČ£ņØä ņ┤ēņ¦äņŗ£ĒéżļŖö ņ×æņÜ®ņØä ļéśĒāĆļéĖļŗżĻ│Ā ļ│╝ ņłś ņ׳Ļ▓Āļŗż.
ļ╣äļĪØ ļ│Ė ņŚ░ĻĄ¼Ļ░Ć ņŗżĒŚśņŗż ļé┤ņŚÉņä£ ņä¼ņ£ĀņŻ╝ļŗ©ņĖĄņäĖĒżņĖĄņØä ņØ┤ņÜ®ĒĢ£ Ēł¼Ļ│╝ļÅäļź╝ ļ╣äĻĄÉ ņŚ░ĻĄ¼ĒĢ£ Ļ▓░Ļ│╝ņØ┤ĻĖ░ļŖö ĒĢśņ¦Ćļ¦ī ņä¼ņ£ĀņŻ╝ņäĖĒżļź╝ ņØ┤ņÜ®ĒĢ£ ņØ┤ņĀäņØś ņŗżĒŚśņŗż ļé┤ ņŚ░ĻĄ¼ņŚÉņä£ LBNņØ┤ LATņŚÉ ļ╣äĒĢ┤ ņ£ĀņØśĒĢśĻ▓ī ņä¼ņ£ĀņŻ╝ļź╝ ņØ┤ņÖäņŗ£ņ╝░ļŗżļŖö Ļ▓░Ļ│╝ļź╝24 ĒĢ©Ļ╗ś Ļ│ĀļĀżĒĢ┤ļ│┤ļ®┤ LBNņØĆ ĒżļÅäļ¦ēĻ│Ąļ¦ēņ£ĀņČ£Ļ│╝ ņä¼ņ£ĀņŻ╝ņ£ĀņČ£ņØä ĒĢ©Ļ╗ś ņ┤ēņ¦äĒĢśļŖö ņØ┤ņżæ ņ×æņÜ®ņØä ļéśĒāĆļé┤ļ®░, ņØ┤ņŚÉ ļö░ļØ╝ ĻĖ░ņĪ┤ņØś ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖ ņĀ£ņ×¼ļ│┤ļŗż ņ×äņāüņĀüņ£╝ļĪ£ ņÜ░ņłśĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļź╝ ļéśĒāĆļéĖļŗżļŖö ņØ┤ņĀä ņ×äņāü ņŚ░ĻĄ¼ļōżņØś Ļ▓░Ļ│╝ļōżņØä ļÆĘļ░øņ╣©ĒĢ£ļŗż.
ļśÉĒĢ£ NOļŖö ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļ┐Éļ¦ī ņĢäļŗłļØ╝ ņé░ĒÖöņŖżĒŖĖļĀłņŖżļź╝ Ļ░Éņåīņŗ£Ēéżļ®░ ņŗ£ņŗĀĻ▓ĮĒśłļźśļź╝ ņ”ØĻ░Ćņŗ£ņ╝£ ņŗĀĻ▓Įļ│┤ĒśĖ ĒÜ©Ļ│╝ļź╝ ļéśĒāĆļéĖļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŖöļŹ░,40 ņØ┤ņŚÉ ļīĆĒĢ£ LBNņØś ņ×æņÜ®ņŚÉ Ļ┤ĆĒĢ┤ņä£ļŖö Ē¢źĒøä ļŹö ņ×ÉņäĖĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢĀ Ļ▓āņØ┤ļŗż.
Ļ▓░ļĪĀņĀüņ£╝ļĪ£ ņä¼ņ£ĀņŻ╝ņäĖĒżņŚÉņä£ LBNņØĆ ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖņŚÉ ņØśĒĢ£ ĒżļÅäļ¦ēĻ│Ąļ¦ēņ£ĀņČ£ ņ”ØĻ░ĆņÖĆ ļŹöļČłņ¢┤ NOņŚÉ ņØśĒĢ£ ņä¼ņ£ĀņŻ╝ņ£ĀņČ£ņØä ĒĢ©Ļ╗ś ņ”ØĻ░Ćņŗ£Ēé┤ņ£╝ļĪ£ņŹ© ĻĖ░ņĪ┤ņØś ļØ╝ĒāĆļģĖĒöäļĪ£ņŖżĒŖĖ ņĀ£ņĀ£ļ│┤ļŗż ņĪ░ĻĖł ļŹö ņÜ░ņłśĒĢ£ ņĢłņĢĢĒĢśĻ░Ģ ņ×æņÜ®ņØä ļéśĒāĆļé╝ ņłś ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
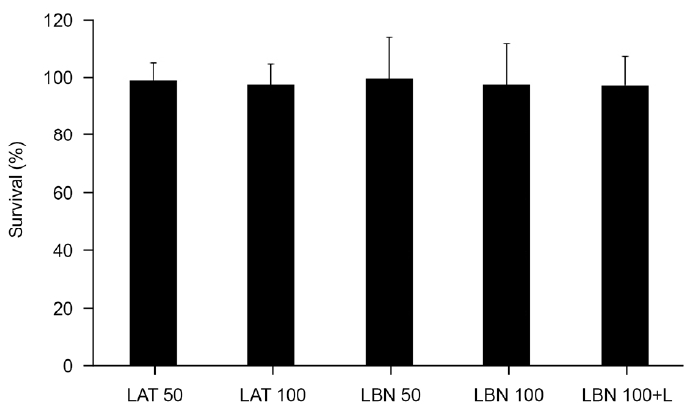
Figure┬Ā1.
Effects of latanoprostene bunod (LBN) or latanoprost free acid (LAT) on the survival of trabecular meshwork cells. Either exposure to 50 or 100 ╬╝M LBN or LAT did not affect cellular survival significantly (all p > 0.05). With co-exposure to L-NAME (L) with 100 ╬╝M LBN also did not affect cellular survival significantly compared to non-exposed control (all p > 0.05).
Figure┬Ā2.
Effects of latanoprostene bunod (LBN) or latanoprost free acid (LAT) on the production of nitric oxide (NO) in trabecular meshwork cells. Exposure to 100 ╬╝M LBN increased NO production significantly compared to non-exposed control (*p = 0.029). Co-exposure to L-NAME (L) and 100 ╬╝M LBN decreased NO production significantly compared to exposure to LBN alone (ŌĆĀp = 0.041).

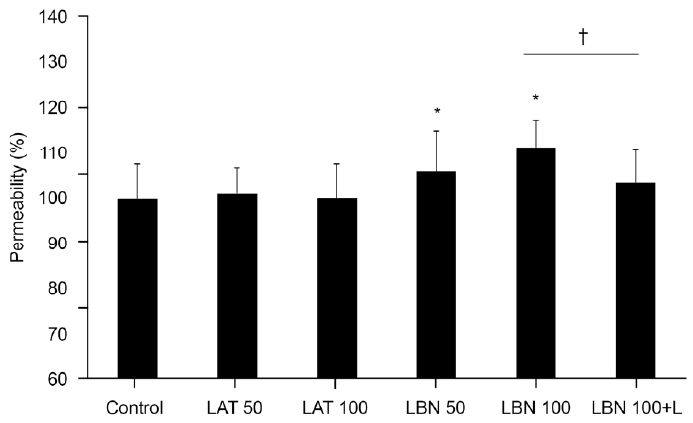
Figure┬Ā3.
Effects of latanoprostene bunod (LBN) or latanoprost free acid (LAT) on the permeability of carboxyfluorescein through the trabecular meshwork cell monolayer. Exposure to 50 or 100 ╬╝M LBN showed an increased permeability of carboxyfluorescein significantly compared with non-exposed controls (*p = 0.010, 0.001). Co-exposure to L-NAME (L) with 100 ╬╝M LBN decreased permeability significantly compared to exposure to 100 ╬╝M LBN alone (ŌĆĀp = 0.001). Carboxyfluorescein intensity of outer chamber normalized to the mean value obtained using non-exposed control (permeability 100%).
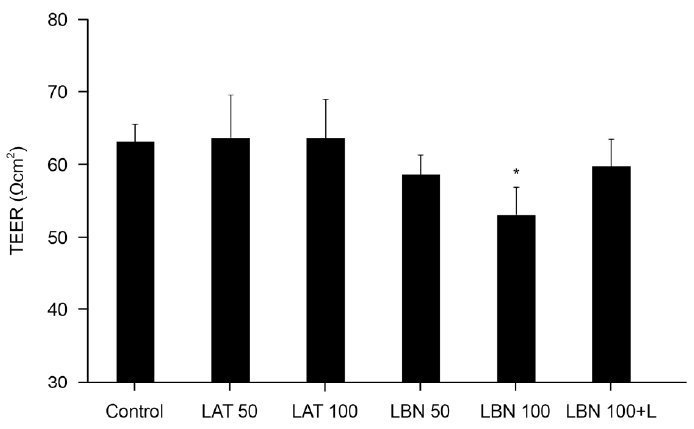
Figure┬Ā4.
Effects of latanoprostene bunod (LBN) or latanoprost free acid (LAT) on the trans-endothelial electrical resistance (TEER) of the trabecular meshwork cell monolayer. Exposure to 100 ╬╝M LBN decreased TEER significantly compared with non-exposed controls (p = 0.047). Compared to exposure to 100 ╬╝M LBN alone, co-exposure to L-NAME (L) with 100 ╬╝M LBN increased TEER but statistically not significant (*p = 0.162). (Data presented as mean ┬▒ standard error of mean).
REFERENCES
1) Alvarado J, Murphy C, Juster R. Trabecular meshwork cellularity in primary open-angle glaucoma and nonglaucomatous normals. Ophthalmology 1984;91:564-79.


2) Rohen JW, L├╝tjen-Drecoll E, Fl├╝gel C, et al. Ultrastructure of the trabecular meshwork in untreated cases of primary open-angle glaucoma. Exp Eye Res 1993;56:683-92.

3) Toris CB, Gabelt BT, Kaufman PL. Update on the mechanism of action of topical prostaglandins for intraocular pressure reduction. Surv Ophthalmol 2008;53 Suppl 1:S107-20.

4) Winkler NS, Fautsch MP. Effects of prostaglandin analogues on aqueous humor outflow pathways. J Ocul Pharmacol Ther 2014;30:102-9.



5) Wu X, Yang X, Liang Q, et al. Drugs for the treatment of glaucoma: targets, structure-activity relationships and clinical research. Eur J Med Chem 2021;226:113842.


6) Nathanson JA. Nitrovasodilators as a new class of ocular hypotensive agents. J Pharmacol Exp Ther 1992;260:956-65.

7) Aliancy J, Stamer WD, Wirostko B. A review of nitric oxide for the treatment of glaucomatous disease. Ophthalmol Ther 2017;6:221-32.



8) Cavet ME, Vittitow JL, Impagnatiello F, et al. Nitric oxide (NO): an emerging target for the treatment of glaucoma. Invest Ophthalmol Vis Sci 2014;55:5005-15.


9) Mao YJ, Wu JB, Yang ZQ, et al. Nitric oxide donating anti-glaucoma drugs: advances and prospects. Chin J Nat Med 2020;18:275-83.


10) Reina-Torres E, De Ieso ML, Pasquale LR, et al. The vital role for nitric oxide in intraocular pressure homeostasis. Prog Retin Eye Res 2021;83:100922.


11) Krauss AH, Impagnatiello F, Toris CB, et al. Ocular hypotensive activity of BOL-303259-X, a nitric oxide donating prostaglandin F2alpha agonist, in preclinical models. Exp Eye Res 2011;93:250-5.

12) Weinreb RN, Ong T, Scassellati Sforzolini B, et al. A randomised, controlled comparison of latanoprostene bunod and latanoprost 0.005% in the treatment of ocular hypertension and open angle glaucoma: the VOYAGER study. Br J Ophthalmol 2014;99:738-45.


13) Medeiros FA, Martin KR, Peace J, et al. Comparison of latanoprostene bunod 0.024% and timolol maleate 0.5% in open-angle glaucoma or ocular hypertension: the LUNAR study. Am J Ophthalmol 2016;168:250-9.


14) Weinreb RN, Scassellati Sforzolini B, Vittitow J, Liebmann J. Latanoprostene bunod 0.024% versus timolol maleate 0.5% in subjects with open-angle glaucoma or ocular hypertension. The APOLLO study. Ophthalmology 2016;123:965-73.


15) Kazuhide K, Vittitow JL, Weinreb RN, Araie M. Long-term safety and efficacy of latanoprostene bunod 0.024% in japanese subjects with open-angle glaucoma or ocular hypertension: the JUPITER study. Adv Ther 2016;33:1612-27.



16) Weinreb RN, Realini T, Varma R. Latanoprostene bunod, a dual-acting nitric oxide donating prostaglandin analog for lowering of intraocular pressure. US Ophthalmic Rev 2016;9:80-7.

17) Kaufman PL. Latanoprostene bunod ophthalmic solution 0.024% for IOP lowering in glaucoma and ocular hypertension. Expert Opin Pharmacother 2017;18:433-44.


18) Fingeret M, Gaddie IB, Bloomenstein M. Latanoprostene bunod ophthalmic solution 0.024%: a new treatment option for openŌĆÉangle glaucoma and ocular hypertension. Clin Exp Optom 2019;102:541-50.



19) Harasymowycz P, Royer C, Cui AX, et al. Short-term efficacy of latanoprostene bunod for the treatment of open-angle glaucoma and ocular hypertension: a systematic literature review and a network meta-analysis. Br J Ophthalmol 2022;106:640-7.


20) Radell JE, Sharma HK, Auyeung KL, et al. Two-year experience with latanoprostene bunod in clinical practice. J Glaucoma 2021;30:776-80.


21) Denninger JW, Marletta MA. Guanylate cyclase and the .NO/cGMP signaling pathway. Biochim Biophys Acta 1999;1411:334-50.


22) Kotikoski H, Alajuuma P, Moilanen E, et al. Comparison of nitric oxide donors in lowering intraocular pressure in rabbits: role of cyclic GMP. J Ocul Pharmacol Ther 2002;18:11-23.


23) Ellis DZ, Dismuke WM, Chokshi BM. Characterization of soluble guanylate cyclase in NO-induced increases in aqueous humor outflow facility and in the trabecular meshwork. Invest Ophthalmol Vis Sci 2009;50:1808-13.


24) Cavet ME, Vollmer TR, Harrington KL, et al. Regulation of endothelin-1-induced trabecular meshwork cell contractility by latanoprostene bunod. Invest Ophthalmol Vis Sci 2015;56:4108-16.


25) Cavet ME, DeCory HH. The role of nitric oxide in the intraocular pressure lowering efficacy of latanoprostene bunod: review of nonclinical studies. J Ocul Pharmacol Ther 2018;34:52-60.



26) Mosmann T. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. J Immunol Methods 1983;65:55-63.


27) Fremoser FM, Jakob CA, Aebi M, Tuor U. The MTT assay is a fast and reliable method for colorimetric determination of fungal cell densities. Appl Environ Microbiol 1999;65:3727-9.



28) Wagner DA, Glogowski J, et al. Analysis of nitrate, nitrite and [15N]nitrate in biologic fluids. Anal Biochem 1982;126:131-8.

29) Araie M. Carboxyfluorescein. A dye for evaluating the corneal endothelial barrier function in vivo. Exp Eye Res 1986;42:141-50.


30) Tsuboi S, Pederson JE. Permeability of the isolated dog retinal pigment epithelium to carboxyfluorescein. Invest Ophthalmol Vis Sci 1986;27:1767-70.

31) Blair NP, Rusin MM. Blood-retinal barrier permeability to carboxyfluorescein and fluorescein in monkeys. Graefes Arch Clin Exp Ophthalmol 1986;224:419-22.


32) Grimes PA. Carboxyfluorescein transfer across the blood retinal barrier evaluated by quantitative fluorescence microscopy: comparison with fluorescein. Exp Eye Res 1988;46:769-83.


33) Rao PV, Deng PF, Kumar J, Epstein DL. Modulation of aqueous humor outflow facility by the Rho kinase specific inhibitor Y-27632. Invest Ophthalmol Vis Sci 2001;42:1029-37.

34) Alvarado JA, Betanzos A, Franse-Carman L, et al. Endothelia of SchlemmŌĆÖs canal and trabecular meshwork: distinct molecular, functional, and anatomic features. Am J Physiol Cell Physiol 2004;286:C621-34.


35) Krauss AH, Impagnatiello F, Toris CB, et al. Ocular hypotensive activity of BOL-303259-X, a nitric oxide donating prostaglandin F2alpha agonist, in preclinical models. Exp Eye Res 2011;93:250-5.

36) Bahler CK, Howell KG, Hann CR, et al. Prostaglandins increase trabecular meshwork outflow facility in cultured human anterior segments. Am J Ophthalmol 2008;145:114-9.


37) Becquet F, Courtois Y, Goureau O. Nitric oxide in the eye: multifaceted roles and diverse outcomes. Surv Ophthalmol 1997;42:71-82.


38) Rees DD, Palmer RMJ, Schulz R, et al. Characterization of three inhibitors of endothelial nitric oxide synthase in vitro and in vivo. Br J Pharmacol 1990;101:746-52.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




