 |
 |
| J Korean Ophthalmol Soc > Volume 61(11); 2020 > Article |
|
국문초록
대상과 방법
유리체내 베바시주맙 주사 후에도 지속되는 당뇨황반부종에 1일 2회 0.1% 브롬페낙 점안액 치료를 받은 14명(14안)의 의무기록을 후향적으로 분석하였다. 브롬페낙 치료 전, 치료 후 1개월, 2개월, 3개월의 중심황반두께와 최대교정시력의 변화를 관찰하였다. 각막독성 등의 이상 반응 발생 여부도 확인하였다.
결과
브롬페낙 치료 전 평균 logarithm of the minimum angle of resolution (logMAR) 시력은 0.40 ± 0.29였고, 중심황반두께는 337.0 ± 97.3 μm였다. 브롬페낙 치료 후 평균 시력은 1개월 0.39 ± 0.29, 2개월 0.38 ± 0.24, 3개월 0.34 ± 0.21로 통계적으로 유의한 호전을 보이지는 않았다(p=0.93, p=0.62, p=0.36). 평균 중심황반두께는 치료 후 1개월 331.4 ± 67.9 μm, 2개월 311.7 ± 89.1 μm, 3개월 282.9 ± 76.7 μm로 브롬페낙 치료 후 3개월째에 통계적으로 유의한 호전을 보였다(p=0.47, p=0.08, p=0.04). 연구 기간 동안 브롬페낙 점안액으로 인해 부작용을 호소하거나 약제 사용을 중단한 사례는 없었다.
ABSTRACT
Purpose
The short-term outcomes of patients with diabetic macular edema (DME) treated with 0.1% Bromfenac eyedrops were evaluated.
Methods
We included 14 eyes of 14 patients diagnosed with persistent macular edema after intravitreal bevacizumab injection to treat DME. Bromfenac sodium hydrate 0.9 mg/mL eyedrops were administered to the affected eye twice daily for 3 months. The best corrected visual acuity (BVCA) and central macular thickness (CMT) were measured before treatment and at 1, 2, and 3 months after treatment. We noted no adverse drug reaction such as corneal toxicity.
Results
After 2 months of intravitreal bevacizumab and before Bromfenac eyedrops treatment, the logarithm of the minimal angle of resolution (logMAR) BCVA and the CMT were 0.40 ± 0.29 and 337 ± 97.3 μm, respectively. The logMAR BCVA decreased from 0.40 ± 0.29 to 0.39 ± 0.29 after 1 month, to 0.38 ± 0.24 after 2 months, and to 0.34 ± 0.21 after 3 months of Bromfenac treatment, but statistical significance was not attained (p = 0.93, p = 0.62, and p = 0.36 respectively). The CMT improved significantly from 337 ± 97.3 μm to 331 ± 67.9 μm after 1 month, 311 ± 89.1 μm after 2 months, and 282.9 ± 76.7 μm after 3 months (p = 0.47, p = 0.08, and p = 0.04, respectively). Treatment was well-tolerated; we noted no topical or systemic side-effect.
당뇨병의 합병증 중에서 당뇨망막병증은 시력손상을 유발하는 주요한 원인이다. 특히 당뇨황반부종은 중심시력손상의 직접적인 원인이 되며, 치료하지 않을 경우 영구적인 시력저하의 위험이 크며 장기간 치료를 필요로 한다[1,2]. 당뇨황반부종의 치료로는 황반 국소레이저 치료, 스테로이드 국소주사 및 항혈관내피성장인자 유리체내주사, 유리체절제술 등이 있으나, 다음과 같은 문제점들이 동반될 수 있다: 1) 황반 국소레이저 치료는 그 적용 범위가 제한적이며 레이저 치료 반흔이 커짐에 따라 황반하섬유화 및 맥락막 신생혈관과 같은 부작용 위험이 있다[3,4]; 2) 유리체내주사는 빠르고 효과적으로 당뇨황반부종을 치료할 수 있지만, 반복적인 유리체내주사로 인해 안내염, 안압상승 및 백내장, 망막박리와 같은 합병증이 발생할 수 있다[5]. 따라서 당뇨황반부종 치료를 위한 비침습적이며, 부작용의 위험이 적은 치료법에 대한 연구가 지속되고 있다.
당뇨황반부종의 발병 기전은 명확히 밝혀지지 않았지만, 망막허혈로 인해 이차적으로 생성되는 혈관내피성장인자(vascular endothelial growth factor, VEGF)가 망막혈관 누출과 황반부종을 일으키는 것으로 알려져 있다. 또한 당뇨황반부종 환자에서 안구내 염증 지표(inflammatory markers)도 상승되어 있어, 염증 반응도 황반부종 발생에 관여하는 것으로 생각된다[6,7]. 비스테로이드 항염증제(non-steroidal anti-inflammatory drugs, NSAIDs) 점안액은 cyclooxygenase를 억제하여 prostaglandin의 합성을 막음으로써 염증 반응을 저해하는 효과를 나타내는데[8], 안염증, 백내장수술 후 낭포황반부종의 치료에 사용되며, 굴절교정수술 후 통증 및 눈부심을 줄이고, 알레르기결막염에서 가려움증을 줄이는 데에 효과가 있다[9,10]. 이러한 NSAID는 항염증 효과로 인해 당뇨황반부종의 치료에도 활용될 수 있을 것으로 생각되는데, 실제로 NSAID 점안액은 망막분지정맥폐쇄에 발생한 황반부종이나, 나이관련황반변성 등 다양한 망막 질환의 치료에 시도되고 있다[11-13]. 이에 저자들은 유리체내 베바시주맙 주사 치료 후에도 지속되는 황반부종 환자들을 대상으로 0.1% 브롬페낙(bromfenac) 점안액 치료의 효과를 알아보고자 하였다.
2016년 2월부터 2018년 12월까지 본원에서 당뇨황반부종으로 진단받은 환자들의 의무기록을 후향적으로 분석하였다. 본 연구는 임상연구윤리 심의위원회(Institutional Review Board [IRB] 승인 번호: PC20RASI0076) 승인을 통해 진행되었으며, 헬싱키선언(Declaration of Helsinki)을 준수하였다.
당뇨황반부종 진단 후 반복적인 유리체내 베바시주맙 주사를 통해 치료 전과 비교하여 시력과 황반부종이 호전되었지만, 중심황반두께가 250 μm 이상, 350 μm 이하로 황반부종이 지속되는 환자 중 추가적인 치료를 거부한 환자들을 대상으로 연구가 이루어졌다. 환자들은 마지막 유리체내 베바시주맙 주사 후 최소 2개월이 경과하였으며, 0.1% bromfenac sodium hydrate (Bronuck® Ophthalmic Solution; Taejoon Pharm., Seoul, Korea)을 하루에 2회 지속적으로 점안하였다. 망막분지정맥폐쇄, 망막중심정맥폐쇄, 포도막염과 같은 황반부종을 일으킬 수 있는 다른 안질환이나 각막혼탁, 심한 백내장, 유리체출혈 등의 매체 혼탁, 녹내장, 망막전막이 있는 경우, 최근 2개월 이내 다른 치료를 받은 경우, 최근 1년 이내 백내장수술 이력이나, 망막수술을 받은 과거력이 있는 경우는 연구 대상에서 제외되었다.
모든 환자에서 병력 문진과 함께 안과적 검사를 시행하였다. 1개월 간격으로 최소 3개월 이상 관찰하였으며, 방문시마다 최대교정시력(best-corrected visual acuity, BCVA) 측정, 세극등현미경검사, 정밀안저검사, 스펙트럼영역 빛간섭단층촬영(spectral domain optical coherence tomography [SD-OCT]; Spectralis OCTTM; Heidelberg Engineering, Heidelberg, Germany)을 시행하였다. 중심망막두께의 측정은 SD-OCT 기계 내에 내장된 프로그램을 사용하여 측정하였다. 최대교정시력은 스넬렌 차트를 이용하여 측정한 후, 통계학적 분석을 위하여 logarithm of the minimal angle of resolution (logMAR)으로 변환하였다.
브롬페낙 점안액 치료 전후의 비교는 Wilcoxon signed-rank test를 이용하였으며, 통계 분석은 IBM SPSS ver. 21.0(IBM Corp., Armonk, NY, USA)을 이용하였다. p값이 0.05 미만인 경우에 통계적으로 유의하다고 판단하였다.
총 14명(14안)의 환자들이 연구에 포함되었으며, 이 중 남자는 8명, 여자는 6명이었다. 평균 나이는 61.5 ± 9.1 (33-76)세였고, 당뇨병의 유병 기간은 평균 13 ± 7.2년이었다(Table 1). 유리체내 베바시주맙 주사 전 평균 최대교정시력은 logMAR 0.50 ± 0.39, 평균 중심황반두께는 413.6 ± 108.7 μm였으며, 유리체내 주사는 평균 2.86 ± 0.93회 시행 받았다(Table 1). 마지막 유리체내 베바시주맙 주사 후 2개월째 최대교정시력은 0.40 ± 0.29였고, 중심황반두께는 337.0 ± 97.3 μm였다. 평균 최대교정시력은 브롬페낙 점안액 치료 후 1개월 0.39 ± 0.29, 2개월 0.38 ± 0.24, 3개월 0.34 ± 0.21이었으며, 치료 전과 비교하여 통계적으로 유의한 호전을 보이지는 않았다(p=0.93, p=0.62, p=0.36) (Table 2). 브롬페낙 점안액 치료 3개월 후 시력이 1줄 이상 호전된 경우는 3안(21.4%), 2줄 이상 호전은 2안(14.2%)이었으며, 8안(57.1%)에서 변화가 없었고 시력이 악화된 경우는 1안(7.1%)이었다.
중심황반두께는 브롬페낙 점안액 치료 후 점진적으로 감소하는 양상을 보였다. 평균 중심황반두께는 치료 전 337.0 ± 97.3 μm였으며, 치료 후 1개월(331.4 ± 67.9 μm)과 2개월(311.7 ± 89.1 μm)에는 치료 전과 비교하여 통계적으로 유의한 호전을 보이지 않았으나, 3개월째에는 282.9 ± 76.7 μm로 치료 전보다 통계적으로 유의하게 감소하였다(p=0.04) (Table 2). 브롬페낙 치료 후 3개월째에 6안(42.8%)에서 황반부종이 완전히 호전되었고(Fig. 1), 5안(35.7%)에서 부분적 호전, 3안(21.4%)에서 변화가 없었다. 관찰 기간 동안 황반부종이 악화된 경우는 없었다. NSAID 점안액의 부작용으로 일시적 따가움, 작열감, 결막충혈, 독성 각막병증 및 각막융해가 보고된 바 있지만[14], 본 연구 기간 동안 부작용을 호소하거나 이로 인해 약제 사용을 중단한 사례는 없었다.
당뇨황반부종은 형태에 따라 국소황반부종(focal macular edema), 확산황반부종(diffuse macular edema), 낭포황반부종(cystoid macular edema)으로 분류되지만, 임상적으로 부종 형태는 명확하게 구분되지 않고 혼재되어 있는 경우가 많다. 그중에 낭포황반부종은 염증 반응으로 인해 혈액망막장벽이 손상되고 모세혈관 누출이 발생하여 세포외액이 축적되고 이로 인해 망막부종이 발생하는 형태이다[15]. 염증반응으로 인해 증가된 prostaglandin이 혈관의 확장과 혈액망막장벽의 손상에 따른 혈관 투과성 증가를 유도하여 부종을 유발한다[16].
NSAID는 강력한 cyclooxygenase 저해제로서 prostaglandin의 생성을 억제하여 염증 반응을 감소시키는데, 실제로 당뇨황반부종 환자에게 경구 NSAID를 투여한 후 형광안저혈관조영에서 누출 감소가 확인된 초기 임상 연구가 있고[17], 당뇨황반부종의 동물 모델 연구에서도 NSAID를 사용하여 황반부종이 개선된 결과가 보고된 바도 있다[18]. 또한 Kern et al [19]의 연구에서 NSAID 점안액 치료가 당뇨에 의한 생화학적인 변화, 망막의 prostaglandin E2 (PGE2), cyclooxygenase-2 (COX2) 및 과산화물 생산을 현저하게 감소시킨다는 것이 밝혀졌다. 이 외에도 백혈구정체, 망막 모세혈관 변성, 내피세포 사멸과 같은 세포 및 형태적 변화가 NSAID 점안액에 의해 억제되는 결과를 보였다.
최근 Shimura and Yasuda [11]은 망막분지정맥폐쇄로 인해 발생한 황반부종에서 유리체내 베바시주맙 주사 후 브롬페낙 점안액 치료의 효과에 대해 연구하였다. 저자들은 망막분지정맥폐쇄에 동반된 황반부종에서 유리체내 베바시주맙 주사 후 브롬페낙 점안액 치료가 시력예후에는 영향을 미치지 않았지만, 유리체내 주사의 횟수를 줄일 수 있었다고 발표하였다. 망막분지정맥폐쇄에 동반된 황반부종과 당뇨황반부종의 발생에 염증의 핵심적인 역할을 고려할 때, 본 연구에서도 당뇨황반부종의 치료에 브롬페낙 점안액의 의미 있는 결과를 확인할 수 있었다. 환자들은 브롬페낙을 점안한 후 중심황반두께가 1달째 5.6 μm, 2달째 25.3 μm, 3달째 54.1 μm 감소하였고, 황반부종이 완전히 회복되기도하였다. 중심황반두께 50 μm 이상 감소는 임상적으로 의미가 있으며, 시기능 유지에 도움이 될 것으로 판단할 수 있는데[20], 브롬페낙 점안액 치료 3개월 후 중심황반두께가 54.1 μm 감소된 결과는 브롬페낙 점안액의 임상적 효용성이 있음을 보여주었다.
본 연구에서 브롬페낙 점안액 치료 후 3개월째 중심황반두께가 유의하게 감소한 반면, 최대교정시력은 관찰 기간동안 유의한 호전을 보이지 않았다. 황반부종의 평가에 유용한 장비인 빛간섭단층촬영을 이용한 중심황반두께와 시력과의 상관관계에 관한 다양한 연구들을 보면, 중심황반두께와 시력 사이의 일부 상관관계를 보고한 연구도 있지만[21], 둘 사이에 유의한 상관관계를 관찰할 수 없었던 연구들도 있다[22]. 이로 미루어 보아 중심황반두께의 감소가 반드시 시력호전으로 이어지는 것은 아닌 것을 알 수 있으며, 중심황반두께 이외에 유리체내 주사 치료 후 시력예후와 관련된 인자로 망막기능을 보는 지표인 retinal sensitivity의 감소와 시세포층의 내절/외절층 경계의 구조적인 손상 등에 의한 영향이 있을 것으로 생각된다[23,24]. 본 연구에서 브롬페낙 점안 후 3개월째에 중심황반두께가 감소되어 해부학적으로 호전을 보였지만, 기능적인 호전이 없었던 것은 망막허혈에 의한 시세포층과 바깥경계막의 구조적인 손상때문일 수 있으며, 이로 인해 황반부종이 호전되어도 시력의 개선이 동반되지 않은 것으로 생각된다[25]. 따라서 당뇨황반부종에서 망막허혈에 의한 세포의 손상을 최소화하고, 시력예후를 향상시키기 위해서는 초기에 적극적인 황반부종의 치료가 필요하겠다.
현재 브롬페낙, 디클로페낙, 플루르비프로펜, 케토롤락 그리고 네파페낙 등 여러 NSAID가 점안액으로 사용되고 있다. 브롬페낙 점안액은 비교적 최신 NSAID 점안액으로 유리체내 침투력이 강화되어 나이관련황반변성, 당뇨황반부종 등 망막질환 치료에 도움이 될 것으로 기대된다[11,16,26]. NSAID 점안액은 스테로이드 점안액과 비교하여 안압상승, 상처 치유 지연, 각막감염 및 천공, 백내장 발생의 위험성이 적은 비교적 안전한 약제이다. 실제로 나이관련황반변성 환자에서 유리체내 항혈관내피세포성장인자 주사 치료와 이 약제를 병행 시 COX2에 선택적으로 작용하여 항염증 효과를 보이며 이로 인해 황반부종을 감소시키게 되어 부가적인 치료로 사용될 수 있음을 보여주는 여러 연구가 있었다[11,27,28]. NSAID 점안액 사용 시 부작용으로 일시적 자극감, 작열감, 결막충혈, 독성 각막병증 및 각막 융해가 보고된 바 있지만[14], 본 연구 기간 동안 브롬페낙 치료와 관련된 전신적 또는 국소적 부작용은 관찰되지 않았다.
브롬페낙 점안액을 이용한 당뇨황반부종의 치료에 대한 연구가 아직 국내에서는 이루어진 바가 없다. 하지만, 본 연구는 최소 2개월 전 유리체내 베바시주맙 주사를 시행받은 환자군을 대상으로 하여 연구 기간 중 황반부종의 호전이 오직 브롬페낙 점안액의 효과로 단정하기 힘든 한계점이 있고, 평균 치료 기간이 5.0 ± 1.6개월(3-8개월)로 비교적 짧았다. 브롬페낙 치료 후 평균 중심황반두께가 점진적인 호전을 보여 3개월째 통계적으로 유의한 결과를 보였지만, 안약 점안을 중단했을 때 황반부종의 재발 여부 등을 포함해 조금 더 장기간 연구를 통해 효과를 평가하는 것이 필요할 것으로 생각한다. 이런 한계점에도 불구하고 브롬페낙 점안액이 당뇨황반부종에서 중심황반두께를 유의하게 감소시킨 것은 임상적으로 의미있는 소견이다.
요약하면 본 연구는 브롬페낙 점안액이 유리체내 베바시주맙 주사 후에도 지속되는 당뇨황반부종의 치료에 효과가 있음을 보여주는 후향적 연구이다. 추후 전향적 연구를 통해 더 많은 환자를 대상으로 충분한 기간의 관찰을 통해 브롬페낙 점안액의 치료 효과에 대해 확인이 필요하고, 낭포 황반부종 외에도 국소 및 확산황반부종에서의 치료 효과, 그리고 유리체내 항혈관내피성장인자 및 스테로이드 주사 치료와의 병합 치료 효과에 대해서도 후속 연구가 필요할 것으로 생각된다.
Figure 1.
Optical coherence tomography images of a 62-year-old male with non-proliferative diabetic retinopathy in both eyes and diabetic macular edema (DME) in the left eye. (A) Before treatment, (B) persistent DME even after bevacizumab treatment, and (C) three months after treatment with topical 0.1% bromfenac solution.
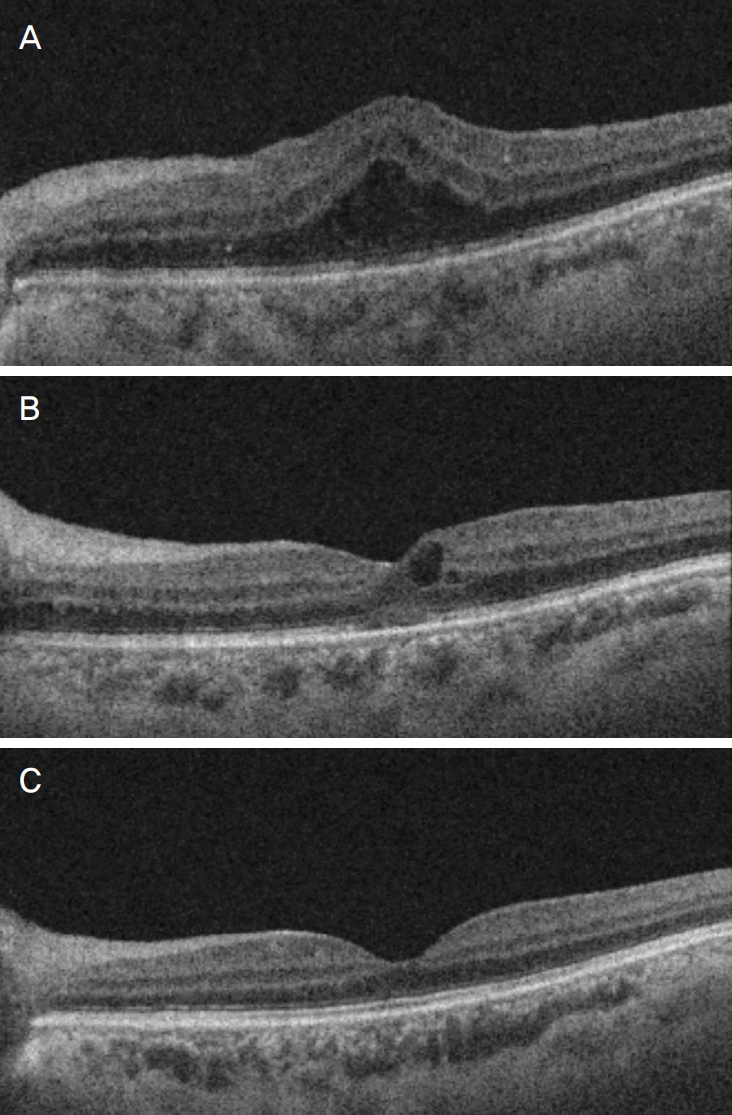
Table 1.
Patient demographics and baseline characteristics
Values are presented as mean ± standard deviation (range) or number (%) unless otherwise indicated.
DM = diabetes mellitus; BCVA = best corrected visual acuity; logMAR = logarithm of the minimum angle of resolution; CMT = central macular thickness; DME = diabetic macular edema; PRP = pan retinal photocoagulation; NPDR = non-proliferative diabetic retinopathy; PDR = proliferative diabetic retinopathy; OCT = optical coherence tomography.
Table 2.
Mean changes in visual acuity and central macular thickness after 0.1% bromfenac solution treatment
| Subject | Baseline | 1 month | 2 months | 3 months |
|---|---|---|---|---|
| BCVA (logMAR) | 0.40 ± 0.29 | 0.39 ± 0.29 | 0.38 ± 0.24 | 0.34 ± 0.21 |
| p-value* | - | 0.93 | 0.61 | 0.36 |
| Mean changes of BCVA | - | -0.01 ± 0.10 | -0.02 ± 0.09 | -0.06 ± 0.11 |
| CMT (μm) | 337.0 ± 97.3 | 331.4 ± 67.9 | 311.7 ± 89.1 | 282.9 ± 76.7 |
| p-value* | - | 0.47 | 0.07 | 0.03 |
| Mean changes of CMT | - | -5.6 ± 7.6 | -25.3 ± 20.6 | -54.1 ± 30.9 |
REFERENCES
1) Acan D, Calan M, Er D, et al. The prevalence and systemic risk factors of diabetic macular edema: a cross-sectional study from Turkey. BMC Ophthalmol 2018;18:91.



2) Ferris FL 3rd, Patz A. Macular edema. A complication of diabetic retinopathy. Surv Ophthalmol 1984;28 Suppl:452-61.


3) Schatz H, Madeira D, McDonald HR, Johnson RN. Progressive enlargement of laser scars following grid laser photocoagulation for diffuse diabetic macular edema. Arch Ophthalmol 1991;109:1549-51.


4) Fong DS, Segal PP, Myers F, et al. Subretinal fibrosis in diabetic macular edema. ETDRS report 23. Early Treatment Diabetic Retinopathy Study Research Group. Arch Ophthalmol 1997;115:873-7.


5) Falavarjani KG, Nguyen QD. Adverse events and complications associated with intravitreal injection of anti-VEGF agents: a review of literature. Eye (Lond) 2013;27:787-94.



6) Funatsu H, Yamashita H, Ikeda T, et al. Vitreous levels of interleukin-6 and vascular endothelial growth factor are related to diabetic macular edema. Ophthalmology 2003;110:1690-6.


7) Noma H, Funatsu H, Mimura T, et al. Vitreous levels of interleukin-6 and vascular endothelial growth factor in macular edema with central retinal vein occlusion. Ophthalmology 2009;116:87-93.


8) Jones J, Francis P. Ophthalmic utility of topical bromfenac, a twice-daily nonsteroidal anti-inflammatory agent. Expert Opin Pharmacother 2009;10:2379-85.


9) Russo A, Costagliola C, Delcassi L, et al. Topical nonsteroidal anti-inflammatory drugs for macular edema. Mediators Inflamm 2013;2013:476525.



10) Schoenberger SD, Kim SJ. Nonsteroidal anti-inflammatory drugs for retinal disease. Int J Inflam 2013;2013:281981.



11) Shimura M, Yasuda K. Topical bromfenac reduces the frequency of intravitreal bevacizumab in patients with branch retinal vein occlusion. Br J Ophthalmol 2015;99:215-9.


12) Gomi F, Sawa M, Tsujikawa M, Nishida K. Topical bromfenac as an adjunctive treatment with intravitreal ranibizumab for exudative age-related macular degeneration. Retina 2012;32:1804-10.


13) Pinna A, Blasetti F, Ricci GD, Boscia F. Bromfenac eyedrops in the treatment of diabetic macular edema: a pilot study. Eur J Ophthalmol 2017;27:326-30.


14) Congdon NG, Schein OD, von Kulajta P, et al. Corneal complications associated with topical ophthalmic use of nonsteroidal antiinflammatory drugs. J Cataract Refract Surg 2001;27:622-31.


15) Gardner TW, Antonetti DA, Barber AJ, et al. Diabetic retinopathy: more than meets the eye. Surv Ophthalmol 2002;47 Suppl 2:S253-62.

16) Miyake K, Ibaraki N. Prostaglandins and cystoid macular edema. Surv Ophthalmol 2002;47 Suppl 1:S203-18.


17) Joussen AM, Poulaki V, Mitsiades N, et al. Nonsteroidal anti-inflammatory drugs prevent early diabetic retinopathy via TNF-alpha suppression. FASEB J 2002;16:438-40.


18) Ayalasomayajula SP, Kompella UB. Celecoxib, a selective cyclooxygenase-2 inhibitor, inhibits retinal vascular endothelial growth factor expression and vascular leakage in a streptozotocin-induced diabetic rat model. Eur J Pharmacol 2003;458:283-9.


19) Kern TS, Miller CM, Du Y, et al. Topical administration of nepafenac inhibits diabetes-induced retinal microvascular disease and underlying abnormalities of retinal metabolism and physiology. Diabetes 2007;56:373-9.


20) Kaya M, Karahan E, Ozturk T, et al. Effectiveness of intravitreal ranibizumab for diabetic macular edema with serous retinal detachment. Korean J Ophthalmol 2018;32:296-302.



21) Kim BY, Smith SD, Kaiser PK. Optical coherence tomographic patterns of diabetic macular edema. Am J Ophthalmol 2006;142:405-12.


22) Browning DJ, Fraser CM, Clark S. The relationship of macular thickness to clinically graded diabetic retinopathy severity in eyes without clinically detected diabetic macular edema. Ophthalmology 2008 115:533-9. e2.


23) Sharief L, Chen YH, Lightman S, Tomkins-Netzer O. Prospective study of morphologic and functional parameter changes post intravitreal therapy for macular edema. Graefes Arch Clin Exp Ophthalmol 2020;258:1941-7.


24) Maheshwary AS, Oster SF, Yuson RMS, et al. The association between percent disruption of the photoreceptor inner segment/outer segment and visual acuity in diabetic macular edema. Am J Ophthalmol 2010 150:63-7. e1.


25) Fursova AZ, Chubar’ NV, Tarasov MS, et al. Clinical associations between photoreceptor status and visual outcomes in diabetic macular edema. Vestn Oftalmol 2017;133:11-8.

26) Zweifel SA, Engelbert M, Khan S, Freund KB. Retrospective review of the efficacy of topical bromfenac (0.09%) as an adjunctive therapy for patients with neovascular age-related macular degeneration. Retina 2009;29:1527-31.


-
METRICS

- Related articles
-
The Effect of Physical Eye Examinations on Job Options2021 October;62(10)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



