 |
 |
| J Korean Ophthalmol Soc > Volume 62(4); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØ┤ ņ׳ļŖö ĒŖ╣ļ░£ļ¦Øļ¦ēņĀäļ¦ē ĒÖśņ×ÉņŚÉņä£ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ Ļ┤æļ▓öņ£äĒĢ£ ļ¦Øļ¦ēņČ£ĒśłņØä Ļ▓ĮĒŚśĒĢśņśĆĻĖ░ņŚÉ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”ØļĪĆņÜöņĢĮ
59ņäĖ ņŚ¼ņ×É ĒÖśņ×ÉĻ░Ć ņłśĻ░£ņøö ņĀäļČĆĒä░ ļ░£ņāØĒĢ£ ņÜ░ņĢłņØś ņŗ£ļĀźņĀĆĒĢśņÖĆ ļ│ĆĒśĢņŗ£ļź╝ ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆļŗż. 20ļģä ņĀä ņ£äņĢöņ£╝ļĪ£ ņ£äņĢäņĀäņĀłņĀ£ņłĀņØä ļ░øņĢä ļ¦īņä▒ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØ┤ ņ׳ļŹś ĒÖśņ×ÉļĪ£ ņĢłĻ│╝ņĀü Ļ▓Ćņé¼ņāü ņÜ░ņĢłņØś ĒÖ®ļ░śļČĆ ļ¦Øļ¦ēņĀäļ¦ē ņ¦äļŗ©ĒĢś ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ļłł ņåŹ ņ¦æĻ▓īļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļÅäņżæ ņāüņØ┤ņĖĪ ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņ£╝ļĪ£ ņČöņĀĢļÉśļŖö ļČĆņ£äņŚÉņä£ Ļ┤æļ▓öņ£äĒĢ£ ņČ£ĒśłņØ┤ ļ░£ņāØĒĢśņśĆĻ│Ā ņ¦ĆĒśł Ēøä ļ│äļŗżļźĖ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ņłśņłĀņØä ļ¦łļ¼┤ļ”¼ĒĢśņśĆļŗż. ņłśņłĀ Ēøä 2Ļ░£ņøöņ¦Ė ņŗ£ļĀźņĀĆĒĢśļź╝ ņŻ╝ņåīļĪ£ ņ×¼ļé┤ņøÉĒĢśņŚ¼ ņŗ£Ē¢ēĒĢ£ ņĢłņĀĆĻ▓Ćņé¼ņāü ņłśņłĀ ņŗ£ ļ░£ņāØĒĢ£ ņČ£Ēśł ļČĆņ£äļź╝ ĻĖ░ņżĆņ£╝ļĪ£ Ļ┤æļ▓öņ£äĒĢ£ ĒÖ®ļ░śļČĆ Ļ▓¼ņØĖļ¦ēņØ┤ ņ×¼ļ░£ĒĢśņśĆĻ│Ā, ņØ┤ļĪ£ ņØĖĒĢ£ ņŗ£ļĀźņĀĆĒĢśļĪ£ 2ņ░© Ļ▓¼ņØĖņä▒ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļ░Å ļé┤Ļ▓ĮĻ│äļ¦ēņĀ£Ļ▒░ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņłśņłĀ Ēøä Ēśäņ×¼ ĒÖśņ×ÉļŖö ļ│äļŗżļźĖ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæņØ┤ļŗż.
Ļ▓░ļĪĀ
ļ¦īņä▒ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśł ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ņĀĢņāüņØĖņŚÉ ļ╣äĒĢ┤ ļ¦Øļ¦ēĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņåÉņāü ņĀĢļÅäĻ░Ć ņŗ¼ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņČ£Ēśł ņ£äĒŚśņä▒ņØ┤ ļåÆņØä ņłś ņ׳ļŗż. ļö░ļØ╝ņä£ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØä ņĢōĻ│Ā ņ׳ļŖö ĒŖ╣ļ░£ļ¦Øļ¦ēņĀäļ¦ē ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ļ¦Øļ¦ēņĀäļ¦ēņØä ņĀ£Ļ▒░ĒĢĀ ļĢī ņäĖņŗ¼ĒĢ£ ņŻ╝ņØśĻ░Ć ĒĢäņÜöĒĢśļŗż.
ABSTRACT
Purpose
To report a case of massive retinal hemorrhage during epiretinal membrane (ERM) peeling in a patient with iron deficiency anemia (IDA).
Case summary
A 59-year-old female presented with gradually decreasing visual acuity and dysmorphopsia in the right eye for several months. She had a history of chronic IDA due to subtotal gastrectomy from gastric cancer 20 years prior. The patient was diagnosed as having macular ERM and underwent vitrectomy. During ERM peeling with intraocular forceps, we found a massive retinal hemorrhage which was presumed to have originated from the superotemporal branched retinal artery. After hemostasis, the operation was completed without critical complications. However, 2 months after surgery, the patient presented with decreased visual acuity once again. In fundus examination, diffuse macular tractional ERM was evident in the proximity of the previous intraoperative hemorrhage site. The patient underwent tractional membrane and internal limiting membrane removal surgery. The patient is currently undergoing follow-up without complications to date following the second surgery.
Conclusions
Our case study describes a patient having experienced massive retinal hemorrhage presumably having originated from a superotemporal branched retinal artery during ERM peeling. We speculate that the endothelial cells of retinal vessels are more vulnerable than normal in patients with severe chronic IDA.
ļ¦Øļ¦ēņĀäļ¦ēņØĆ ĻĄÉņäĖĒż, ļ¦Øļ¦ēņāēņåīņāüĒö╝ņäĖĒż, ļīĆņŗØņäĖĒż, ņä¼ņ£ĀņäĖĒż, ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀļĪ£ ĻĄ¼ņä▒ļÉśļ®░ ļ¦Øļ¦ēņØś ņŻ╝ļ”äĻ│╝ ļÆżĒŗĆļ”╝ņ£╝ļĪ£ ņØĖĒĢ┤ ņŗ£ļĀźĻ░Éņåī ļ░Å ļ│Ćņŗ£ņ”ØņØä ņØ╝ņ£╝ĒéżļŖö ņ¦łĒÖśņØ┤ļŗż[1]. ļīĆĻ░£ņØś Ļ▓ĮņÜ░ ĒŖ╣ļ░£ņä▒ņ£╝ļĪ£ ļ░£ņāØĒĢśļ®░ ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀņØä ĒåĄĒĢ£ ļ¦ēņØś ņĀ£Ļ▒░ļĪ£ 70% ņØ┤ņāüņŚÉņä£ ņŗ£ļĀźĒśĖņĀäņØä Ļ░ĆņĀĖņśżļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż. ņ×¼ļ░£ļźĀņØĆ 10% ņĀĢļÅäļĪ£ ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ņ£╝ļ®░ ņØ┤ ņżæ ņĢĮ 3%ņŚÉņä£ ņ×¼ņłśņłĀņØ┤ ĒĢäņÜöĒĢ£ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[2,3]. ņĄ£ĻĘ╝ ļ¦Øļ¦ēņĀäļ¦ēņØś ņ×¼ļ░£ļźĀņØä ņżäņØ┤ĻĖ░ ņ£äĒĢśņŚ¼ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ņŗ£ ļé┤Ļ▓ĮĻ│äļ¦ē ņĀ£Ļ▒░ļź╝ ļÅÖņŗ£ņŚÉ ĒĢśļŖö ņłśņłĀ ĻĖ░ļ▓ĢņØ┤ Ē¢ēĒĢ┤ņ¦ĆĻ│Ā ņ׳Ļ│Ā, ļé┤Ļ▓ĮĻ│äļ¦ēņØä ļ▓ŚĻ╣Ćņ£╝ļĪ£ņŹ© ĻĘ╝ņä¼ņ£Āļ¬©ņäĖĒż ņ”ØņŗØņØś ļ░£ĒīÉņØä ņĀ£Ļ▒░ĒĢśņŚ¼ ļ¦Øļ¦ēņĀäļ¦ēņØś ņ×¼ļ░£ļźĀņØä ņżäņØ╝ ņłś ņ׳ļŗżĻ│Ā ĒĢśņśĆļŗż[4]. ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņłĀņØś ņĢīļĀżņ¦ä ĻĖ░Ļ│äņĀü ĒĢ®ļ│æņ”Øņ£╝ļĪ£ļŖö ļ¦Øļ¦ēĒæ£ņĖĄ ļ¬©ņäĖĒśłĻ┤ĆĻ│äļĪ£ļČĆĒä░ņØś ņĀÉņāüņČ£Ēśł, ļ¦Øļ¦ēņŚ┤Ļ│Ą, ĒÖ®ļ░śņøÉĻ│Ą ļō▒ņØ┤ ņ׳ņ£╝ļ®░[2] ļō£ļ¼╝Ļ▓ī ļé┤Ļ▓ĮĻ│äļ¦ē ņĀ£Ļ▒░ļĪ£ ņØĖĒĢ£ ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄņØś ņåÉņāüņØ┤ļéś ņŗ£ņĢ╝Ļ▓░ņåÉ[5]ņŚÉ ļīĆĒĢ£ ļ¬ćļ¬ć ļ│┤Ļ│ĀĻ░Ć ņ׳ļŗż.
ļ│Ė ņ”ØļĪĆļŖö ļ¦īņä▒ņĀüņ£╝ļĪ£ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØ┤ ņ׳ļŖö ĒŖ╣ļ░£ļ¦Øļ¦ēņĀäļ¦ē ĒÖśņ×ÉņŚÉņä£ ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀ ļÅÖņĢł ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ņāüņØ┤ņĖĪ ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņŚÉņä£ ĻĖ░ņØĖĒĢ£ Ļ▓āņ£╝ļĪ£ ņČöņĀĢļÉśļŖö Ļ┤æļ▓öņ£äĒĢ£ ļ¦Øļ¦ē ņČ£ĒśłņØ┤ ļ░£ņāØĒĢśņśĆĻ│Ā, ņØ┤Ēøä ņČ£Ēśł ļČĆņ£äļź╝ ĻĖ░ņŗ£ņĀÉņ£╝ļĪ£ ĒĢśņŚ¼ ņØ┤ņ░©ņĀüņ£╝ļĪ£ Ļ▓¼ņØĖļ¦ēņØ┤ ļ░£ņāØĒĢ£ Ļ▓ĮņÜ░ņØ┤ļŗż. ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļ░£ņāØĒĢśļŖö ņČ£ĒśłņØĆ ļīĆļČĆļČä ņĀÉņāüņČ£ĒśłņØ┤ļ®░ ļ│Ė ņ”ØļĪĆņÖĆ Ļ░ÖņØ┤ ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņŚÉņä£ ĻĖ░ņØĖĒĢ£ Ļ▓āņ£╝ļĪ£ ņČöņĀĢļÉśļŖö ļīĆļ¤ēņØś ņČ£ĒśłņØĆ ĻĄŁļé┤ņÖĖ ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåĻĖ░ņŚÉ ļ│Ė ņ”ØļĪĆļź╝ ļ░£ņāØ Ļ░ĆļŖźĒĢ£ ĻĖ░ņĀä ļ░Å ļ¼ĖĒŚīĻ│Āņ░░Ļ│╝ ĒĢ©Ļ╗ś ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
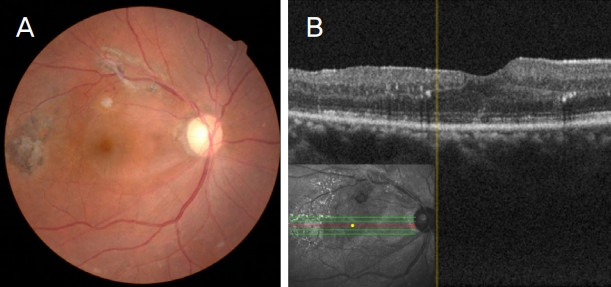
59ņäĖņØś ņŚ¼ņ×É ĒÖśņ×ÉĻ░Ć ņłśĻ░£ņøö ņĀäļČĆĒä░ ļ░£ņāØĒĢ£ ņÜ░ņĢłņØś ņŗ£ļĀź ņĀĆĒĢśņÖĆ ļ│ĆĒśĢņŗ£ļź╝ ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆļŗż. ņĢłĒåĄņØä ĒżĒĢ©ĒĢ£ ļŗżļźĖ ņĢłņ”Øņāü ļ░Å ņĢłņÖĖņāü, ņĢłņłśņłĀļĀź ļō▒ņØś ņĢłĻ│╝ņĀü Ļ│╝Ļ▒░ļĀźņāü ĒŖ╣ņØ┤ ņåīĻ▓¼ņØĆ ņŚåņŚłņ¦Ćļ¦ī ļŗ╣ļć©ļ│æ, ļ¦īņä▒ ĒÅÉņćäņä▒ ĒÅÉņ¦łĒÖś, ĒīīĒé©ņŖ©ļ│æņØś Ļ│╝Ļ▒░ļĀźņØ┤ ņ׳ņŚłņ£╝ļ®░ 20ļģä ņĀä ņ£äņĢöņ£╝ļĪ£ ņØĖĒĢ┤ ņ£äņĢäņĀäņĀłņĀ£ņłĀņØä ļ░øņØĆ ņāüĒā£ļĪ£ ļ¦īņä▒ņĀüņ£╝ļĪ£ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØä ņĢōĻ│Ā ņ׳ņŚłļŗż. ĒĢ£ņ▓£ņäØ ņŗ£ļĀźĒæ£ ĻĖ░ņżĆņ£╝ļĪ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ņÜ░ņĢł 0.5, ņóīņĢł 1.0ņØ┤ņŚłĻ│Ā ņĢłņĢĢņØĆ ņÜ░ņĢł 11 mmHg, ņóīņĢł 12 mmHgņśĆļŗż. ņĀäņĢłļČĆ Ļ▓Ćņé¼ņāü ņżæļō▒ļÅäņØś ļ░▒ļé┤ņן ņØ┤ņÖĖņŚÉ ĒŖ╣ņØ┤ ņåīĻ▓¼ņØĆ ņŚåņŚłņ£╝ļ®░, ņÜ░ņĢłņØś ņłśņ¦ü ņ£ĀļæÉ ĒĢ©ļ¬░ļ╣äļŖö 0.48ņØ┤ņŚłĻ│Ā ļģ╣ļé┤ņןņä▒ ņŗ£ņŗĀĻ▓Į ļ│ĆĒÖöļŖö Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. ņĢłņĀĆĻ▓Ćņé¼ņÖĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼ņŚÉņä£ ņÜ░ņĢłņØś ĒŖ╣ļ░£ņä▒ ĒÖ®ļ░śļČĆ ļ¦Øļ¦ēņĀäļ¦ēņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 1). ņØ┤ņŚÉ ņĀäņŗĀļ¦łņĘ©ĒĢś ņÜ░ņĢł ļ░▒ļé┤ņן ņ┤łņØīĒīīņ£ĀĒÖöņłĀ ļ░Å ņØĖĻ│ĄņłśņĀĢņ▓┤ņéĮņ×ģņłĀĻ│╝ ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀņØä Ļ│äĒÜŹĒĢśņśĆļŗż. ņłśņłĀ ņĀä ņĀäļ░śņĀüņØĖ ļé┤Ļ│╝ņĀü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ĒśłņĢĪĻ▓Ćņé¼ņāü Hemoglobin 8.1 g/dL (ņĀĢņāü 12-16 g/dL), Hematocrit 28.0% (ņĀĢņāü 36-46%), MCV 73.3 fL (ņĀĢņāü 80-99.5 fL), MCH 23.7 pg (ņĀĢņāü 26-38 pg), MCHC 32.1 g/dL (ņĀĢņāü 30-37 g/dL), Iron (Fe) 39 ╬╝g/dL (ņĀĢņāü 70-180 ╬╝/dL), Ferritin 4.7 ng/mL (ņĀĢņāü 5.5-300 ng/mL), TIBC 485 ╬╝g/dL (ņĀĢņāü 250-400 ╬╝g/dL)ļĪ£ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØś ņåīĻ▓¼ņØä ļ│┤ņØ┤Ļ│Ā ņ׳ņŚłļŗż. ĒśłņåīĒīÉņØĆ 427 ├Ś 103/╬╝L (ņĀĢņāü 130-400 ├Ś 103/╬╝L)ļĪ£ ņĀĢņāüļ│┤ļŗż ņĢĮĻ░ä ņ”ØĻ░ĆĒĢ┤ ņ׳ņŚłņ£╝ļ®░, ĒśłņĢĪņØæĻ│ĀĻ▓Ćņé¼ļŖö prothrombin time 12.5 (ņĀĢņāü 11.9-13.9 seconds), activated partial thromboplastin time 34.3 (ņĀĢņāü 29.6-41.0 seconds), bleeding time 4 minutes (3-10 minutes)ļĪ£ ļ¬©ļæÉ ņĀĢņāü ļ▓öņ£äļĪ£ ņĖĪņĀĢļÉśņŚłļŗż. ĒÖśņ×ÉļŖö ņÜ░ņĢłņØś ņ¦ĆņåŹņĀüņØĖ ņŗ£ļĀźņĀĆĒĢśņÖĆ ļ│ĆĒśĢņŗ£ļź╝ ļČłĒÄĖĒĢ┤ ĒĢśņŚ¼ ļ│ĖņØĖņØś ņĀäņŗĀ ņāüĒā£ļź╝ Ļ░ÉņĢłĒĢśĻ│ĀļÅä ņłśņłĀņØä ņøÉĒĢśņśĆĻ│Ā, ĒÖśņ×ÉĻ░Ć ļ¦ÄņØ┤ ļČłņĢłĒĢ┤ĒĢśĻ│Ā ņśłļ»╝ĒĢśņŚ¼, ņłśņłĀņØĆ ņĀäņŗĀļ¦łņĘ©ĒĢśņŚÉ ņ¦äĒ¢ēĒĢśņśĆļŗż. ļ│äļŗżļźĖ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ļ░▒ļé┤ņןņłśņłĀņØä ņ¦äĒ¢ēĒĢ£ ļÆż, 23Ļ▓īņØ┤ņ¦Ć ņ║Éļē╝ļØ╝ ņŗ£ņŖżĒģ£ņØä ņØ┤ņÜ®ĒĢ£ ņ£Āļ”¼ņ▓┤ ņĀä ņĀłņĀ£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņżæņŗ¼ļČĆ ņ£Āļ”¼ņ▓┤ļź╝ ņĀ£Ļ▒░ĒĢ£ ļÆż ņŗ£ņŗĀĻ▓Įņ£ĀļæÉļČĆ ļ╣äņĖĪ ņĢäļלņŚÉņä£ļČĆĒä░ Ēøäņ£Āļ”¼ņ▓┤ļź╝ ļ░Ģļ”¼ĒĢśņśĆļŗż. Triamcinolone acetonideļź╝ ļÅäĒżĒĢśņŚ¼ ņĀäļ¦ēņØä Ļ░Ćņŗ£ĒÖöĒĢ£ Ēøä ļłłņåŹņ¦æĻ▓īļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ĒīÉņØä ļ¦īļōżĻ│Ā ĻĘĖ ļüØņØä ņ×ĪĻ│Ā ņżæņŗ¼ņÖĆļź╝ ņČĢņ£╝ļĪ£ ņøÉņØä ĻĘĖļ”¼ļ®░ ņĀäļ¦ēņØä ņĀ£Ļ▒░ĒĢśļŖö ļÅäņżæ ņāüņØ┤ņĖĪ ĒśłĻ┤ĆļČäņ¦ĆņŚÉņä£ Ļ┤æļ▓öņ£äĒĢ£ ņČ£ĒśłņØ┤ ļ░£ņāØĒĢśņśĆļŗż(Fig. 2). ņØ┤ņŚÉ ņłĀņ×ÉļŖö ņ¦ĆĒśł ļ¬®ņĀüņ£╝ļĪ£ ļłł ņåŹ ņĪ░ļ¬ģĻ│╝ ļłł ņåŹ ņ¦æĻ▓īļź╝ ļ╣╝ņ¦Ć ņĢŖņØĆ ņ▒ä ļłł ņåŹ Ļ┤Ćļźśļ│æņØś ļåÆņØ┤ļź╝ ļåÆņŚ¼ 50 mmHgņØś Ļ│ĀņĢłņĢĢņØä ņ×Āņŗ£ ņ£Āņ¦ĆĒĢśņśĆļŗż. ņČöĻ░ĆņĀüņØĖ ņČ£Ēśł ņåīĻ▓¼ņØ┤ ņŚåņØīņØä ĒÖĢņØĖĒĢ£ Ēøä ņĢłņĢĢņØä ļé«ņČöĻ│Ā ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ņČ£ĒśłņØä ņĀ£Ļ▒░ĒĢ£ Ēøä ņĀäļ¦ē ņĀ£Ļ▒░ļź╝ ņÖäļŻīĒĢśņśĆļŗż. ĒĢ®ļ│æņ”Ø ņśłļ░®ņØä ņ£äĒĢ┤ ņČ£ĒśłņØ┤ ņ׳ņŚłļŹś ļ│æļ│Ć ņŻ╝ļ│Ćņ£╝ļĪ£ ņĢłļé┤ļĀłņØ┤ņĀĆņłĀ(200 mW, 30 shots)ņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ņŻ╝ļ│ĆļČĆ ņ£Āļ”¼ņ▓┤ļź╝ ņĀłņĀ£ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņłśņłĀņØä ļ¦łļ¼┤ļ”¼ĒĢśņśĆļŗż. ņłśņłĀ Ēøä 3ņØ╝ņ¦Ė ņĢłņĀĆĻ▓Ćņé¼ņāü ļ¦Øļ¦ēņĀäļ¦ēņØĆ ņל ņĀ£Ļ▒░ļÉśņŚłņ£╝ļ®░, ņČöĻ░ĆņĀüņØĖ ņČ£ĒśłņØĆ ņŚåņŚłņ£╝ļéś ņČ£ĒśłņØ┤ ņ׳ņŚłļŹś ĒśłĻ┤Ć ļČĆņ£äļź╝ ļö░ļØ╝ņä£ ļ¦Øļ¦ēņØś ĒŚłĒśłņä▒ ļ│ĆĒÖöĻ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 3A, B). ņłśņłĀ ņØ╝ņŻ╝ņØ╝ Ēøä ņ▓½ ņÖĖļל ļé┤ņøÉ ļŗ╣ņŗ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ņÜ░ņĢł 0.6, ņóīņĢł 1.0ņ£╝ļĪ£ ņĖĪņĀĢļÉśņŚłņ£╝ļ®░, ņĢłņĀĆĻ▓Ćņé¼ņāü ņāüņØ┤ņĖĪ ļ¦Øļ¦ē ĒøäĻĘ╣ļČĆ ņ¬ĮņØś ĒŚłĒśłņä▒ ļ│ĆĒÖöĻ░Ć ļ│ĆĒĢ©ņŚåņØ┤ Ļ┤Ćņ░░ļÉśĻ│Ā ņ׳ņŚłņ£╝ļ®░, ņłśņłĀĒøä 1Ļ░£ņøöĻ╣īņ¦Ć ļ│äļŗżļźĖ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæņØ┤ņŚłļŗż. ĻĘĖļ¤¼ļéś ņłśņłĀ Ēøä 2Ļ░£ņøöņ¦Ė ņÜ░ņĢłņØś ņŗ£ļĀźņĀĆĒĢśļź╝ ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņŚ¼ ņŗ£Ē¢ēĒĢ£ Ļ▓Ćņé¼ņāü ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ņÜ░ņĢł ņĢłņĀäņłśņ¦Ć 50 cmļĪ£, ņĢłņĀĆĻ▓Ćņé¼ņāü ņØ┤ņĀä ņłśņłĀ ļŗ╣ņŗ£ ņ׳ņŚłļŹś ņČ£Ēśł ļČĆņ£äļź╝ ĻĖ░ņżĆņ£╝ļĪ£ ĒÖ®ļ░śļČĆļź╝ Ļ▓¼ņØĖĒĢśļŖö Ļ┤æļ▓öņ£äĒĢ£ Ļ▓¼ņØĖļ¦ēņØ┤ ņ׳ņŚłņ£╝ļ®░, ĒĢ┤ļŗ╣ļÉśļŖö ĒśłĻ┤Ć ņŻ╝ļ│Ćņ£╝ļĪ£ ļ¦Øļ¦ēņČ£ĒśłņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 3C, D). ņØ┤ņŚÉ ņĀĆņ×ÉļōżņØĆ ņØ┤ņĀä ņłśņłĀ ļŗ╣ņŗ£ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļÅäņżæ ļ░£ņāØĒĢ£ ņČ£Ēśł ļČĆņ£äņØś ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦ź ņł£ĒÖśņןņĢĀņÖĆ Ļ┤ĆļĀ©ļÉ£ Ļ▓āņ£╝ļĪ£ ņČöņĀĢļÉśļŖö ļ¦Øļ¦ēņČ£Ēśł ļ░Å 2ņ░© Ļ▓¼ņØĖļ¦ēņ£╝ļĪ£ ņ¦äļŗ©ĒĢśņŚÉ 2ņ░© Ļ▓¼ņØĖņä▒ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļ░Å ļé┤Ļ▓ĮĻ│äļ¦ēņĀ£Ļ▒░ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņłśņłĀ 3Ļ░£ņøö Ēøä ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź ņÜ░ņĢł 0.2, ņóīņĢł 1.0ņ£╝ļĪ£ ņĖĪņĀĢļÉśņŚłĻ│Ā, ņĢłņĀĆĻ▓Ćņé¼ņāü ļ¦Øļ¦ēņØś Ļ▓¼ņØĖļ¦ēņØĆ ļ¬©ļæÉ ņĀ£Ļ▒░ļÉśņŚłņ£╝ļ®░ ņČ£Ēśł ĒØĪņłśļÉśņ¢┤ ņĢłņĀĢņĀüņØĖ ņāüĒā£ļĪ£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæņØ┤ļŗż(Fig. 4).
ĒŖ╣ļ░£ļ¦Øļ¦ēņĀäļ¦ē ĒÖśņ×ÉņŚÉņä£ ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀņØä ĒåĄĒĢ£ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļ░£ņāØĒĢĀ ņłś ņ׳ļŖö ĒĢ®ļ│æņ”ØņØĆ ļ¦Øļ¦ēņØś ņĀÉņāüņČ£ĒśłņØ┤ļéś, ļ¦Øļ¦ēņŚ┤Ļ│Ą, ĒÖ®ļ░śņøÉĻ│ĄņØ┤ ņ׳ņØä ņłś ņ׳Ļ│Ā[2], ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļÅÖņŗ£ņŚÉ ļé┤Ļ▓ĮĻ│äļ¦ēņØ┤ ņĀ£Ļ▒░ļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć ĒØöĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ[6], ļé┤Ļ▓ĮĻ│äļ¦ē ņĀ£Ļ▒░ļĪ£ ņØĖĒĢ£ ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄņØś ņåÉņāüņŚÉ ļö░ļźĖ ņŗ£ņĢ╝Ļ▓░ņåÉ[7] ļō▒ņØś ĒĢ®ļ│æņ”Ø ļśÉĒĢ£ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż.
ļ│Ė ņ”ØļĪĆļŖö ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØ┤ ņ׳ļŖö ĒŖ╣ļ░£ļ¦Øļ¦ēņĀäļ¦ē ĒÖśņ×ÉņŚÉņä£ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļÅäņżæ ļ¦Øļ¦ēņČ£ĒśłņØ┤ ļ░£ņāØĒĢśņśĆļŗż. ņØ┤ļŖö ĒØöĒ׳ ļ│┤Ļ│ĀļÉ£ Ēæ£ņĖĄļ¬©ņäĖĒśłĻ┤ĆņØś ņåÉņāüņ£╝ļĪ£ ņØĖĒĢ£ ņĀÉņāüņČ£ĒśłņØś ņ¢æņāüņØ┤ ņĢäļŗī ļīĆļ¤ē ņČ£ĒśłņØ┤ņŚłĻ│Ā ņłśņłĀ ņØ┤Ēøä ņŗ£Ē¢ēĒĢ£ ņĢłņĀĆĻ▓Ćņé¼ņāü ĻĖ░ņĪ┤ ņČ£Ēśł ļČĆņ£äļź╝ ĻĖ░ņĀÉņ£╝ļĪ£ ĒĢśņŚ¼ ļ¦Øļ¦ēļČäņ¦ĆļÅÖļ¦źņ¬ĮņØś ĒŚłĒśł ņ¢æņāüņØä ļ│┤ņśĆĻĖ░ņŚÉ ņłśņłĀņŗ£ ņāüņØ┤ņĖĪ ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņŚÉ ņåÉņāüņØ┤ ņ׳ņŚłņØīņØä ņ£ĀņČöĒĢ┤ ļ│╝ ņłś ņ׳ņŚłļŗż(Fig. 3A). ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļÅÖņĀĢļ¦źņØś ņåÉņāüņŚÉ ļīĆĒĢ┤ņä£ļŖö ĻĄŁļé┤ņÖĖ ļ│┤Ļ│ĀļÉ£ ļ░ö ņŚåņ£╝ļ®░, ļ│Ė ņ”ØļĪĆņÖĆ Ļ░ÖņØ┤ ņØ┤ņ░©ņĀüņØĖ ĒĢ®ļ│æņ”ØņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņĀĆņ×ÉļōżņØĆ ļ░£ņāØ Ļ░ĆļŖźĒĢ£ ĻĖ░ņĀäĻ│╝ ĒĢ®ļ│æņ”ØņØä ņśłļ░®ĒĢśĻĖ░ ņ£äĒĢ£ ļ░®ņĢłņŚÉ ļīĆĒĢśņŚ¼ Ļ│Āņ░░ĒĢ┤ļ│┤ņĢśļŗż.
ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļÅäņżæ ļ¦Øļ¦ē ņāüņØ┤ņĖĪ ļČäņ¦ĆļÅÖļ¦ź ļ░Å ņĀĢļ¦ź ļČĆņ£äņŚÉņä£ Ļ┤æļ▓öņ£äĒĢ£ ļīĆļ¤ē ņČ£ĒśłņØ┤ ļ░£ņāØĒĢśņśĆĻ│Ā, ņłśņłĀņŗ£ ņČ£ĒśłņØś ņ¢æņāüņØĆ ļ░ĢļÅÖņä▒ņØĆ ņĢäļŗłņŚłņ£╝ļéś ņČ£Ēśł ņ¢æņØ┤ Ēü¼Ļ│Ā ņČ£ĒśłņØś ņ”ØĻ░Ć ņåŹļÅäĻ░Ć ņĢäņŻ╝ ļ╣©ļ×ÉļŹś ņĀÉņØä ĻĘ╝Ļ▒░ļĪ£ ņŗĀĻ▓Įņä¼ņ£ĀņĖĄņŚÉ ņ׳ļŖö ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņØś ņåÉņāüņ£╝ļĪ£ ņØĖĒĢ£ Ļ▓āņ£╝ļĪ£ ņČöņĀĢĒĢ┤ ļ│╝ ņłś ņ׳ņŚłļŗż. ĻĖ░ņĪ┤ ļ¦Øļ¦ēņĀäļ¦ēņłśņłĀ ļÅäņżæ ļ░£ņāØĒĢśļŖö ņČ£ĒśłņŚÉ ļīĆĒĢ┤ņä£ļŖö Ēæ£ņĖĄļ¬©ņäĖĒśłĻ┤ĆņØś ņåÉņāüņŚÉ ņØśĒĢ£ ņĀÉņāü ņČ£ĒśłņŚÉ ļīĆĒĢ£ ļ¬ćļ¬ć ļ│┤Ļ│Ā[2,6]ļ¦ī ņ׳ņØä ļ┐É, ļ│Ė ņ”ØļĪĆņÖĆ Ļ░ÖņØ┤ ļÅÖļ¦ź ņåÉņāüņ£╝ļĪ£ ņØĖĒĢ£ ņČ£ĒśłņØĆ ļ¦żņÜ░ ļō£ļ¼Ė Ļ▓ĮņÜ░ļĪ£ ņČöĻ░ĆņĀüņØĖ ĻĖ░ņĀäņØ┤ ņ×æņÜ®Ē¢łņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üĒĢśņśĆļŗż.
ņłśņłĀ ņżæ ļ¦Øļ¦ēņĀäļ¦ēņØä ņĀ£Ļ▒░ĒĢśļŖö Ļ│╝ņĀĢņŚÉņä£ ņŻ╝ļ│ĆņØś ļČäņ¦Ćļ¦Øļ¦ēņĀĢļ¦źņØ┤ļéś ļÅÖļ¦źņŚÉ ļīĆĒĢśņŚ¼ ņ¦üņĀæņĀüņØĖ ĻĖ░Ļ│äņĀüņØĖ ņ×ÉĻĘ╣ņØ┤ļéś ņåÉņāüņØä ņŻ╝ņ¦ĆļŖö ņĢŖņĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņłĀņŗ£ ļ░£Ē¢ēĒĢ£ ļīĆļ¤ē ņČ£ĒśłņØś ņøÉņØĖ ļ░Å ĻĖ░ņĀäņ£╝ļĪ£ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ Ļ│╝ņĀĢ ņżæ ļ¦Øļ¦ēņĀäļ¦ēņØś Ļ▓¼ņØĖļĀźņŚÉ ņØśĒĢśņŚ¼ ļÅÖļ¦źņŚÉ ņ×ÉĻĘ╣ņØä ņŻ╝ņ¢┤ ņČ£ĒśłņØ┤ ņ£Āļ░£ļÉśņŚłņØä Ļ▓āņ£╝ļĪ£ ņČöļĪĀĒĢ┤ ļ│╝ ņłś ņ׳ļŗż. ĻĘĖļ”¼Ļ│Ā ņØ┤ļ¤¼ĒĢ£ ņČ£ĒśłņØś ņøÉņØĖņ£╝ļĪ£ļŖö ļ¦īņä▒ņĀüņ£╝ļĪ£ ļ╣łĒśłņØä ņĢōĻ│Ā ņ׳ļŖö ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ņĀĢņāüņØĖņŚÉ ļ╣äĒĢ┤ ļ¦Øļ¦ēĒśłĻ┤Ćļé┤Ēö╝ņäĖĒżņØś ņåÉņāü ņĀĢļÅäĻ░Ć ņŗ¼ĒĢ£ Ļ▓āņØ┤ ņøÉņØĖņØ┤ ņĢäļŗłņŚłņØäĻ╣ī ņāØĻ░üĒĢ┤ ļ│╝ ņłś ņ׳ņŚłļŗż. ļ│Ė ņ”ØļĪĆņØś ĒÖśņ×ÉļŖö ņĢĮ 30ļģä ņĀä ņ£äņĢö ņłśņłĀ ņØ┤Ēøä ļ░£ņāØĒĢ£ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņŚÉ ļīĆĒĢ┤ ņ▓ĀļČäņĀ£ņĀ£ ļ│ĄņÜ® ļ░Å Ļ░äĒŚÉņĀü ņłśĒśł ņ╣śļŻīļź╝ ļ░øĻ│Ā ņ׳ņŚłĻ│Ā, ņłśņłĀ ņĀä ņŗ£Ē¢ēĒĢ£ ĒśłņĢĪĻ▓Ćņé¼ Ļ▓░Ļ│╝ hemoglobin 8.1 g/dL (ņĀĢņāü 12-16 g/dL)ņśĆņ£╝ļéś, ņØ┤ņĀä ļ│ĖņøÉ ĒśłņĢĪļé┤Ļ│╝ ņ¦äļŻī ļŗ╣ņŗ£ ņŗ£Ē¢ēĒĢ£ ĒśłņĢĪĻ▓Ćņé¼ Ļ▓░Ļ│╝ hemoglobin 7 g/dL (ņĀĢņāü 12-16 g/dL)ļĪ£ ņ¦ĆņåŹņĀüņ£╝ļĪ£ ļČłņĢłņĀĢĒĢ£ ņłśņ╣śļź╝ ļ│┤ņØ┤Ļ│Ā ņ׳ņŚłĻĖ░ņŚÉ, ĻĘĖļÅÖņĢł ļ¦īņä▒ņĀüņ£╝ļĪ£ ļ╣łĒśłņØ┤ ņל ņĪ░ņĀłļÉśņ¦Ć ņĢŖļŖö ņāüĒā£ņśĆņØīņØä ņĢī ņłś ņ׳ņŚłļŗż. ĻĖ░ņĪ┤ ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤ ļ╣łĒśłņØĆ ĒśłĻ┤Ć ļé┤ Ļ│╝ņŚŁļÅÖĒĢÖ ņāüĒā£ļź╝ ņØ╝ņ£╝ņ╝£ ĻĘĖ ļ¼╝ļ”¼ņĀü Ēלņ£╝ļĪ£ ņØĖĒĢ┤ ĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņåÉņāüņØä ņØ╝ņ£╝Ēé©ļŗżĻ│Ā ĒĢśņśĆņ£╝ļ®░[8], ĒŖ╣Ē׳ ļŗ╣ļć© ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ņĀĆņé░ņåīņ”ØņŚÉ ļīĆĒĢ£ ņĪ░ņ¦üņØś ļ░śņØæņØ┤ ļ¢©ņ¢┤ņ¦ĆĻ│Ā ĒśłĻ┤Ćļé┤Ēö╝ņĀäĻĄ¼ņäĖĒżņØś ĻĖ░ļŖź ņĀĆĒĢśļĪ£ ņØĖĒĢ┤ ņĪ░ņ¦ü ņåÉņāüņØ┤ ļŹöņÜ▒ ņĢģĒÖöļÉ£ļŗżĻ│Ā ĒĢśņśĆļŗż[9]. ļ│Ė ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ļ¦īņä▒ ļ╣łĒśłĻ│╝ ļŹöļČłņ¢┤ 20ļģä ņĀäļČĆĒä░ ļŗ╣ļć©Ļ░Ć ņ׳ņŚłļŹś ĒÖśņ×ÉļĪ£, ļ¦īņä▒ ļ╣łĒśłļĪ£ ņØĖĒĢ£ ĒśłĻ┤Ćļé┤Ēö╝ ņäĖĒż ņåÉņāüņŚÉ ļŗ╣ļć©ļĪ£ ņØĖĒĢ£ ĒśłĻ┤Ćļé┤Ēö╝ņĀäĻĄ¼ņäĖĒż ĻĖ░ļŖź ņĀĆĒĢśĻ░Ć ļŹöĒĢ┤ņĀĖ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļé«ņØĆ ĻĖ░Ļ│äņĀü ņןļĀźņŚÉ ņØśĒĢ┤ņä£ļÅä ļÅÖļ¦ź ļé┤Ēö╝ņäĖĒżņØś ņåÉņāüņØ┤ ļ░£ņāØĒĢśņŚ¼ ņČ£ĒśłņØ┤ ņØ╝ņ¢┤ļé£ Ļ▓āņØ┤ ņĢäļŗīĻ░Ć ņāØĻ░üļÉ£ļŗż.
ĻĘĖļ”¼Ļ│Ā ņłśņłĀ ņØ┤Ēøä ņČ£Ēśł ļČĆņ£ä ņāüņØ┤ņĖĪ ļ¦Øļ¦ēļČäņ¦ĆļÅÖļ¦ź ņŻ╝ļ│Ćņ£╝ļĪ£ ļ¦Øļ¦ēņØś ĒŚłĒśłņä▒ ņåīĻ▓¼ņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŖöļŹ░, ņØ┤ļŖö ĒśłĻ┤Ćļé┤Ēö╝ņäĖĒżņØś ņåÉņāüĻ│╝ Ļ┤ĆļĀ©ĒĢśņŚ¼ ņ£Āļ░£ļÉ£ ĒśłņĀä ĒśĢņä▒ņ£╝ļĪ£ ņØĖĒĢ£ Ļ▓āņØĖņ¦Ć ņĢäļŗłļ®┤ ņłśņłĀ ņżæ ļ░£ņāØĒĢ£ ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņØś ņåÉņāüņ£╝ļĪ£ ņØĖĒĢ£ ņåīĻ▓¼ņØĖņ¦ĆļŖö ĒÖĢņŗżĒĢśņ¦Ć ņĢŖļŗż. ļ│Ė ņ”ØļĪĆļŖö ņłśņłĀ ņĀäĒøä ĒśłĻ┤ĆņĪ░ņśüņłĀņØä ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņĢśņ£╝ļ®░, ņłśņłĀņŗ£ņØś ņāüĒÖ® ļ░Å ņłśņłĀ ņĀäĒøäņØś ņĢłņĀĆ ņé¼ņ¦ä ļ╣äĻĄÉļĪ£ ņ¢┤ļ¢ż ĒśłĻ┤ĆņŚÉ ņåÉņāüņØ┤ ņ׳ņŚłļŖöņ¦Ć ņČöņĀĢĒĢśņśĆļŗżļŖö ņĀÉņŚÉņä£ ņĀ£ĒĢ£ņĀÉņØ┤ ņ׳ļŗż. ļśÉĒĢ£ 1ņ░© ļ¦Øļ¦ēņĀäļ¦ēņĀ£Ļ▒░ņÖĆ ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀ Ēøä ļ¦Øļ¦ēņĀäļ¦ēņØ┤ ņ×¼ļ░£ĒĢśļŖö Ļ▓ĮņÜ░ļŖö ĒØöĒĢ£ ņåīĻ▓¼ņ£╝ļĪ£ 2ņ░© Ļ▓¼ņØĖļ¦ēņØ┤ ņāØĻĖ┤ Ļ▓āņØ┤ ļČäņ¦Ćļ¦Øļ¦ēļÅÖļ¦źņØś ņł£ĒÖśņןņĢĀļĪ£ ņØĖĒĢ£ Ļ▓āņØĖņ¦Ć ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀņØś ĒĢ®ļ│æņ”ØņØĖ Ļ▓āņØĖņ¦Ć ĒÖĢņŗżĒ׳ ĻĄ¼ļČäĒĢśĻĖ░ ņ¢┤ļĀĄļŗżļŖö Ļ▓āļÅä ļ│Ė ņ”ØļĪĆļ│┤Ļ│ĀņØś ļśÉ ĒĢśļéśņØś ņĀ£ĒĢ£ņĀÉņØ┤ļŗż.
ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░ ļ│Ėļל 1ņ░© ņłśņłĀ ļŗ╣ņŗ£ ļé┤Ļ▓ĮĻ│äļ¦ē ņĀ£Ļ▒░ļź╝ ĒĢ©Ļ╗ś ņŗ£Ē¢ēĒĢĀ ņśłņĀĢņØ┤ņŚłņ¦Ćļ¦ī, ņČ£Ēśłļ¤ēņØ┤ ļ¦ÄņĢä ļ¦Øļ¦ēņĀäļ¦ēļ¦ī ņĀ£Ļ▒░ļź╝ ĒĢśņśĆĻ│Ā, ņØ┤Ēøä ņČ£Ēśł ļČĆņ£äļź╝ ĻĖ░ņŗ£ņĀÉņ£╝ļĪ£ ĒĢśņŚ¼ ĒÖ®ļ░śļČĆņŚÉ Ēü░ Ļ▓¼ņØĖļ¦ēņØ┤ ņāØĻ▓╝ļŗż. ļö░ļØ╝ņä£ Ļ▓¼ņØĖļĀźņØä ņĀ£Ļ▒░ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö Ļ▓¼ņØĖļ¦ēĻ│╝ ļé┤Ļ▓ĮĻ│äļ¦ēņØä ļ¬©ļæÉ Ļ░ÖņØ┤ ņĀ£Ļ▒░ĒĢśļŖö Ļ▓āņØ┤ ĒÜ©Ļ│╝ņĀüņØ┤ļØ╝Ļ│Ā ĒīÉļŗ©ĒĢśņŚ¼ 2ņ░© ņłśņłĀņŗ£ņŚÉ ļé┤Ļ▓ĮĻ│äļ¦ēĻ│╝ ņØ┤ņ░© Ļ▓¼ņØĖļ¦ēņØä ĒĢ©Ļ╗ś ņĀ£Ļ▒░ĒĢśņśĆĻ│Ā, Ļ▓░Ļ│╝ņĀüņ£╝ļĪ£ļŖö 1ņ░© ņłśņłĀņŗ£ ļé┤Ļ▓ĮĻ│äļ¦ēņØä ĒĢ©Ļ╗ś ņĀ£Ļ▒░ĒĢśļŖö Ļ▓āņØ┤ ļŹö ņØ┤ļĪŁņ¦Ć ņĢŖņĢśņØäĻ╣ī ņśłņāüĒĢĀ ņłś ņ׳ļŖö ļČĆļČäņØ┤ļŗż.
ņĀĆņ×ÉļōżņØĆ ļ¦īņä▒ņĀüņØĖ ņ▓Ā Ļ▓░ĒĢŹņä▒ ļ╣łĒśłņØä ņĢōĻ│Ā ņ׳ļŖö ĒŖ╣ļ░£ļ¦Øļ¦ēņĀäļ¦ē ĒÖśņ×ÉņŚÉĻ▓īņä£ ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀņŗ£ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ ļÅäņżæ ņśłņĖĪĒĢśĻĖ░ ĒלļōĀ, ļ¦Øļ¦ēļČäņ¦ĆļÅÖļ¦źņŚÉņä£ ĻĖ░ņŗ£ĒĢ£ Ļ▓āņ£╝ļĪ£ ņČöņĀĢļÉśļŖö ļīĆļ¤ēņØś ļÅÖļ¦ź ņČ£ĒśłņØä Ļ▓ĮĒŚśĒĢśņśĆĻ│Ā, ņØ┤Ēøä ņČ£Ēśł ļČĆņ£äļź╝ ĻĖ░ņĀÉņ£╝ļĪ£ ĒĢśņŚ¼ ĒÖ®ļ░śļČĆņŚÉ Ēü░ Ļ▓¼ņØĖļ¦ēņØ┤ ļ░£ņāØĒĢśņŚ¼ 2ņ░© ņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņØ┤ņÖĆ Ļ░ÖņØ┤ ļ¦īņä▒ņĀüņØĖ ļ╣łĒśłņØ┤ ņ׳ļŖö ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ņĀĢņāüņØĖņŚÉ ļ╣äĒĢ┤ ļ¦Øļ¦ēĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņåÉņāü ņĀĢļÅäĻ░Ć ņŗ¼ĒĢśĻĖ░ ļ¢äļ¼ĖņŚÉ ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļÅÖņĀĢļ¦ź ļČĆļČäņØĆ ļ¦żņÜ░ ņĪ░ņŗ¼ņŖżļ¤ĮĻ▓ī ņĀ£Ļ▒░ĒĢśļŖö Ļ▓āņØ┤ ņóŗĻ▓Āņ£╝ļ®░, ļ¦Øļ¦ēņĀäļ¦ē ņĀ£Ļ▒░ņŗ£ ļé┤Ļ▓ĮĻ│äļ¦ēņØä ĒĢ©Ļ╗ś ņĀ£Ļ▒░ĒĢśļŖö Ļ▓āņØ┤ Ļ▓¼ņØĖļĀź ĒĢ┤ņåīļéś 2ņ░©ņä▒ ļ¦Øļ¦ēņĀäļ¦ē ļō▒ņØś ņ×¼ļ░£ņØä ņśłļ░®ĒĢśĻĖ░ ņ£äĒĢ┤ ļŹöņÜ▒ ņóŗņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
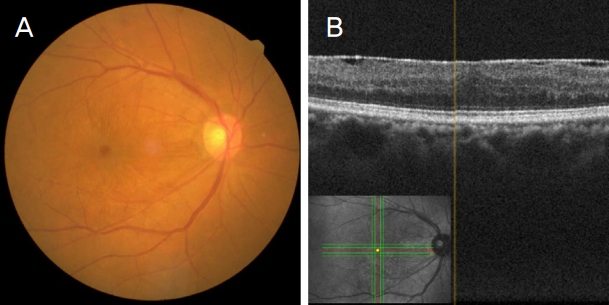
Figure┬Ā1.
The preoperative fundus photograph and optical coherence tomography (OCT) scan images. (A) The fundus photograph shows proliferative membranes on the surface of the macula. (B) The OCT image shows thick hyperreflective epiretinal membrane on macular with retinal distortion.
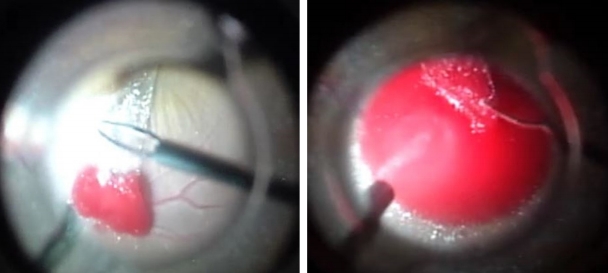
Figure┬Ā2.
The intraoperative fundus findings. Massive retinal bleeding from superior temporal branch of retinal vessels during epiretinal membrane peeling.
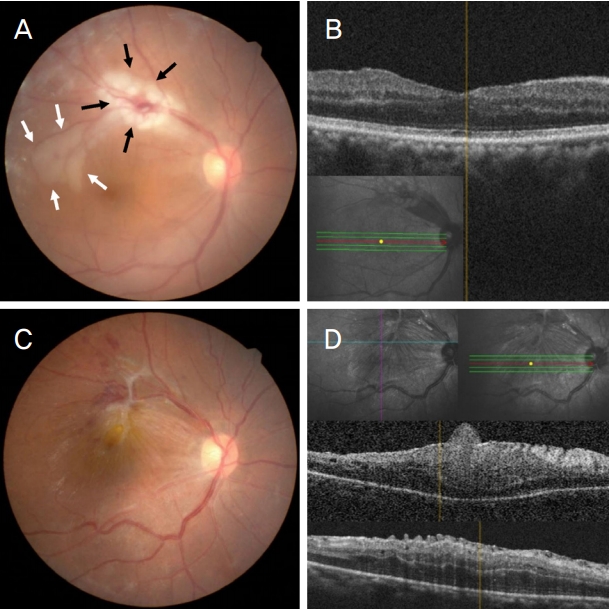
Figure┬Ā3.
The postoperative fundus photographs and optical coherence tomography scan images. 3 days after the surgery, (A) retinal ischemic change (white arrows) was observed along the superotemporal branch retinal artery region and post laser scar can be seen (black arrows). (B) No epiretinal membrane with normal macular appearance was observed. Two months after the surgery, (C) diffuse macular tractional membrane with retinal hemorrhage can be seen and (D) Diffuse tractional membrane with retinal distortion was observed.
REFERENCES
2) Donati G, Kapetanios AD, Pournaras CJ. Complications of surgery for epiretinal membranes. Graefes Arch Clin Exp Ophthalmol 1998;236:739-46.


3) Grewing R, Mester U. Results of surgery for epiretinal membranes and their recurrences. Br J Ophthalmol 1996;80:323-6.



4) Kwok A, Lai TY, Yuen KS. Epiretinal membrane surgery with or without internal limiting membrane peeling. Clin Exp Ophthalmol 2005;33:379-85.


5) Haritoglou C, Gass CA, Schaumberger M, et al. Macular changes after peeling of the internal limiting membrane in macular hole surgery. Am J Ophthalmol 2001;132:363-8.


6) Kim JH, Park HJ, Lee JE, Oum BS. Retinal dot hemorrhage and internal limiting membrane injury during epiretinal membrane peeling. J Korean Ophthalmol Soc 2012;53:786-91.

7) Kim KH, Lee JW, Lee JE, Oum BS. Visual field defect developed after internal limiting membrane peeling in a patient with epiretinal membrane. J Korean Ophthalmol Soc 2011;52:378-84.





 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




