 |
 |
| J Korean Ophthalmol Soc > Volume 62(3); 2021 > Article |
|
국문초록
목적
안와에 발생하는 고립성 섬유종은 매우 드문 질환으로 알려져 있다. 저자들은 아직까지 국내에 보고된 적이 없는 낭성 안와 고립성 섬유종 1예를 경험하였기에 이를 보고하고자 한다.
증례요약
71세 남자가 2년 6개월 전부터 느낀 복시를 주소로 내원하였다. 안과 검사에서 좌안에 10 mm의 안구돌출이 관찰되었고 하이측으로 편위되어 있었으며 전방향 운동장애가 있었다. 안면부 전산화단층촬영 및 자기공명영상검사에서 안와 상비측에 경계가 명확한 분엽성 종괴가 관찰되었다. 종괴는 불균등하게 조영증강되었으며 일부 영역에서 낭성 조직이 의심되었다. 앞쪽 안와절개술을 통한 종괴 절제생검을 시행하였고 43 × 30 × 28 mm의 종괴를 완전 절제하였다. Hematoxyline and eosin 염색을 이용한 병리조직검사상 방추세포가 교원기질에 불규칙하게 배열되어 있었다. 면역조직화학적 검사에서 CD34, CD99 양성이 나와 고립성 섬유종으로 진단하였다.
ABSTRACT
Purpose
To present a case of a cystic solitary fibrous tumor (SFT), the first report of its kind in Korea, along with a review of the literature of SFTs affecting the orbit.
Case summary
A 71-year-old male was referred to our practice due to diplopia for 2 years and 6 months. On ophthalmologic examination, 10-mm proptosis and inferolateral globe displacement were observed in the left eye, and extraocular movements were limited in all directions of gaze. A facial computed tomography scan and magnetic resonance imaging showed a lobulated, well-enhanced mass in the superonasal extraconal space. The tumor appeared to be heterogeneous; cystic tissue was suspected. An excisional biopsy was performed through anterior orbitotomy to remove the mass (dimensions, 43 × 30 × 28 mm3). Histological examination showed the tumor to be composed of spindle cells in collagenous tissue. Immunohistochemical staining was positive for CD34, CD99, and orbital SFT with cystic changes.
고립성 섬유종(solitary fibrous tumor)은 중배엽에서 기원하는 매우 드문 종양으로[1] 흉막, 심장막, 가슴세로칸 등에 주로 발생한다고 알려져 있다[2]. 1994년 Westra et al [3]이 안와에 발생한 고립성 섬유종을 최초로 보고한 이래 지금까지 전 세계적으로 118건의 안와 고립성 섬유종이 보고되었다[1-15]. 고립성 섬유종은 드물지만 안와내 어느 위치에서도 발생할 수 있어 다른 안와 종양들과의 감별이 반드시 필요한 질환이다[2]. 주된 임상양상은 눈꺼풀부종이나 서서히 진행하는 무통성 안구돌출이다[1]. 안와에 발생하는 고립성 섬유종은 대부분 고형 종양이고[4] 낭성 고립성 섬유종은 매우 드물게 보고되고 있는데 현재까지 전 세계적으로 6건의 낭성 고립성 섬유종이 보고되었다[4-7]. 저자들은 아직 국내에서 보고된 바 없는 안와 내에 발생한 낭성 고립성 섬유종 1예를 경험하였기에 이를 문헌 고찰과 함께 보고하고자 한다.
71세 남자가 2년 6개월 전부터 느낀 복시를 주소로 내원하였다. 외상이나 전신적 감염, 특이 병력은 없었고 안압은 양안 정상, 시력은 우안 1.0, 좌안은 0.4까지 교정되었다. Hertel 안구돌출계 검사상 우안 12 mm, 좌안 22 mm로 좌안에 10 mm의 안구돌출 소견을 보였다. 환자의 좌안은 하이측으로 편위되어 있었으며 안구운동검사에서 전방향 주시 시 좌안에 안구운동장애 소견이 관찰되었다(Fig. 1A). 안면부 전산화단층촬영과 자기공명영상촬영을 시행하였고, 좌측 안와 상비측 근원추 밖의 장축의 길이가 40 mm이고 경계가 명확한 분엽성 종괴가 관찰되었다. 전산화단층촬영에서 저음영과 중간음영이 구획화되어 나타나는 소견을 보였고 조영증강 시 불규칙하게 조영증강되면서 일부 저음영 지역은 조영증강이 되지 않아 종양의 낭성 변성이 의심되었다(Fig. 1B). 자기공명영상에서는 T1 강조영상에서 뇌의 회색질과 비교하여 동일한 신호 강도가 종양의 뒷부분에서 관찰되었고, 종양의 앞부분에서는 구획화된 여러 개의 낭성 변화가 뇌의 회색질보다 낮은 신호 강도로 관찰되었다(Fig. 1C). T2 강조영상에서는 뇌의 회색질과 동일한 신호 강도와 낮은 신호 강도가 혼재한 가운데 부분적으로 매우 강한 조영증강 소견이 있었는데 그 내부에는 관 모양의 공동화 소견도 보였다(Fig. 1D).
전신마취를 하고 종양의 절제 생검을 시행하였다. 가쪽 눈구석절개술 및 가쪽눈구석인대의 위쪽 갈래 절단술을 시행하고 상비측 결막원개접근법을 이용하여 앞쪽 안와절개술을 시행하였다. 근원추 외에 위치한 종괴는 여러 겹의 섬유화조직에 싸여 있어 섬유화피막을 박리해가며 종괴의 전절제를 시행하였다. 육안으로 관찰하였을 때 종괴는 43 × 30 × 28 mm 크기였으며 뒤쪽은 흰색의 고형질이면서 앞쪽은 붉은색 낭성 조직 소견을 보였다(Fig. 2A). Hematoxylin-Eosin 염색 결과 방추세포가 교원질에 불규칙하게 배열되어 있었고(Fig. 2B) 면역조직화학 검사에서 CD34, CD99에 양성(Fig. 2C, D), desmin, S-100, Ki-67, p53에 대해 음성으로 판명되어 낭성 변성이 동반된 양성 안와 고립성 섬유종으로 최종 진단하였다. 수술 후 현재까지 재발된 소견 없이 경과 관찰 중이다.
고립성 섬유종(solitary fibrous tumor)은 안와에서 매우 드물게 발생하는 종양으로 대부분 양성의 고형종양으로 보고되고 있다[6]. 낭성 변성을 보인 안와 고립성 섬유종은 2003년 처음 보고되었는데[4], 이후 현재까지 단 5건만이 추가로 보고되어[5-7] 그 임상양상 및 예후에 대한 고찰이 부족하다. 저자들은 안와에 발생한 낭성 고립성 섬유종 1예를 경험하였기에 이를 문헌 고찰과 함께 보고하고자 한다.
고립성 섬유종은 40-50대에 주로 발생한다고 알려져 있다[1,6]. 지금까지 보고된 118건의 증례를 종합해 보면 종양을 발견한 평균 나이는 43세였고, 5세에서 77세까지 넓은 연령 범위를 보였으며 남자 55건(46.6%), 여자 63건(53.4%)이었다. 본 증례는 71세 남성에서 발견되었는데 안와 고립성 섬유종은 중장년의 나이에 진단되는 경우가 많았으나 어떤 연령과 성별에서도 발생 가능하다는 것을 염두에 두어야 하겠다.
환자들이 병원을 찾는 주된 임상증상을 살펴보면 단안의 무통성 안구돌출이 118건 중 86건(72.9%)으로 가장 많았고 눈꺼풀부종 25건(21.2%), 눈물흘림 6건(5.1%)이 그 뒤를 이었다. 다른 증상 없이 시력저하만을 호소하여 병원을 찾은 후 안와 고립성 섬유종을 진단받은 경우는 1건(0.8%)에 그쳤다. 안와에 발생하는 고립성 섬유종은 서서히 크기가 커지면서 안구돌출, 안구운동장애, 안검부종 등을 유발하나 시력저하는 대부분 발생하지 않으며 세극등현미경검사에서도 특이 소견을 보이지 않았다[1,2,4,6]. 종양의 크기나 종양이 위치한 영역에 따라 안구운동장애를 일으키거나 시신경에 영향을 줄 수 있는데[1], 위치가 명시된 86건의 증례 중 4건(4.7%)만이 원추 내에 종양이 위치하였고 나머지 82건(95.3%)은 원추 밖에 위치한 종양이었다. 원추 밖에 위치한 종양 82건 중 상비측에 발생한 종양이 28건(34.1%)으로 가장 많았고 상이측이 17건(20.7%), 비측이 17건(20.7%)이었다. 눈물샘오목에 발생한 종양이 8건(9.8%)이며, 하이측에서 8건(9.8%), 하비측에서 4건(4.9%)의 고립성 섬유종이 발견되었다. 저자가 경험한 증례는 상비측 근원추 밖에 위치한 고립성 섬유종으로 안와 고립성 섬유종이 가장 호발하는 위치에서 발견되었다고 할 수 있다. 그러나 고립성 섬유종은 안와 어디에서나 발생할 수 있다.
영상검사에서 안과 고립성 섬유종은 경계가 명확하고 조영증강이 잘되는 연조직 종괴로 나타난다[8]. 전산화단층촬영에서 균일 또는 불균일하게 조영증강이 되는 종괴가 보이며 경계가 명확하고 주변 안와를 침범하는 공격적인 성향은 고립성 섬유종에서 대부분 보이지 않는다[9]. 자기공명영상검사의 전형적 소견은 T1 강조영상에서는 뇌의 회색질과 비슷한 신호 강도가, T2 강조영상에서는 뇌의 회색질과 비슷하거나 낮은 신호 강도가 불균등하게 분포하는 소견이다[8]. 특히 T2 강조영상에서 매우 낮은 신호 강도가 중심부에 위치하는 경우가 많은데 이는 고립성 섬유종에서도 콜라겐 섬유가 풍부한 부분을 의미한다[8]. T2 강조영상에서 아주 높은 신호 강도가 나타난다면 이는 출혈이나 낭성 변성 조직에서 보이는 소견이다[8]. 본 증례에서는 T1 강조영상에서 뇌의 회색질과 비슷한 부분이 대부분이었으나 종양의 앞쪽에는 구획화된 낮은 신호 강도가 보여 이를 통해 종양의 낭성 변성을 의심할 수 있었다. 또한 T2 강조영상에서 종양의 뒤쪽은 낮은 신호 강도를 보여 콜라겐 섬유가 풍부한 조직임을 유추할 수 있는 반면 종양의 앞쪽은 아주 높은 신호 강도가 나타나 출혈이나 낭성 변성을 의심하게 했다. 이러한 자기공명영상검사 결과는 전형적인 고립성 섬유종과는 다소 차이가 있으며 신경초종의 자기공명영상검사 결과와 유사하였다. 신경초종은 안와 종양의 1%를 차지하는 종양으로 조직학적으로 Antoni A와 Antoni B pattern이 동시에 나타나는 특징이 있다[9]. 이 중에서 Antoni B pattern 구역이 성긴 점액 조직으로 이루어져 본 증례의 자기공명영상검사 결과와 유사하게 나타난다[9]. 본 증례에서는 영상학적 검사만으로 낭성 변성이 동반된 고립성 섬유종과 신경초종을 감별하기 어려웠다.
한편 고립성 섬유종의 조영증강이 된 구역에서 공동화된 관형의 모습으로 혈관이 보이는 것을 종종 볼 수 있는데, 이는 종양 내부에 혈액의 움직임이 빠르게 일어나는 혈관의 모습을 보여주는 소견이다[8]. 본 증례에서도 T2 강조영상에서 일부 구부러진 혈관이 조영증강되지 않아 어둡게 보이는 소견을 보였다. 이러한 영상 소견은 혈관이 풍부한 모세혈관종, 해면혈관종, 혈관주위종, 거대세포혈관섬유종 등의 안와종양에서도 보일 수 있어 감별 진단이 필요하며, 자기공명영상검사가 이들의 감별에 도움이 된다[9].
안와 고립성 섬유종은 혈관주위종, 거대세포혈관섬유종, 섬유조직구종과 비슷한 조직학적 소견을 가져 감별을 요한다[3]. 이들 모두 섬유아세포 모양의 방추세포가 콜라겐 기질을 바탕으로 널려 있으며 혈관이 풍부하고 확장된 혈관이 특징적인 사슴뿔 모양을 보이기도 한다. 따라서 추가로 면역화학염색이 필요한데 CD34는 1994년 최초로 고립성 섬유종의 진단에 의미가 있다고 소개된 이후[3] 고립성 섬유종의 진단에 꼭 필요한 검사 항목이 되었다[10]. 고립성 섬유종은 CD34 (90-100%)뿐만 아니라 CD99 (70%)에 양성을 보이며 고립성 섬유종의 3분의 1에서 BCL2에도 양성을 나타낸다[2]. 신경초종과는 달리 S-100 단백질에는 음성이며 상피막 항원에도 음성이어서 이를 통해 수막종과도 감별할 수 있다[9]. Ki-67과 p53은 악성 고립성 섬유종에서 양성을 나타내는 것으로 알려져 있다[11].
고립성 섬유종은 대부분 양성으로 알려져 있으나 악성으로 진단된 고립성 섬유종도 보고되어 현재까지 총 7건 (5.9%)이 악성 안와 고립성 섬유종으로 진단되었다[9,11-13]. 안와 고립성 섬유종 118건 중에서 절제 후 재발하였다고 보고된 경우는 총 30건(25.4%)으로 이 중 26건(86.6%)은 종양의 불완전 절제 이후 일어난 재발이었다[1,7,9,14]. 재발한 고립성 섬유종 중에서 2건(6.7%)은 악성 고립성 섬유종으로의 조직학적 변성을 보이기도 했다[15]. 따라서 종양의 완전한 절제와 조직검사가 고립성 섬유종의 정확한 진단 및 재발 방지를 위해서 반드시 필요하다. 특히 낭성 변성을 동반한 고립성 섬유종의 경우 종양의 절제 과정에서 낭의 파열에 유의해야 할 것으로 생각된다. 절제 과정에서 낭성 고립성 섬유종이 파열된 증례는 아직까지 명확히 보고된 바 없으나, 안와 내에서 낭이 파열될 경우 내용물의 유출로 인해 주변 조직의 염증과 종양의 재발을 예상할 수 있다. Graue et al [7]은 절제 후 재발한 안와 고립성 섬유종 3건을 보고하였는데, 세 건 모두 낭성 변성을 보인 고립성 섬유종이었다. 따라서 술 전 영상학적 검사를 통해 고립성 섬유종의 낭성 변성이 확인된 경우에는 수술 중 낭의 파열 없이 완전 절제를 하기 위하여 더 유의해야 하며, 술 후에 종양의 재발 여부에 대하여 더 면밀히 관찰해야 할 것이다.
본 증례는 2년 6개월 만에 단안에 10 mm의 무통성 안구 돌출을 유발한 안와 고립성 섬유종에 대한 증례로 영상검사 결과에서 낭성 변성 소견이 동반되어 고립성 섬유종을 의심하기에 어려움이 있었으나 조직검사 결과 및 면역화학 염색을 통해 최종적으로 낭성 고립성 섬유종을 진단받은 경우이다. 낭성 고립성 섬유종은 아직 그 발생기전이 명확히 밝혀지지는 않았다[5]. 혈액공급 역량을 넘어 너무 빠르고 크게 종양이 성장하다 보면 내부에 괴사되는 부분이 발생하고 이것이 낭성 변성을 유발한다는 가설이 있으나[10] 추가적인 연구가 필요하다. 또한 안와에 오래 존재한 고립성 섬유종일수록 낭성 변성을 가져올 것이라는 주장도 있으나[5] 보고된 증례들을 살펴보면 6개월에서 1년 사이에 낭성 변성을 보인 고립성 섬유종 증례도 있어[6,10] 이를 단정 짓기는 어렵다. 고립성 섬유종의 낭성 변성이 악성을 시사한다는 주장도 있다[5]. 그러나 실제 보고된 6건의 낭성 고립성 섬유종 중에서 악성을 진단받은 사례는 없다. 본 증례에서도 면역화학염색 검사에서 Ki-67, p53이 모두 음성으로 나와 낭성 변성과 악성은 아직까지 큰 연관성을 찾기 어려워 보인다.
안와에 생기는 고립성 섬유종은 매우 드물고 낭성 고립성 섬유종은 국내에 아직 보고된 적 없기에 저자들이 경험한 안와의 낭성 고립성 섬유종을 소개하고 문헌 고찰을 시행하였다. 진행하는 무통성 안구돌출이 있는 환자에서 경계가 명확하고 조영증강이 잘되는 영상학적 검사 소견을 보이는 경우에 안와 고립성 섬유종에서도 낭성 변성이 있을 수 있음에 유의하여 감별진단을 하고 완전히 절제하는 치료를 계획해야 종양의 재발을 막고 확실한 진단을 할 수 있겠다.
Figure 1.
(A) Preoperative facial photograph showing proptosis and inferolateral displacement of the globe. (B) Axial postcontrast computed tomography image of the orbit shows a 40 mm-sized, well marginated heterogeneously enhancing soft tissue mass in the superomedial aspect of the left orbit. (C) Axial T1 magnetic resonance (MR) image demonstrates a lobulated mass which shows isosignal intensity to gray matter on posterior portion and multiple cysts (arrows) on anterior portion, and the cyst shows hyposignal intensity to gray matter. (D) Axial T2 MR image showing a hypointense tumor with marked hyperintense lesion with cystic space (arrows). The patient consented to the use of these photographs.
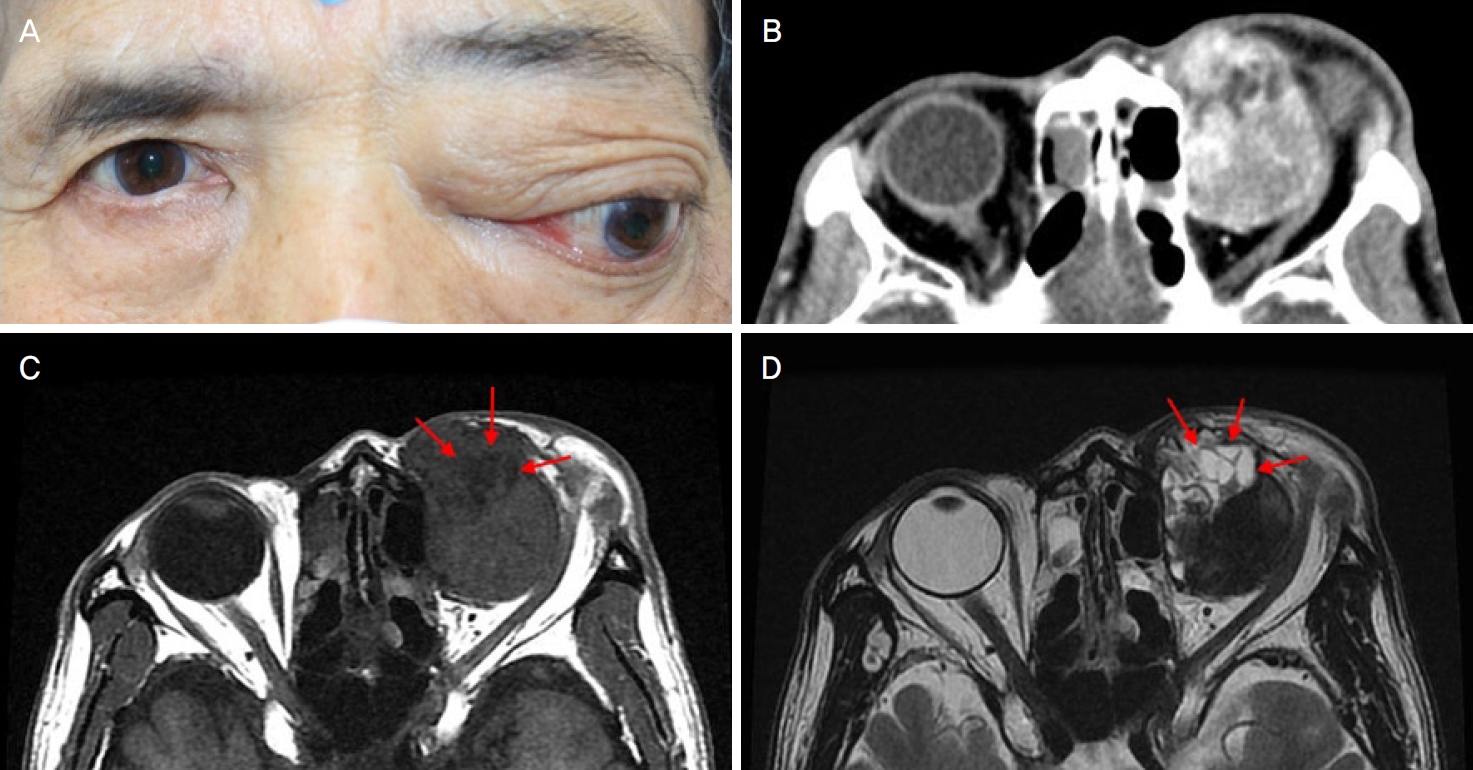
Figure 2.
(A) Excised mass on gross examination showing whitish solid mass with cystic lobulated lesion on anterior portion of the mass (arrows). (B) Areas of hyper- and hypocellularity of spindle cells with abundant fibrous stroma intermixed with vasculature (hematoxylin and eosin, ×200). (C) Immunohistochemistry showing positive staining for CD34 (×400). (D) Immunohistochemistry showing positive for CD99 (×400).

REFERENCES
1) Le CP, Jones S, Valenzuela AA. Orbital solitary fibrous tumor: a case series with review of the literature. Orbit 2014;33:145-51.


2) Bernardini FP, de Conciliis C, Schneider S, et al. Solitary fibrous tumor of the orbit: is it rare? Report of a case series and review of the literature. Ophthalmology 2003;110:1442-8.


3) Westra WH, Gerald WL, Rosai J. Solitary fibrous tumor. Consistent CD34 immunoreactivity and occurrence in the orbit. Am J Surg Pathol 1994;18:992-8.


4) Krishnakumar S, Subramanian N, Mehan ER, et al. Solitary fibrous tumor of the orbit a clinicopahtologic study of six cases with review of the literature. Surv Ophthalmol 2003;48:544-54.

5) Alam S, Backiavathy V, Mukherjee B, Subramanian K. A rare case of giant multicystic solitary fibrous tumor of the orbit. Orbit 2018;37:69-72.


6) Feuerman JM, Flint A, Elner VM. Cystic solitary fibrous tumor of the orbit. Arch Ophthalmol 2010;128:385-7.


7) Graue GF, Schubert HD, Kazim M, et al. Correlation between clinical features, imaging and pathologic findings in recurrent solitary fibrous tumor of the orbit. Orbit 2013;32:375-80.


8) Kim H, Kim HJ, Kim YD, et al. Solitary fibrous tumor of the orbit: CT and MR imaging findings. Am J Neuroradiol 2008;29:857-62.



9) Zhang Z, Shi J, Guo J, et al. Value of MR imaging in differentiation between solitary fibrous tumor and schwannoma in the orbit. AJNR Am J Neuroradiol 2013;34:1067-71.



10) Polomsky M, Sines DT, Dutton JJ. Solitary fibrous tumor of the orbit with multiple cavities. Ophthalmic Plast Reconstr Surg 2013;29:e117-9.


11) Kim J, Kim YD, Woo KI. Malignant solitary fibrous tumor of the orbit. J Korean Ophthalmol Soc 2013;54:1599-604.

12) Girnita L, Sahlin S, Orrego A, Seregard S. Malignant solitary fibrous tumour of the orbit. Acta Ophthalmol 2009;87:464-7.


13) Mascarenhas L, Lopes M, Duarte A, et al. Histologically malignant solitary fibrous tumor of the orbit. Neurochirurgie 2006;52:415-8.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




