 |
 |
| J Korean Ophthalmol Soc > Volume 61(8); 2020 > Article |
|
국문초록
대상과 방법
결과
ABSTRACT
Purpose
Methods
Results
Figure 1.
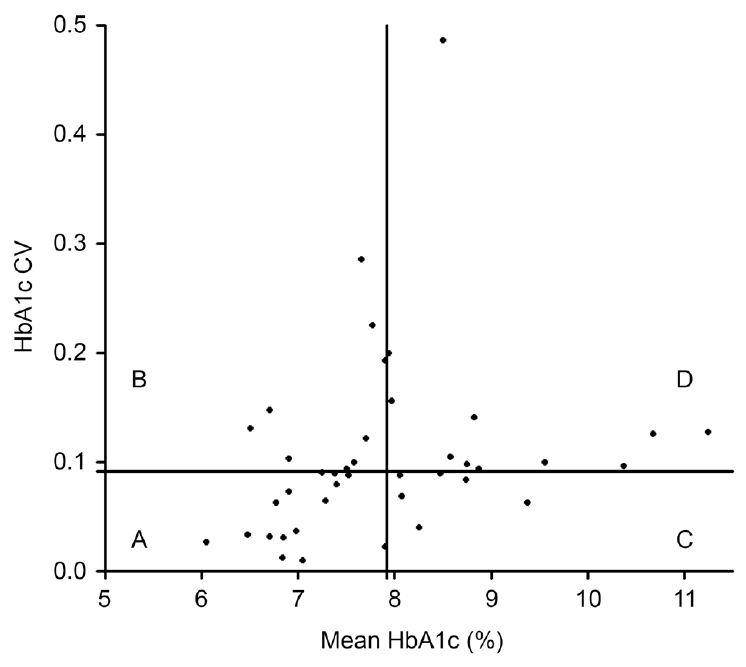
Table 1.
Values are presented as mean ± standard deviation (range) or number (%).
HbA1c = glycated hemoglobin A; CV = coefficient of variation; Hb = hemoglobin; BUN = blood urea nitrogen; eGFR = estimated glomerular filtration rate; LDL = low density lipoprotein; HDL = high density lipoprotein; TG = triglyceride; BCVA = best corrected visual acuity; LogMAR = logarithm of the minimal angle of resolution; CMT = central macular thickness; NPDR = non-proliferative diabetic retinopathy; PDR = proliferative diabetic retinopathy.
Table 2.
|
Low mean HbA1c |
High mean HbA1c |
||||||
|---|---|---|---|---|---|---|---|
| Low CV Group A (n = 18) | High CV Group B (n = 10) | p-value* | Low CV Group C (n = 10) | High CV Group D (n = 11) | p-value* | ||
| Age (years) | 58.1 ± 10.9 | 65.0 ± 12.2 | 0.146 | 57.9 ± 7.9 | 53.6 ± 13.0 | 0.605 | |
| Mean HbA1c_pre-injection (%) | 7.1 ± 0.5 | 7.3 ± 0.5 | 0.191 | 8.5 ± 0.5 | 9.4 ± 1.2 | 0.114 | |
| HbA1c CV_pre-injection | 0.05 ± 0.03 | 0.15 ± 0.06 | <0.001 | 0.08 ± 0.02 | 0.16 ± 0.11 | <0.001 | |
| Mean HbA1c_post-injection (%) | 7.1 ± 0.7 | 7.5 ± 0.6 | 0.080 | 8.6 ± 0.6 | 8.6 ± 1.0 | 0.809 | |
| HbA1c CV_post-injection | 0.06 ± 0.04 | 0.07 ± 0.04 | 0.308 | 0.08 ± 0.04 | 0.16 ± 0.06 | 0.006 | |
| HbA1c differences compared to previous exams (%) | |||||||
| Highest increase | 0.8 ± 0.6 | 1.4 ± 1.2 | 0.121 | 1.2 ± 0.4 | 1.6 ± 0.7 | 0.132 | |
| Lowest increase | 0.2 ± 0.2 | 0.4 ± 0.4 | 0.654 | 0.3 ± 0.2 | 0.4 ± 0.5 | 0.223 | |
| Highest decrease | 0.7 ± 0.7 | 2.0 ± 1.0 | 0.001 | 1.3 ± 0.8 | 3.1 ± 1.9 | 0.006 | |
| Lowest decrease | 0.2 ± 0.1 | 0.5 ± 0.7 | 0.160 | 0.4 ± 0.3 | 0.7 ± 0.9 | 0.918 | |
| Highest absolute change | 0.9 ± 0.7 | 2.0 ± 1.0 | 0.003 | 1.6 ± 0.6 | 3.2 ± 1.8 | 0.003 | |
| Lowest absolute change | 0.1 ± 0.1 | 0.3 ± 0.3 | 0.436 | 0.2 ± 0.2 | 0.1 ± 0.1 | 0.072 | |
| Previous injection number | 2.6 ± 2.5 | 2.8 ± 2.9 | 0.944 | 1.2 ± 1.7 | 1.1 ± 1.3 | 0.973 | |
| Post injection number (6 months) | 0.8 ± 1.4 | 0.1 ± 0.3 | 0.265 | 0.6 ± 0.8 | 0.6 ± 1.0 | 0.973 | |
| Hb (g/dL) | 13.2 ± 2.4 | 11.4 ± 2.7 | 0.072 | 13.6 ± 2.8 | 11.4 ± 1.4 | 0.132 | |
| BUN (mg/dL) | 20.7 ± 11.2 | 23.1 ± 11.3 | 0.308 | 32.2 ± 22.2 | 26.8 ± 10.9 | 0.484 | |
| Creatinine (mg/dL) | 1.6 ± 1.8 | 1.5 ± 0.9 | 0.382 | 1.9 ± 1.8 | 1.7 ± 2.3 | 0.809 | |
| eGFR (mL/min×1.73 m2) | 71.1 ± 25.1 | 54.9 ± 35.6 | 0.265 | 67.7 ± 41.9 | 66.1 ± 38.7 | 0.654 | |
| Total cholesterol (mg/dL) | 149.9 ± 52.9 | 135.0 ± 34.7 | 0.555 | 140.3 ± 34.3 | 195.5 ± 45.3 | 0.006 | |
| LDL cholesterol (mg/dL) | 88.4 ± 35.0 | 84.4 ± 37.2 | 0.604 | 88.2 ± 24.9 | 118.5 ± 28.3 | 0.013 | |
| HDL cholesterol (mg/dL) | 45.2 ± 11.2 | 47.1 ± 7.3 | 0.443 | 35.9 ± 9.0 | 46.0 ± 13.0 | 0.114 | |
| TG (mg/dL) | 134.8 ± 78.6 | 127.7 ± 46.7 | 0.570 | 153.5± 71.2 | 264.8 ± 182.2 | 0.114 | |
| Baseline CMT (μm) | 436.9 ± 140.6 | 394.2 ± 103.0 | 0.495 | 421.3 ± 145.6 | 331.7 ± 68.8 | 0.061 | |
| CMTD_1 month (μm) | 122.4 ± 123.2 | 5.2 ± 37.0 | 0.027 | 29.5 ± 72.1 | 43.2 ± 63.2 | 0.557 | |
| CMTD_6 months (μm) | 44.3 ± 65.6 | 71.2 ± 96.1 | 0.553 | 51.7 ± 93.8 | -7.9 ± 128.2 | 0.968 | |
| Baseline BCVA (logMAR) | 0.5 ± 0.3 | 0.6 ± 0.4 | 0.796 | 0.7 ± 0.5 | 0.7 ± 0.6 | 0.809 | |
| VG_1 month | 0.1 ± 0.2 | 0.1 ± 0.1 | 0.654 | 0.3 ± 0.4 | 0.3 ± 0.4 | 0.973 | |
| VG_6 months | 0.1 ± 0.2 | 0.1 ± 0.2 | 0.591 | 0.2 ± 0.4 | 0.4 ± 0.3 | 0.720 | |
| Injection drug | |||||||
| Avastin | 13 (66.6) | 8 (75.0) | 0.759 | 6 (55.6) | 8 (70.0) | 0.605 | |
| Eylea | 5 (33.3) | 2 (25.0) | - | 3 (33.3) | 2 (20.0) | - | |
| Lucentis | 0 | 0 | - | 1 (11.1) | 1 (10.0) | - | |
| Macular edema type | |||||||
| Diffuse retinal thickening | 5 (26.7) | 2 (25.0) | 0.689 | 3 (33.3) | 7 (60.0) | 0.349 | |
| Cystoid macular edema | 9 (46.7) | 8 (75.0) | 4 (44.4) | 1 (10.0) | |||
| Serous retinal detachment | 4 (26.7) | 0 | 3 (22.2) | 3 (30.0) | |||
Values are presented as mean ± standard deviation or number (%).
HbA1c = glycated hemoglobin A; CV = coefficient of variation; Hb = hemoglobin; BUN = blood urea nitrogen; eGFR = estimated glomerular filtration rate; LDL = low density lipoprotein; HDL = high density lipoprotein; TG = triglyceride; CMT = central macular thickness; CMTD = central macular thickness difference; BCVA = best corrected visual acuity; VG = visual gain.
Table 3.
|
CMTD 1 months after injection |
VG 1 months after injection |
|||||||
|---|---|---|---|---|---|---|---|---|
| CHR (95% CI) | p-value* | aHR (95% CI) | p-value† | CHR (95% CI) | p-value* | aHR (95% CI) | p-value† | |
| Age (years) | 0.4 (-2.4 to 3.0) | 0.797 | - | - | -0.002 (-0.010 to 0.005) | 0.521 | - | - |
| Previous injection number | 19.6 (6.1 to 33.2) | 0.006 | 8.3 (-3.8 to 20.4) | 0.172 | 0.002 (-0.035 to 0.039) | 0.911 | - | - |
| Post injection number (6 months) | 5.7 (-23.7 to 35.1) | 0.696 | - | - | 0.090 (0.014 to 0.167) | 0.022 | 0.049 (-0.011 to 0.108) | 0.105 |
| Baseline CMT | 0.5 (0.4 to 0.7) | <0.001 | 0.5 (0.3 to 0.7) | <0.001 | 0.000 (-0.001 to 0.001) | 0.836 | - | - |
| Baseline BCVA (logMAR) | 7.1 (-59.2 to 73.4) | 0.829 | - | - | 0.421 (0.289 to 0.552) | <0.001 | 0.395 (0.261 to 0.528) | <0.001 |
| eGFR | -0.2 (-1.1 to 0.8) | 0.733 | - | - | 0.001 (-0.002 to 0.003) | 0.487 | - | - |
| Creatinine | 1.4 (-15.6 to 18.5) | 0.866 | - | - | -0.011 (-0.059 to 0.036) | 0.635 | - | - |
| BUN | 0.3 (-1.9 to 2.5) | 0.780 | - | - | 0.000 (-0.006 to 0.006) | 0.992 | - | - |
| Total cholesterol | -0.0 (-0.6 to 0.6) | 0.971 | - | - | 0.001 (-0.001 to 0.002) | 0.547 | - | - |
| LDL cholesterol | -0.1 (-1.0 to 0.8) | 0.836 | - | - | 0.000 (-0.002 to 0.003) | 0.699 | - | - |
| HDL cholesterol | 0.5 (-2.3 to 3.3) | 0.728 | - | - | 0.004 (-0.004 to 0.012) | 0.306 | - | - |
| Mean HbA1c_pre-injection | -21.6 (-47.4 to 4.2) | 0.098 | - | - | 0.052 (-0.019 to 0.122) | 0.148 | - | - |
| Mean HbA1c_post-injection | -25.1 (-54.8 to 4.5) | 0.094 | - | - | 0.060 (-0.023 to 0.142) | 0.150 | - | - |
| HbA1c CV_pre-injection | -311.6 (-675.7 to 52.5) | 0.075 | - | - | 0.374 (-0.668 to 1.415) | 0.430 | - | - |
| HbA1c CV_post-injection | -173.7 (-707.9 to 360.5) | 0.515 | - | - | 0.313 (-1.134 to 1.759) | 0.666 | - | - |
| Ranibizumab or Aflibercept (vs. bevacizumab) | 1.0 (0.9 to 1.0) | 0.297 | - | - | 1.520 (0.160 to 14.430) | 0.715 | - | - |
CMT = central macular thickness; CMTD = central macular thickness difference; VG = visual gain; CHR = crude hazard ratio; CI = confidence interval; aHR = adjusted hazard ratio; BCVA = best corrected visual acuity; logMAR = logarithm of the minimal angle of resolution; eGFR = estimated glomerular filtration rate; BUN = blood urea nitrogen; LDL = low density lipoprotein; HDL = high density lipoprotein; HbA1c = glycated hemoglobin A; CV = coefficient of variation.
Table 4.
|
CMTD 6 months after injection |
VG 6 months after injection |
|||
|---|---|---|---|---|
| CHR (95% CI) | p-value* | CHR (95% CI) | p-value* | |
| Age (years) | 0.6 (-1.9 to 3.2) | 0.614 | -0.003 (-0.010 to 0.004) | 0.406 |
| Previous injection number | 4.5 (-9.8 to 18.8) | 0.348 | -0.014 (-0.050 to 0.022) | 0.432 |
| Post injection number (6 months) | -0.7 (-29.3 to 28.0) | 0.962 | 0.091 (0.016 to 0.166) | 0.059 |
| Baseline CMT | 0.3 (0.0 to 0.5) | 0.023 | 0.000 (-0.001 to 0.001) | 0.938 |
| Baseline BCVA (logMAR) | -16.9 (-88.3 to 54.6) | 0.381 | 0.405 (0.253 to 0.556) | <0.001 |
| eGFR | 0.5 (-0.4 to 1.4) | 0.247 | 0.001 (-0.002 to 0.003) | 0.599 |
| Creatinine | -6.3 (-22.4 to 9.9) | 0.437 | -0.013 (-0.059 to 0.033) | 0.576 |
| BUN | -0.4 (-2.5 to 1.6) | 0.687 | 0.001 (-0.005 to 0.007) | 0.771 |
| Total cholesterol | -0.5 (-1.1 to 0.1) | 0.077 | 0.001 (-0.001 to 0.003) | 0.188 |
| LDL cholesterol | -0.7 (-1.6 to 0.2) | 0.106 | 0.002 (-0.001 to 0.004) | 0.212 |
| HDL cholesterol | 0.8 (-2.0 to 3.6) | 0.565 | 0.005 (-0.002 to 0.013) | 0.177 |
| Mean HbA1c_pre-injection | -9.3 (-39.4 to 20.7) | 0.534 | 0.037 (-0.049 to 0.124) | 0.385 |
| Mean HbA1c_post-injection | -13.7 (-44.6 to 17.1) | 0.373 | 0.020 (-0.070 to 0.110) | 0.652 |
| HbA1c CV_pre-injection | -7.5 (-383.7 to 368.7) | 0.968 | 0.375 (-0.678 to 1.427) | 0.476 |
| HbA1c CV_post-injection | -350.2 (-966.8 to 266.4) | 0.257 | 0.638 (-1.026 to 2.301) | 0.443 |
| Ranibizumab or aflibercept (vs. bevacizumab) | 1.0 (0.9 to 1.0) | 0.348 | 0.868 (0.062 to 12.096) | 0.916 |
CMT = central macular thickness; CMTD = central macular thickness difference; VG = visual gain; CHR = crude hazard ratio; CI = confidence interval; aHR = adjusted hazard ratio; BCVA = best corrected visual acuity; logMAR = logarithm of the minimal angle of resolution; eGFR = estimated glomerular filtration rate; BUN = blood urea nitrogen; LDL = low density lipoprotein; HDL = high density lipoprotein; HbA1c = glycated hemoglobin A; CV = coefficient of variation.




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




