 |
 |
| J Korean Ophthalmol Soc > Volume 61(6); 2020 > Article |
|
국문초록
목적
습성 연령관련황반변성 환자를 대상으로 재발 시 주사하는 방식(as-needed) 으로 치료를 시작하였으나 치료 경과 도중 지속주사 방식(proactive)으로 변경한 환자들의 장기 임상결과를 보고하고자 한다.
대상과 방법
본 후향적 연구는 습성 연령관련황반변성으로 진단 후 as-needed 방식으로 치료를 진행하던 중 proactive 방식으로 치료 방침을 변경하였던 23안을 대상으로 시행되었다. As-needed 기간과 proactive 기간을 서로 비교하였으며, 두 기간 사이에 연평균 주사 횟수 및 시력 변동의 정도를 추가적으로 비교하였다.
결과
평균 as-needed 기간은 17.9 ± 8.3개월이었으며, 평균 proactive 기간은 31.3 ± 13.2개월로 proactive 기간이 더 길었다(p<0.001). Proactive 기간의 연평균 주사 횟수(4.4 ± 1.0회)는 as-needed (2.8 ± 1.0)의 기간에 비해 더 높았다(p<0.001). As-needed 기간 동안 나타난 연평균 시력저하의 정도(0.08 ± 0.14)는 proactive 기간에 나타난 정도(0.04 ± 0.08)에 비해 약간 높았으나 그 차이는 유의하지 않았다(p=0.229).
ABSTRACT
Purpose
To evaluate long-term clinical outcomes in patients with neovascular age-related macular degeneration (AMD) who were treated with an as-needed regimen but were switched to a proactive regimen during the course of treatment.
Methods
This retrospective study included 23 eyes with neovascular AMD which were initially treated with an as-needed regimen, but switched to a proactive regimen during the course of treatment. The duration of the as-needed phase was compared to that of the proactive phase. In addition, the number of injections per year and the degree of visual deterioration per year were compared between the two phases.
Results
The duration of the as-needed and proactive phases were 17.9 ± 8.3 months and 31.3 ± 13.2 months, respectively. The duration of the proactive phase was significantly longer (p < 0.001). The number of injections per year during the proactive phase (4.4 ± 1.0) was significantly more than that during the as-needed phase (2.8 ± 1.0) (p < 0.001). The degree of visual deterioration per year during the as-needed phase (0.08 ± 0.14) was slightly greater than that during the proactive phase (0.04 ± 0.08). However, the difference was not statistically significant (p = 0.229).
Conclusions
The number of injections was higher after switching to the proactive regimen. However, the degree of visual deterioration was slightly lower than that noted during the as-needed phase. Further studies with a more controlled design are needed to determine more clearly the impact of switching treatment regimens on long-term clinical outcomes.
습성 연령관련황반변성(neovascular age-related macular degeneration)은 그 자연 경과가 매우 나쁜 질환으로 적절한 치료가 시행되지 않는 경우 심각한 시력손상이 발생하게 된다[1]. 과거에는 레이저광응고술이나 광역학요법(photodynamic therapy)이 주된 치료 방법으로 이용되었으나 보다 최근 항혈관내피성장인자 요법(anti-vascular endothelial growth factor therapy)이 도입되면서 그 치료 결과가 뚜렷하게 향상되었다[2-4].
습성 연령관련황반변성에 대한 항혈관내피성장인자 요법의 유용성을 증명한 주요 임상시험들인 Minimally Classic/Occult Trial of the Anti-VEGF Antibody Ranibizumab in the Treatment of Neovascular Age-Related Macular Degeneration (MARINA) study [2]와 VEGF Trap-Eye: Investigation of Efficacy and Safety in Wet AMD (VIEW) study [3]에서는 대부분의 안에서 치료 후 시력이 호전되거나 유지되는 결과를 보였다. 그러나 항혈관내피성장인자는 고가의 약제로 임상시험에서와 같이 1-2개월 간격으로 지속 주사하는 방법을 실제 진료 환경에서 적용하는 경우 환자의 경제적 부담이 매우 커지게 되어 보다 효율적인 치료방법의 필요성이 대두되었다.
As-needed 방법은 첫 3회 주사 후 경과 관찰하며 재발할 때에만 추가 주사를 시행하는 방법으로 약제를 효율적으로 이용할 수 있는 방법이다[5]. Treat-and-extend [6,7]로 대표되는 재발이 없는 경우에도 지속적으로 주사(proactive)하며, 검사 결과에 따라 병원 방문/주사 기간을 조절하는 방식 역시 보다 효율적으로 약제를 이용함과 동시에 병원 방문 횟수 도 감소시켜줄 수 있는 방법으로 널리 이용되고 있다. 이들 두 방법 모두 효과적으로 습성 연령관련황반변성을 치료할 수 있는 것으로 알려져 있으나 일부 연구들에서는 treat-and-extend 방식이 보다 나은 결과를 보일 수 있는 것으로 나타났다[8,9].
실제 임상에서 환자를 진료하다 보면 as-needed 방식으로 치료를 시작하였다 하더라도 치료 경과 도중 treat-and-extend와 같이 지속적으로 주사하는 방식으로 치료 방식을 변경하는 경우가 있다. 이렇게 치료 방식을 변경하는 경우의 임상결과에 대해서는 유럽을 중심으로 소수의 연구 결과만이 발표되어 있으며[10-12], 아직 국내 환자를 대상으로 한 연구 결과는 보고된 바 없다. 지속적으로 주사하는 방식은 국내에서도 널리 이용되는 추세에 있어 국내 환자를 대상으로 한 관련 분야의 연구가 필요한 실정이다. 결절맥락막혈관병증(Polypoidal choroidal vasculopathy) [13]은 결절 모양의 과형광 병변을 특징으로 하는 습성 연령관련황반변성의 한 행태로 동양인에서 주로 호발하는 것으로 알려져 있다[14]. 이에 본 연구에서는 결절맥락막혈광병증을 포함한 국내 습성 연령관련황반변성 환자를 대상으로 as-needed 방식으로 치료를 시작하였으나 치료 경과 도중 proactive 방식으로 변경한 환자들의 임상결과를 보고하고자 한다.
본 연구는 단일 기관에서 시행된 후향적 연구로 헬싱키선언에 입각하여 시행되었으며, Institutional Review Board (IRB) 승인을 획득하였다(Kim's Eye Hospital IRB, #2019-12-001). 2014년 5월부터 2015년 5월 사이에 4명의 의사에 의해 습성연령관련황반변성으로 진단되어 항혈관내피성장인자 치료를 시행 받은 환자들 중 as-needed 방식으로 치료하다 치료 경과 도중 proactive 방식으로 치료 방식을 변경한 환자들을 대상으로 후향적 의무기록 분석을 시행하였다.
다음과 같은 경우 연구에서 제외하였다; 1) 24개월 미만의 경과 관찰기간, 2) 첫 3회 주사 후 망막내액/망막하액이 완전히 가라앉지 않은 경우, 3) 심한 매체 혼탁, 4) 이전에 유리체망막수술을 받은 병력이 있는 경우, 5) 증식당뇨망막병증, 망막혈관폐쇄, 6) 황반원공이나 망막전막 등 황반미세구조와 시기능에 영향을 미칠 수 있는 기타 유리체망막 질환이 동반된 경우.
진단 시 환자의 최대교정시력을 측정하였으며, 세극등을 이용한 안저검사 및 빛간섭단층촬영(SLO-OCT®: OTI Ophthalmic Technologies Inc., Toronto, Canada; Spectralis®: Heidelberg Engineering, Dossenheim, Germany; RS 3000®: Nidek Co., Ltd., Tokyo, Japan)을 시행하였다. 또한 형광안저혈관조영술 및 인도시아닌그린혈관조영술을 시행하였다. 인도시아닌그린혈관조영술에서 분지혈관망을 동반하거나 동반하지 않는 결절 모양 과형광 병변이 관찰되는 경우 결절맥락막혈관병증으로 진단하였다. 연구에 포함된 환자들 중 결절맥락막혈관병증의 특징을 보이지 않은 환자들은 전형적 습성 연령관련황반변성으로 진단하였다.
모든 환자는 진단 후 1개월 간격으로 3회의 라니비주맙(0.5 mg/0.05 mL) 혹은 애플리버셉트(2.0 mg/0.05 mL) 주사를 시행 받았다. 유리체내 주사는 외래 수술실에서 시행되었다. 시술 전 0.5% proparacaine (Alcaine®, Alcon, Fort Worth, TX, USA)을 점안한 뒤 1.25% povidone iodine을 시술할 눈에 점안하고 속눈썹을 포함하여 눈 주위를 닦았다. 개검기를 끼우고 1.25% povidone iodine을 한 번 더 점안한 뒤 각막 윤부에서 3.0 mm 혹은 3.5 mm 하이측 사분면 혹은 상이측 사분면에 30게이지 일회용 바늘을 이용하여 애플리버셉트를 주사하였다.
첫 3회 주사 이후에는 재발할 때에만 주사하는 as-needed 방식을 이용하여 치료하였다. 1-2개월 간격으로 경과 관찰을 시행하였으며, 장기간 재발이 없던 경우 의사의 판단에 따라 3-4개월까지 경과 관찰간격을 연장하였다. 모든 환자들은 추적 관찰 시 세극등을 이용한 안저검사 및 빛간섭단층촬영을 시행하였다. 빛간섭단층촬영에서 중심와를 침범하거나 위협하는 망막하액/망막내액이 발생한 경우 혹은 안저검사에서 망막/망막하 출혈이 발생한 경우를 질환의 활동성이 재발한 것으로 판단하고 추가 주사를 시행하였다.
As-needed에 준한 치료 도중 보다 효과적인 치료가 필요하다고 판단된 경우 재발 유무와 관계 없이 지속적으로 주사하는 proactive 방법으로 치료 방법을 변경하였다. 모든 치료 방침 결정은 환자를 진료해 오던 의사가 계속 진행하였으며, 주사치료 역시 진료한 의사가 직접 시행하였다.
Proactive 치료는 검사 결과에 따라 망막내액/망막하액이 발생하거나 유지되는 경우 주사 사이 간격을 2주 단축하고, 이러한 소견이 관찰되지 않는 경우 주사 사이 간격을 2주 연장하는 treat-and-extend 방식[6]을 바탕으로 하였다. 그러나 본 연구에서는 주사 사이의 간격을 치료자의 판단에 따라 2-4주 간격으로 연장하고, 2-8주 간격으로 단축하는 수정된 방식을 이용하였다. 모든 환자는 첫 3회 주사 시 라니비주맙 혹은 애플리버셉트만을 이용하였으나 이후 치료부터는 베바시주맙(1.25 mg/0.05 mL) 약제도 의사의 판단에 따라 이용하였다.
As-needed 기간은 첫 3회 주사 후 망막하액/망막내액이 완전히 흡수된 것을 확인한 시점으로부터 마지막 as-needed 치료 후 바로 다음 방문에서 망막하액/망막내액이 완전히 흡수된 것을 확인한 시점까지로 정의하였다. Proactive 기간은 망막하액/망막내액이 관찰되지 않았음에도 주사를 시행한 첫 번째 시점으로부터 마지막 proactive 주사를 시행한 시점으로 정의하였다. 결과적으로 as-needed 종료 시점과 proactive 시작 시점은 동일하다. 진단 시, 3개월(최초 3회 주사 직후), as-needed 기간 종료 시점, proactive 기간 종료 시점에 측정된 최대교정시력을 서로 비교하였다. 추가적으로 as-needed 기간 동안의 1년 평균 주사 횟수 및 시력 변화량을 proactive 기간 동안의 값과 서로 비교하였다.
전형적 습성 연령관련황반변성과 결절맥락막혈관병증으로 진단된 환자를 대상으로 as-needed 기간, proactive 기간, as-needed 기간 동안의 1년 평균 주사 횟수 및 시력 변화량, proactive 기간 동안의 1년 평균 주사 횟수 및 시력 변화량을 양 군 사이에 서로 비교하였다. 또한 첫 3회 주사를 라니비주맙으로 시행한 환자를 라니비주맙군, 애플리버셉트로 시행한 환자를 애플리버셉트군으로 나누어 양 군 사이에 as-needed 기간, proactive 기간, as-needed 기간 동안의 1년 평균 주사 횟수 및 시력 변화량, proactive 기간 동안의 1년 평균 주사 횟수 및 시력 변화량을 서로 비교하였다. 추가적으로 전형적 습성 연령관련황반변성군과 결절맥락막 혈관병증군 내에서 3개월(최초 3회 주사 직후), as-needed 기간 종료 시점, proactive 기간 종료 시점에 측정된 최대교정시력을 서로 비교하였다.
통계 분석에는 SPSS Version 12.0 (SPSS Inc., Chicago, IL, USA)를 이용하였다. 전체 안을 대상으로 서로 다른 네 시점에 측정된 전반적인 평균값을 비교하는 데에는 repeated-measures analysis of variances (repeated-measures ANOVA) 방법을 이용하였으며, 네 시점 중 두 시점에서 측정된 값을 서로 비교하는 데에는 repeated-measures ANOVA 후 Bonferroni’s method를 이용하였다. As-needed 기간 및 proactive 기간 동안 측정된 값의 비교에는 independent samples t-test를 이용하였다. 전형적 습성 연령관련황반변성군과 결절맥락막혈관병증군 사이의 비교 및 라니비주맙군과 애플리버셉트군 사이의 비교에는 Mann-WhitneyU test를 이용하였다. 전형적 습성 연령관련황반변성군과 결절맥락막혈관병증군 내에서 시행한 시력 비교의 경우 Wilcoxon signed-ranks test 후 Bonferroni’s correction을 시행하였다. 0.05 미만의 p값을 통계적으로 유의한 값으로 정의하였다. 시력은 logarithm of minimal angle of resolution (logMAR) 값으로 바꾸어 분석에 이용하였다.
전체 23명(23안)의 환자를 대상으로 연구를 시행하였으며, 평균 연령은 70.1 ± 8.2세였다(Table 1). 12안은 전형적 습성 연령관련황반변성, 10안은 결절맥락막혈관병증으로 진단되었으며, 나머지 1명의 경우 인도사이아닌그린혈관조영술을 시행하지 않아 정확한 감별진단이 불가하였다.
평균 as-needed 기간은 17.9 ± 8.3개월이었으며, 상기 기간 동안 평균 4.3 ± 2.6회의 항혈관내피성장인자 주사가 시행되었다. 평균 proactive 기간은 31.3 ± 13.2개월이었으며, 상기 기간 동안 11.4 ± 5.1회의 주사가 시행되었다. 주사 사이 최대 간격은 1안에서 2.5개월, 8안에서 3개월, 7안에서 3.5개월, 7안에서 4개월이었다. As-needed 기간 동안의 연 평균 주사 횟수는 2.8 ± 1.0회였으며, proactive 기간 동안은 4.4 ± 1.0회였다. Proactive 기간이 as-needed 기간에 비해 유의하게 더 길었으며(p<0.001, independent samples t-test), proactive 기간 동안의 연평균 주사 횟수는 as-needed 기간에 비해 유의하게 더 높았다(p<0.001, independent samples t-test).
진단 시, 3개월, as-needed 기간 종료 시점, 및 proactive 기간 종료 시점에 측정된 logMAR 최대교정시력은 각각 0.45 ± 0.27, 0.27 ± 0.20, 0.39 ± 0.23, 0.50 ± 0.27이었다(Fig. 1). 네 시점에 측정된 시력에는 유의한 차이가 있었다(p=0.001, repeated-measures ANOVA). 3개월 시점과 비교하였을 때, as-needed 기간 종료 시점에 측정된 시력에는 유의한 차이가 없었으나(p=0.106, repeated-measures ANOVA with Bonferroni’s method), proactive 기간 종료 시점에 측정된 시력은 유의하게 악화되었다(p=0.007, repeated-measures ANOVA with Bonferroni’s method). As-needed 기간 종료 시점과 proactive 기간 종료 시점 사이에는 시력에 유의한 차이가 없었다(p=0.197, repeated-measures ANOVA with Bonferroni’s method). As-needed 기간 동안 연평균 0.08 ± 0.14의 시력저하가 나타났으며, proactive 기간 동안은 연평균 0.04 ± 0.08의 시력저하가 나타났다(p=0.229, Mann-WhitneyU test). Fig. 2는 본 연구에 포함된 안 중 대표 증례의 임상경과를 보여준다.
LogMAR 시력 0.3 이상의 뚜렷한 시력저하가 나타난 경우는 as-needed 기간 중 2안(8.7%), proactive 기간 중 3안(13.0%)이었다. As-needed 기간 중 시력저하가 나타난 2안 중 1안은 망막하출혈의 발생이 시력저하의 원인이었다. Proactive 기간 중 시력저하가 나타난 3안 중 2안은 망막하출혈의 발생이 시력저하의 원인이었으며, 나머지 1안의 경우 지도모양위축의 발생이 원인이었다. 지도모양위축이 발생한 안의 경우 as-needed 기간이 22개월, proactive 기간이 36개월이었다.
전형적 습성 연령관련황반변성으로 진단된 12안의 경우 as-needed 기간은 평균 18.8 ± 5.3개월이었으며, proactive 기간은 평균 37.3 ± 9.3개월이었다. 3개월, as-needed 기간 종료 시점 및 proactive 기간 종료 시점에 측정된 logMAR 최대교정시력은 각각 0.44 ± 0.24, 0.25 ± 0.17, 0.36 ± 0.18, 0.54 ± 0.23이었다(Fig. 3). 3개월 시력과 비교하였을 때, as-needed 기간 종료 시점(p=0.027) 및 proactive 기간 종료 시점(p=0.015)의 시력은 유의하게 악화되었으며, as-needed 기간 종료 시점과 proactive 기간 종료 시점의 시력에는 유의한 차이가 없었다(p=0.051).
결절맥락막혈관병증으로 진단된 10안의 경우 경우 as-needed 기간은 평균 17.7 ± 11.2개월이었으며, proactive 기간은 평균 25.1 ± 14.7개월이었다. 진단 시, 3개월, as-needed 기간 종료 시점, 및 proactive 기간 종료 시점에 측정된 logMAR 최대교정시력은 각각 0.44 ± 0.31, 0.25 ± 0.19, 0.39 ± 0.29, 0.43 ± 0.31이었다(Fig. 3). 3개월 시력은 as-needed 기간 종료 시점(p=0.294) 및 proactive 기간 종료 시점(p=0.165)의 시력과 유의한 차이가 없었으며, as-needed 기간 종료 시점과 proactive 기간 종료 시점의 시력 역시 유의한 차이가 없었다(p=1.000).
전형적 습성 연령관련황반변성군과 결절맥락막혈관병증군 사이의 비교 결과는 Table 2에 정리하였다. As-needed 기간의 경우 양 군 사이에 유의한 차이가 없었으나(p=0.418, Mann-WhitneyU test), proactive 기간의 경우 전형적 습성 연령관련황반변성군에서 유의하게 더 길었다(p=0.021, Mann-WhitneyU test). As-needed 기간 및 proactive 기간 동안 시행된 연평균 주사 횟수는 전형적 습성 연령관련 황반변성군에서 2.9 ± 0.9회 및 4.4 ± 0.9회로 결절맥락막혈관병증군에서 시행된 연평균 2.9 ± 0.9회(p=0.923, Mann-WhitneyU test) 및 4.6 ± 0.9회(p=0.582, Mann-WhitneyU test)와 유의한 차이가 없었다. As-needed 기간 및 proactive 기간 동안의 연평균 logMAR 시력 변화량은 전형적 습성 연령관련황반변성군에서 0.07 ± 0.07 및 0.06 ± 0.09로 결절맥락막혈관병증군에서 나타난 연평균 0.09 ± 0.19 (p=0.974) 및 0.01 ± 0.07 (p=0.069, Mann-WhitneyU test)와 유의한 차이가 없었다.
라니비주맙군과 애플리버셉트군 사이의 비교에서는 as-needed 기간(p=0.101, Mann-WhitneyU test), proactive 기간(p=0.648, Mann-WhitneyU test), as-needed 기간 동안의 1년 평균 주사 횟수(p=0.693, Mann-WhitneyU test) 및 시력 변화량(p=0.879, Mann-WhitneyU test), proactive 기간 동안의 1년 평균 주사 횟수(p=0.446, Mann-WhitneyU test) 및 시력 변화량(p=0.976, Mann-WhitneyU test)에 유의한 차이가 없었다(Table 3).
As-needed 방식은 습성 연령관련황반변성에서 보다 효율적인 항혈관내피성장인자 약제의 이용을 위해 본격적으로 도입된 최초의 방법이다[5]. Fung et al [5]은 첫 3회 주사 후 매달 경과 관찰하며 재발할 때에만 주사하는 방법을 통해 매달 주사하는 방법과 비슷한 수준의 치료 결과를 얻을 수 있었는데, 주사 횟수는 1년 간 평균 5.6회로 매달 주사하는 방법에 비해 뚜렷하게 감소하였다[5].
그러나 as-needed 방식은 매달 병원을 방문해야 한다는 제한점이 있었는데, 이후 도입된 treat-and-extend 방식[6,7]은 주사 횟수뿐 아니라 병원 방문 횟수 역시 줄여줄 수 있는 방법으로 소개되었다. Treat-and-extend 방식을 이용하는 경우 매 방문 시 재발 여부와 관계 없이 지속적인 주사를 시행하는데, 빛간섭단층촬영 결과에서 망막하액이나 망막내액이 관찰되는 경우 다음 방문까지의 기간을 2주 단축하고, 이러한 소견이 나타나지 않는 경우 다음 방문까지의 기간을 2주 연장하게 된다. 제3형 혈관신생(type 3 neovascularization)을 대상으로 한 Engelbert et al [6]의 연구에서 매년 평균 약 6-7회의 주사를 시행하였으며, 그 결과 36개월의 추적 관찰 기간 동안 시력이 유지되는 좋은 결과를 보였다.
As-needed 방식과 treat-and-extend 방식을 서로 비교하였을 때, 효율성의 측면에서 재발이 나타날 때에만 주사하는 as-needed 방식이 더 우월할 수 있다. 실제로 습성 연령 관련황반변성 환자의 일부는 초기 치료 후 장기간 재발이 없기 때문에, 이런 환자들에서 처음부터 treat-and-extend 방식을 이용하는 경우 불필요한 주사가 시행될 수 있다는 우려도 제기되어 왔다[15,16]. 그러나 시력을 유지하고 호전시키는 효과의 측면에서는 지속적인 주사를 통해 재발 자체를 억제하여 망막 손상이 누적되는 것을 최소화할 수 있는 treat-and-extend 방식이 조금 더 우월한 결과를 보였다[8,9]. 실제 진료 환경에서 as-needed 방식을 이용하는 경우 시간의 경과와 함께 지속적인 시력저하가 나타나는 경우가 많은 반면[17], treat-and-extend 방식을 이용하는 경우 장기간 동안 호전된 시력이 유지되는 결과가 보고되었다[18]. 이와 같은 결과를 고려하였을 때, as-needed 방식으로 치료를 시작하였다고 하더라도 보다 효과적인 시력보전이 필요할 경우 treat-and-extend 방식으로 치료 방법을 바꾸어 볼 수 있을 것으로 생각된다.
Hatz and Prünte [10]의 연구에 따르면 as-needed에서 treat-and-extend로 치료 방식을 바꾼 후 시력이 호전되고 장기간 유지되었을 뿐 아니라 중심망막두께 역시 변동의 폭이 줄어들면서 장기간 안정되는 결과를 보였다. 이와 같은 결과를 바탕으로 Hatz and Prünte [10]은 treat-and-extend로의 치료 방식 변화를 통해 더 나은 치료 결과를 얻을 수 있을 뿐 아니라 자주 병원을 방문하는 데에서 기인한 환자들의 부담을 역시 줄여줄 수 있다고 주장하였다.
비슷한 주제의 연구를 시행한 Giannakaki-Zimmermann et al [11]에 따르면 treat-and-extend로 치료 방식을 바꾸면서 주사 횟수는 더 늘어났으나 시력이 안정되고 중심망막두께는 뚜렷하게 감소하는 경향을 보였다. Kvannli and Krohn [12]의 연구에서는 treat-and-extend로 치료 방식을 바꾼 후 중심망막두께에는 변화가 없었으나 시력이 뚜렷하게 호전되는 경향이 나타났다.
국내 환자를 대상으로 한 본 연구에서 주사 횟수의 경우 as-needed 기간 동안 평균 1년에 2.8회에서 proactive 기간 동안 평균 1년에 4.4회로 뚜렷하게 증가하였다. Proactive 기간 동안 나타난 시력의 변화는 as-needed 기간 동안 나타난 값과 큰 차이가 없었다. 그러나 as-needed 기간(평균 17.9개월)에 비해, proactive 기간(평균 31.3개월)이 뚜렷하게 더 길었다는 점을 고려하였을 때, proactive 치료가 장기간 안정적인 시력 유지에 있어서 어느 정도 효과가 있음을 시사하는 결과로 생각된다.
본 연구에서는 전체 환자의 13.0%에서 proactive 기간 동안 logMAR 0.3 이상의 뚜렷한 시력저하가 나타났으며, 그 원인은 황반하출혈과 지도모양위축으로 확인되었다. 습성 연령관련황반변성에서 치료 도중 나타나는 망막하출혈의 발생은 좋지 않은 임상결과와 연관된 것으로 알려져 있다[19,20]. 습성 연령관련황반변성에서 출혈의 발생은 병변의 재발을 의미하며, 주사 치료가 필요한 상황으로 인식되어 왔다[5]. 따라서 지속적인 주사를 통해 재발 자체를 억제하는 방법은 출혈의 발생 위험 역시 저하시킬 수 있을 것으로 추측된다. 과거 treat-and-extend 방식을 이용하여 처음부터 환자를 치료하였던 Engelbert et al [6]의 연구에서는 출혈의 발생이 보고되지 않았으며, Hatz and Prünte [10]의 연구에서 역시 treat-and-extend로 치료 방식을 변경하고 난 이후에는 시력을 위협하는 출혈의 발생은 나타나지 않았다. 본 연구의 결과가 기존의 결과와 조금 다르게 나타난 이유는 확실하지 않다. 망막하출혈이 발생하였던 두 환자 모두 최대주사간격은 3개월로 유지되고 있던 상태였으며, 이는 일반적으로 treat-and-extend 방식을 이용할 때 설정하는 최대주사 간격[6,7]과 차이가 없었다. 향후 보다 많은 안을 대상으로 한 연구를 통해 proactive 치료에도 불구하고 출혈이 발생하는 안의 특성과 위험인자를 확인하고자 하는 시도가 필요할 것이다.
지도모양위축의 발생은 습성 연령관련황반변성의 치료 과정 중 드물지 않게 나타나는 소견으로[21] 시력의 저하를 유발할 수 있는 것으로 알려져 있다. 일부 연구에서는 항혈관내피성장인자 주사를 자주 시행하는 것이 지도모양위축의 위험을 증가시킬 수 있는 것으로 나타났다[21,22]. 본 연구에서는 as-needed 기간에 비해 proactive 기간 동안 주사 횟수가 뚜렷하게 증가하였는데, 이러한 주사 횟수의 증가가 지도모양위축의 진행을 촉진시켰을 가능성을 배제할 수 없다. 그러나 주사 횟수의 증가와 지도모양위축의 발생과의 연관성은 아직 논란의 여지가 있으며[23], 본 연구에서 지도 모양위축이 발생한 환자의 경우 proactive 기간(36개월)이 as-needed 기간(22개월)에 비해 훨씬 길었다는 결과를 고려하였을 때, 지도모양위축의 발생이 단순히 주사 횟수의 증가와 관련된 결과가 아닐 수 있다.
결절맥락막혈관병증이 습성 연령관련황반변성의 한 아형인지 아니면 습성 연령관련황반변성과 뚜렷하게 구분되는 질환인지에 대해서는 아직 완전한 결론이 내려지지는 않은 상태이다. 최근 Li et al [24]은 결절맥락막혈관병증 환자의 조직병리 소견을 분석하였으며, 그 결과 결절맥락막혈관병증 역시 혈관의 팽대(aneurysm)를 특징으로 하는 제1형 혈관신생(type 1 neovascularization)의 한 형태라 주장하였다. 그러나 습성 연령관련황반변성과 비교하였을 때, 결절맥락막혈관병증은 발생하는 안의 특성에 차이가 있고[25], 덜 파괴적인 자연 경과를 보이며[26], 항혈관내피성장인자에 불충분한 반응을 보이는 경우도 적지 않은 것으로 보고되어[27] 치료 방침 선택에 있어서 이러한 차이점을 고려해야 한다.
본 연구에서는 as-needed에서 proactive로 치료 방식을 변경하였을 때의 임상결과에 있어서 전형적 습성 연령관련 황반변성과 결절맥락막혈관병증 사이에 차이가 있는가에 대하여 분석하였는데, 전반적인 주사 횟수나 as-needed 기간 동안의 연간 시력 변화량에는 거의 차이가 없었다. 그러나 proactive 기간 동안의 연간 시력 변화량의 경우 전형적 습성 연령관련황반변성군에서 평균 0.06, 결절맥락막혈관병증군에서 평균 0.01로 어느 정도 차이를 보였다. 비록 통계적으로 유의한 차이는 아니었으나 이는 소수의 안을 대상으로 분석을 시행한 데에서 비롯된 결과일 수 있다. 그러나 전형적 습성 연령관련황반변성군에서 proactive 기간이 유의하게 더 길었다는 점을 고려하였을 때, 본 연구의 결과를 바탕으로 양 군 간에 차이를 확정하기는 어려울 것으로 판단된다.
본 연구의 제한점은 다음과 같다. 본 연구는 실제 진료 환경에서 치료한 결과를 바탕으로 한 후향적 연구로 비교적 소수의 안을 대상으로 시행되었다. As-needed 기간 동안 Fung et al [5]의 연구에서와 같은 매달 경과 관찰하는 방법이 엄격하게 이루어지지 않았으며, proactive 기간 동안 역시 Engelbert et al [6]의 연구에서와 같이 2주 간격으로 엄격하게 경과 관찰 일정을 조정하는 방법이 시행되지 않았다. 따라서 본 연구의 결과는 엄격한 as-needed 방식에서 엄격한 treat-and-extend 방식으로 치료 방식을 변경하는 경우를 반영하기는 어려울 것으로 생각된다. 추가적으로 본 연구에서는 라니비주맙, 애플리버셉트, 베바시주맙 세 약제가 혼용되었다. 비록 세 약제 모두 황반변성의 치료에 있어서 효과적인 약제이나 약제 효과에 약간의 차이가 있는 것으로 알려져 있어[28,29], 이 차이가 연구 결과에 영향을 주었을 가능성을 배제할 수 없을 것이다. 마지막으로 본 연구에는 대조군이 따로 설정되지 않았다. 본 후향적 연구에서는 proactive 치료로 전환하는 데 있어서 일관된 기준이 없었으며, 의사의 판단에 따라 환자와 토의 후 치료 방침을 변경하였기에 적절한 대조군을 설정하기 어려운 면이 있었다. 지속적으로 as-needed 치료를 시행 받은 군과의 적절한 비교를 위해서는 향후 전향적으로 통제된 연구가 필요할 것이다.
요약하면 본 연구에서는 습성 연령관련황반변성으로 진단 후 as-needed 방식으로 항혈관내피성장인자 치료를 받던 환자에서 proactive 방식으로 치료 방식을 바꾼 경우의 임상결과를 분석하였다. 평균 31.3개월의 비교적 긴 proactive 기간 동안 평균 logMAR 0.11 정도로 경도의 시력저하가 나타났으며, logMAR 0.3 이상의 시력저하를 보인 안은 13.0%에 불과하였다. 평균 17.9개월의 as-needed 기간 동안 비슷한 정도의 시력저하가 나타났다는 점을 고려하였을 때, as-needed 방식으로 치료 받던 환자에서 proactive 방식으로 치료 방식을 변경하는 것은 장기간 시력을 유지하는 데 있어서 어느 정도 유용한 방법으로 생각된다. 전형적 습성 연령관련황반변성과 결절맥락막혈관병증 사이에 유의한 치료 경과의 차이는 없었으나 본 연구의 제한점들을 고려하였을 때, 이를 보다 정확하게 확인하기 위해서는 추가 연구가 필요할 것으로 생각된다.
Figure 1.
Changes in logarithm of minimal angle of resolution (logMAR) best-corrected visual acuity (BCVA) in the included eyes. The BCVA after as-needed phase was not significantly different from the baseline value and the BCVA after proactive phase was not significantly different from that after as-needed phase. Statistical analysis was performed using repeated-measures analysis of variances with a Bonferroni’s method.
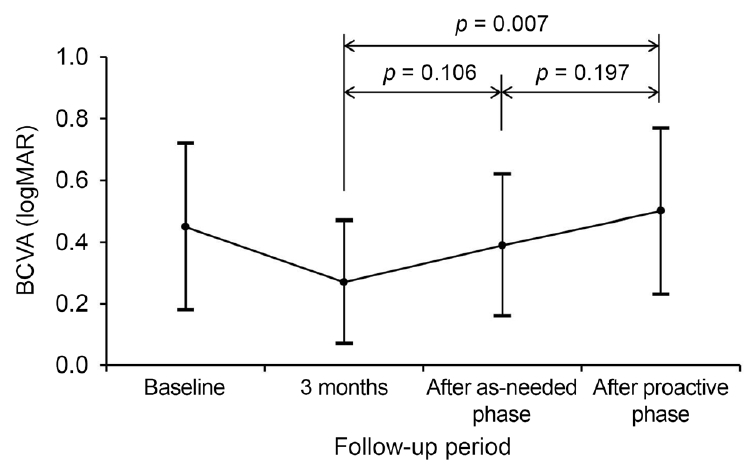
Figure 2.
A representative case showing clinical course of a 71-year-old patient who was diagnosed with neovascular age-related macular degeneration. At diagnosis (A, B), the best-corrected visual acuity (BCVA) was 0.6. After three loading injections using aflibercept (C), retinal/subretinal fluid was completely resolved and the BCVA was improved to 0.7. The patient was followed-up without additional injection. Six months after the third injection (D), reactivation of the lesion was noted and additional injection was administered. The as-needed basis retreatment was continued up to 27 months after the third injection and 8 injections were performed during this period. At 27 months (E), the BCVA was measured as 0.5. At this time, the treatment regimen was changed to proactive regimen and the first proactive injection was performed. Nine injections were performed during the 25-month of proactive period. The BCVA was maintained as 0.5 when the last proactive injection was performed (F).
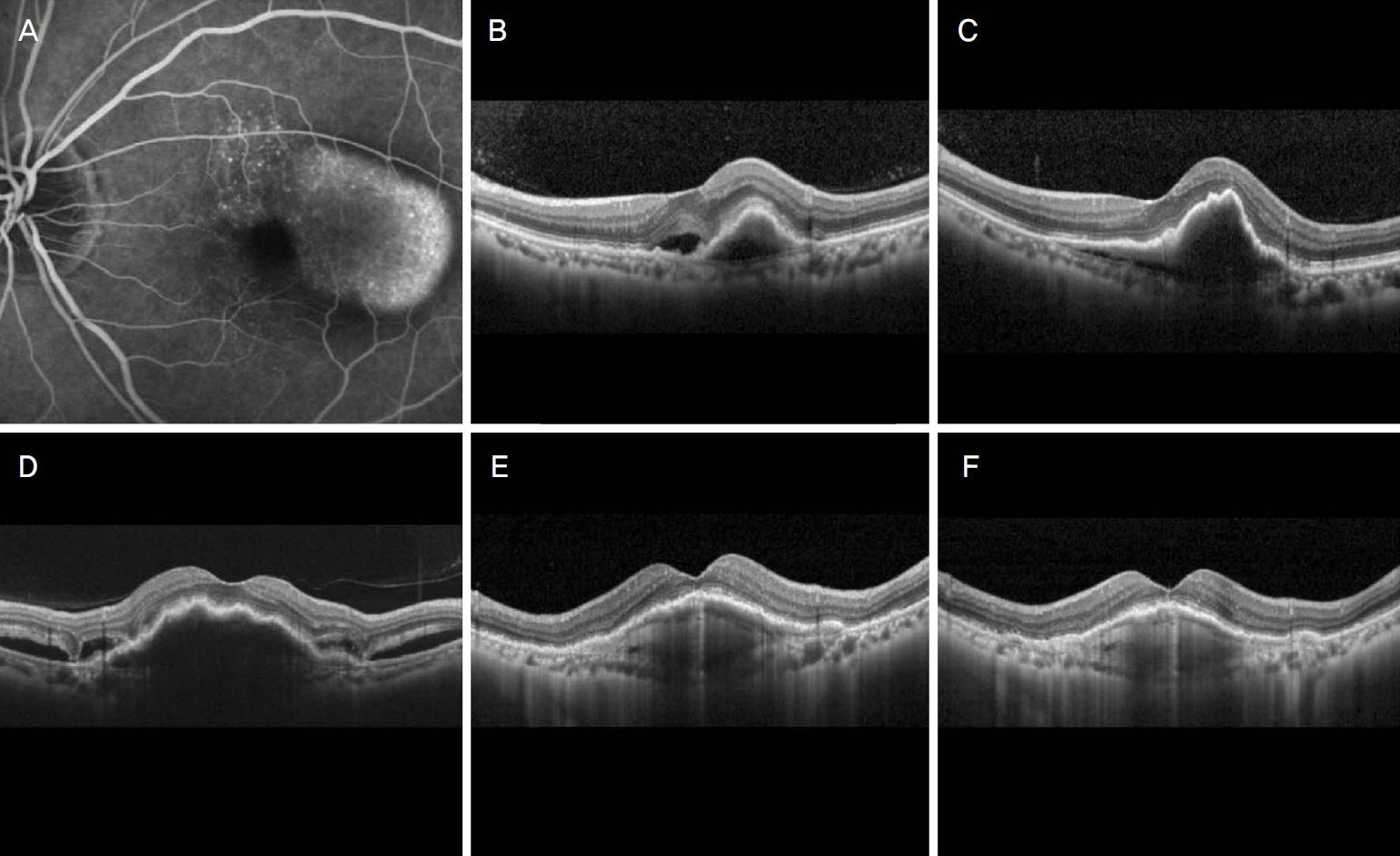
Figure 3.
Changes in logarithm of minimal angle of resolution (logMAR) best-corrected visual acuity (BCVA), according to the follow-up period. The BCVA during the proactive phase maintained relatively stable in polypoidal choroidal vasculopathy group (n = 10, dotted line) than typical neovascular age-related macular degeneration group (n = 12, solid line). However, the degree of change in BCVA during the proactive phase was not significantly different between the 2 groups (p = 0.069, Mann-WhitneyU test). Presented p-values were derived from Wilcoxon signed-ranks test with a Bonferroni’s correction.

Table 1.
Baseline characteristics of the included patients (n = 23)
Table 2.
Comparison of characteristics between typical neovascular AMD group and polypoidal choroidal vasculopathy group
| Characteristic | Typical neovascular AMD (n = 12) | PCV (n = 10) | p-value* |
|---|---|---|---|
| Duration of as-needed phase (months) | 18.8 ± 5.3 | 17.7 ± 11.2 | 0.418 |
| Duration of proactive phase (months) | 37.3 ± 9.3 | 25.1 ± 14.7 | 0.021 |
| Number of injections/years | |||
| During as-needed phase | 2.9 ± 0.9 | 2.9 ± 0.9 | 0.923 |
| During proactive phase | 4.4 ± 0.9 | 4.6 ± 0.9 | 0.582 |
| Changes in logMAR BCVA | |||
| During as-needed phase | 0.07 ± 0.07 | 0.09 ± 0.19 | 0.974 |
| During proactive phase | 0.06 ± 0.09 | 0.01 ± 0.07 | 0.069 |
Table 3.
Comparison of characteristics between ranibizumab group and aflibercept group
| Characteristic | Ranibizumab group (n = 10) | Aflibercept group (n = 13) | p-value* |
|---|---|---|---|
| Duration of as-needed phase | 19.9 ± 6.3 | 15.2 ± 6.9 | 0.101 |
| Duration of proactive phase | 31.6 ± 10.9 | 32.2 ± 14.1 | 0.648 |
| Number of injections/years | |||
| During as-needed phase | 2.8 ± 0.8 | 2.9 ± 1.1 | 0.693 |
| During proactive phase | 4.2 ± 0.8 | 4.6 ± 1.1 | 0.446 |
| Changes in logMAR BCVA | |||
| During as-needed phase | 0.06 ± 0.08 | 0.09 ± 0.17 | 0.879 |
| During proactive phase | 0.05 ± 0.11 | 0.03 ± 0.05 | 0.976 |
REFERENCES
1) Pauleikhoff D. Neovascular age-related macular degeneration: natural history and treatment outcomes. Retina 2005;25:1065-84.


2) Rosenfeld PJ, Brown DM, Heier JS, et al. Ranibizumab for neovascular age-related macular degeneration. N Engl J Med 2006;355:1419-31.


3) Heier JS, Brown DM, Chong V, et al. Intravitreal aflibercept (VEGF trap-eye) in wet age-related macular degeneration. Ophthalmology 2012;119:2537-48.


4) Sloan FA, Hanrahan BW. The effects of technological advances on outcomes for elderly persons with exudative age-related macular degeneration. JAMA Ophthalmol 2014;132:456-63.



5) Fung AE, Lalwani GA, Rosenfeld PJ, et al. An optical coherence tomography-guided, variable dosing regimen with intravitreal ranibizumab (Lucentis) for neovascular age-related macular degeneration. Am J Ophthalmol 2007;143:566-83.


6) Engelbert M, Zweifel SA, Freund KB. “Treat and extend” dosing of intravitreal antivascular endothelial growth factor therapy for type 3 neovascularization/retinal angiomatous proliferation. Retina 2009;29:1424-31.


7) Freund KB, Korobelnik JF, Devenyi R, et al. Treat-and-extend regimens with anti-vegf agents in retinal diseases: a literature review and consensus recommendations. Retina 2015;35:1489-506.


8) Okada M, Kandasamy R, Chong EW, et al. The treat-and-extend injection regimen versus alternate dosing strategies in age-related macular degeneration: a systematic review and meta-analysis. Am J Ophthalmol 2018;192:184-97.


9) Augsburger M, Sarra GM, Imesch P. Treat and extend versus pro re nata regimens of ranibizumab and aflibercept in neovascular age-related macular degeneration: a comparative study. Graefes Arch Clin Exp Ophthalmol 2019;257:1889-95.


10) Hatz K, Prünte C. Changing from a pro re nata treatment regimen to a treat and extend regimen with ranibizumab in neovascular age-related macular degeneration. Br J Ophthalmol 2016;100:1341-5.


11) Giannakaki-Zimmermann H, Ebneter A, Munk MR, et al. Outcomes when switching from a pro re nata regimen to a treat and extend regimen using aflibercept in neovascular age-related macular degeneration. Ophthalmologica 2016;236:201-6.


12) Kvannli L, Krohn J. Switching from pro re nata to treat-and-extend regimen improves visual acuity in patients with neovascular age-related macular degeneration. Acta Ophthalmol 2017;95:678-82.


13) Yannuzzi LA, Sorenson J, Spaide RF, Lipson B. Idiopathic polypoidal choroidal vasculopathy (IPCV). Retina 1990;10:1-8.


14) Byeon SH, Lee SC, Oh HS, et al. Incidence and clinical patterns of polypoidal choroidal vasculopathy in Korean patients. Jpn J Ophthalmol 2008;52:57-62.


15) Kim JH, Chang YS, Kim JW, et al. Recurrence in patients with type 3 neovascularization (retinal angiomatous proliferation) after intravitreal ranibizumab. Retina 2017;37:1508-15.


16) Kuroda Y, Yamashiro K, Miyake M, et al. Factors associated with recurrence of age-related macular degeneration after anti-vascular endothelial growth factor treatment: a retrospective cohort study. Ophthalmology 2015;122:2303-10.


17) Holz FG, Tadayoni R, Beatty S, et al. Multi-country real-life experience of anti-vascular endothelial growth factor therapy for wet age-related macular degeneration. Br J Ophthalmol 2015;99:220-6.


18) Adrean SD, Chaili S, Ramkumar H, et al. Consistent long-term therapy of neovascular age-related macular degeneration managed by 50 or more anti-VEGF injections using a treat-extend-stop protocol. Ophthalmology 2018;125:1047-53.


19) Cho JH, Ryoo NK, Cho KH, et al. Incidence rate of massive submacular hemorrhage and its risk factors in polypoidal choroidal vasculopathy. Am J Ophthalmol 2016;169:79-88.


20) Chang YS, Kim JH, Kim JW, et al. Development of submacular hemorrhage in neovascular age-related macular degeneration: influence on visual prognosis in a clinical setting. Korean J Ophthalmol 2018;32:361-8.



21) Grunwald JE, Daniel E, Huang J, et al. Risk of geographic atrophy in the comparison of age-related macular degeneration treatments trials. Ophthalmology 2014;121:150-61.


22) Grunwald JE, Pistilli M, Ying GS, et al. Growth of geographic atrophy in the comparison of age-related macular degeneration treatments trials. Ophthalmology 2015;122:809-16.


23) Abdelfattah NS, Al-Sheikh M, Pitetta S, et al. Macular atrophy in neovascular age-related macular degeneration with monthly versus treat-and-extend ranibizumab: findings from the TREX-AMD trial. Ophthalmology 2017;124:215-23.


24) Li M, Dolz-Marco R, Messinger JD, et al. Clinicopathologic correlation of aneurysmal type 1 neovascularization in age-related macular degeneration. Ophthalmol Retina 2019;3:99-111.


25) Chung SE, Kang SW, Lee JH, Kim YT. Choroidal thickness in polypoidal choroidal vasculopathy and exudative age-related macular degeneration. Ophthalmology 2011;118:840-5.


26) Uyama M, Wada M, Nagai Y, et al. Polypoidal choroidal vasculopathy: natural history. Am J Ophthalmol 2002;133:639-48.


27) Cho M, Barbazetto IA, Freund KB. Refractory neovascular age-related macular degeneration secondary to polypoidal choroidal vasculopathy. Am J Ophthalmol 2009 148:70-8. e1.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




