치료 병력이 없는 85세 이상 습성 나이관련황반변성 환자들의 치료 결과
Treatment Results of Treatment-naïve Neovascular Age-related Macular Degeneration in Patients Over 85 Years of Age
Article information
Abstract
목적
85세 이상 치료 병력이 없는 습성 나이관련황반변성 환자들의 특성 및 치료 결과를 보고하고자 한다.
대상과 방법
습성 나이관련황반변성으로 처음 진단된 환자들 중 진단 당시 85세 이상이었고, 최소 12개월 이상 추적 관찰 가능하였던 대상의 의무기록을 후향적으로 분석하였다. 전체 기간 동안 유리체강 내 주사 횟수와 주사 약제의 종류를 조사하였다. 치료 전과 후의 최대교정시력과 빛간섭단층촬영 결과를 조사 및 분석하였고, 추가적으로 초진 시 반대안의 시력도 수집하였다.
결과
총 40명 40안이 연구에 포함되었고, 평균 연령은 87.5 ± 2.4세였다. 초진 시 연구안의 평균 logarithm of minimal angle of resolution (logMAR) 최대교정시력은 0.85 ± 0.57이었고, 반대안의 경우 평균 0.93 ± 0.99였다. 유리체강 내 주사 치료 후 시력은 치료 전과 비교하여 유의한 차이를 보이지 않았다. 중심망막두께의 경우 치료 후 모든 시기에서 치료 전에 비해 유의한 호전을 보였다.
결론
초진 시 나이가 85세 이상의 환자에서도 유리체강 내 주사 치료를 통해 시력의 악화를 막을 수 있었고 성공적인 해부학적 결과를 얻을 수 있었다. 특히 반대안의 시력이 나쁜 경우가 많아 시력의 유지가 의미 있을 것으로 생각되어, 고령에서도 적극적인 치료가 필요하다.
Trans Abstract
Purpose
To investigate the characteristics and treatment results of patients aged ≥ 85 years who were diagnosed with treatment-naïve neovascular age-related macular degeneration (nAMD).
Methods
The medical records of patients diagnosed with treatment-naïve nAMD who were ≥ 85 years old at the time of diagnosis with at least 12 months follow-up were retrospectively reviewed. The number of intravitreal injections of anti-vascular endothelial growth factor (VEGF) and agents used during the entire period were investigated. Best-corrected visual acuity and optical coherence tomography results before and after treatment were analyzed. Visual acuity of the fellow eye was also collected.
Results
A total of 40 eyes of 40 patients with mean age of 87.5 ± 2.4 were included in the study. The mean logarithm of the minimal angle of resolution visual acuity was 0.85 ± 0.57, and the mean of the fellow eye was 0.93 ± 0.99. Compared to before the treatment, there was no significant difference after intravitreal injection in terms of visual acuity. Central retinal thickness showed significant reduction at all time points after treatment.
Conclusions
In patients aged ≥ 85 years at the time of diagnosis, intravitreal injections of anti-VEGF prevented deterioration of visual acuity and showed successful anatomical outcomes. Especially, many had poor visual acuity in the fellow eye, suggesting the importance of maintaining visual acuity. Therefore, active treatment is necessary in the elderly.
나이관련황반변성은 비교적 고연령층에서 황반부에 드루젠이라고 하는 침착물들과 다양한 형태의 변성이 오는 질환으로, 후기로 진행될 경우 황반부 위축이나 맥락막신생혈관이 발생하여 심한 시력상실을 초래하게 된다. 선진국에서 실명의 주요 원인 중 하나이고, 발생 기전은 다양한 인자들이 관여하는 복합적인 과정으로 받아들여지고 있으며, 그중 가장 중요한 위험인자는 노화이다.1
통계청 발표 자료에 의하면 2020년 국민 기대수명은 83.5년으로 10년 전보다 3.26년 증가하였다.2 의료기술의 발달과 풍부한 영양 섭취로 기대수명은 계속 소폭 증가할 것으로 전망되고, 기대수명이 증가하면서 노인 인구 또한 증가할 것으로 예상된다. 우리나라 국민건강영양조사 자료를 이용한 연구에서, 후기 황반변성의 유병률을 10세 간격으로 나누어 분석해본 결과 80대 이상에서 다소 급격하게 증가하였다.3 점차 증가하는 노인 인구와 80세 이후 가파른 유병률의 증가를 보이는 질병의 특성을 고려하면, 향후 유병률은 더욱 증가할 것으로 생각된다.
현재까지 습성 나이관련황반변성에 대한 수많은 연구 결과들이 발표되었음에도 불구하고 연구에 포함된 대부분의 환자들(82.2-86.8%)은 85세 미만이었다.4-6 우리나라에서 고령의 습성 나이관련황반변성 환자들의 특성을 조사한 연구가 보고된 바 있으나, 처음 진단받은 환자가 아니었으며 단기적 결과만 있었다.7 이에 본 연구에서는 85세 이상 치료 병력이 없는 습성 나이관련황반변성 환자들의 특성 및 치료 결과를 보고하고자 한다.
대상과 방법
본 연구는 다기관 후향적 관찰 연구로 헬싱키선언을 준수하였으며, 기관생명윤리위원회 승인을 획득하였다(HPIRB 2022-08-018). 2011년 1월 1일부터 2021년 5월 31일까지 인제대학교 해운대백병원과 인제대학교 부산백병원, 고신대학교 복음병원에서 습성 나이관련황반변성으로 처음 진단된 환자들 중 진단 당시 85세 이상이었고, 최소 12개월 이상 추적 관찰 가능하였던 대상의 의무기록을 후향적으로 분석하였다. 황반변성 외의 시력저하를 일으킬 만한 유의한 안과적 질환이 있는 경우 대상에서 제외하였다.
모든 환자들의 치료 전 전신 질환의 과거력과 안과적 질환의 과거력을 확인하였다. 진단 시 환자의 최대교정시력, 세극등현미경검사, 안저검사, 안저촬영(TRC-NW8 [Topcon, Tokyo, Japan], Nonmyd7 [Kowa, Tokyo, Japan], TRC-50DX [Topcon]), 빛간섭단층촬영(Cirrus HD-OCT [Carl Zeiss Meditec, Dublin, CA, USA], DRI OCT-1 [Topcon], Spectralis OCT [Heidelberg Engineering, Heidelberg, Germany]), 형광안저혈관조영술과 인도시아닌그린혈관조영술(Spectralis HRA, Heidelberg Engineering)을 조사하였다. 인도시아닌그린혈관조영술의 결과에 따라 습성 나이관련황반변성의 세부 분류를 조사하였다. 인도시아닌그린혈관조영술에서 분지혈관망을 동반하는 결절모양 과형광병변이 관찰되는 경우 결절맥락막혈관병증으로 진단하였고, 망막-망막 혹은 망막-맥락막혈관 문합이 관찰되는 경우 망막혈관종성증식으로 진단하였으며, 결절맥락막혈관병증이나 망막혈관종성증식으로 분류되지 않은 나머지 경우를 전형적 습성 나이관련황반변성으로 분류하였다. 초진 시 반대안의 최대교정시력을 수집하여 0.5 미만이 확인되었을 경우, 시력저하의 원인을 조사하였다.
전체 추적 관찰 기간 및 그 기간 동안의 유리체강 내 주사 횟수와 주사 약제의 종류를 조사하였다. 약제의 종류는 bevacizumab, ranibizumab, aflibercept 중 연구자의 판단에 따라 결정하였다. Ranibizumab과 aflibercept가 약제로 선정된 경우 환자들은 초기 치료로 3개월 동안 매달 유리체강 내 주입술을 시행받았고(loading phase), 첫 3회 주사 이후에는 연구자의 판단에 따라 고정주기 방법(fixed dosing)이나 치료 및 연장 방법(treat-and-extend regimen)을 채택하거나 재발이 발생하면 주사를 시행하는 방법(pro re nata)을 시행하였다. Bevacizumab을 약제로 선정한 경우에는 loading phase 없이 pro re nata 방식으로 주사를 시행하였다.
치료 전, 치료 후 3개월, 6개월, 12개월 및 마지막 방문 시의 최대교정시력, 세극등현미경검사, 안저검사, 안저촬영과 빛간섭단층촬영을 조사하였고, 마지막 방문 시 시력이 0.1 미만으로 측정된 경우 그 원인을 조사하였다. 전체 추적 관찰 기간 동안 연구안에서 발생한 주사 관련 합병증을 조사하였고, 반대안의 습성 나이관련황반변성 진행을 조사하였다.
시력 결과 분석은 치료 후 3개월, 6개월, 12개월 및 마지막 방문의 최대교정시력을 치료 전 시력과 비교하였다. 최대교정시력은 Snellen 시력표를 이용하여 측정된 값을 logarithm of the minimal angle of resolution (logMAR) 시력으로 환산하여 분석하였다. 해부학적 결과로는 치료 후 3개월, 6개월, 12개월 및 마지막 방문의 빛간섭단층촬영에서 중심망막두께를 치료 전 두께와 비교하였다. 중심망막두께는 중심와 위치에서 내경계막으로부터 망막색소상피의 외부 경계까지 수직으로 측정한 거리로 정의하였다. 치료 약제에 따라서 연구안을 세 군으로 나누어 시력 및 해부학적 결과도 비교 분석하였다.
최대교정시력과 중심망막두께에 대한 통계 분석은 paired t-test로 시행하였다. 치료 약제에 따른 시력 및 해부학적 결과 분석에는 Mann-Whitney U test를 사용하였다. 모든 통계 분석은 IBM SPSS Statistics version 25.0 (SPSS Inc., Chicago, IL, USA)을 이용하였으며, p-value가 0.05보다 작은 경우를 유의한 것으로 판정하였다.
결 과
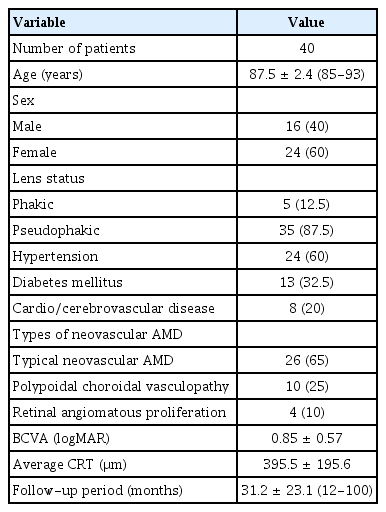
총 40명 40안이 연구에 포함되었다. 남성 16명, 여성 24명이었으며, 평균 연령은 87.5 ± 2.4세(85-93세)였다(Table 1). 초진 시 35안(87.5%)은 백내장수술을 시행받고 위수정체안 상태였고, 5안(12.5%)은 시행받지 않은 상태였다. 전신 질환으로 고혈압을 동반한 환자는 24명(60%), 당뇨를 동반한 환자는 13명(32.5%), 심뇌혈관 질환을 동반한 환자는 8명(20%)이었다. 안과 질환으로는 정상안압녹내장이 2안(5%) 에서, 중등도 비증식당뇨망막병증이 1안(2.5%)에서 동반되었다.
인도시아닌그린혈관조영술 결과 10안(25%)이 결절맥락막혈관병증, 4안(10%)이 망막혈관종성증식, 26안(65%)이 전형적 습성 나이관련황반변성으로 분류되었다. 초진 시 연구안의 평균 logMAR 최대교정시력은 0.85 ± 0.57이었다.
반대안의 경우 평균 logMAR 최대교정시력은 0.93 ± 0.99였다. 최대교정시력이 0.5 미만으로 측정된 경우가 22안(55%)이었고, 그중 3안은 안구위축으로 인해 광각 없음으로 측정되었다. 나머지 19안에서 시력저하의 원인은 10안은 지도모양위축을 포함한 황반부 위축, 6안은 습성 나이관련황반변성으로 확인되었고, 나머지 3안은 시력저하의 원인에 대한 정보를 확인할 수 없었다.
연구안의 평균 추적 관찰 기간은 31.2 ± 23.1개월(12-100개월)이었고, 평균 주사 횟수는 첫 1년간 4.9 ± 1.9회(1-8회), 전체 기간 동안 7.7 ± 4.8회(3-23회)였다. 치료 약제의 경우 10안(25%)이 bevacizumab을, 16안(40%)이 aflibercept를, 14안(35%)이 ranibizumab을 주입받았다.
치료 전, 치료 후 3개월, 6개월, 12개월 및 마지막 방문에 측정한 평균 logMAR 최대교정시력은 0.85 ± 0.57, 0.84 ± 0.62, 0.81 ± 0.61, 0.81 ± 0.64 및 0.95 ± 0.70이었다(Fig. 1A). 치료 전과 비교하여 치료 후 모든 시기에서 유의한 차이를 보이지는 않았다(3개월 p=0.770, 6개월 p=0.895, 12개월 p=0.586, 마지막 방문 p=0.311). 마지막 방문에서 14안은 황반부 위축 및 섬유화로 인해 시력이 0.1 미만으로 측정되었다.

Mean changes in best-corrected visual acuity (BCVA) and central retinal thickness (CRT). (A) BCVA was maintained at all post-treatment periods, although there was no significant difference compared to baseline. (B) CRT had improved significantly at all post-treatment periods compared to baseline. Bars on graph represent standard deviation. *Statistically significant difference from the baseline (p < 0.05).
치료 전, 치료 후 3개월, 6개월, 12개월 및 마지막 방문에 측정한 평균 중심망막두께는 395.5 ± 195.6 µm, 279.9 ± 158.9 µm, 275.4 ± 111.8 µm, 266.7 ± 123.6 µm 및 293.2 ± 179.4 µm였다(Fig. 1B). 치료 전과 비교하여 치료 후 모든 시기에서 유의한 호전을 보였다(3개월 p=0.003, 6개월 p<0.001, 12개월 p<0.001, 마지막 방문 p=0.018).
치료 약제에 따른 시력 및 해부학적 결과의 분석에서, 초진 시 나이, 성별, 최대교정시력, 중심망막두께는 세 군 간 유의한 차이가 없었다(Table 2). 마지막 방문 시의 평균 최대교정시력은 bevacizumab군에서 0.98 ± 0.65, aflibercept군에서 0.97 ± 0.70, ranibizumab군에서 0.93 ± 0.79로 세 군 간 유의한 차이가 없었고(p=0.982), 초진 시와 마지막 방문 시의 시력 차이도 세 군 간 유의한 차이가 없었다(p=0.801). 마지막 방문 시의 평균 중심망막두께 또한 세 군에서 유의한 차이가 없었고(p=0.114), 초진 시와 마지막 방문 시의 중심망막두께의 변화도 세 군 간 유의한 차이가 없었다(p=0.059).
전체 연구 기간 동안 안내염이나 망막박리와 같은 주사 관련 합병증은 나타나지 않았다. 초진 시 유수정체안이었던 5안 중 4안에서 치료 도중 백내장수술을 시행받았다. 당뇨망막병증이 동반되었던 1안에서 연구 기간 동안 당뇨망막병증의 악화는 관찰되지 않았다. 초진 시 반대안의 습성 황반변성이 없었던 환자 34명 중 3명에서 습성 황반변성이 발생하였고, 3안 모두 연구안과 같은 유형의 황반변성이 발생하였다. 아래는 본 연구의 대표 증례이다(Fig. 2). 초진 나이 92세 남성이 우안 망막혈관종성증식으로 진단받았다. 초진 시 우안 최대교정시력은 0.4였으며 ranibizumab 주사 치료를 시작하였다. 총 36개월의 추적 관찰 기간 동안 13번의 안구 내 ranibizumab 주사를 시행받았고, 마지막 진료 시 우안 최대교정시력은 0.6으로 측정되었다.

Representative case of an eye diagnosed with retinal angiomatous proliferation in right eye at the age of 92. A 92-year-old male visited the hospital with decreased vision in his right eye, and was diagnosed with retinal angiomatous proliferation ((A) fundus photography, (B) optical coherence tomography, (C) fluorescein angiography and (D) indocyanine green angiography at the initial visit). Best-corrected visual acuity at the time of diagnosis was 0.4, and intravitreal injection of ranibizumab was started. During a total of 36 months of follow-up, 13 intravitreal injections were performed, and the best-corrected visual acuity was 0.6 at the final visit ([E] fundus photography and [F] optical coherence tomography at the final visit).
고 찰
본 연구에서 초진 나이 85세 이상인 습성 나이관련황반변성 환자에서 1년간 평균 4.9회, 평균 31개월의 추적 관찰 기간 동안 평균 7.7회의 유리체강 내 주사를 통해 시력을 유지할 수 있었고 중심망막두께는 감소하였다. 주사 약제에 따른 기능적 및 해부학적 결과에 차이는 없었으며, 반대안의 평균 시력은 logMAR 0.94로 낮았다.
한국의 인구는 빠르게 고령화되고 있다. 2020년 65세 이상 인구는 전체 인구의 15.7%를 차지하였고, 점점 더 증가하여 2035년에는 30.1%, 2050년에는 40.1%를 차지할 것으로 예측된다. 85세 이상 고령 인구는 2020년 78만 명에서 2023년에 100만 명을 넘고 2070년 544만 명으로 2020년 대비 7배 수준으로 증가할 전망이다.8 이에 나이관련황반변성과 같은 연령 관련 질병이 국가의 공중보건에서 점점 중요한 부분을 차지할 것은 분명하다. 고령에서 시력저하는 정서적 행복, 신체기능 및 독립성에 부정적인 영향을 미친다. 과거 보고들에서 고령에서의 시력저하가 낙상 및 골절 가능성을 유의하게 증가시킨다는 것이 확인되었으며,9,10 더 나아가 사망 위험 증가와도 관련 있음이 관찰되었다.11-15 따라서 고령 환자에서 시력의 보전은 매우 중요하다.
고령에서의 질병도 나이에 따라 다르게 나타날 수 있기 때문에, 고령을 더 자세히 분류하려는 노력이 시도되어 왔다. 일부 연구들에서는 65-74세를 youngest-old, 75-84세를 middle-old, 85세 이상을 oldest-old로 분류하였다.16 미국노인의학회와 세계보건기구는 80세 이상을, 영국노인의학회는 85세 이상을 oldest-old로 정의하였다.17 이를 바탕으로 본 저자들은 본 연구에서 85세를 고령의 기준으로 삼았다.
본 연구에 포함된 40안 중 10안(25%)은 결절맥락막혈관병증, 4안(10%)은 망막혈관종성증식, 26안(65%)은 전형적 습성 나이관련황반변성으로 분류되었다. Lee et al7은 90세 이상 환자군에서 결절맥락막혈관병증이 0%, 망막혈관종성 증식이 43.3%, 전형적 습성 나이관련황반변성이 56.7%였고, 90세 미만 대조군에서 결절맥락막혈관병증이 45.9%, 망막혈관종성증식이 11.5%, 전형적 습성 나이관련황반변성이 42.6%로 확인되어, 90세 이상에서 결절맥락막혈관병증의 비율이 낮고 망막혈관종성증식 비율이 높다고 보고하였다. 50세 이상을 대상으로 한 국내의 나이관련황반변성에 대한 기초역학조사에 따르면, 습성 나이관련황반변성의 31.7%가 결절맥락막혈관병증, 6.2%가 망막혈관종성증식, 62.1%가 전형적 습성 나이관련황반변성으로 진단되었다.18 전체 연령에 비해 고령에서 결절맥락막혈관병증이 적고 망막혈관종성증식이 많이 관찰되는 것으로 보인다.
본 연구에서는 진단 당시 87.5%에서 위수정체안이었고, 유수정체안이었던 5안 중 4안에서 치료 도중 백내장수술을 시행받았다. Lee et al7도 90세 이상 습성 나이관련황반변성 환자들에서 위수정체안의 비율이 81.8%라고 보고하여 본 연구와 유사하였으며, 이는 90세 미만 대조군의 위수정체안 비율인 30.6%보다 2.5배 이상 높은 수치이다. 우리나라에서 백내장수술 시행 당시 환자들의 평균 나이가 69.25세임을 고려하면, 85세 이상 환자들에서 관찰된 높은 위수정체안의 비율은 납득할 수 있는 수준이다.19
본 연구에서 평균 31.2개월에 환자들의 시력은 초진 시와 비교하여 약간의 악화를 보였으나 통계적으로 유의한 호전은 보이지 않았다. Subhi and Sørensen20은 덴마크 환자를 대상으로 진단 당시 90세 이상이었던 습성 나이관련 황반변성 환자들의 의무기록을 후향적으로 분석하였고, 치료 12개월째 최대교정시력은 유의한 차이를 보이지 못하였으나 중심망막두께는 유의한 감소를 보여 본 연구와 같은 결과를 보였다. 우리나라에서 90세 이상 습성 나이관련 환자를 대상으로 그 특성을 조사한 Lee et al7도 치료 12개월 시점에 측정한 시력이 진단 당시와 유의한 차이를 보이지 않았다고 하였다. Chatziralli et al21은 영국의 보건의료제도 자료를 활용한 통계 연구에서 90세 이상의 환자들에서 aflibercept의 치료 효과가 90세 미만에 비해 떨어진다고 보고하여 본 연구의 결과와 일치하였고, 나이가 많은 군에서 위축성 변화가 더 많이 발생하고, 노화된 망막외층이 항혈관 내피성장인자에 반응이 적었기 때문일 것이라고 발표하였다. 본 연구에서도 마지막 방문 시 14안(35%)은 황반부 위축 및 섬유화로 인해 시력이 0.1 미만으로 측정되어 고령의 환자에서 시력 호전의 한계가 있음을 시사하였다.
본 연구에서 수집된 반대안의 평균 logMAR 최대교정시력은 0.93이었고, 55%에서 시력이 0.5 미만이었다. 우리나라 환자들을 대상으로 한 Lee et al7의 연구에서도 반대안의 시력이 0.5 미만으로 측정된 환자가 59.1%였으며, 90세 미만인 대조군과 비교하였을 때 90세 이상의 환자에서 연구안 및 반대안의 시력이 유의하게 나빴다. Subhi and Sørensen20은 시력을 제시하지는 않았으나, 90세 이상 습성 황반변성 환자 모두에서 반대안에 초기 나이관련황반변성, 지도모양 위축, 섬유성 흉터 조직 등 황반 병변을 가졌다고 보고하였다. 연구들에서 공통적으로 보인 반대안의 나쁜 시력은 치료안에서 시력 유지의 중요성을 강조한다.
치료 약제에 따른 최종 시력 및 해부학적 결과 분석에서 약제에 따른 차이는 관찰되지 않았다. 연구자의 판단에 따라 약제 종류 및 추적 관찰 기간을 정하였으므로 약제 간 효능의 비교를 직접적으로 할 수는 없으나, 이러한 결과는 Subhi and Sørensen20의 연구 결과와 유사하다. Subhi and Sørensen20은 90세 이상 환자들을 aflibercept로 치료한 군과 ranibizumab으로 치료한 군으로 나누어 비교한 결과, aflibercept가 시력 측면에서 더 우수하였으나 그 차이가 통계학적으로 유의한 수준에 미치지는 않았다고 하였다.
본 연구에서는 초진 시 반대안의 습성 황반변성이 없었던 환자 34명 중 3명(8.8%)에서 습성 황반변성이 발생하였다. 일본의 한 연구에 따르면 단안 습성 나이관련황반변성 환자에서 반대안의 누적 발생률은 1년에 3.4%, 3년에 9.3%, 5년에 11.3%였다.22 또 다른 연구에서 반대안 습성 황반변성의 연간 추정 발병률은 nonexudative neovascularization이 있는 경우 18.1%, 없는 경우 2.0%라고 보고하였다.23 황반변성 환자에서 반대안의 습성 변화는 환자의 삶의 질에 큰 영향을 미치며, 상대적으로 젊은 연령에 비해 시력이 유의하게 나쁜 고령에서는 그 영향이 더 클 것으로 생각된다.7 따라서 반대안의 신생혈관의 징후를 감지하기 위해 치료안뿐만 아니라 반대안의 정기적인 모니터링도 중요하겠다.
본 연구에는 다음과 같은 제한점들이 있다. 본 연구는 후향적 연구였고, 연구 대상자 수가 적었으며 모든 환자의 추적 관찰 기간과 주사 치료 방법이 달랐다. 또한 대조군이 없어 더 젊은 나이의 환자들과의 비교나 질병이 없는 고령 인구와의 비교를 시행할 수 없었다. 그리고 다기관 연구로 안저 및 빛간섭단층촬영을 단일 기종으로 검사하지 못해 측정한 기기에 따른 중심망막두께에 약간의 차이가 있을 것으로 생각된다. 그러나 85세 이상 고령에서 습성 나이관련황반변성으로 첫 진단된 환자들에서 장기 치료 결과를 분석하고 보고하였다는 점에서 의미가 있다.
결론적으로 초진 시 나이가 85세 이상의 환자에서도 유리체강 내 주사 치료를 통해 시력의 악화를 막을 수 있었고 성공적인 해부학적 결과를 얻을 수 있었다. 특히 반대안의 시력이 나쁜 경우가 많아 시력의 유지가 의미 있을 것으로 생각되어, 고령에서도 적극적인 치료가 필요하다.
Notes
Conflicts of Interest
The authors have no conflicts to disclose.
References
Biography
권지민 / Ji Min Kwon
인제대학교 의과대학 해운대백병원 안과학교실
Department of Ophthalmology, Haeundae Paik Hospital, Inje University College of Medicine