 |
 |
| J Korean Ophthalmol Soc > Volume 63(1); 2022 > Article |
|
국문초록
대상과 방법
면역 결핍 상태가 아니면서 당뇨가 있던 환자에게서 거대세포바이러스망막염이 발생한 5례의 의무기록을 후향적으로 분석하였다. 모든 환자들은 당뇨가 있었고, 다양한 정도의 당뇨망막병증이 관찰되었으며, 망막병증 진단 시에 환자의 면역 상태를 확인하기 위해 장기 이식 등의 과거력과 면역억제제를 포함한 약물 복용력을 확인하고 피검사를 포함한 전신적 검사를 시행하여 면역 저하가 없음을 확인하였다. 거대세포망막염이 의심되었던 5명의 환자들 모두에게 전방천자를 통한 viral polymerase chain reaction (PCR) 검사를 시행하였으며, 거대세포바이러스가 검출되었다. 5명 모두 전방천자를 통한 PCR 검사를 반복해 바이러스에 음성이 나올 때까지 유리체강내 항바이러스 주입술 치료를 받았다.
ABSTRACT
Purpose
We report five cases of cytomegalovirus (CMV) retinitis in immunocompetent patients with diabetes mellitus (DM).
Methods
This was a retrospective observational case series of five immunocompetent patients with CMV retinitis. All patients had DM and variable degrees of DM retinopathy. After discovery of the retinitis, we assessed the patients in terms of ophthalmologic history, systemic conditions, underlying disease, and the medications used for treatment, such as immunosuppressants. This was followed by blood and immunology tests. None of the five patients were immunocompromised. We confirmed the diagnosis of CMV retinitis by polymerase chain reaction (PCR) analysis; samples were collected by anterior chamber paracentesis. All patients were treated with intravitreal antiviral injection until negative results were obtained for the anterior chamber PCR.
Results
All five immunocompetent patients who had developed CMV retinitis, had a history of diabetes of at least 15 years. The average duration of diabetes was 17.4 ± 2.4 (15-20) years, the average HbA1c was 7.3 ± 0.5% (6.8-8.0%), and the average duration and numbers of Intravitreal antiviral injections were 23.8 ± 8.5 months (14-36 months) and 14.8 ± 3.2 times (10-18 times), respectively.
거대세포바이러스는 흔한 병원균이지만 면역기능이 정상인 사람에서는 대부분 안구내 감염으로 인한 임상 증상을 일으키지 않으며, 후천면역결핍증후군(acquired immune deficiency syndrome, AIDS), 백혈병, 림프종 및 면역억제 치료를 받는 환자들에게 주로 안구내 감염으로 인한 임상 증상이 나타난다고 알려져 있다[1]. 특히 AIDS 환자의 경우, 병의 경과 중에 환자의 70%에서 안과적 증상이 발생하며, 이는 파종성 감염의 첫 번째 징후일 수 있고, 전신적 감염이 일어나고 있다는 것을 의미한다. 증상은 안검염에서부터 거대세포바이러스망막염까지 광범위하며, 이 중에서도 망막염은 20-30%를 차지하고 CD4 cell이 50/mm3 이하로 저하된 진행된 단계의 AIDS 환자에서 주로 동반된다. 거대세포바이러스망막염은 AIDS 환자에서 실명을 일으키는 가장 흔한 원인이다[1,2]. 본 저자는, 후천면역결핍증후군이나 면역 억제 치료의 과거력 등의 기저질환이 없는 당뇨 환자에서 거대세포바이러스망막염이 합병된 5예를 경험하여 이를 보고하고자 한다.
2016년 6월부터 2020년 3월까지 3년 9개월간 본원 안과 외래에서 당뇨망막병증으로 경과 관찰하던 환자들 중 면역 능력의 저하 없이 거대세포바이러스망막염이 발생한 5안의 후향적 차트 분석을 시도하였다. 본 연구는 본원의 연구윤리심의위원회(Institutional Review Board, IRB)의 승인을 받았다(승인 번호: KC21RASI0452).
환자들은 공통적으로 당뇨를 가지고 있었으며, 경도의 비증식당뇨망막병증에서 당뇨황반부종을 동반한 증식당뇨망막병증까지 다양한 정도의 당뇨망막병증을 가지고 있었다. 5명의 환자 모두 전방천자를 통해 시행한 viral PCR, 안저검사와 초광각안저촬영술(Optos Carfornia®, Optos PLC, Dunfermline, UK)을 이용하여 거대세포바이러스망막염을 진단하였으며, 진단 시에 환자의 면역 상태를 확인하기 위해 장기 이식 등의 과거력과 면역억제제를 포함한 약물 복용력을 확인하고, 피검사를 포함한 전신적 검사를 시행하여 면역 능력의 저하가 없음을 확인하였다. 거대세포바이러스망막염 진단을 위한 viral polymerase chain reaction (PCR) 검사를 위해 환자가 편하게 누운 상태에서 점안마취 후 전방천자를 통해 검체를 채취하였다. 또한 추후 치료의 효과를 확인하기 위해 전방천자를 통한 PCR 검사를 반복하여 바이러스에 음성이 나올 때까지 5명 모두 유리체강내항바이러스 주입술 치료를 받았다.
Table 1은 면역 능력이 정상이지만 거대세포바이러스망막염이 발생한 5명 환자의 당뇨 유병 기간 및 거대세포바이러스망막염 진단 시 측정한 환자의 당화혈색소 등을 포함한 기본적인 정보이다.
53세 남자로, 당뇨 유병 기간은 16년, 당화혈색소는 8%였으며 인슐린 주사로 당뇨를 조절하고 있었다. 이외에도 당뇨병에 의한 말기 콩팥병증으로 1년 전부터 혈액투석 중이었다. 안과적으로는 발병 2년 전 양안의 백내장수술을 받았으며 양안 증식당뇨망막병증과 당뇨황반부종으로 범망막광응고술을 시행하였고, 발병 3년 전부터 19개월 전까지 유리체강내 주사를 우안은 베바시주맙 4회, 트리암시놀론 4회, 좌안은 베바시주맙 3회, 트리암시놀론 4회 시행하였다. 마지막 주사는 우안 16개월 전 트리암시놀론, 좌안 17개월 전 트리암시놀론을 주사하였으며 이후 유리체강내 주사 없이 3-4개월 간격으로 경과 관찰 중, 환자는 갑자기 발생한 좌안 안압상승 및 시력저하를 주소로 내원하였다. 내원 당시 환자의 최대교정시력은 우안 0.4, 좌안 0.125였으며, 골드만압평안압계를 통해 측정한 안압은 우안 12 mmHg, 좌안 38 mmHg였다. 세극등현미경검사상에서 전방의 cell은 1+ 정도로 관찰되었다. 안저검사에서 좌안 후극부에서부터 이측 망막혈관 주위로 흰색의 망막침윤과 망막출혈을 확인할 수 있었다(Fig. 1). 정확한 진단을 위해 전방천자를 통한 viral PCR 검사를 시행하였으며 cytomegalovirus (CMV) PCR 결과 381,550 IU/mL로 거대세포바이러스망막염을 진단하였다. PCR이 음성으로 확인될 때까지 22주에 걸쳐 ganciclovir 2 mg/0.1 mL 8회, foscarnet 1.2 mg/0.05 mL 2회 유리체강내 주입술을 받았다. 마지막 유리체강내 주입술 치료 후 경과 관찰 시 3개월째 좌안 시력은 0.1이었으며 이후 경과 관찰 중 재발은 없었다.
75세 남자로, 당뇨 유병 기간은 20년, 당화혈색소는 7.5%였으며 경구약으로 당뇨를 조절하고 있었다. 이외에도 10년 전 비ST분절상승심근경색(non-ST elevation myocardial infarction)으로 관상동맥중재술을 받은 후 aspirin과 clopidogrel을 복용하며 지속적으로 경과 관찰 중이었다. 안과적으로는 우안은 중등도 비증식당뇨망막병증, 좌안은 심한 비증식당뇨망막병증으로 좌안에는 범망막광응고술을 시행하고 2-3개월 간격으로 본원 경과 관찰 중이었다. 망막염 발견 시에도 특별한 증상 호소 없이 정기적인 경과 관찰 위해 외래 내원하였으며, 최대교정시력은 이전 내원 시와 동일하게 우안 1.0, 좌안 0.2였고, 비접촉안압계를 통해 측정한 안압은 우안 16 mmHg, 좌안 18 mmHg였으나, 안저검사에서 좌안의 하이측 망막에 희고 노란 과립상의 망막침윤 및 망막출혈을 확인할 수 있었다(Fig. 2). 정확한 진단을 위해 전방천자를 통한 viral PCR 검사를 시행하였으며 CMV PCR 결과 7,540 IU/mL로 거대세포바이러스망막염을 진단하였다. PCR이 음성으로 확인될 때까지 31주에 걸쳐 ganciclovir 2 mg/0.1 mL 12회, foscarnet 1.2 mg/0.05 mL 5회 유리체강내 주입술을 받았다. 마지막 유리체강내 주입술 치료 후 경과 관찰 시 1개월째 좌안 시력은 안전수지 30 cm, 3개월째 0.02였으며 이후 경과 관찰 중 재발은 없었다.
72세 남자 환자로, 당뇨 유병 기간은 20년, 당화혈색소는 7%였으며 경구약으로 당뇨를 조절하고 있었다. 이외에도 당뇨로 인한 3단계 만성 콩팥병증 및 고혈압과 대동맥확장증이 있었다. 안과적으로는 발병 3년 전 좌안에 백내장수술을 받았으며, 양안의 중등도 비증식당뇨망막병증으로 4개월 간격으로 타병원에서 경과 관찰 중이었다. 일주일 전 갑자기 발생한 좌안 시력저하로 타병원에서 전방천자를 통한 CMV PCR 시행 후 거대세포바이러스망막염으로 진단 받고 유리체강내 항바이러스 주입술 2회 시행 후 유리체의 혼탁이 지속되어 본원으로 의뢰되었다. 본원 초진 시 최대교정시력은 우안 1.0, 좌안 안전수동이었으며, 비접촉안압계를 통해 측정한 안압은 우안 10 mmHg, 좌안 8 mmHg였다. 세극등현미경검사상에서 좌안에 광범위한 각막후면침착물(keratic precipitate, KP)과 전방에 cell 1+이 관찰되었으며, 안저검사상 좌안의 유리체혼탁과 두껍고 노란 망막침윤과 부종을 관찰할 수 있었다(Fig. 3). 거대세포망막염과 급성괴사성망막염 의심 하에 전방천자를 통한 viral PCR 검사를 시행하였으며 varicella zoster virus (VZV) PCR에서는 바이러스가 검출되지 않았고, CMV PCR 결과 86,710 IU/mL로 거대세포바이러스망막염을 진단하였다. 환자는 PCR이 음성으로 확인될 때까지 36주에 걸쳐 ganciclovir 2 mg/0.1 mL 4회, foscarnet 1.2 mg/0.05 mL 8회 유리체강내 주입술을 받았다. 마지막 유리체강내 주입술 치료 후 경과 관찰 시 3개월째 좌안 시력은 0.06까지 회복되었으며 이후 경과 관찰 중 재발은 없었다.
63세 남자 환자로, 당뇨 유병 기간은 15년, 당화혈색소는 6.8%였으며 경구약으로 당뇨를 조절하고 있었다. 이외에도 30세에 폐결핵을 앓고 완치된 과거력이 있었다. 안과적으로는 중등도 비증식당뇨망막병증으로 타병원 경과 관찰 중이었으며, 10일 전부터 발생한 우안 변형시 및 시력저하로 본원 내원하였다. 본원 초진 시 최대교정시력은 우안 0.06, 좌안 0.8이었고, 비접촉안압계를 통해 측정한 안압은 우안 12 mmHg, 좌안 20 mmHg였다. 세극등현미경검사상에서 우안에 KP와 전방에 cell 1-2+이 관찰되었으며 안저검사상 우안 망막혈관 전반에 걸쳐 혈관초 형성 및 이측 망막에 과립상의 흰색 망막침윤과 동반된 망막출혈을 확인할 수 있었다(Fig. 4). 정확한 진단을 위해 전방천자를 통한 viral PCR 검사를 시행하였으며 VZV, herpes simplex virus PCR에서는 모두 음성임을 확인하였고, CMV PCR 결과 736,279 IU/mL로 거대세포바이러스망막염을 진단하였다. 이후 14주에 걸쳐 CMV PCR이 음성으로 확인될 때까지 ganciclovir 2 mg/0.1 mL 16회, foscarnet 1.2 mg/0.05 mL 2회 유리체강내 주입술을 받았다. 마지막 유리체강내 주입술 치료 후 1개월째 우안 시력은 0.16으로 치료 전 0.06과 비교하여 시력이 회복되는 경과를 보였다.
66세 남자 환자로, 당뇨 유병 기간은 16년, 당화혈색소는 7%였으며 경구약으로 당뇨를 조절하고 있었다. 이외에도 1년 전 협심증으로 타병원에서 관상동맥 우회술(coronary artery bypass graft, CABG)을 시행 받았다. 안과적으로는 양안 증식당뇨망막병증과 당뇨황반부종으로 3년 전 양안 범망막광응고술 시행 및 11개월 전에 양안 유리체강내 베바시주맙주사 치료를 1회 시행 받은 후, 2개월 간격으로 경과 관찰하던 중이었다. 일주일 전부터 발생한 좌안의 시력저하를 주소로 경과 관찰 예정일보다 앞당겨 내원하였을 때 최대교정시력은 우안 1.0, 좌안 0.4였고, 비접촉안압계를 통해 측정한 안압은 우안 14 mmHg, 좌안 12 mmHg였다. 세극등현미경 검사상에서 좌안 전방에 cell 1+이 관찰되었으며 안저검사상 좌안의 유리체혼탁과 비측과 이측 망막에 노랗고 하얀 망막침윤을 확인할 수 있었다(Fig. 5). 정확한 진단을 위해 전방천자를 통한 viral PCR 검사를 시행하였으며, CMV PCR 결과 56,940 IU/mL로 거대세포바이러스망막염을 진단하였다. 이후 16주에 걸쳐 PCR이 음성으로 확인될 때까지 ganciclovir 2 mg/0.1 mL 13회, foscarnet 1.2 mg/0.05 mL 4회 유리체강내 주입술을 받았다. 치료 후 경과 관찰 시 3개월 째 좌안의 최대교정시력은 0.25였다.
환자들은 공통적으로 15년 이상의 당뇨 유병 기간을 가지고 있었으며, 평균 유병 기간은 17.4 ± 2.4 (15-20)년, 진단 시의 평균 당화혈색소는 7.3 ± 0.5 (6.8-8.0)%였다. 유리체강내 항바이러스제 치료 기간은 평균 23.8 ± 8.5 (14-36)개월이었으며, 주사 횟수는 14.8 ± 3.2 (10-18)회였다. 또한 당뇨병 이외에도 혈관벽의 구조적 변화를 유발할 수 있는 고혈압 등의 혈관질환과 혈액투석의 과거력을 가지고 있었다[3-5]. 이 중에서도 특히 당뇨의 경우 미세혈관 합병증의 하나로 당뇨망막병증을 유발하는 것으로 알려져 있다[6].
거대세포바이러스 감염은 건강한 성인에서 흔하게 발생하며, 건강한 성인의 40-100%에서 혈청학적으로 바이러스가 검출되었다는 연구 결과가 있어 이를 뒷받침한다[7]. 거대세포바이러스는 건강한 환자들에서는 증상을 일으키지 않으며 인체 내에 잠복해 있다가 면역 저하 발생 시 기회 감염의 형태로 발현된다. 특히 AIDS 환자에서는 거대세포바이러스 침범으로 인한 망막염이 주로 동반되며, 고강도 항레트로바이러스 치료(highly active antiretroviral therapy)가 개발되기 전까지는 발병 빈도가 매우 높아, AIDS 환자 실명의 주된 원인이 되었다[8].
하지만 이러한 면역 결핍 환자 이외에 거대세포바이러스망막염이 발생한 경우가 국외에서 증례보고 형식으로 보고된 바 있다. Saidel et al [9]은 유리체강내 트리암시놀론 주사 이후 발생한 거대세포바이러스망막염을 처음 보고하였으며, 발생 원인으로 트리암시놀론의 ocular local immunosuppression 때문일 것이라고 하였다. 이후에 Delyfer et al [10] 또한 유리체강내 트리암시놀론 주사 이후 거대세포바이러스망막염이 발병한 두 가지 증례를 보고하였으며, 이들의 공통점으로는 트리암시놀론의 주사량을 첫 번째 환자의 경우 20 mg, 두 번째 환자는 8 mg씩 3차례 주사하여 high dose steroid를 사용하였다는 것과 제2형 당뇨병(type 2 diabetes mellitus [type 2DM])이 있었고, 백내장수술이나 유리체수술과 같은 안구내 수술의 과거력이 있다는 것이었다. 하지만 면역억제 효과가 없는 bevacizumab이나 ranibizumab의 주사 이후에도 거대세포바이러스망막염의 발생이 보고되었다[11,12]. Ranibizumab 주사 환자의 경우, 당뇨황반부종과 배경 망막병증으로 주사치료를 시행하였고, 4번째 주사 이후 15일째 시력저하와 비문증을 호소하며 발병하였으며, bevacizumab 주사 환자의 경우 증식당뇨망막병증과 낭포황반부종이 동반되어 주사치료를 시행하였고, 주사 1주 후 시력저하와 안구통증을 호소하며 발병하였다. Ranibizumab과 bevacizumab 주사 이후 거대세포바이러스망막염이 발병한 환자 두 명 모두 공통적으로 당뇨를 가지고 있었으며, 저자들은 거대세포바이러스망막염 발병의 원인으로 주사 전부터 존재하던 당뇨망막병증에 의한 허혈성 변화를 제시하였다[11]. 또한 당뇨 환자의 경우 혈액 망막 장벽이 손상된다는 Zhang et al [13]의 연구 결과도 있어 이를 뒷받침하며, 이는 후천면역결핍증 환자에서 거대세포바이러스망막염이 발생하는 원인과도 연관을 보인다.
후천면역결핍증 환자에서 거대세포바이러스망막염의 원인으로, Glasgow and Weisberger [14]은 망막의 내측혈액망막 장벽인 혈관내피세포의 손상과 혈류 속도의 저하가 동반되면서 발생한다고 하였다. 당뇨 환자들에게서도 이와 같은 혈관내피세포의 손상과 망막혈관의 혈류 속도의 저하가 동반된다는 결과가 있어, 이로 인해 당뇨에서 거대세포바이러스망막염이 발병할 수 있음을 제시하고자 한다.
먼저, 혈관내피세포의 손상과 관련하여, 망막과 관련된 혈액망막장벽은 내측과 외측의 두 가지가 있으며, 내측혈액망막장벽은 망막혈관내피세포의 치밀 이음부에 의한 것이고, 외측혈액망막장벽은 망막색소상피세포의 치밀 이음부에 의한 것이다. Vinores et al [15]에 따르면 알부민을 이용하여 망막혈관에서의 누출을 연구하였을 때, 당뇨가 없거나 당뇨가 있더라도 당뇨망막병증은 없는 환자들에서는 혈관 외 누출이 없었으며, 당뇨망막병증이 있는 경우의 혈관 외 누출의 정도는 각각 경한 비증식당뇨망막병증에서 12.5%, 중등도 비증식당뇨망막병증에서 20%, 증식당뇨망막병증에서 89%로 당뇨망막병증의 정도가 심할수록 혈관 외 누출의 정도도 심해지는 것을 알 수 있었다. 또한, 당뇨 환자의 경우 유병 기간이 길어질수록 당뇨망막병증의 발생률도 증가하기 때문에[16], 당뇨 유병 기간과 망막혈관의 취약성 간에도 상관관계가 있다고 볼 수 있다. 당뇨망막병증이 진행할수록 내측 망막의 혈관에 먼저 알부민을 포함한 혈관 외 누출이 생기며, 시간이 흐르면서 망막색소상피층에도 추가적으로 누출이 생기게 된다[15]. 이러한 점들로 미루어 보았을 때 당뇨 환자에서 거대세포바이러스망막염의 발생에 대한 병인으로 내측, 외측 망막혈액장벽의 파괴와 이로 인해 잠복해 있던 바이러스가 약해진 망막혈관을 통해 침투하는 것으로 생각된다.
두 번째로, 망막혈관에서 백혈구는 일정한 속도로 망막의 모세혈관들을 통과하게 된다. Miyamoto et al [17]에 따르면, 당뇨병 쥐를 통해 fluorescent nuclear dye인 acridine orange로 leukocyte를 labeling하여 시행한 실험에서 당뇨망막병증이 있는 쥐에서는 망막혈관의 microvasculature가 변화함에 따라 leukocyte entrapment가 많이 일어나게 되어 dye의 wash out이 늦어지는 것이 확인되었으며, 이에 따라 망막혈류의 속도가 저하되면서 잠복기의 거대세포바이러스가 망막에 갇혀 감염되는 것으로 생각된다.
Tabatabaei et al [18]에 의하면 당뇨의 혈액망막장벽의 손상에 의한 영향과 함께 당뇨가 subclinical immunosuppresion을 일으킨다고 하였다. 당뇨는 진행하면서 cytokine이나 chemokine, complement의 변화를 일으킴으로써 면역세포에 영향을 끼쳐 면역능력에 이상을 일으킨다[19]. Critchley et al [19]은 당뇨 환자들에서 혈당조절에 따른 감염률을 연구하였으며, 당뇨가 없는 환자와 당화혈색소 6-7%인 환자, 7-8%인 환자, 8-9%인 환자, 9-10%인 환자와 11% 이상으로 조절이 잘 안 되는 환자를 비교하였다. 당뇨가 없는 대조군과 비교한 각 군에서의 발생률 비율(incidence rate ratio, IRR)은 당화혈색소 6-7%, 7-8%, 8-9%, 9-10%, 10-11%, 11% 이상에서 각각 1.41, 1.58, 2.02, 2.44, 3.43, 4.70으로 당화혈색소가 높을수록 감염 발생률도 높아졌다[19]. Lederman et al [20]의 연구에 따르면, 사람의 면역체계를 선천면역과 후천면역, 그리고 후천면역을 다시 체액성 면역과 세포성 면역으로 나누었을 때, 당뇨 환자를 당뇨가 없는 환자와 비교해보았을 때 혈청 항체 농도는 정상 범위로 측정되고 Pneumococcal 백신에 의한 항체의 생성도 당뇨가 없는 환자와 동일하게 나타나 후천 체액성 면역은 정상이라고 하였다. Moutschen et al [21]은 세포성 면역의 경우 당뇨가 매우 조절이 안되었던 환자에서는 자극이 들어왔을 때 면역세포의 증식성 반응의 정도가 저하된다고 하였으나, 이런 환자들에서도 후천성 세포면역 결핍질환인 HIV 환자들과는 다르게 Pneumocystis carinii에 의한 폐렴이나, mycobacteria에 의한 감염이 일어나지는 않는 것으로 보고되어 in vivo와 in vitro에서의 차이를 보였다[21]. 따라서 세포면역의 경우, 당뇨가 잘 조절되지 않는 환자에서 기능이 떨어질 수 있으며 더 연구가 필요할 것으로 생각된다.
또한 Tabatabaei et al [18]은 면역 저하 상태가 아닌 환자에게서 우안에 거대세포바이러스망막염이 발병한 후 2년 뒤 좌안에도 이어서 발생한 증례도 보고하여 당뇨가 있거나, 유리체강내 주사를 지속적으로 맞아야 하는 경우 등 위험요소가 있는 환자에게는 한 눈 발병 뒤 예방적으로 항바이러스 경구약을 복용하는 것을 추천한다고 하였으며, 이에 대해서도 추후 연구가 필요한 부분으로 생각된다.
본 연구에서는 증례 1의 경우 발병안에 백내장수술의 과거력과 bevacizumab 3회, triamcinolone 4회의 유리체강내 주사를 시행한 바가 있으며, 마지막 주사는 17개월 전이었다. 증례 3의 경우 발병안에 백내장수술의 과거력이 있었다. 증례 5의 경우 11개월 전 유리체강내 bevacizumab 1회 주사한 과거력이 있었다. 증례 2와 4의 경우에는 안구수술력이나 주사치료를 받은 과거력이 없었고 당뇨만 가지고 있었다. 앞서 Delyfer et al [10]에 의해 제시된 세 가지 요인인 high dose steroid의 사용, type 2 DM, 백내장수술이나 유리체수술과 같은 안구내 수술의 과거력 중 5명의 환자 모두에게서 해당하는 요인으로는 type 2 DM이 있었다.
본 연구의 제한점은 증례보고인 만큼 대상자의 수가 적은 것과 당뇨 이외에도 관상동맥중재술을 한 과거력이나, 만성 콩팥병증, 대동맥확장증과 같은 질환이 같이 합병되었다는 것이며, 특히, 4번 환자의 경우 망막혈관 전반에 심한 혈관초가 형성되어 있어 이것이 당뇨망막병증과 함께 거대세포바이러스망막염 발생의 선행 원인이 될 수도 있을 것으로 생각된다. 추후 당뇨망막병증으로 경과 관찰하는 환자 군을 대상으로 당뇨망막병증의 정도에 따른 거대세포바이러스망막염의 발생 빈도에 차이가 있는지, 또한 양안성으로 발병한 경우도 이전에 한 명의 환자에서 증례보고가 된 바가 있어, 장기간 경과 관찰하면서 반대안에도 망막염이 발병하는지를 확인해 보는 것도 의미 있을 것으로 생각된다. 본 연구의 결과로 저자들은 당뇨와 당뇨망막병증이 있는 환자에게서 거대세포바이러스망막염의 발병에 대한 주의가 필요하며, 특히 당뇨망막병증이나 유리체강내 주사 치료를 요하는 망막질환을 가진 환자의 경우 더욱 각별한 주의가 필요함을 제시하는 바이다.
Figure 1.
Cytomegalovirus retinitis in the left eye. (A) Right eye shows well applied pan-retinal photocoagulation with some retinal hemorrhage. (B) Left eye shows perivascular hemorrhage and whitish lesion at the posterior pole-temporal retina. (C) Three months after treatment of intravitreal antiviral therapy, negative result was shown in polymerase chain reaction in the left eye.
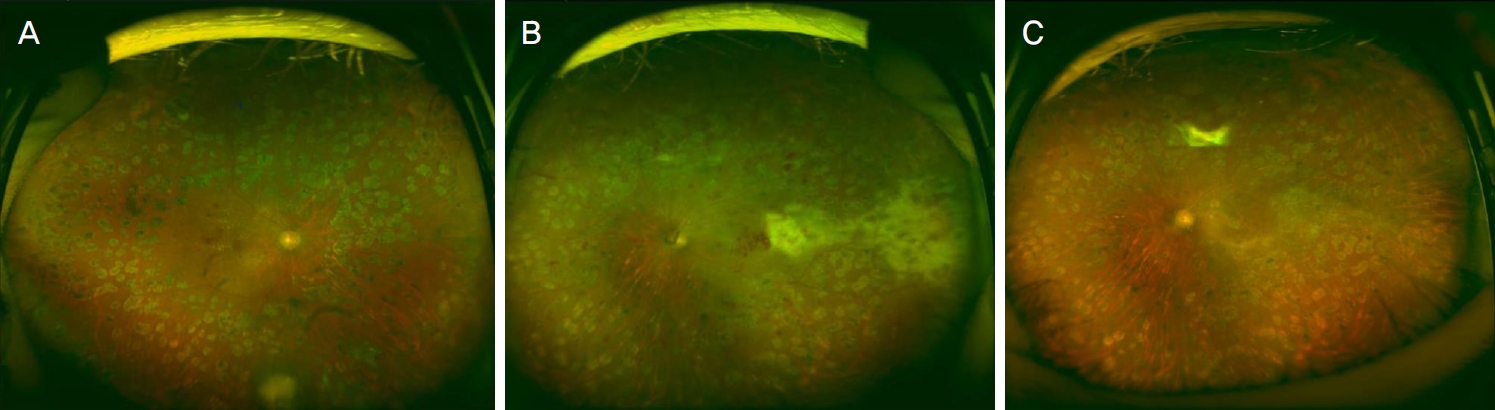
Figure 2.
Cytomegalovirus retinitis in the left eye. (A) Right eye shows normal optic disc and dot retinal hemorrhage at the 2/4 quadrant. (B) Left eye shows confluent whitish yellow lesions at 3-5 o/c peripheral retina. (C) Three months after treatment of intravitreal antiviral therapy, negative result was shown in polymerase chain reaction in the left eye.
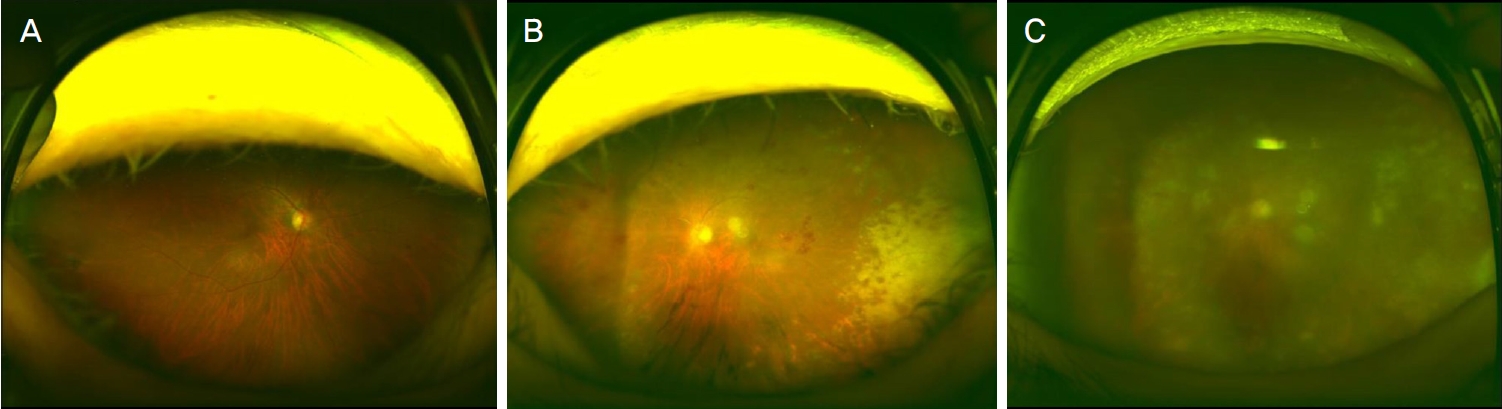
Figure 3.
Cytomegalovirus retinitis in the left eye. (A) Diffuse endothelial keratic precipitate in the left eye. (B) Right eye shows normal optic disc with some dot shaped retinal hemorrhage. (C) Left eye was blurry visible because of corneal keratic precipitate and vitritis, but seems yellowish lesion with retinal hemorrhage at 2-10 o/c peripheral retina. (D) Four months after treatment of intravitreal antiviral therapy, negative result was shown in polymerase chain reaction in the left eye.
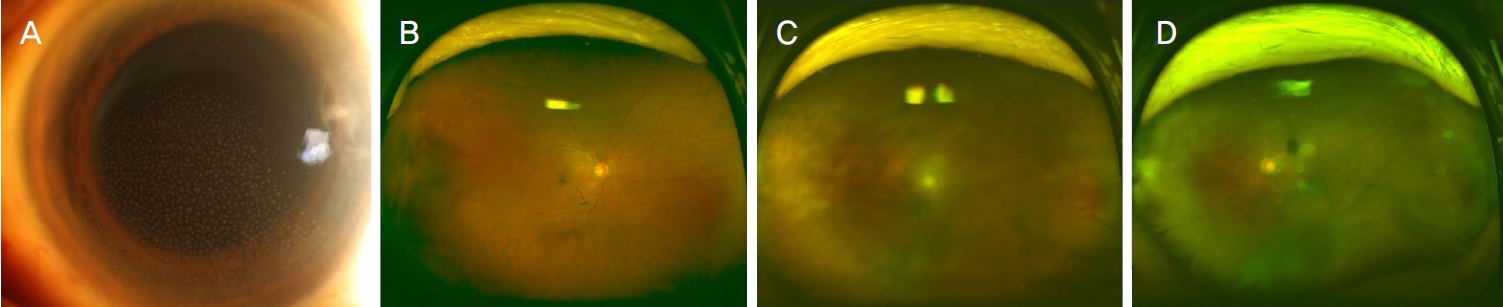
Figure 4.
Cytomegalovirus retinitis in the right eye. (A) Right eye shows diffuse perivascular sheathing and whitish geographic lesion with hemorrhage at the temporal retina. (B) Left eye shows normal optic disc with some dot shaped retinal hemorrhage. (C) Three months after treatment of intravitreal antiviral therapy, negative result was shown in polymerase chain reaction in the right eye.
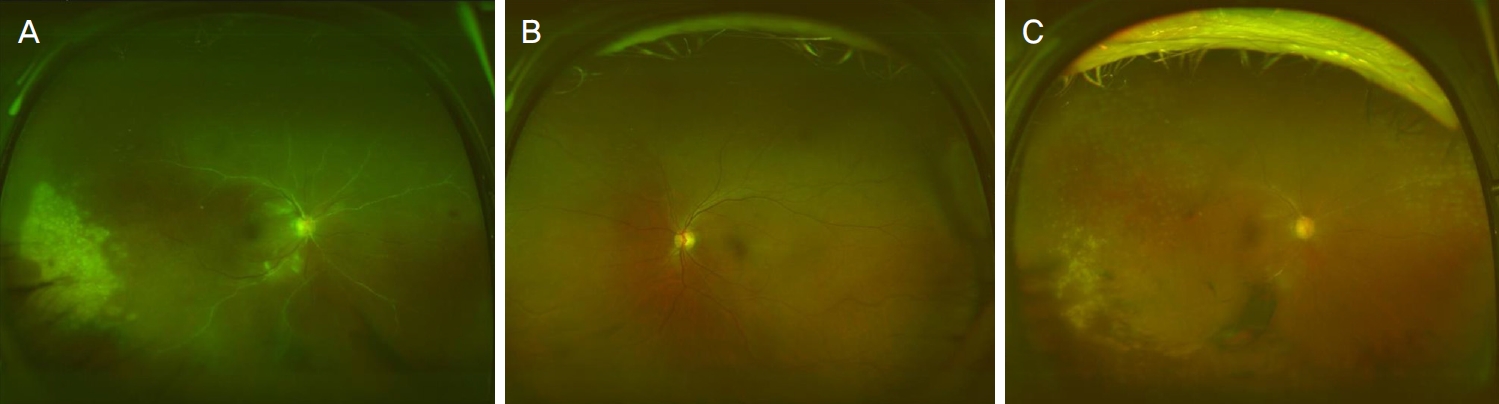
Figure 5.
Cytomegalovirus retinitis in the left eye. (A) Right eye shows normal optic disc with well applied pan-retinal photocoagulation. (B) Left eye shows obstructive vasculopathy with yellow-whitish geographic infiltration and hemorrhage at 1-7 o/c peripheral retina. (C) Four months after treatment of intravitreal antiviral therapy, negative result was shown in polymerase chain reaction in the left eye.
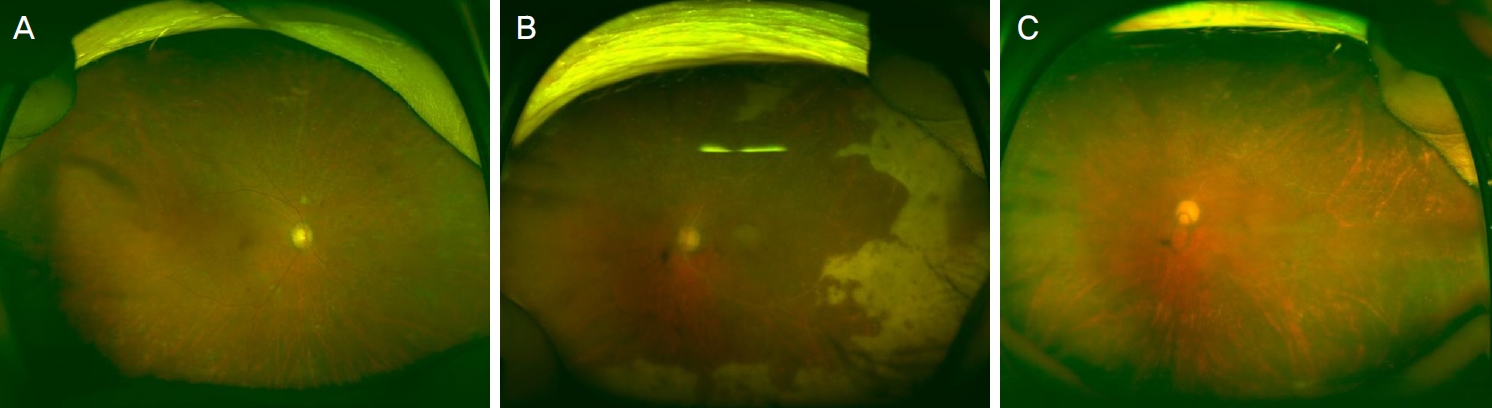
Table 1.
Summary of immunocompetent patients who developed cases of cytomegalovirus retinitis
REFERENCES
2) Chiotan C, Radu L, Serban R, et al. Cytomegalovirus retinitis in HIV/AIDS patients. J Med Life 2014;7:237-40.


3) Hayashi K, Naiki T. Adaptation and remodeling of vascular wall; biomechanical response to hypertension. J Mech Behav Biomed Mater 2009;2:3-19.


5) Ahmadmehrabi S, Tang WHW. Hemodialysis-induced cardiovascular disease. Semin Dial 2018;31:258-67.



6) Wang W, Lo ACY. Diabetic retinopathy: pathophysiology and treatments. Int J Mol Sci 2018;19:1816.



7) Krech U. Complement-fixing antibodies against cytomegalovirus in different parts of the world. Bull World Health Organ 1973;49:103-6.


8) Lin DY, Warren JF, Lazzeroni LC, et al. Cytomegalovirus retinitis after initiation of highly active antiretroviral therapy in HIV infected patients: natural history and clinical predictors. Retina 2002;22:268-77.


9) Saidel MA, Berreen J, Margolis TP. Cytomegalovirus retinitis after intravitreous triamcinolone in an immunocompetent patient. Am J Ophthalmol 2005;140:1141-3.


10) Delyfer MN, Rougier MB, Hubschman JP, et al. Cytomegalovirus retinitis following intravitreal injection of triamcinolone: report of two cases. Acta Ophthalmol Scand 2007;85:681-3.


11) Bae SH, Kim TW, Chung H, Heo JW. Cytomegalovirus retinitis after intravitreal bevacizumab injection in an immunocompetent patient. Korean J Ophthalmol 2013;27:61-3.



12) Zafeiropoulos P, Tamboura P, Dimou M, et al. Cytomegalovirus retinitis, in a diabetic immunocompetent patient, after intravitreal ranibizumab injection. Eur J Ophthalmol 2019;29:NP10-2.


13) Zhang M, Xin H, Atherton SS. Murine cytomegalovirus (MCMV) spreads to and replicates in the retina after endotoxin-induced disruption of the blood-retinal barrier of immunosuppressed BALB/c mice. J Neurovirol 2005;11:365-75.


14) Glasgow BJ, Weisberger AK. A quantitative and cartographic study of retinal microvasculopathy in acquired immunodeficiency syndrome. Am J Ophthalmol 1994;118:46-56.


15) Vinores SA, Gadegbeku C, Campochiaro PA, Green WR. Immunohistochemical localization of blood-retinal barrier breakdown in human diabetics. Am J Pathol 1989;134:231-5.


16) Klein R, Klein BE, Moss SE, et al. The Wisconsin epidemiologic study of diabetic retinopathy. II. Prevalence and risk of diabetic retinopathy when age at diagnosis is less than 30 years. Arch Ophthalmol 1984;102:520-6.


17) Miyamoto K, Hiroshiba N, Tsujikawa A, Ogura Y. In vivo demonstration of increased leukocyte entrapment in retinal microcirculation of diabetic rats. Invest Ophthalmol Vis Sci 1998;39:2190-4.

18) Tabatabaei SA, Cheraqpour K, Pour EK, Bohrani Sefidan B. Long-term prophylaxis in an immunocompetent patient with Cytomegalovirus retinitis: a case report and review of literature. J Ophthalmic Inflamm Infect 2020;10:16.



19) Critchley JA, Carey IM, Harris T, et al. Glycemic control and risk of infections among people with type 1 or type 2 diabetes in a large primary care cohort study. Diabetes Care 2018;41:2127-35.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,211 View
- 113 Download
- Related articles
-
Lipemia Retinalis in a Patient with Diabetic Retinopathy.2014 April;55(4)
Central Serous Chorioretinopathy in a Patient with Retinal Macrovessel.2013 July;54(7)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



