접이식 홍채고정안내렌즈삽입술 후 각막내피세포 밀도의 5년간 변화
Five-year Change in Corneal Endothelial Cell Density after Foldable Iris-fixed Lens Insertion
Article information
Abstract
목적
접이식 홍채고정안내렌즈(Artiflex; Ophtec BV, Groningen, The Netherlands) 삽입 수술 후 5년간 각막내피세포 밀도의 변화를 보고하고, 전방부피와 전방깊이의 영향을 분석하였다.
대상과 방법
본 연구는 2009년 3월부터 2014년 3월까지 근시교정을 위한 접이식 유수정체 홍채고정렌즈(Artiflex) 수술을 받은 88명, 146안이 포함되었다. 정상인 20세, 25세, 30세 각각 100명의 각막내피세포 밀도를 측정 후 연령에 따른 각막내피세포 변화를 추정한 모방대조군으로 설정하여 수술 후 변화와 비교하였다. 렌즈와 각막내피까지의 거리 및 전방부피, 전방깊이를 4군으로 나눈 후 각막내피세포 밀도의 변화를 비교하였다.
결과
각막내피세포 밀도의 평균값은 수술 전, 수술 후 1년, 3년, 5년이 각각 3,038.8 ± 223.2, 2,985.3 ± 235.5, 2,905.1 ± 231.3, 2,814.9 ± 250.5 cells/mm2로 나타났다(각각 1.73%, 4.36%, 7.31% 감소, p<0.001). 이는 수술을 받지 않은 20세와 25세군의 2.2%의 차이, 25세와 30세군의 1.2% 차이와 비교하여 통계적으로 유의한 감소였다(p<0.001). 귀쪽의 렌즈와 각막내피 거리와 전방부피가 작은 군에서 각막내피세포 밀도의 감소가 다른 군에 비해 유의하게 컸다.
결론
접이식 홍채고정렌즈 삽입 수술 후 5년간 각막내피세포 밀도의 유의한 감소가 있으며, 렌즈와 각막내피까지의 거리와 전방부피가 적을수록 각막내피감소가 크게 나타났다.
Trans Abstract
Purpose
To investigate changes in corneal endothelial cell density over 5 years after implantation of Artiflex lenses (Ophtec BV, Groningen, The Netherlands) and to explore the influence of anterior chamber depth and volume on changes in endothelial cell density.
Methods
This study included 146 eyes of 88 patients implanted with foldable phakic iris-fixation intraocular (Artiflex) lenses for myopia correction from March 2009 to March 2014. To simulate chronological changes in endothelial cell density with age, we collected normal endothelial cell density data from 100 healthy subjects aged 20, 25, or 30 years, and compared the changes among these groups at 5 years after surgery. Changes in corneal endothelial cell density were compared among four groups to which subjects were assigned based on the distance from the intraocular lens to the corneal endothelium, and the volume and depth of the preoperative anterior chamber.
Results
The mean endothelial cell density, pre-operatively and at 1, 3, and 5 years post-operatively, was 3,038.8 ± 223.2, 2,985.3 ± 235.5, 2,905.1 ± 231.3, and 2,814.9 ± 250.5 cells/mm2, respectively (1.73%, 4.36%, and 7.31% reduction, respectively, vs. pre-operatively, p < 0.001). These differences were greater than those observed among different age groups (2.2% difference between 20- and 25-year-olds, and 1.2% difference between 25- and 30-year-olds, p < 0.001). A shorter distance from the lens to the endothelium and smaller anterior chamber volume were associated with greater decreases in endothelial cell density following surgery.
Conclusions
Corneal endothelial cell density significantly decreased during a 5-year follow-up after Artiflex lens implantation. The distance from the intraocular lens to the corneal endothelium, and the anterior chamber volume, were negatively correlated with the rate at which endothelial cell density decreased over time.
굴절이상을 교정하기 위한 수술은 엑시머레이저에 의한 레이저각막절삭가공성형술(laser-assisted in-situ keratomileusis, LASIK), 굴절교정레이저각막절제술(photorefractive keratectomy)부터 유수정체 안내렌즈삽입술 등이 있으며, 현재까지 활발하게 시행되고 있다. 하지만 엑시머레이저를 이용한 근시교정수술은 고도근시 환자에서는 각막확장증, 각막혼탁 등의 발생을 초래할 수 있으며[1] 안전하게 제거할 수 있는 각막 조직의 양은 제한되어 있다[2-4].
알티산(Artisan®; Ophtec BV, Groningen, The Netherlands) 혹은 알티플렉스(Artiflex®; Ophtec BV, Groningen, The Netherlands) 렌즈는 전방에 위치하여 고도근시나 원시 등을 교정하는 데 사용하는 유수정체 홍채고정렌즈이다. 알티산 렌즈는 다른 유수정체 안내렌즈에 비해 홍채에 고정이 가능하여 난시교정에 있어 회전 안정성이 좋고[5-8] 야간 눈부심이 덜하다는 장점이 있다[9-11]. 또한 알티플렉스 렌즈는 알티산 렌즈의 장점을 가지면서 더 작은 3.2 mm의 절개창을 통해 렌즈를 삽입할 수 있다[12]. 하지만 홍채고정렌즈 수술 방법은 선행 연구들을 통하여 단기적인 안전성은 인정받고 있으나[13-17], 아직 장기적인 각막내피세포 밀도에 대한 영향에 대해서는 보고가 부족하고, 일반적으로 나이가 들어감에 따라 전방이 감소한다는 것을 고려하면 홍채고정 렌즈로 인한 각막내피세포 감소는 장기적인 관점에서 지속적인 관찰이 필요하다[18,19]. 또한 국내에는 알티산 렌즈와 관련된 연구는 몇몇 있으나, 알티플렉스 렌즈와 관련된 연구는 거의 없는 실정이다.
Doors et al [20]의 242안을 대상으로 진행한 연구에서 렌즈의 모서리와 각막내피 사이의 거리가 짧을수록 각막내피세포 밀도의 감소가 통계적으로 유의하게 높았다고 보고하였다. 본 저자들도 렌즈의 중심부터 각막내피까지의 거리도 중요하지만, 모서리로부터 각막내피까지의 가장 가까운 거리가 짧은 경우 내피 손상을 일으킬 수 있는 위험이 증가한다고 생각하였고, 술 전에 이러한 요소들을 반영할 수 있는 전방부피가 각막내피세포 밀도 감소에 미치는 영향을 미칠 것이라고 가정하였다.
이 연구의 목적은 접이식 유수정체 홍채고정렌즈인 알티플렉스 렌즈 삽입 후 5년간 각막내피세포 밀도의 변화를 수술을 받지 않은 20세, 25세, 30세 모방대조군의 연령 간 차이와 비교하여 실제로 유의미한 감소가 있는지 알아보고, 각막내피세포 밀도 변화에 전방깊이, 전방부피, 렌즈로부터 각막내피까지의 거리가 영향을 주는지 알아보고자 하였다.
대상과 방법
본 연구는 한 명의 숙련된 술자(D.S.Y.K)에게 2009년 3월부터 2014년 3월까지 알티플렉스 혹은 토릭 알티플렉스(toric Artiflex®; Ophtec BV, Groningen, The Netherlands) 렌즈삽입술을 시행 받고, 5년 이상 경과 관찰한 146안의 의무기록을 후향적으로 조사하였다. 본 연구는 헬싱키선언을 준수하였으며, 연세대학교 원주세브란스기독병원 연구윤리심의위원회의 승인을 받았다(승인 번호: CR319110).
연구 대상자는 최근 1년 이상 굴절 상태가 안정된 환자였으며, 모두 수술 전 전방깊이가 2.84 mm 이상이었고, 각막내피세포밀도는 2,468 cells/mm² 이상이었다. 백내장, 녹내장, 포도막염, 각막질환, 망막의 이상 등의 다른 안질환이 있거나 고혈압, 당뇨 등의 전신질환이 있는 환자는 연구 대상에서 제외되었다.
모든 환자에서 수술 전 검사로 병력문진, 굴절검사, 최대교정시력, 각막곡률검사, 안압측정, 안저검사, 세극등검사, 각막지형도검사, 각막내피세포검사를 시행하였다. 각막내피세포 밀도는 비접촉성 경면현미경 검사기(SP-2000P; Topcon, Tokyo, Japan)를 통해 측정되었으며, 세포면적변이계수와 육각세포 비율까지 같이 측정하였다. 전방깊이와 수술 후 각막내피세포부터 렌즈까지의 거리는 전방 빛간섭단층촬영기(Visante OCT, Carl Zeiss Meditec, Germany)를 통해 측정하였다. 렌즈 중심으로부터 수직으로 각막내피까지의 거리를 측정하였고 동공의 중심을 지나는 180° 수평선으로 코 쪽과 귀 쪽으로 나누어 렌즈 모서리로부터 각막내피까지의 가장 가까운 거리를 측정하였다(Fig. 1). 각막지형도검사기(Oculus Pentacam; OCULUS Optikgerate GmbH, Wetzlar, Germany)를 통해 각막두께와 전방부피를 측정하였다. 수술 후 검사는 1달, 1년, 3년, 5년에 굴절검사, 최대교정시력, 안압측정, 세극등검사, 각막지형도검사, 전방 빛간섭단층촬영, 각막내피세포검사를 시행하였다. 삽입하고자 하는 렌즈의 도수는 전방깊이, 각막곡률, 굴절력, 난시축 등을 이용하여 제조사(Ophtec BV, Groningen, the Netherlands)에서 제시하는 Van der heijde Nomogra에 의해 계산된 도표를 참고하여 결정하였다. 모든 수술은 숙련된 1인(D.S.Y.K)에 의해 시행되었으며 이전 연구들과 같은 수술 방법과 과정으로 진행되었다[21].
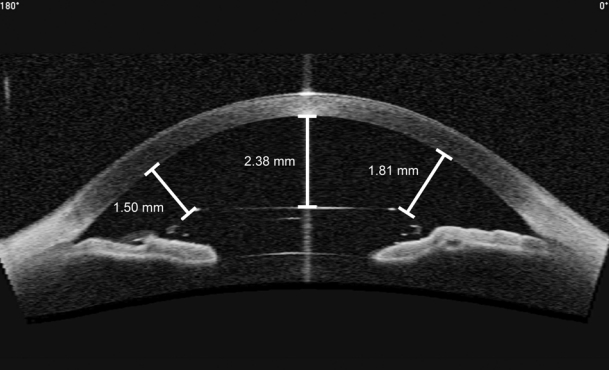
Measurement of intraocular lens to endothelium distance. Indicators are distance of intraocular lens to endothelium at temporal, center and nasal, respectively, from the left.
렌즈와 각막내피까지의 거리 및 전방부피, 전방깊이가 각막내피세포 밀도에 주는 영향을 알아보기 위해 해당 요인들을 중앙값을 중심으로 4군으로 나눈 뒤 평균을 비교하였다. 거리 혹은 부피가 25% 측정치까지 1군, 그 이후 값부터 중앙값까지 2군, 중앙값에서 75% 측정치까지를 3군, 75% 이후부터 최대 측정치까지 4군으로 정의하였다. 렌즈로부터 각막내피 중심까지의 거리를 기준으로 나눈 네 군은 1군이 1.79-2.02 mm, 2군이 2.03-2.25 mm, 3군이 2.26-2.55 mm 4군이 2.56-2.86 mm였다. 렌즈로부터 각막내피 코 쪽 거리를 기준으로 나눈 네 군은 1군이 1.11-1.37 mm, 2군이 1.38-1.64 mm, 3군이 1.65-1.94 mm, 4군이 1.95-2.25 mm였다. 렌즈로부터 각막내피 귀 쪽 거리를 기준으로 나눈 네 군은 1군이 1.00-1.33 mm, 2군이 1.34-1.67 mm, 3군이 1.68-1.95 mm, 4군이 1.96-2.23 mm였다. 전방깊이를 기준으로 나눈 네 군은 1군이 2.84-3.10 mm, 2군이 3.11-3.37 mm, 3군이 3.38-3.63 mm, 4군이 3.64-3.91 mm였다. 전방 부피의 네 군은 1군이 146-177 μL, 2군이 178-207 μL, 3군이 208-245 μL, 4군이 246-283 μL였다(Fig. 2).
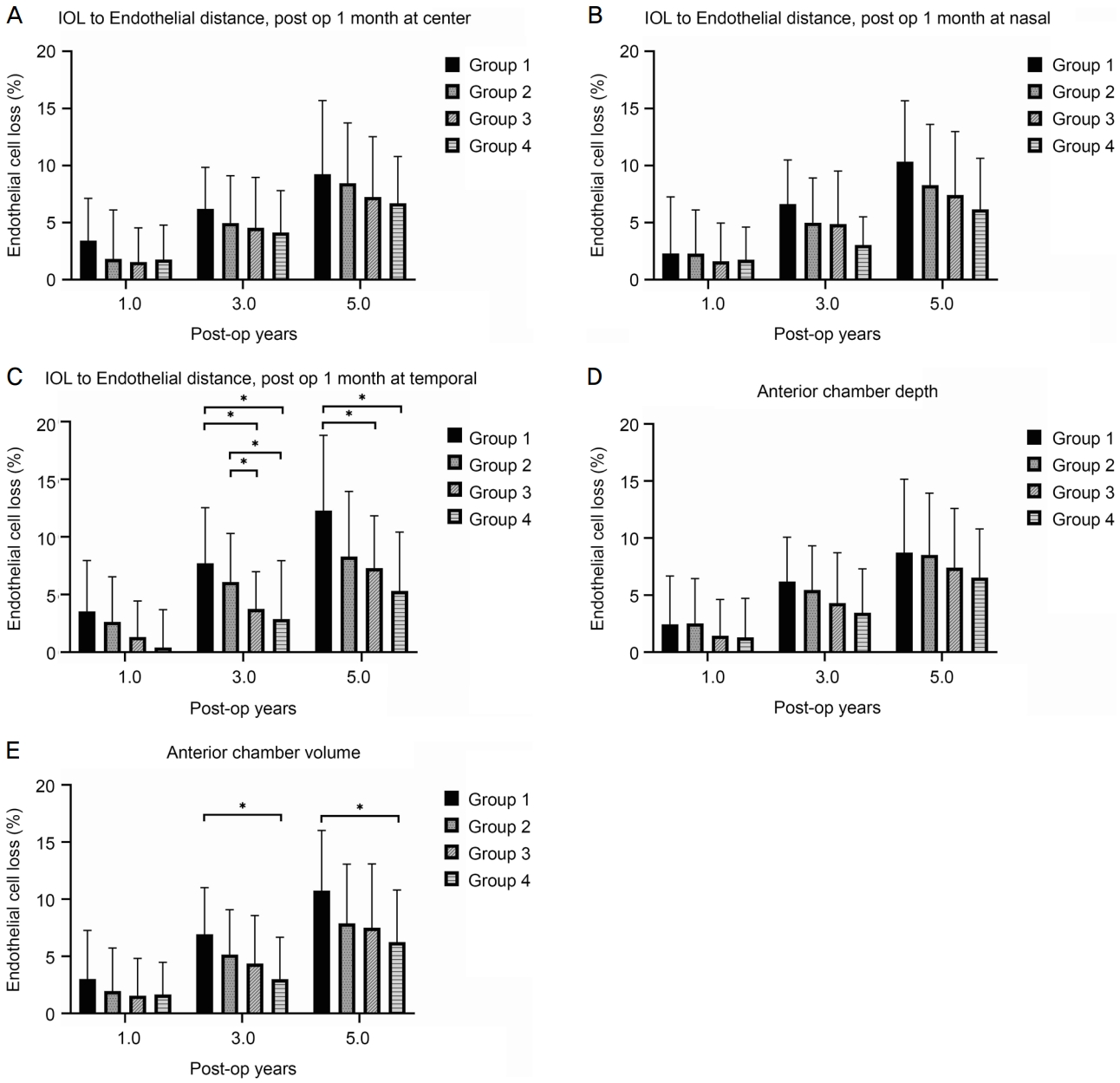
Comparison of endothelial cell density loss (%) between 4 groups divided by the distance (post op 1 month) from intraocular lens to endothelium, anterior chamber depth and anterior chamber volume (A-E). In the (C) divided by the distance (post op 1 month) from intraocular lens to endothelium at temporal and the (E) divided by anterior chamber volume, the difference between group 1 and group 4 was statistically significant at 3 and 5 years postoperatively as indicated by asterisks (p < 0.05). Error bars represent the standard deviation. IOL = intraocular lens.
통계 분석은 SPSS 22.0 (SPSS® statistics, IBM Corp., Armonk, NY, USA)을 이용하였다. 본 연구의 주요 관심 변수인 각막내피세포는 나이가 들어감에 따라 생리적으로 감소하게 된다. 수술 후 추적 관찰 기간 중에도 연령 증가에 따른 생리적 변화는 나타날 수 있으므로 이를 가늠하기 위하여 수술을 받지 않은 정상군의 측정치와 비교하였다. 이상적인 대조군은 5년간 경과 관찰한 데이터이지만 이러한 데이터를 얻기 힘들기 때문에, 동일 기관에서 동일 장비로 측정한 정상군 데이터를 모방대조군으로 설정하였다. 즉, 수술 대상군을 모방할 수 있는 연령인 20, 25, 30세 각 100명씩의 각막내피세포검사 결과를 연령별 참고치로 활용하였다. 수술 전과 수술 후 추적 관찰 시점에 각막내피세포 밀도의 분석은 반복측정분산분석을 시행하였고, 모방대조군과 수술군의 차이는 독립 t-검정을 시행하였으며, 여러 시점의 변수 비교를 위해서는 Tukey와 Bonferroni 교정을 통한 사후분석을 시행하였다. 각막내피세포 밀도와 렌즈와 각막내피까지의 거리 및 전방 부피, 전방깊이의 요인들을 기준으로 네 군으로 나눈 후 분산분석을 시행하였다. p값이 0.05 미만인 경우 통계적으로 유의하다고 판단하였다.
결 과
총 88명 중 146안이 대상이 되었으며, 평균연령은 27 ± 4.55세, 평균 구면렌즈 대응치는 -7.78 ± 2.52 diopters (D)를 보였다. 평균 각막내피세포 밀도는 3,058 ± 230.33 cells/mm2였으며 이들의 인구통계학적 특성은 Table 1에 표시하였다. 수술 후 평균 굴절 오차는 구면도수가 0.05 ± 0.35, 난시 도수가 -0.29 ± 0.25 D였으며, 평균 최대교정시력은 -0.1 ± 0.08 logMAR였다.
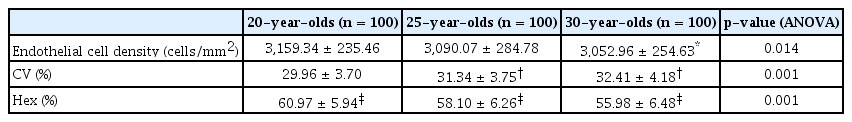
수술군과 비슷한 연령대에서 나이에 따른 변화를 가늠하기 위해 20세, 25세, 30세 각 100명씩에서 추출한 모방대조군을 보면, 20세의 평균 각막내피세포 밀도는 3,159.34 ± 235.46 cells/mm2, 25세는 3,090.07 ± 284.78 cells/mm2, 30세는 3,052.96 ± 254.63 cells/mm2였다(Table 2). 이 차이는 20세와 25세는 2.2%, 25세와 30세는 1.2%로서, 기존에 보고된 매년 0.6%씩 감소하는 생리적인 감소율과 큰 차이 없는 결과였다[22-24].
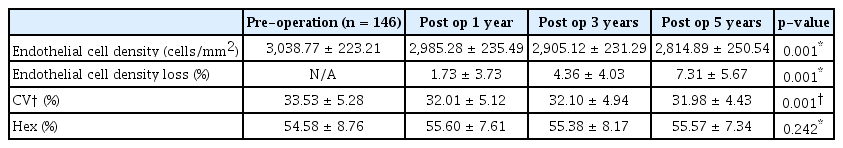
각막내피세포 밀도는 수술 전에 비해 1년 동안 1.73% 감소를, 3년 동안 4.36% 감소를, 5년 동안 7.31% 감소를 보였다(Table 3). 또한, 각막내피세포 밀도의 수술 후 5년 감소율은 모방대조군에서 20세에서 25세까지 군의 5년간 2.2%의 차이, 25세에서 30세까지 5년간 1.2% 차이 수치에 비교하여 통계적으로 유의한 감소였다(p<0.001, independent t-test) (Fig. 3). 수술 전의 세포면적 변이계수는 33.53 ± 5.28%, 술 후 1년에서 32.01 ± 5.12%, 3년에서 32.10 ± 4.94%, 5년에서 31.98 ± 4.43%로 나타났고, 수술 전과 술 후 1년, 술 후 3년, 술 후 5년 사이는 통계적으로 유의한 차이가 있으나, 수술 후 측정치들은 통계적인 차이가 없었다(Table 3). 모방대조군의 세포면적 변이계수는 20세에서 29.96 ± 3.70%, 25세에서 31.34 ± 3.75%, 30세에서 32.41 ± 4.18%였으며 20세와 25세, 20세와 30세 사이는 통계적으로 유의한 차이였다(Table 2).
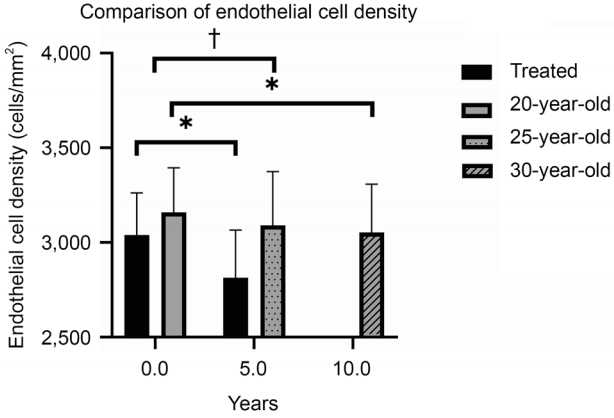
Comparison of endothelial cell density. *In the Bonferroni post-hoc analysis, comparison between 20-year-olds and 30-year-olds and between pre-operation and post-op 5 years p < 0.05; †independent t-test, p < 0.001.
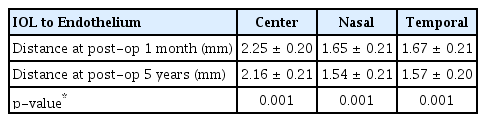
술 후 1달에 측정한 렌즈로부터 각막내피중심까지 거리의 평균은 2.25 ± 0.208 mm (1.79-2.86)였으며, 술 후 5년에 측정한 거리의 평균은 2.16 ± 0.210 mm (1.59-2.70)였다. 술 후 1달에 측정한 렌즈 모서리로부터 코 쪽에 가장 가까운 각막내피와의 거리 평균은 1.65 ± 0.216 mm (1.08-2.37), 술 후 5년에 측정한 거리의 평균은 1.54 ± 0.216 mm (1.04-2.17)였다. 렌즈 모서리로부터 귀 쪽에 가장 가까운 각막내피와의 거리 평균은 술 후 1달에 1.67 ± 0.212 mm(1.00-2.23), 술 후 5년에 1.57 ± 0.208 mm (0.77-2.17)로 측정되었다. 술 후 1달과 술 후 5년에 측정한 렌즈와 각막내피 사이의 거리를 비교하면 모든 방향인 중심, 코 쪽, 귀 쪽에서 통계적으로 유의하게 감소하였다(p<0.001, paired t-test) (Table 4).
술 후 1달에 측정한 렌즈에서 중심 각막내피까지의 거리에 따라 네 군으로 나눌 때, 렌즈 모서리에서 코 쪽 각막내피까지의 거리를 기준으로 4군으로 나눌 때와 술 전 전방 깊이를 기준으로 네 군으로 나눌 때는 거리가 가장 가까운 1군에서 각막내피세포 감소가 크고, 네 군으로 갈수록 각막내피세포 감소가 작은 경향이 보였으나 통계적으로 유의한 차이는 보이지 않았다.
귀 쪽 방향 측정에서는 술 후 3년에서 1군은 7.71 ± 4.83%, 2군은 6.09 ± 4.21%, 3군은 3.75 ± 3.22%, 4군은 2.87 ± 5.07%의 감소를 보였다(p<0.001, analysis of variance). 사후검정에서 1군과 2군, 3군과 4군 간 비교를 제외하고 나머지 군 사이에서 모두 통계적으로 유의한 차이를 보였다(p<0.05, Bonferroni). 술 후 5년에서는 1군은 각막내피세포 감소가 12.28 ± 6.52%, 2군은 8.30 ± 5.65%, 3군은 7.30 ± 4.53%, 4군은 5.31 ± 5.11%였으며(p=0.006) 1군과 3, 4군 사이의 차이는 통계적으로 유의한 차이였다(p=0.017, p=0.007, Bonferroni).
전방부피를 기준으로 4군으로 나눌 때, 술 후 3년에서는 1군은 6.92 ± 4.08%, 2군은 5.15 ± 3.93%, 3군은 4.36 ± 4.20%, 4군은 2.99 ± 3.67%의 감소를 보였다(p=0.018). 사후검정에서 1군과 4군은 통계적으로 유의한 차이를 보였다(p=0.016, Bonferroni). 술 후 5년에서는 1군은 10.75 ± 5.26%, 2군은 7.88 ± 5.18%, 3군은 7.49 ± 5.58%, 4군은 6.23 ± 4.57%의 감소를 보였다(p=0.048). 사후검정에서 1군과 4군은 통계적으로 유의한 차이를 보였다(p=0.050, Bonferroni).
고 찰
국내외에서 고도근시 혹은 난시를 교정하기 위한 유수정체 안내렌즈삽입술이 많이 시행되고 있다[23,25,26]. 하지만 아직 국내 보고가 부족한 상태이며, 수술 후 장기적인 영향에 대해서는 아직까지 우려가 있다[18,19]. 유수정체 홍채 고정 안내렌즈는 각막내피세포의 손상을 유발할 수 있어 수술 전 각막내피세포에 대한 검사가 면밀히 필요하고, 술 후에도 정기적인 각막내피세포검사가 중요하다[17,27,28].
Doors et al [20] (2008)은 알티산과 알티플렉스를 모두 포함하여 242안에 대해서 연구하였고, 각막내피세포 밀도의 변화가 2년 동안 1.28% 감소, 5년 동안 3.25% 감소, 7년 동안 5.02% 감소를 보고하였다. 또한 전방 빛간섭단층촬영을 통해 측정한 결과, 안내렌즈로부터 각막내피세포까지의 거리가 가까울수록 각막내피세포 밀도의 감소가 심했고, 유의한 영향이 있다고 보고하였다.
Doors et al [12] (2012)의 알티플렉스에 대한 연구에서는 수술 후 3개월에는 처음에 비해 4.8%의 각막내피세포의 감소가 있었으나, 이후 추가적인 감소는 없었다고 보고하였다. Jonker et al [29]은 알티플렉스에 대한 192안에 대한 연구에서 각막내피세포 밀도의 변화가 6개월 동안 2.15% 감소, 1년동안 2.99% 감소, 5년 동안 9.46% 감소를 보고하였다.
본 연구에서는 각막내피세포 밀도가 수술 전에 비해 1년동안 1.73% 감소, 3년 동안 4.36% 감소, 5년 동안 7.31% 감소했다. Doors et al [20] (2008)의 연구에 비해서는 5년간 감소가 크지만, Jonker et al [29]의 연구에서보다는 적은 수치였다.
각막내피세포는 나이가 들어감에 따라 생리적으로 감소하게 된다. 이 생리적 변화를 감안하여 수술 후 변화를 평가하기 위해 본 연구에서는 정상군의 측정치를 분석하였다. 정상군에서 수술한 환자들처럼 5년간 경과 관찰한 데이터는 사실상 얻기 힘들기 때문에 나이가 같은 무작위 100명을 선정하여 각막내피세포를 측정하였다. 20세에서 25세까지 2.2%의 차이를, 25세에서 30세에서 1.2% 차이를 확인할 수 있었으며, 이 수치는 이전에 보고된 생리적 감소율인 1년의 0.6%와 큰 차이를 보이진 않았다[22-24].
세포면적 변이계수는 앞선 연구들에 의하면 연령에 따라 생리적으로 증가하는 양상이며 본 연구의 모방 대조군에서도 이러한 경향을 보였다[30-33]. 하지만 Benedetti et al [34]은 알티산 삽입 수술 후 세포면적계수의 감소를 보고하였다. 본 연구에서도 마찬가지로 수술 전 33.53 ± 5.28%에서 술 후 1년 32.01 ± 5.12%, 3년 32.10 ± 4.94%, 5년 31.98 ± 4.43%로 술 후 측정치가 감소하였다. 본 연구에서 수술 후 세포 면적계수의 감소와 술 후 1-5년 사이에 변화가 없는 이유는 수술 후 각막내피세포의 리모델링 과정에서 안정화되었기 때문으로 생각된다.
전방깊이는 나이가 증가함에 따라 생리적으로 감소함이 이전 연구들로부터 확인되었다. 또한 감소 속도도 나이에 따라 달라진다. 본 연구에서는 대상자들은 동양인이며, 평균 -7.78 ± 2.52 D의 근시를 가지고, 평균 나이 27 ± 4.55세인 특징을 가졌다. 수술 후 5년 뒤, 렌즈로부터 각막내피까지의 거리가 중심부에서 0.09 mm, 코 쪽에서 0.11 mm, 귀쪽에서 0.10 mm씩 감소하였고 이는 통계적으로 유의한 차이였다(p=0.001). Foster et al [35]의 연구에서는 20대에서 30대 사이 남성에서는 1년에 0.011 mm, 여성에서는 1년에 0.012 mm의 생리적인 전방깊이 감소율을 보고하였고 이는 본 연구의 감소율보다 작은 수치였다. He et al [36]의 연구에서는 벨기에인이 20대에서 40대 사이 전방깊이 감소율이 1년에 0.013 mm로 보고되었고, 이누이트는 20대에서 30대 사이 전방깊이 감소율이 1년에 0.021 mm로 보고되었다. 인종에 따라 연령 증가에 따른 전방깊이 감소율이 다르지만, 본 연구에서의 홍채고정렌즈 삽입 후 전방깊이는 생리적 감소량보다 2배 더 감소한 것으로 보이며, 이러한 원인에 대해서는 추가적인 연구가 더 필요할 것으로 사료된다. 기존 연구들에서 전방깊이의 생리적인 감소량은 20세에서 50세에서 가장 많았으며, 렌즈삽입술의 수술 시기가 보통이 범위 내에 있다는 것을 감안하면 수술 후 전방깊이의 변화에도 관심을 가져야 할 것으로 생각된다[35-37].
Doors et al [12]의 연구에서 렌즈 표면으로부터 각막내피까지의 거리가 가까울수록 더 높은 각막내피세포 밀도의 감소를 보이는 결과가 본 연구에서도 확인되었다. 본 연구에서는 렌즈에서부터 각막내피 중심까지의 거리와 렌즈의 모서리부터 코 쪽 각막내피까지의 거리를 기준으로 나누었을 때는 유의한 차이를 보이진 않았으나, 귀 쪽 각막내피까지의 거리를 네 군으로 나눠서 비교하였을 때, 술 후 3년과 5년에서 거리가 가장 짧은 1군과 가장 긴 4군 사이의 각막내피세포 감소는 통계적으로 유의한 차이를 보였다. 이는 렌즈에서 각막내피까지의 거리가 추후 각막내피세포 밀도에 주요한 영향을 끼치는 인자임을 시사한다. 하지만 이 거리는 수술 후에 측정할 수 있는 거리이기 때문에, 수술 전에 환자의 예후를 파악, 예측할 수 있는 직접적인 항목은 아니다.
본 연구에서 전방깊이에 따라 네 군으로 나누었을 때 시간에 따른 각막내피세포 감소의 차이가 유의하지 않았다. 하지만, 전방깊이가 중요한 인자가 아니라고 단정할 수는 없다. 본 연구는 후향적 연구로서 연구에 포함된 대상자들은 자연스럽게 술 전 검사에서 매우 안정적일 것으로 예상되었던 환자만 포함되었다는 한계점이 있다. 즉, 전방깊이가 가장 작은 사람은 2.84 mm이고 3.00 mm 이하는 단지 4명으로 전방깊이가 더 낮은 위험군이 포함되어 있지 않기 때문에 그룹 간 통계적인 차이가 나타나지 않았을 것으로 생각된다. 물론 이 연구가 각막내피세포 감소의 위험요인을 완전하게 분석하기 어려운 요인도 후향적 연구에서 기인하기 때문에, 각막내피세포 변화와 관련하여서는 보다 많은 전향적인 연구들이 필요할 것으로 생각된다.
본 연구에서는 전방부피가 적은 1군이 부피가 큰 4군보다 각막내피세포 감소가 통계적으로 유의하게 크다는 것을 확인하였다. 이는 전방부피가 중심부 전방깊이뿐만 아니라 주변부의 전방깊이와 직경을 반영하는 값이기 때문으로 생각할 수 있다. 중심부로부터 각막내피까지의 거리보다 일반적으로 렌즈 모서리부터 주변부 각막내피까지의 거리가 더 가깝고 우연히 외상이나 눈을 비비는 행위 등으로 렌즈와 각막내피의 접촉이 일어날 확률이 더 높을 수 있기 때문에, 주변부 각막내피까지의 거리가 더 중요한 인자로 보인다. 이 주변부 각막내피까지의 거리를 더 많이 반영하는 수술 전 인자가 전방부피이며, 그렇기 때문에 전방깊이 보다 더 좋은 예후 인자일 수 있다.
국내에서는 알티산 렌즈와 관련된 몇몇의 연구가 있으나 알티플렉스 렌즈와 관련된 연구는 거의 없으며, 50안 이상, 2년 이상의 추적 관찰 기간을 가진 연구는 없었다. 이 연구는 국내 단일기관에서 시행한 총 146안을 5년간 추적 관찰하였으며 이는 이 연구의 강점이 될 수 있겠다.
결론적으로 알티플렉스 렌즈삽입술 5년간 지속적인 각막내피세포감소를 확인할 수 있었다. 수술 전 전방부피가 적을수록 각막내피세포감소가 증가함을 확인하였다. 따라서, 전방깊이 뿐만 아니라 전방부피를 수술 전 평가 요소로 고려하는 것이 좋을 것으로 생각된다. 생리적으로 전방깊이와 전방 부피는 나이가 들면서 감소하기 때문에 장기적인 환자의 예후를 면밀히 평가하여 유수정체용 홍채고정렌즈 수술을 시행해야 할 것이다.
Notes
Conflict of Interest
The authors have no conflicts to disclose.
References
Biography
남명식 / Myungsik Nam
연세대학교 원주의과대학 안과학교실
Department of Ophthalmology, Yonsei University Wonju College of Medicine