 |
 |
| J Korean Ophthalmol Soc > Volume 62(3); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ĒåĀļü╝ņŚÉņä£ ņŖżĒÄÖĒŖĖļ¤╝ņśüņŚŁ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(spectral domain optical coherence tomography, SD-OCT)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗ£ņŗĀĻ▓Įņ£ĀļæÉ(optic nerve head, ONH)ļĪ£ļČĆĒä░ Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ļ¦Øļ¦ē Ļ░ü ņĖĄņØś ļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśĻ│Ā ņØ┤ļź╝ ĒåĄĒĢ┤ ļ¦Øļ¦ē ļÅÖļ¼╝ņŗżĒŚśļ¬©ļŹĖņŚÉņä£ņØś ĻĖ░ļ│Ė ņ×ÉļŻīļź╝ ņ¢╗Ļ│Āņ×É ĒĢ£ļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
ĒåĀļü╝ 15ļ¦łļ”¼ņØś ņÜ░ņĢłņŚÉņä£ SD-OCT ņśüņāüņØä ņ¢╗ņØĆ Ēøä, ONH ĒģīļæÉļ”¼ņŚÉņä£ ņŗ£ņ×æĒĢśņŚ¼ ĒĢśļ░®ņ£╝ļĪ£ 1, 2, 3, 4 ĻĘĖļ”¼Ļ│Ā 5 mm ņ£äņ╣śņŚÉņä£ ņĀäņ▓┤ ļ¦Øļ¦ēņĖĄ, ļé┤ļ¦Øļ¦ēņĖĄ, ņÖĖļ¦Øļ¦ēņĖĄ, ļ¦źļØĮļ¦ēņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ, ļé┤ĒĢĄņĖĄ, ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄņØś ļæÉĻ╗śļź╝ ņ¢╗ņŚłņ£╝ļ®░, ņĖĪņĀĢ ņ£äņ╣śņŚÉ ļö░ļźĖ Ļ░ü ņĖĄņØś ļæÉĻ╗śļź╝ ļ╣äĻĄÉĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗ś(PearsonŌĆÖs correlation coefficient [CC]=-0.778, p<0.05), ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗ś(CC=-0.710, p<0.05), ņÖĖļ¦Øļ¦ēņĖĄ ļæÉĻ╗ś(CC=-0.495, p<0.05), ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ ļæÉĻ╗ś(CC=-0.292, p<0.05), ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ ļæÉĻ╗ś(CC=-0.284, p<0.05), ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄ ļæÉĻ╗ś(CC=-0.760, p<0.05)ļŖö ONHņŚÉņä£ ņĢäļלļĪ£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ░ÉņåīĒĢśņśĆļŗż. ļé┤ĒĢĄņĖĄ ļæÉĻ╗śļÅä ONHņŚÉņä£ņØś Ļ▒░ļ”¼ņÖĆ ņØīņØś ņāüĻ┤ĆĻ┤ĆĻ│äļź╝ ļ│┤ņśĆņ£╝ļéś ņāüĻ┤ĆĻ│äņłśļŖö ļé«ņĢśļŗż(CC=-0.263, p<0.05). ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ONHņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ ņ”ØĻ░ĆĒĢśņśĆļŗż(CC=0.511, p<0.05).
ABSTRACT
Purpose
We used spectral domain optical coherence tomography (SD-OCT) to assess the retinal and choroidal thicknesses of the rabbit, a commonly used animal model of ophthalmic disease. We report normative datasets.
Methods
Semi-automated measurements were made on 15 normal right eyes of New Zealand white rabbits. Total retinal, inner retinal layer, outer retinal layer, choroidal, ganglion cell layer, ganglion cell complex, inner nuclear layer, and outer nuclear layer thicknesses were measured at fixed distances (0, 1, 2, 3, 4, and 5 mm) below the optic nerve head.
Results
Total retinal layer (PearsonŌĆÖs correlation coefficient [CC] = -0.778, p < 0.05), inner retinal layer (CC = -0.710, p < 0.05), outer retinal layer (CC = -0.495, p < 0.05), ganglion cell complex (CC = -0.292, p < 0.05), ganglion cell layer (CC = -0.284, p < 0.05), and outer nuclear layer thicknesses (CC = -0.760, p < 0.05) decreased with the distance from the optic nerve head. Inner nuclear layer thickness correlated negatively with the distance from the optic nerve head, but the correlation coefficient was low (CC = -0.263, p < 0.05). Choroidal thickness increased with the distance from the optic nerve head (CC = 0.511, p < 0.05).
ļ¦Øļ¦ēļæÉĻ╗śņØś ņĖĪņĀĢ ļ░Å ĻĘĖņŚÉ ļīĆĒĢ£ ļČäņäØņØĆ ļŗżņ¢æĒĢ£ ņĢłĻ│╝ ņ¦łĒÖśņØś ņ¦äļŗ© ļ░Å ņ╣śļŻīņŚÉ ņØśļ»Ė ņ׳Ļ▓ī ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż[1,2]. ņØ┤ļź╝ ņ£äĒĢ£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(optical coherence tomography, OCT)ņØĆ ļ╣äņ╣©ņŖĄņĀüņ£╝ļĪ£ ļ¦Øļ¦ē Ļ░ü ņĖĄņØä Ļ│ĀĒĢ┤ņāüļÅäļĪ£ ņŗ£Ļ░üĒÖöĒĢśņŚ¼ ļ¦Øļ¦ē ļ»ĖņäĖĻĄ¼ņĪ░ļź╝ ĒÖĢņØĖĒĢśĻ│Ā ĻĘĖ ļæÉĻ╗śļź╝ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŖö Ļ▓Ćņé¼ļĪ£ 1991ļģä ņ▓śņØī ņåīĻ░£ļÉ£ ņØ┤Ēøä ņŚ¼ļ¤¼ ļ¦Øļ¦ē ņ¦łĒÖśņØś ļČäņäØņŚÉ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż[2,3]. ĻĖ░ņĪ┤ņŚÉļŖö ņ┤łļŗ╣ 400ĒÜīņØś ņŖżņ║öņ£╝ļĪ£ ņČĢ ĒĢ┤ņāüļÅä(axial resolution) 8-10 ╬╝mņØĖ ņŗ£Ļ░äņśüņŚŁ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(time domain OCT, TD-OCT)ņØ┤ ļäÉļ”¼ ņØ┤ņÜ®ļÉśņŚłņ£╝ļéś, ņĄ£ĻĘ╝ņŚÉļŖö ĻĖ░ņĪ┤ OCTņŚÉ ļ╣äĒĢ┤ ņŖżņ║ö ņåŹļÅäĻ░Ć 50-100ļ░░ ņØ┤ņāü ļ╣Āļź┤Ļ│Ā ĒĢ┤ņāüļÅäļÅä ļŹö ļåÆņØĆ ņŖżĒÄÖĒŖĖļ¤╝ņśüņŚŁ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(spectral domain OCT, SD-OCT)ņØä ņŻ╝ļĪ£ ņé¼ņÜ®ĒĢśĻ│Ā ņ׳ļŗż[1]. SD-OCTļŖö ņ┤łļŗ╣ 25,000-100,000ĒÜīņØś ņŖżņ║öņ£╝ļĪ£ ņČĢ ĒĢ┤ņāüļÅä 5-10 ╬╝mņØĖ ņśüņāüņØä ņ¢╗ņØä ņłś ņ׳ņ¢┤ņä£ ņŗ£ņäĖĒż ņĢłņ¬ĮĻ│╝ ļ░öĻ╣źņ¬ĮņØś ņĀæĒĢ®ļČĆ(inner segment/outer segment junction)ļÅä ļ│┤ņŚ¼ņżä ļ┐Éļ¦ī ņĢäļŗłļØ╝ ļ¦Øļ¦ē ņĖĄļ│ä ļæÉĻ╗śļź╝ ļ│┤ļŗż ņĀĢĒÖĢĒ׳ ņé┤ĒÄ┤ļ│╝ ņłś ņ׳Ļ▓ī ĒĢ┤ņŻ╝ņŚłļŗż[4-6]. ņØ┤ņŚÉ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ĒåĄĒĢ£ ļ¦Øļ¦ēņØś ĒĢ┤ļČĆĒĢÖņĀü ĒÅēĻ░ĆļŖö ļ¦Øļ¦ēņ¦łĒÖśņØś ņŚ░ĻĄ¼ ļ░Å ņ¦äļŗ©ņŚÉ ĒĢäņłś ņÜöņåīĻ░Ć ļÉśņŚłļŗż[2].
ļÅÖļ¼╝ņŚÉņä£ ļ¦Øļ¦ēņØś ņĪ░ņ¦üĒĢÖņĀü ĒÅēĻ░ĆļŖö ņśżļ×½ļÅÖņĢł ļ¦Øļ¦ēņØś ļ»ĖņäĖĻĄ¼ņĪ░ļź╝ ņŚ░ĻĄ¼ĒĢśļŖö ņŻ╝ļÉ£ ļ░®ļ▓ĢņØ┤ņŚłļŖöļŹ░[7], ļÅÖļ¼╝ ļ¬©ļŹĖņŚÉņä£ ļ¦Øļ¦ēņØś SD-OCTļŖö ĻĘĖ ņĪ░ņ¦üĒĢÖņĀü Ļ▓░Ļ│╝ņÖĆ ļ¦żņÜ░ ļ░ĆņĀæĒĢ£ ņŚ░Ļ┤Ćņä▒ņØä Ļ░Ćņ¦ł ļ┐É ņĢäļŗłļØ╝ ļ╣ĀļźĖ ņŗ£Ļ░äņŚÉ ļ╣äņ╣©ņŖĄņĀüņ£╝ļĪ£ ļ¦Øļ¦ē ņĖĄļ│ä ĻĄ¼ņĪ░ļź╝ ļ│╝ ņłś ņ׳Ļ▓ī ĒĢ┤ņżśņä£[8-10] ņÜ░ļ”¼ļŖö ņĪ░ņ¦üĒĢÖņĀü ĒÅēĻ░Ćļź╝ ņ£äĒĢ┤ ļÅÖļ¼╝ņØä ĒؼņāØņŗ£ĒéżĻĖ░ ņĀäņŚÉ ļ¦Øļ¦ēņØś ļ»ĖņäĖ ļ│ĆĒÖöļź╝ ņČöņĀĢĒĢĀ ņłś ņ׳Ļ▓ī ļÉśņŚłļŗż. ļÅÖļ¼╝ļ¬©ļŹĖ ņżæ ĒåĀļü╝(rabbit)ļŖö ĻĖ░ļź┤Ļ│Ā ļŗżļŻ©ļŖö Ļ▓āņØ┤ ņēĮĻ│Ā, ĒĢ┤ļČĆĒĢÖņĀü ĻĄ¼ņĪ░Ļ░Ć ņל ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░, ņŚ¼ļ¤¼ ļ¦Øļ¦ē ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśĻĖ░ ņóŗņØĆ ņżæĻ░ä Ēü¼ĻĖ░ņØś ļÅÖļ¼╝ņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ļ¦Øļ¦ēņ¦łĒÖśņØä ņŚ░ĻĄ¼ĒĢśļŖö ļŹ░ ņ£ĀņÜ®ĒĢśļŗż[11]. ĒŖ╣Ē׳ ĒåĀļü╝ļŖö ņ£Āļ”¼ņ▓┤ļé┤ ņĢĮļ¼╝ļÅÖļĀźĒĢÖĻ│╝ ņĢĮļ¼╝ņØś ļÅģņä▒ ņŚ░ĻĄ¼ņŚÉņä£ Ļ░Ćņן ĒØöĒ׳ ņØ┤ņÜ®ļÉśļŖö ļÅÖļ¼╝ņØĖļŹ░ ņØ┤ļŖö ĒåĀļü╝ņØś ņ£Āļ”¼ņ▓┤ļé┤ ļČäĒż ņÜ®ņĀü, ņ▓Łņåīņ£©, ļ░śĻ░ÉĻĖ░Ļ░Ć ņé¼ļ×īņØś ļłłĻ│╝ ņ£Āņé¼ĒĢśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż[12,13].
ĻĖ░ņĪ┤ņŚÉļÅä SD-OCTļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗ£ņŗĀĻ▓Įņ£ĀļæÉ(optic nerve head, ONH) Ļ░Ćņןņ×Éļ”¼ļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ĒåĀļü╝ ļ¦Øļ¦ēļæÉĻ╗śņŚÉ ļīĆĒĢ£ ņĀĢļ¤ēĒÖöļÉ£ ļČäņäØņØä ņŗ£Ē¢ēĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ņ׳ņŚłņ£╝ļéś[8,9], ĻĘĖ ļČäņäØņØĆ ļ¦Øļ¦ē ņĀäņĖĄņØś ļæÉĻ╗ś ļČäņäØ Ēś╣ņØĆ ļ¦Øļ¦ē ņŗ£ņŗĀĻ▓Įņä¼ņ£ĀņĖĄ ļČäņäØņŚÉ ĻĄŁĒĢ£ļÉ£ ņŚ░ĻĄ¼ļĪ£ ņŗżĒŚśņĀü ĒÅēĻĘĀ ņ×ÉļŻīļĪ£ ĒÖ£ņÜ®ĒĢśĻĖ░ņŚÉļŖö ĒĢ£Ļ│äņĀÉņØ┤ ņ׳ņŚłļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀäņ▓┤ ļ¦Øļ¦ēļ┐É ņĢäļŗłļØ╝ ļé┤ļ¦Øļ¦ēņĖĄ(inner retinal layer), ņÖĖļ¦Øļ¦ēņĖĄ(outer retinal layer), ļ¦źļØĮļ¦ēņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ(ganglion cell layer, GCL), ļé┤ĒĢĄņĖĄ(inner nuclear layer, INL), ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄ(outer nuclear layer, ONL)ņØś 8Ļ░Ćņ¦Ć ņĖĄņØś ļæÉĻ╗śļź╝ ļ¬©ļæÉ ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░, ļ¦Øļ¦ē ņ£äņ╣śņŚÉ ļö░ļØ╝ Ļ░ü ņĖĄņØś ļæÉĻ╗śĻ░Ć ņ¢┤ļ¢╗Ļ▓ī ļŗżļźĖņ¦Ćļź╝ ņé┤ĒÄ┤ļ│┤ņĢśļŗż.
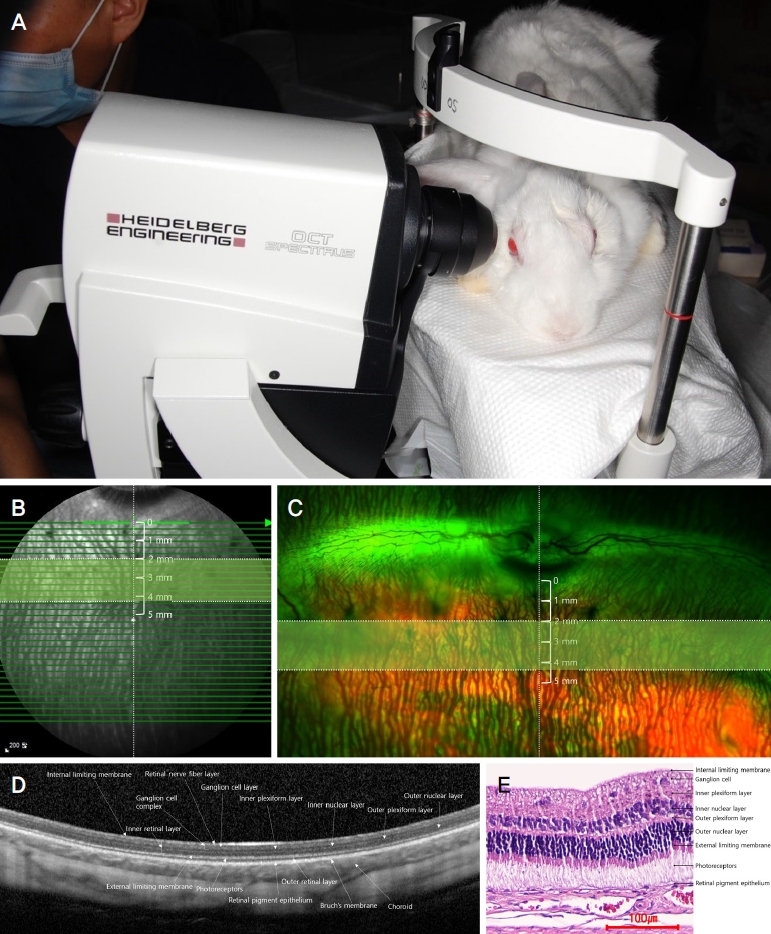
ņÖĖĻ▓¼ņāü ņ¦łĒÖśņØ┤ ņŚåĻ│Ā, Ļ░üļ¦ē ļ░Å ņłśņĀĢņ▓┤ņØś Ēś╝ĒāüņØ┤ ņŚåļŖö 20ņŻ╝, 2.5-3.0 kgņØś ļē┤ņ¦łļ×£ļō£ ĒØ░ ĒåĀļü╝(New zealand white rabbit, Hallym Experimental Animal Research Institute, Hwaseong, Korea) 15ļ¦łļ”¼ļź╝ ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö The Association for Research in Vision and Ophthalmology (ARVO) StatementņØś ļÅÖļ¼╝ņŗżĒŚś ņ£żļ”¼ņŚÉ ļīĆĒĢ£ ĻČīĻ│Āņé¼ĒĢŁņØä ņżĆņłśĒĢśņśĆļŗż. Spectralis┬« OCT (Heidelberg Engineering GmbH, Heidelberg, Germany)ņŚÉ 55┬░C ļĀīņ”łļź╝ ņןņ░®ĒĢśĻ│Ā(Fig. 1A), ONHļź╝ 12ņŗ£ ļ░®Ē¢źņŚÉ ņ£äņ╣śņŗ£Ēé© ļÆż 333 ╬╝m Ļ░äĻ▓®ņ£╝ļĪ£ 33ņןņØś raster b-scanņØä ņ┤¼ņśüĒĢśņŚ¼ Ļ░ü b-scanņØĆ 44ĒÜī ļ░śļ│Ą ņĖĪņĀĢĒĢśņŚ¼ ņśüņāüņØä ņ¢╗Ļ│Ā(Fig. 1B), ņĢłņĀĆ ņ┤¼ņśü(widefield fundus photography)ņØä ņŗ£Ē¢ēĒĢśņŚ¼ ņĢłņĀĆ ĻĄ¼ņĪ░ļź╝ ĒÖĢņØĖĒĢśņśĆļŗż(Fig. 1C). Visual streakņŚÉ ĒÅēĒ¢ēĒĢ£ raster scanņØä ņ¢╗ĻĖ░ ņ£äĒĢ┤ ļ╣äņĖĪĻ│╝ ņØ┤ņĖĪņØś ņ¢æņĖĪ ļ¦Øļ¦ēņŚÉ ņ׳ļŖö ĒśłĻ┤ĆĻ│╝ raster scan axisĻ░Ć ņłśĒÅēņØä ņØ┤ļŻ░ ņłś ņ׳ļÅäļĪØ OCTļź╝ ņ┤¼ņśüĒĢśņśĆļŗż(Fig. 1B) [9]. Ļ┤æĻ░üņĢłņĀĆņ┤¼ņśüņŚÉļŖö Optomap 200Tx (Optos PLC, Dunfermline, UK) ņ┤łĻ┤æĻ░ü ņŻ╝ņé¼ļĀłņØ┤ņĀĆ Ļ▓ĆņĢłĻ▓ĮņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. ļśÉĒĢ£ medullary rayņŚÉ ņłśņ¦üņØĖ ļŗ©ļ®┤ņ£╝ļĪ£ hematoxylin-eosin stainingņØ┤ ļÉ£ ņĪ░ņ¦ü ņé¼ņ¦äņØä ņ¢╗ņŚłļŗż(Fig. 1E).
ĒåĀļü╝ņØś ļ¦Øļ¦ēņØĆ ņé¼ļ×īņØś ļ¦Øļ¦ēņ▓śļ¤╝ OCTņāüņŚÉņä£ ņĢłņ¬ĮņØś ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ(ganglion cell layer, GCL)ļČĆĒä░ Ļ░Ćņן ļ░öĻ╣źņ¬ĮņØś ļ¦Øļ¦ēņāēņåīņāüĒö╝(retinal pigment epithelium, RPE)Ļ╣īņ¦Ć 11Ļ░£ņØś Ļ│Āļ░śņé¼ņÖĆ ņĀĆļ░śņé¼ļź╝ ļ│┤ņØ┤ļŖö ņĖĄļōżļĪ£ ļéśļē£ļŗż(Fig. 1D) [14,15]. ļ¦Øļ¦ēņØś ņĖĄņØĆ ļé┤Ļ▓ĮĻ│äļ¦ē(internal limiting membrane, ILM), ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄ(retinal nerve fiber layer, RNFL), GCL, ļé┤ļ¦ØņāüņĖĄ(inner plexiform layer, IPL), INL, ņÖĖļ¦ØņāüņĖĄ(outer plexiform layer, OPL), ONL, ņÖĖĻ▓ĮĻ│äļ¦ē(external limiting membrane, ELM), Ļ┤æņłśņÜ®ņ▓┤ņĖĄ(photoreceptor layers) ĻĘĖļ”¼Ļ│Ā ļ¦Øļ¦ēņāēņåīņāüĒö╝ņÖĆ Ļ░ÖņØĆ ņĖĄļōżļĪ£ ļéśļłäņ¢┤ņ¦äļŗż(Fig. 1D, E). ņĀäņ▓┤ ļ¦Øļ¦ēļæÉĻ╗ś(total retinal layer thickness, TRT)ļŖö ļé┤Ļ▓ĮĻ│äļ¦ēņŚÉņä£ ļ¦Øļ¦ēņāēņåīņāüĒö╝ņĖĄĻ╣īņ¦ĆņØś ļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśņśĆĻ│Ā, ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗ś(inner retinal layer thickness, IRT)ļŖö ļé┤Ļ▓ĮĻ│äļ¦ēņŚÉņä£ ņÖĖĻ▓ĮĻ│äļ¦ē ļé┤ņĖĪ Ļ▓ĮĻ│äĻ╣īņ¦ĆļĪ£ ĒĢśņśĆļŗż[16,17]. ņÖĖļ¦Øļ¦ēņĖĄ ļæÉĻ╗ś(outer retinal layer thickness, ORT)ļŖö ņÖĖĻ▓ĮĻ│äļ¦ē ļé┤ņĖĪ Ļ▓ĮĻ│äņŚÉņä£ ļ¦Øļ¦ēņāēņåīņāüĒö╝ņĖĄĻ╣īņ¦ĆņØś ļæÉĻ╗śļĪ£, ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀäņ▓┤ ļ¦Øļ¦ēļæÉĻ╗śņÖĆ ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļź╝ ļ©╝ņĀĆ ĻĄ¼ĒĢ£ Ēøä ņĀäņ▓┤ ļ¦Øļ¦ēļæÉĻ╗śņŚÉņä£ ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗śņØś ņ░©(ORT=TRT-IRT)ļĪ£ ņĀĢņØśĒĢśņśĆļŗż. ļśÉĒĢ£ ņŗĀĻ▓ĮņĀłņäĖĒż ņČĢņéŁļÅīĻĖ░ļĪ£ ņØ┤ļżäņ¦ä ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄ(RNFL), ņŗĀĻ▓ĮņĀłņäĖĒżņ▓┤ļĪ£ ņØ┤ļżäņ¦ä GCL, ņŗĀĻ▓ĮņĀłņäĖĒż ņłśņ¦ĆņāüļÅīĻĖ░ļĪ£ ņØ┤ļżäņ¦ä ļé┤ļ¦ØņāüņĖĄ(IPL)ņØś ņäĖ ņĖĄņØä ĒżĒĢ©ĒĢśļŖö ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤(ganglion cell complex, GCC)ņØś ļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ļŖö ļģ╣ļé┤ņןņ£╝ļĪ£ ņŗĀĻ▓ĮņĀłņäĖĒżĻ░Ć ņåÉņāüļÉĀņłśļĪØ ņ¢ćņĢäņĀĖ ļģ╣ļé┤ņןņØś ņ┤łĻĖ░ ņ¦äļŗ©Ļ│╝ ĻĘĖ ņ¦äĒ¢ē ņĀĢļÅäļź╝ ĒÅēĻ░ĆĒĢśļŖö ļŹ░ ņ£ĀņÜ®ĒĢśņŚ¼ ņ×äņāüņŚÉņä£ ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśļŖö ņ¦ĆĒæ£ņØ┤ļ®░[18,19], ĒåĀļü╝ņŚÉņä£ ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ, ļé┤ļ¦ØņāüņĖĄņØś ņäĖ ņĖĄņØä ĻĄ¼ļČäĒĢśņŚ¼ ņĖĪņĀĢĒĢśļŖö Ļ▓āņŚÉ ĒĢ£Ļ│äĻ░Ć ņ׳ņ¢┤ ĒĢ©Ļ╗ś ņĖĪņĀĢĒĢśņśĆļŗż.
ONHņŚÉņä£ ņĢäļלļĪ£ 0, 1, 2, 3, 4, ĻĘĖļ”¼Ļ│Ā 5 mm ļ¢©ņ¢┤ņ¦ä ņ£äņ╣śņŚÉņä£ ņĀäņ▓┤ ļ¦Øļ¦ēļæÉĻ╗ś, ļé┤ļ¦Øļ¦ēņĖĄĻ│╝ ņÖĖļ¦Øļ¦ēņĖĄņØś ļæÉĻ╗ś, ļ¦źļØĮļ¦ēļæÉĻ╗ś(choroidal thickness, CT), ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ ļæÉĻ╗ś, ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ ļæÉĻ╗ś, ļé┤ĒĢĄņĖĄ ļæÉĻ╗ś, ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄ ļæÉĻ╗śļź╝ ņ¢╗ņŚłļŗż. ņāüĻĖ░ 8Ļ░Ćņ¦Ć ņĖĄņØś ļæÉĻ╗śļŖö Ļ░üĻ░ü ļŗżļźĖ 3ļ¬ģņØś ņĖĪņĀĢņ×ÉļōżņŚÉ ņØśĒĢ┤ ņ┤Ø 3ĒÜī ņĖĪņĀĢļÉśņ¢┤ ĒåĄĻ│ä ļČäņäØņŚÉ ņØ┤ņÜ®ļÉśņŚłļŗż. SD-OCT imageņŚÉņä£ Ļ│Ąļ¦ēļź£(scleral ring)ņØä ņŗ£ņŗĀĻ▓Į ņĢäļלņ¬Į Ļ░Ćņןņ×Éļ”¼ļĪ£ ļ│┤Ļ│Ā ņØ┤ļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ļź╝ ņĖĪņĀĢĒĢśņŚ¼ Ļ░ü ļ¦Øļ¦ēņĖĄĻ│╝ ļ¦źļØĮļ¦ēņĖĄņØś ļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░ ņØ┤ļź╝ 15ļ¦łļ”¼ ĒåĀļü╝ļōż Ļ░äņŚÉ ļ╣äĻĄÉĒĢśņśĆļŗż.
ņ×ÉļŻīņØś ĒåĄĻ│äņĀüņØĖ ļČäņäØņØĆ SPSS for Windows software version 22.0 (IBM Corp., Armonk, NY, USA)ņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. ONHņŚÉņä£ ņĢäļלļĪ£ 0, 1, 2, 3, 4, ĻĘĖļ”¼Ļ│Ā 5 mm ļ¢©ņ¢┤ņ¦ä ņ£äņ╣śņØś ļŗżņä» ĻĄ░ Ļ░äņØś ļ¦Øļ¦ē Ļ░ü ļæÉĻ╗śļōżņØś ļ╣äĻĄÉņŚÉļŖö one-way analysis of variance (ANOVA) testļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, Ļ░ü ņ£äņ╣śļ│äļĪ£ ļæÉ ĻĄ░ Ļ░äņØś ļ¦Øļ¦ēļæÉĻ╗ś ņĖĪņĀĢņ╣śņØś ļ╣äĻĄÉļŖö repeated ANOVA testļĪ£ ĒĢśņśĆļŗż. ONHļĪ£ļČĆĒä░ ļ¢©ņ¢┤ņ¦ä ņ£äņ╣śņÖĆ ļ¦Øļ¦ēņäĖļČĆņĖĄ ļæÉĻ╗śņÖĆņØś ļ╣äļ¬©ņłś ņāüĻ┤ĆĻ┤ĆĻ│ä Ļ▓ĆņĀĢ(Pearson correlation test)ņØä ņŗ£Ē¢ēĒĢśņŚ¼ ļ¦Øļ¦ē ņäĖļČĆņĖĄ ļæÉĻ╗ś ļ│ĆĒÖöņØś Ļ▓ĮĒ¢źņä▒ņØä ņĢīņĢäļ│┤ņĢśļŗż. p-valueĻ░Ć 0.05 ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ļź╝ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ĒĢśņśĆļŗż.
ņ┤Ø 15ļ¦łļ”¼ņØś ĒåĀļü╝ļź╝ ļīĆņāüņ£╝ļĪ£ ņŚ░ĻĄ¼ĒĢśņśĆļŗż. 3ļ¬ģņØś ņĖĪņĀĢņ×Éļōż Ļ░ä reliability analysis ņŗ£Ē¢ēņŗ£ intra-class correlation coefficient (ICC)ļŖö ņĀäņ▓┤ ļ¦Øļ¦ēļæÉĻ╗ś 99.5%, ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗ś 99.3%, ņÖĖļ¦Øļ¦ēņĖĄ ļæÉĻ╗ś 97.5%, ļ¦źļØĮļ¦ēļæÉĻ╗ś 99.2%, ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ ļæÉĻ╗ś 93.8%, ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ ļæÉĻ╗ś 93.6%, ļé┤ĒĢĄņĖĄ ļæÉĻ╗ś 81.2%, ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄ ļæÉĻ╗ś 99.3%ņśĆļŗż. ĒŖ╣Ē׳ ņĀäņ▓┤ ļ¦Øļ¦ē, ļé┤ļ¦Øļ¦ēņĖĄ, ņÖĖļ¦Øļ¦ēņĖĄ, ļ¦źļØĮļ¦ē, ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤, ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄņØś 7Ļ░£ ņĖĄņØś ļæÉĻ╗ś ņĖĪņĀĢņ╣śņŚÉņä£ ICCļŖö 90% ņØ┤ņāüņØ┤ņŚłļŗż.
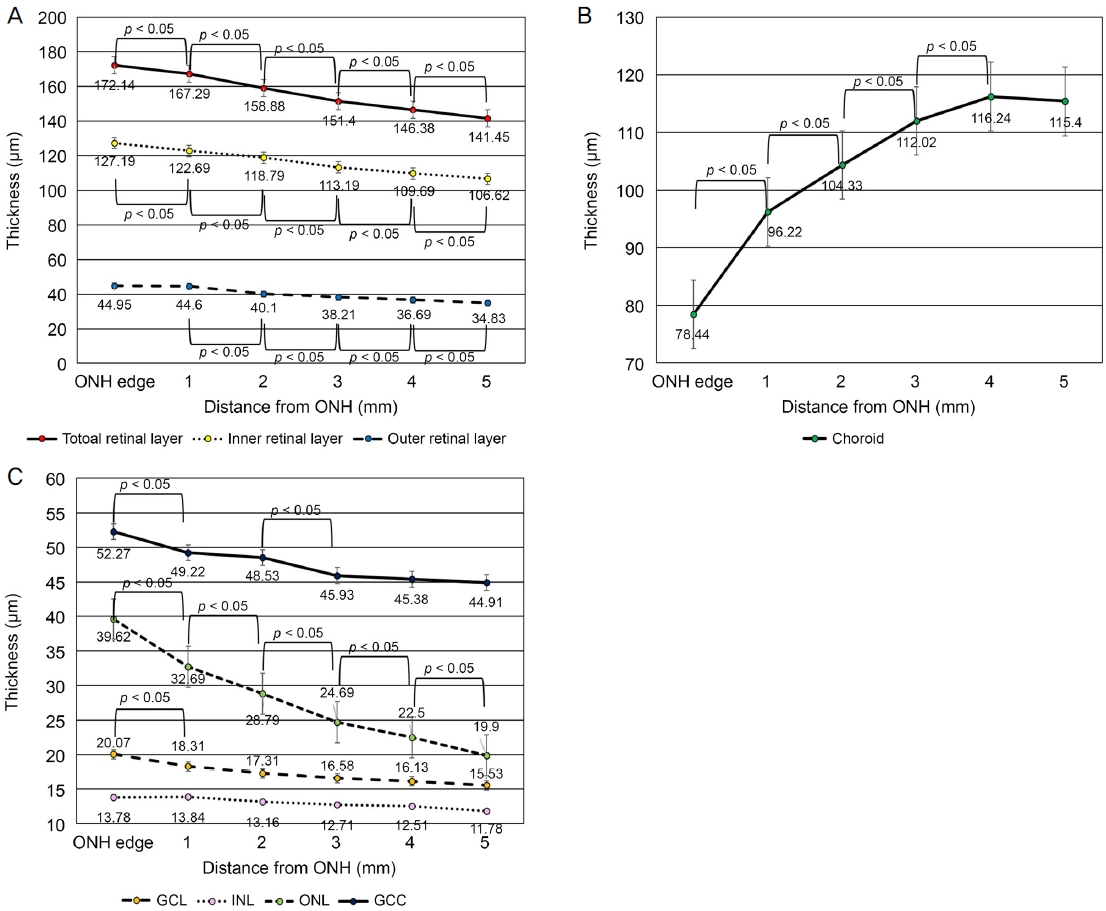
ļ¦Øļ¦ē Ļ░ü ņĖĄņØś ļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ņÖĆ ĻĘĖļĪ£ļČĆĒä░ 1, 2, 3, 4, ĻĘĖļ”¼Ļ│Ā 5 mm ļ¢©ņ¢┤ņ¦ä ņ£äņ╣śņŚÉņä£ ĒÅēĻĘĀĻ░Æ ┬▒ Ēæ£ņżĆĒÄĖņ░©(╬╝m)ļĪ£ Ļ│äņé░ĒĢśņśĆļŗż. ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 172.14 ┬▒ 7.28 ╬╝m, 167.29 ┬▒ 8.60 ╬╝m, 158.88 ┬▒ 9.48 ╬╝m, 151.40 ┬▒ 8.98 ╬╝m, 146.38 ┬▒ 9.69 ╬╝m, 141.45 ┬▒ 8.96 ╬╝mņśĆļŗż. ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ ļ®Ćņ¢┤ņ¦ÉņŚÉ ļö░ļØ╝ ņ░©ņØ┤Ļ░Ć ņ׳ņŚłņ£╝ļ®░(ANOVA test, p<0.05), Ļ░ÉņåīĒĢśļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņśĆļŗż(PearsonŌĆÖs CC=-0.778, p<0.05, Table 1). ņŚ░ņåŹļÉ£ ļæÉ ņ¦ĆņĀÉ ņé¼ņØ┤ņØś ņ░©ņØ┤ļź╝ ļ╣äĻĄÉĒĢśņśĆņØä ļĢī, ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤, ONHļĪ£ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤, 2 mmņÖĆ 3 mm ņé¼ņØ┤, 3 mmņÖĆ 4 mm ņé¼ņØ┤, ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤ņŚÉņä£ ļ¬©ļæÉ Ļ░ÉņåīĒĢśņśĆļŗż(p<0.05, Fig. 2A). ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 127.19 ┬▒ 5.06 ╬╝m, 122.69 ┬▒ 7.16 ╬╝m, 118.79 ┬▒ 6.74 ╬╝m, 113.19 ┬▒ 7.55 ╬╝m, 109.69 ┬▒ 7.93 ╬╝m, 106.62 ┬▒ 8.29 ╬╝mņśĆļŗż. ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ░ÉņåīĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=-0.710, p<0.05; Table 1). ņŚ░ņåŹļÉ£ ļæÉ ņ¦ĆņĀÉ Ļ░ä ļ╣äĻĄÉņŚÉņä£ ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤, ONHļĪ£ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤, 2 mmņÖĆ 3 mm ņé¼ņØ┤, 3 mmņÖĆ 4 mm ņé¼ņØ┤, ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤ņŚÉņä£ ļ¬©ļæÉ Ļ░ÉņåīĒĢśņśĆļŗż(p<0.05, Fig. 2A). ņÖĖļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 44.95 ┬▒ 6.50 ╬╝m, 44.60 ┬▒ 4.91 ╬╝m, 40.10 ┬▒ 6.04 ╬╝m, 38.21 ┬▒ 6.85 ╬╝m, 36.69 ┬▒ 7.39 ╬╝m, 34.83 ┬▒ 7.39 ╬╝mņśĆļŗż. ņÖĖļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ░ÉņåīĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=-0.495, p<0.05; Table 1). ņŚ░ņåŹļÉ£ ļæÉ ņ¦ĆņĀÉ Ļ░ä ļ╣äĻĄÉņŚÉņä£ ņÖĖļ¦Øļ¦ēņĖĄ ļæÉĻ╗śļŖö ONHļĪ£ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤, 2 mmņÖĆ 3 mm ņé¼ņØ┤, 3 mmņÖĆ 4 mm ņé¼ņØ┤, ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤ņŚÉņä£ ļ¬©ļæÉ Ļ░ÉņåīĒĢśņśĆļŗż(p<0.05, Fig. 2A). ĻĘĖļ¤¼ļéś ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤ņØś ņ░©ņØ┤ļŖö ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņĢśļŗż(p=0.577, Fig. 2A). ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 78.44 ┬▒ 27.71 ╬╝m, 96.22 ┬▒ 20.31 ╬╝m, 104.33 ┬▒ 16.23 ╬╝m, 112.02 ┬▒ 18.39 ╬╝m, 116.24 ┬▒ 16.97 ╬╝m, 115.40 ┬▒ 15.24 ╬╝mņśĆļŗż. ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ONHņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ ņ”ØĻ░ĆĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=0.511, p<0.05; Table 1). ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤, ONHļĪ£ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤, 2 mmņÖĆ 3 mm ņé¼ņØ┤, ĻĘĖļ”¼Ļ│Ā 3 mmņÖĆ 4 mm ņé¼ņØ┤ņŚÉņä£ ļ¬©ļæÉ ņ”ØĻ░ĆĒĢśņśĆņ£╝ļéś(p<0.05, Fig. 2B). ONH Ļ░Ćņן ņ×Éļ”¼ļČĆĒä░ 4 mmņÖĆ 5 mm ņé¼ņØ┤ņØś ņ░©ņØ┤ļŖö ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņĢśļŗż(p=0.407, Fig. 2B).
ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 52.27 ┬▒ 4.64 ╬╝m, 49.22 ┬▒ 7.22 ╬╝m, 48.53 ┬▒ 8.59 ╬╝m, 45.93 ┬▒ 9.27 ╬╝m, 45.38 ┬▒ 8.51 ╬╝m, 44.91 ┬▒ 9.09 ╬╝mņśĆļŗż. ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ│äņåŹ Ļ░ÉņåīĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=-0.292 p<0.05; Table 2). ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ ļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤ņÖĆ 2 mmņÖĆ 3 mm ņé¼ņØ┤ņŚÉņä£ Ļ░ÉņåīĒĢśņśĆņ¦Ćļ¦ī(p<0.05), ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤(p=0.377), 3 mmņÖĆ 4 mm ņé¼ņØ┤(p=0.374), ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤(p=0.448)ņØś ņ░©ņØ┤ļŖö ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņĢśļŗż(Fig. 2C). ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 20.07 ┬▒ 6.69 ╬╝m, 18.31 ┬▒ 5.00 ╬╝m, 17.31 ┬▒ 4.75 ╬╝m, 16.58 ┬▒ 4.56 ╬╝m, 16.13 ┬▒ 5.27 ╬╝m, 15.53 ┬▒ 5.59 ╬╝mņśĆĻ│Ā, ONHņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ░ÉņåīĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=-0.284, p<0.05; Table 2). ņŚ░ņåŹļÉ£ ļæÉ ņ¦ĆņĀÉ Ļ░ä ļ╣äĻĄÉņŚÉņä£ ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ ļæÉĻ╗ś Ļ░ÉņåīļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤(p<0.05)ņŚÉņä£ļ¦ī ņ£ĀņØśļ»ĖĒĢśņśĆņ£╝ļ®░, 1 mmņÖĆ 2 mm ņé¼ņØ┤(p=0.054), 2 mmņÖĆ 3 mm ņé¼ņØ┤(p=0.159), 3 mmņÖĆ 4 mm ņé¼ņØ┤(p=0.462), ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤(p=0.353)ņØś ĻĄ¼Ļ░äņŚÉņä£ ĻĘĖ Ļ░ÉņåīĻ░Ć ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż. ļé┤ĒĢĄņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 13.78 ┬▒ 2.44 ╬╝m, 13.84 ┬▒ 2.44 ╬╝m, 13.16 ┬▒ 2.50 ╬╝m, 12.71 ┬▒ 2.67 ╬╝m, 12.51 ┬▒ 3.56 ╬╝m, 11.78 ┬▒ 2.73 ╬╝mņśĆļŗż. ļé┤ĒĢĄņĖĄ ļæÉĻ╗śļÅä ONHņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ░ÉņåīĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=-0.263, p<0.05, Table 2), ņŚ░ņåŹļÉ£ ļæÉ ņ¦ĆņĀÉ Ļ░ä ļ╣äĻĄÉņŚÉņä£ļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤(p=0.846), 1 mmņÖĆ 2 mm ņé¼ņØ┤(p=0.093), 2 mmņÖĆ 3 mm ņé¼ņØ┤(p=0.209), 3 mmņÖĆ 4 mm ņé¼ņØ┤(p=0.571), ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤(p=0.068)ņØś ļ¬©ļōĀ ĻĄ¼Ļ░äņŚÉņä£ ĻĘĖ ļ│ĆĒÖöĻ░Ć ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż. ņÖĖĒĢĄņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ņĢäļלļĪ£ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņĖĪņĀĢ ņŗ£ ņ░©ļĪĆļīĆļĪ£ 39.62 ┬▒ 5.06 ╬╝m, 32.69 ┬▒ 5.31 ╬╝m, 28.79 ┬▒ 6.40 ╬╝m, 24.69 ┬▒ 6.65 ╬╝m, 22.50 ┬▒ 6.57 ╬╝m, 19.90 ┬▒ 6.56 ╬╝mņśĆļŗż. ņÖĖĒĢĄņĖĄ ļæÉĻ╗śļŖö ONHņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ Ļ░ÉņåīĒĢśņśĆļŗż(ANOVA test, p<0.05; CC=-0.760, p<0.05; Table 2). ņŚ░ņåŹļÉ£ ļæÉ ņ¦ĆņĀÉ Ļ░ä ļ╣äĻĄÉņŚÉņä£ ņÖĖĒĢĄņĖĄ ļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤, ONHļĪ£ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤, 2 mmņÖĆ 3 mm ņé¼ņØ┤, 3 mmņÖĆ 4 mm ņé¼ņØ┤, ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤ņŚÉņä£ ļ¬©ļæÉ Ļ░ÉņåīĒĢśņśĆļŗż(p<0.05, Fig. 2C).
ļ¦Øļ¦ēņ¦łĒÖśņØś ņŚ░ĻĄ¼ņŚÉņä£ ŌĆśņāØņ▓┤ ņÖĖ(ex vivo)ŌĆÖ ņĪ░ņ¦üĒĢÖņØ┤ ĻĄ¼ņĪ░ņĀüņØĖ ĒśĢĒā£ļź╝ ĒÅēĻ░ĆĒĢśļŖö Ēæ£ņżĆņĀüņØĖ ļ░®ļ▓Ģ(gold standard)ņØ┤ņ¦Ćļ¦ī, ņśüņāüĒÖö ĻĖ░ņłĀņØś ļ╣äņĢĮņĀüņØĖ ļ░£ņĀäņ£╝ļĪ£ ļ¦Øļ¦ē ĻĄ¼ņĪ░ņØś ĒÅēĻ░ĆņŚÉ ŌĆśņāØņ▓┤ ļé┤(in vivo)ŌĆÖ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(OCT)ņØ┤ ņĪ░ņ¦üĒĢÖņØä ļīĆņ▓┤ĒĢĀ ņłś ņ׳Ļ▓ī ļÉśņŚłļŗż[7]. ĒŖ╣Ē׳ SD-OCTņØś ļō▒ņןņØĆ ĒĢ┤ņāüļÅäņØś ļ╣äņĢĮņĀüņØĖ Ē¢źņāüņ£╝ļĪ£ ņĪ░ņ¦üĒĢÖņØś ĒĢ┤ļČĆĒĢÖņĀü ļ¼śņé¼ņŚÉ ņāüņØæĒĢśļŖö ņłśņżĆņØś ļ¦Øļ¦ēņĖĄ ļ¼śņé¼ņÖĆ ļ¦źļØĮļ¦ēņØś ļæÉĻ╗ś ņĖĪņĀĢņØä Ļ░ĆļŖźĒĢśĻ▓ī ĒĢśņśĆļŗż[1,7]. ņØ┤ņĀäņØś ļ¦ÄņØĆ ņŚ░ĻĄ¼ļōżņØä ĒåĄĒĢ┤ ņé¼ļ×ī ļ¦Øļ¦ēņØś ņĀäņ▓┤ ļ¦Øļ¦ēļæÉĻ╗ś, ļ¦Øļ¦ē Ļ░ü ņĖĄ ļ░Å ļ¦źļØĮļ¦ēļæÉĻ╗śņŚÉ ļīĆĒĢ£ Ēæ£ņżĆĒÖöļÉ£ ņĀĢļ¤ēņĀü ņłśņ╣śļōżņØ┤ ņĢīļĀżņĀĖ ņ£ĀņÜ®ĒĢśĻ▓ī ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ£╝ļéś[20], ĒåĀļü╝ņŚÉņä£ļŖö ņØ┤ņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ņāüļīĆņĀüņ£╝ļĪ£ ņĀüņŚłļŗż. ļÅÖļ¼╝ ņŗżĒŚśņØś ĒĢ┤ņäØņŚÉņä£ ļ¦Øļ¦ē ĻĄ¼ņĪ░ņØś ņĀĢļ¤ēņĀüņØĖ ļČäņäØņØĆ ĒĢäņłśņĀüņØĖ ņÜöņåīļĪ£[9] ņØ┤ņŚÉ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒåĀļü╝ņØś ņĀäņ▓┤ ļ¦Øļ¦ēņĖĄ, ļé┤ļ¦Øļ¦ēņĖĄ, ņÖĖļ¦Øļ¦ēņĖĄ, ļ¦źļØĮļ¦ēņĖĄ, ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄ, GCL, INL, ĻĘĖļ”¼Ļ│Ā ONLņØś 8Ļ░Ćņ¦Ć ņĖĄņØś ļæÉĻ╗śļź╝ ņĀĢļ¤ēĒÖöĒĢśĻ│Ā, ONHļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ļæÉĻ╗ś ļ│ĆĒÖöņØś Ļ▓ĮĒ¢źņä▒ļÅä ļČäņäØĒ¢łļŗż. ĒåĀļü╝ņØś ļ¦Øļ¦ēņŚÉļŖö ņØĖĻ░äņØś ĒÖ®ļ░ś(macula) ļīĆņŗĀ ņŗ£Ļ░üļØĀ(visual streak)Ļ░Ć ņ׳ļŖöļŹ░, ņŗ£Ļ░üļØĀļŖö ĒÖ®ļ░śņ▓śļ¤╝ ņøÉļ┐öņäĖĒż(cone)ņÖĆ Ļ░äņāüņäĖĒż(rod) Ļ┤æņłśņÜ®ņ▓┤ņÖĆ ņŗĀĻ▓ĮņĀłņäĖĒżņØś ļ░ĆļÅäĻ░Ć Ļ░Ćņן Ēü¼ņ¦Ćļ¦ī ĻĘĖ ĒśĢĒā£ļŖö ĒÖ®ļ░śĻ│╝ ņ░©ņØ┤Ļ░Ć ņ׳ļŗż[11]. ņŗ£Ļ░üļØĀļŖö ĻĖĖņØ┤ 26 mm, ļäłļ╣ä 2-2.5 mm ņĀĢļÅäļĪ£ ĒåĀļü╝ņØś ļ¦Øļ¦ēņØä ņłśĒÅēņ£╝ļĪ£ Ļ░ĆļĪ£ņ¦Ćļź┤ļ®░, ONHņØś ņżæņŗ¼ņ£╝ļĪ£ļČĆĒä░ ņĢĮ 2.8-3.0 mm ņĢäļלņŚÉ ņ£äņ╣śĒĢśĻ│Ā, ņŗĀĻ▓ĮņĀł ņäĖĒżĻ░Ć ļ░Ćņ¦æļÉśņ¢┤ ņ׳ļŗż[11,21,22]. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĒåĀļü╝ ļ¦Øļ¦ē Ļ░ü ņäĖļČĆņĖĄ ļ¬©ļæÉ ONHļĪ£ļČĆĒä░ ņŗ£Ļ░üļØĀļź╝ ņ¦Ćļéś ĒĢśļ░®ņ£╝ļĪ£ ļé┤ļĀżĻ░łņłśļĪØ ļæÉĻ╗śĻ░Ć Ļ░ÉņåīĒĢśņśĆņ£╝ļ®░, ļ¦źļØĮļ¦ēņĖĄņØĆ ņ”ØĻ░ĆĒĢśņśĆļŗż. ĒŖ╣Ē׳ ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗śļŖö ONH Ļ░Ćņןņ×Éļ”¼ļČĆĒä░ 1 mm ņé¼ņØ┤(p<0.05), ONHļĪ£ļČĆĒä░ 1 mmņÖĆ 2 mm ņé¼ņØ┤(p<0.05), 2 mmņÖĆ 3 mm ņé¼ņØ┤(p<0.05), 3 mmņÖĆ 4 mm ņé¼ņØ┤(p<0.05), ĻĘĖļ”¼Ļ│Ā 4 mmņÖĆ 5 mm ņé¼ņØ┤(p<0.05)ņŚÉņä£ņØś Ļ░ÉņåīĻ░Ć ļ¬©ļæÉ ņ£ĀņØśļ»ĖĒ¢łļŗż(Fig. 2A). ONH Ļ░Ćņןņ×Éļ”¼ļĪ£ļČĆĒä░ ĒĢśļ░®ņ£╝ļĪ£ ļé┤ļĀżĻ░łņłśļĪØ ļé┤ļ¦Øļ¦ēņĖĄĻ│╝ ņÖĖļ¦Øļ¦ēņĖĄņØś ļæÉĻ╗śļÅä ņ£ĀņØśļ»ĖĒĢśĻ▓ī Ļ░ÉņåīĒĢśņśĆļŗż(Fig. 2A). ONH Ļ░Ćņןņ×Éļ”¼ņŚÉņä£ ļ®Ćņ¢┤ņ¦łņłśļĪØ ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗śĻ░Ć Ļ░ÉņåīĒĢ©ņØĆ ĻĖ░ņĪ┤ņØś ņĀĢņāü ĒåĀļü╝ņØś ļ¦Øļ¦ēļæÉĻ╗śņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ņŚÉ ļČĆĒĢ®ĒĢśņśĆļŗż[9]. ņØ┤ļŖö ļé┤ļ¦Øļ¦ēņĖĄĻ│╝ ņÖĖļ¦Øļ¦ēņĖĄņØś ļæÉĻ╗ś Ļ░ÉņåīņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņäżļ¬ģĒĢĀ ņłś ņ׳ņ£╝ļ®░, ĒŖ╣Ē׳ ļé┤ļ¦Øļ¦ēņĖĄņØś ļæÉĻ╗ś Ļ░ÉņåīļŖö ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄ, ļé┤ĒĢĄņĖĄ, ĻĘĖļ”¼Ļ│Ā ņÖĖĒĢĄņĖĄņØś ļæÉĻ╗ś Ļ░Éņåī Ļ▓ĮĒ¢źņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż. ONHļĪ£ļČĆĒä░ ļ®Ćņ¢┤ņ¦łņłśļĪØ ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄņØś ļæÉĻ╗śĻ░Ć Ļ░ÉņåīĒĢśļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņØĖ Ļ▓āņØĆ ONHļĪ£ļČĆĒä░ ļ¦ÄņØ┤ ļ¢©ņ¢┤ņ¦łņłśļĪØ ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄņØś ļæÉĻ╗śĻ░Ć Ļ░ÉņåīĒĢ£ļŗżļŖö ĻĖ░ņĪ┤ ļ│┤Ļ│ĀņÖĆ[9] ņØ╝ņ╣śĒĢ£ļŗż. ņŗ£Ļ░üļØĀ ļČĆņ£äņŚÉņä£ļÅä ņ£ĀņØśļ»ĖĒĢ£ ļé┤ļ¦Øļ¦ēņĖĄņØś ļæÉĻ╗ś Ļ░ÉņåīĻ░Ć ņ׳ņŚłļŖöļŹ░(Fig. 2A), ņØ┤ļŖö ņŗ£ņŗĀĻ▓Į ĒĢśļČĆ 2-3 mmņŚÉņä£ņØś ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄĻ│╝ ņÖĖĒĢĄņĖĄņØś ļæÉĻ╗ś Ļ░ÉņåīņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż(Fig. 2C). Oyster et al [22]ņØ┤ ļ│┤Ļ│ĀĒĢ£ ĒåĀļü╝ņŚÉņä£ņØś ņŗĀĻ▓ĮņĀłņäĖĒżņØś ļ░ĆļÅäņÖĆ ļČäĒż ļ│┤Ļ│ĀņŚÉ ļö░ļź┤ļ®┤, ņŗĀĻ▓ĮņĀłņäĖĒżņØś ļ░ĆļÅäļŖö ņŗ£ņŗĀĻ▓Į ņĢäļלĻ░Ć Ļ░Ćņן ļåÆĻ│Ā ņŗ£Ļ░üļØĀ ļČĆĻĘ╝Ļ╣īņ¦Ć Ļ░ÉņåīĒĢśļ®░ ņŗ£Ļ░üļØĀļ│┤ļŗż ņĢäļלņŚÉņä£ļŖö ļŹö ļŹö Ļ░ÉņåīĒĢśļ®░, ņŗĀĻ▓ĮņĀłņäĖĒż ļ¬Ėņ▓┤ Ēü¼ĻĖ░ņØś ļ│ĆĒÖöļŖö ņĀüņØĆ Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż. ļśÉĒĢ£ ĒåĀļü╝ņŚÉņä£ ņøÉņČöņäĖĒż ļ░ĆļÅäļŖö ņŻ╝ļ│ĆļČĆņŚÉņä£ ņĢĮ 7,500/mm┬▓ņØ┤Ļ│Ā ņŗ£Ļ░üļØĀņŚÉņä£ ņĢĮ 13,000 mm┬▓ļĪ£, ņŗ£Ļ░üļØĀ ļČĆĻĘ╝ņŚÉņä£ Ļ░Ćņן ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ļŖöļŹ░[23], ĒåĀļü╝ņØś ņØ┤ļ¤¼ĒĢ£ ĒĢ┤ļČĆĒĢÖņĀüņØĖ ĒŖ╣ņ¦Ģņ£╝ļĪ£ ņŗ£Ļ░üļØĀ ļČĆĻĘ╝ņØś ņŗĀĻ▓ĮņĀłņäĖĒżļ│ĄĒĢ®ņ▓┤ņĖĄ ļæÉĻ╗śņÖĆ ļé┤ļ¦Øļ¦ēņĖĄ ļæÉĻ╗śņØś Ļ░ÉņåīĻ░Ć ņ׳ņŚłņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉśļ®░, ļ│Ė ņŚ░ĻĄ¼ņØś OCTņŚÉņä£ņØś ļæÉĻ╗ś ļ│ĆĒÖöļŖö ĻĘĖ ĒĢ┤ļČĆĒĢÖņĀüņØĖ ļ│ĆĒÖöļź╝ ļ░śņśüĒĢ£ Ļ▓āņ£╝ļĪ£, ņØ┤ļ¤¼ĒĢ£ ļæÉĻ╗ś ļ│ĆĒÖöļŖö ĻĖ░ņĪ┤ņŚÉ ļ│┤Ļ│ĀļÉ£ ļģ╝ļ¼ĖņŚÉņä£ņØś Ļ▓░Ļ│╝ņÖĆ ņØ╝ņ╣śĒĢśņśĆļŗż[11]. ļśÉĒĢ£ ONHļĪ£ļČĆĒä░ ĒĢśļ░®ņ£╝ļĪ£ ļé┤ļĀżĻ░łņłśļĪØ ļ¦źļØĮļ¦ēņĖĄ ļæÉĻ╗śļŖö ņ”ØĻ░ĆĒĢśņśĆļŖöļŹ░, ņé¼ļ×īņŚÉņä£ ĒÖ®ļ░ś ļČĆņ£äņØś ļ¦źļØĮļ¦ēņĖĄ ļæÉĻ╗śĻ░Ć Ļ░Ćņן ļæÉĻ╗ŹĻ│Ā ļ╣äņĖĪņ£╝ļĪ£ Ļ░łņłśļĪØ ņ”ē, ņŗ£ņŗĀĻ▓ĮņŚÉ Ļ░ĆĻ╣īņÜĖņłśļĪØ ĻĘĖ ļæÉĻ╗śĻ░Ć ņ¢ćņĢäņ¦äļŗżļŖö ņĀÉņØä ņāØĻ░üĒĢ┤ļ│┤ļ®┤[24], ĒåĀļü╝ ļ¦Øļ¦ēņŚÉņä£ļÅä ĻĘĖ ļ│ĆĒÖöĻ░Ć ļ╣äņŖĘĒĢ©ņØä ņĢī ņłś ņ׳ņŚłļŗż.
ĒåĀļü╝ļŖö ļ¦Øļ¦ēĒśłĻ┤ĆņØ┤ ONHļĪ£ļČĆĒä░ ņ£ĀņłśņŗĀĻ▓Į(myelinated nerve fibres)ņØ┤ ļ╣äņĖĪ(nasal)Ļ│╝ ņØ┤ņĖĪ(temporal)ņ£╝ļĪ£ ļäōĻ▓ī ņłśĒÅēņ£╝ļĪ£ ļČäņé░ļÉśņ¢┤ ļ¦Øļ¦ēņØś ņØ╝ļČĆļČäņŚÉļ¦ī ņ£äņ╣śĒĢśļŖö ĒŖ╣ņ¦ĢņØä Ļ░Ćņ¦ĆļŖö merangiotic ļÅÖļ¼╝ļĪ£ņŹ©[25,26], ļ¦Øļ¦ēĒśłĻ┤ĆņØ┤ ņŚåļŖö ļČĆļČäņØĖ ņŗ£Ļ░üļØĀļŖö ļ¦źļØĮļ¦ēļ¬©ņäĖĒśłĻ┤ĆņĖĄ(choriocapillaris)ņŚÉņä£ņØś ĒÖĢņé░ņØä ĒåĄĒĢ┤ ņé░ņåīņÖĆ ņśüņ¢æļČäņØś Ļ│ĄĻĖēņØ┤ ņØ┤ļŻ©ņ¢┤ņ¦äļŗż[26]. ņØ┤ļ¤¼ĒĢ£ ņŗ£Ļ░üļØĀļŖö ņé¼ļ×īņŚÉņä£ņØś ĒÖ®ļ░śļČĆņÖĆ ĻĖ░ļŖźņĀüņ£╝ļĪ£ ņ£Āņé¼ĒĢ£ ĒŖ╣ņ¦ĢņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ņ£╝ļ»ĆļĪ£, ĒåĀļü╝ņØś ņĢłĻĄ¼Ļ░Ć ņśüņןļźśņŚÉ ļ╣äĒĢ┤ ņāüļīĆņĀüņ£╝ļĪ£ ņ×æņ¦Ćļ¦ī ļ¦Øļ¦ē ņŗżĒŚś ļ¬©ļŹĖņŚÉ ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ¢┤[27] ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļź╝ ņé¼ļ×ī ļ¦Øļ¦ē ļČäņäØņŚÉļÅä ņØæņÜ®ĒĢśĻĖ░ņŚÉ ņĀüĒĢ®ĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
SD-OCTņŚÉņä£ļŖö Ļ░üļ¦ēĻ│ĪļźĀņØ┤ A-scanņØś ĻĘ£ļ¬©ļź╝ ņżäņØ┤Ļ▒░ļéś ļŖśļĀż Ļ┤æĒĢÖņĀü ĒĢ┤ņāüļÅäļź╝ Ļ▓░ņĀĢĒĢ£ļŗż[9]. ņä▒ņØĖ ĒåĀļü╝ņØś Ļ░üļ¦ē ĻĄ┤ņĀłļĀźņØĆ ņĢĮ 42-44ļööņśĄĒä░ņØ┤ļ»ĆļĪ£ ņé¼ļ×īņØś Ļ░üļ¦ēĻ│╝ ĻĘĖ Ļ░ÆņØ┤ ļ¦żņÜ░ Ļ░ĆĻ╣īņøī ĒåĀļü╝ ļ¬©ļŹĖņŚÉņä£ SD-OCT ņĖĪņĀĢņ╣śļź╝ ĻĄ¼ĒĢśļ®┤ ņØ┤ļź╝ ņé¼ļ×ī ļ¦Øļ¦ēņŚÉ ņĀüņÜ®ņŗ£ ņČöĻ░ĆņĀüņØĖ ļ│ĆĒÖśņØ┤ ĒĢäņÜöĒĢśņ¦Ć ņĢŖļŗż[9]. ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļ│┤Ļ│ĀļÉ£ ĒåĀļü╝ņØś ļ¦Øļ¦ē ļ░Å ļ¦źļØĮļ¦ēļæÉĻ╗śņŚÉ ļīĆĒĢ£ ņĀĢļ¤ēĒÖöļÉ£ ņłśņ╣śņÖĆ ONHļČĆļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ļæÉĻ╗ś ļ│ĆĒÖöņŚÉ ļīĆĒĢ£ ļČäņäØņØĆ ļÅÖļ¼╝ ļ¦Øļ¦ē ņŗżĒŚśņØä ņ£äĒĢ£ Ēæ£ņżĆĒÖöļÉ£ ņ×ÉļŻīĻ░Ć ļÉĀ ņłś ņ׳ņØä ļ┐Éļ¦ī ņĢäļŗłļØ╝ ņØĖĻ░ä ļ¦Øļ¦ēņ¦łĒÖśņØś ņ¦äļŗ© ļ░Å ņ╣śļŻīņŚÉļÅä ļ¦ÄņØĆ ĻĖ░ņŚ¼ļź╝ ĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. SD-OCTļĪ£ ņĖĪņĀĢļÉ£ ņ┤Ø ļ¦Øļ¦ēļæÉĻ╗śļŖö ņŗ£ņäĖĒż ļ░öĻ╣źņ¬Į(outer segment), ļ¦Øļ¦ēņāēņåīņāüĒö╝ņĖĄņØś ņĖĪņĀĢņØä ļ¬©ļæÉ ĒżĒĢ©ĒĢśļ»ĆļĪ£ TD-OCTņŚÉņä£ ņĖĪņĀĢļÉ£ ļæÉĻ╗śļ│┤ļŗż ļīĆļץ 70 ╬╝m (61.9-74.1 ╬╝m) ļŹö ļæÉĻ╗Źļŗż[28]. ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņĀĢļ¤ēĒÖöļÉ£ ĒåĀļü╝ņØś ļ¦Øļ¦ē ļ░Å ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö SD-OCTļĪ£ ņĖĪņĀĢĒĢ£ Ļ▓āņ£╝ļĪ£ ĻĖ░ņĪ┤ņØś TD-OCTļĪ£ ņĖĪņĀĢļÉ£ ļ¦Øļ¦ēļæÉĻ╗śņÖĆ ņ░©ņØ┤ ņ׳ņØīņØä ņĢīĻ│Ā ņĀüņÜ®ĒĢ┤ņĢ╝ ĒĢśĻ▓Āļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö SD-OCTņŚÉņä£ ļéśĒāĆļéśļŖö ļ¦Øļ¦ē Ļ░ü ņĖĄņØś ļæÉĻ╗śļź╝ ņłśļÅÖņ£╝ļĪ£ ņĖĪņĀĢĒĢśņŚ¼ Ļ▓Ćņé¼ņ×ÉņØś ņŻ╝Ļ┤ĆņĀü ĒĢ┤ņäØņØ┤ ņŚ░ĻĄ¼ņØś ņśżņ░©ņŚÉ Ļ┤ĆņŚ¼Ē¢łļŗżļŖö ņĀÉņŚÉņä£ ņĀ£ĒĢ£ņĀÉņØ┤ ņ׳ņŚłļŗż. ĻĘĖļ¤¼ļéś ņØ┤ ņŻ╝Ļ┤ĆņĀüņØĖ ĒÄĖĒ¢źņØä ņżäņØ┤ĻĖ░ ņ£äĒĢ┤ 3ļ¬ģņØś Ļ▓Ćņé¼ņ×ÉļōżņØ┤ Ļ▓Ćņé¼ņ╣śļź╝ ĻĄ¼Ē¢łĻ│Ā ļīĆļČĆļČäņØś ņĖĪņĀĢņ╣śņŚÉņä£ 90% ņØ┤ņāüņØś ņŗĀļó░ĒĢĀ ļ¦īĒĢ£ Ļ▓Ćņé¼ņ×É Ļ░ä ņØ╝ņ╣śļÅäļź╝ ļ│┤ņśĆļŗż. ņØ┤ļŖö ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņłśļÅÖņ£╝ļĪ£ ļ»ĖņäĖĒĢ£ ņĖĄņØä ņĖĪņĀĢĒĢ©ņŚÉ ņ׳ņ¢┤ ņāØĻĖĖ ņłś ņ׳ļŖö ņŻ╝Ļ┤ĆņĀüņØĖ ĒīÉļŗ©ņØś ņśüĒ¢źļĀźņØ┤ ņ×æņĢśņØīņØä ļ│┤ņŚ¼ņżĆļŗż. ļśÉĒĢ£ ļ│Ė ņŚ░ĻĄ¼ļŖö ONHļČĆļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ļ¦Øļ¦ē ņĖĄļ│ä ļæÉĻ╗śņØś ļ│ĆĒÖöļź╝ SD-OCTņāüņŚÉņä£ļŖö ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłņ¦Ćļ¦ī ņĪ░ņ¦ü ņé¼ņ¦äņ£╝ļĪ£ļŖö ĒÖĢņØĖĒĢśņ¦Ć ļ¬╗ĒĢśņśĆļŗżļŖö ĒĢ£Ļ│äņĀÉņØ┤ ņ׳ņŚłļŗż. Medullary rayņŚÉ ņłśņ¦üņØĖ ļŗ©ļ®┤ņØś Hematoxylin-eosin stainingņØ┤ ļÉ£ ņĪ░ņ¦ü ņé¼ņ¦äņØĆ ņ¢╗ņŚłņ£╝ļéś(Fig. 1E), ONHļČĆļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ņĪ░ņ¦üņŚÉņä£ņØś ļ¦Øļ¦ē ņĖĄļ│ä ļæÉĻ╗śļź╝ ĒÖĢņØĖ Ēøä SD-OCTņāüņŚÉņä£ņØś ņĖĄļ│ä ļæÉĻ╗śņÖĆ ļ╣äĻĄÉĒĢśņ¦Ć ļ¬╗ĒĢśņśĆļŗżļŖö ņĀÉņŚÉņä£ ĒĢ£Ļ│äĻ░Ć ņ׳ņŚłļŗż. ļö░ļØ╝ņä£ ņĪ░ņ¦üĻ│╝ OCTņāüņŚÉņä£ņØś ņĖĄļ│ä ļæÉĻ╗śļź╝ ņĀĢĒÖĢĒ׳ ļ╣äĻĄÉĒĢśņ¦Ć ļ¬╗Ē¢łĻĖ░ ļĢīļ¼ĖņŚÉ OCTņŚÉņä£ņØś ļæÉĻ╗śĻ░Ć ņŗżņĀ£ ļ¦Øļ¦ē ņĪ░ņ¦ü ļæÉĻ╗śņÖĆ ņ¢┤ļŖÉ ņĀĢļÅäņØś ņØ╝ņ╣śņä▒ņØä Ļ░Ćņ¦ĆļŖöņ¦ĆļŖö ņ”Øļ¬ģĒĢśņ¦Ć ļ¬╗ĒĢśņśĆļŗż. ĒŖ╣Ē׳ ņØ┤ļŖö ņĪ░ņ¦üĻ│╝ OCTņāüņŚÉņä£ņØś ļ¦Øļ¦ē ņĖĄļ│ä ļæÉĻ╗ś ļ│ĆĒÖöņØś Ļ▓ĮĒ¢źņä▒ņØ┤ ņØ╝ņ╣śĒĢśņ¦Ć ņĢŖņØä ņłś ņ׳ļŗżļŖö ņĀÉņŚÉņä£[16], ņĢäņē¼ņÜ┤ ņĀÉņØ┤ļØ╝Ļ│Ā ĒĢĀ ņłś ņ׳Ļ▓Āļŗż.
ĒåĀļü╝ņŚÉņä£ SD-OCTļź╝ ņØ┤ņÜ®ĒĢ£ ONHļČĆļĪ£ļČĆĒä░ņØś Ļ▒░ļ”¼ņŚÉ ļö░ļźĖ ļ¦Øļ¦ē ļ░Å ļ¦źļØĮļ¦ēņØś ņĖĄļ│ä ļæÉĻ╗ś ļČäņäØņØä ĒåĄĒĢ┤ ļÅÖļ¼╝ ļ¦Øļ¦ē ņŗżĒŚśņØä ņ£äĒĢ£ ĻĖ░ļ│Ė ņ×ÉļŻīļź╝ ņ¢╗ņØä ņłś ņ׳ņŚłļŗżļŖö ņĀÉņŚÉņä£ ļ│Ė ņŚ░ĻĄ¼ņØś ņØśņØśĻ░Ć ņ׳ļŗż. ĒŖ╣Ē׳ ļ╣äņ╣©ņŖĄņĀüņ£╝ļĪ£ ļ¦Øļ¦ēņØś ĻĄ¼ņĪ░ ļ░Å ĒŖ╣ņ¦ĢņØä ļČäņäØĒĢĀ ņłś ņ׳ļŖö SD-OCTļĪ£ ĒåĀļü╝ ļ¦Øļ¦ē ĻĄ¼ņĪ░ņŚÉ ļīĆĒĢ£ ņĀĢļ¤ēĒÖöļÉ£ ĻĖ░ļ│Ė ņ×ÉļŻīļź╝ ņ¢╗ņŚłĻĖ░ņŚÉ ņĢ×ņ£╝ļĪ£ ņŗ£Ē¢ēļÉĀ ļÅÖļ¼╝ ļ░Å ņØĖĻ░ä ļ¦Øļ¦ē ņŚ░ĻĄ¼ņŚÉ ļ│Ė ņŚ░ĻĄ¼Ļ░Ć ĻĖ░ņŚ¼ĒĢĀ ņłś ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üĒĢ£ļŗż.
NOTES
Figure┬Ā1.
Experimental setup for measurement of rabbit retinal thickness. (A) The rabbit placed to take a Heidelberg Spectralis® OCT (Heidelberg Engineering GmbH, Heidelberg, Germany). (B) Optical coherence tomography (OCT) projection providing an overview of a rabbit fundus, including the optic nerve head (ONH) and presumed visual streak area (green area between dotted lines). Retinal layers were segmented along 33 raster b-scans. The measurements were repeated at 6 different positions at 0, 1, 2, 3, 4, and 5 mm ventral to the ONH edge. (C) Widefield fundus photography of the rabbit retina of the right eye. The presumed visual streak (green area between dotted lines) is located under the optic disc overlapping with the avascular field. (D) Spectral domain OCT scan of the rabbit retina. Total retinal layer thickness (TRT) = internal limiting membrane (ILM) to retinal pigment epithelium (RPE); inner retinal layer thickness (IRT) = ILM to anterior border of external limiting membrane (ELM); outer retinal layer thickness = anterior border of ELM to RPE (= TRT-IRT); ganglion cell complex thickness = retinal nerve fiber layer to anterior border of inner nuclear layer. (E) Histologic features of the rabbit retina with hematoxylin-eosin staining.
Figure┬Ā2.
(A) Retinal layer thickness at a distance from the optic nerve head. Total retinal layer thickness (p < 0.05), inner retinal layer thickness (p < 0.05), and outer retinal layer thickness (p < 0.05) decrease with distance from the optic nerve head (ONH). (B) Choroidal layer thickness at a distance from the optic nerve head. Choroidal thickness increases with distance from the ONH (p < 0.05). (C) Inner retinal layer thickness at a distance from the ONH. Ganglion cell complex (GCC) thickness (p < 0.05), ganglion cell layer (GCL) thickness (p < 0.05), inner nuclear layer (INL) thickness (p < 0.05), and outer nuclear layer (ONL) thickness (p < 0.05) decrease with distance from the optic nerve head.
Table┬Ā1.
Layer thickness at a distance from the optic nerve head edge
| Layer thickness (╬╝m) |
Distance from the ONH edge (mm) |
p-value* | |||||
|---|---|---|---|---|---|---|---|
| ONH edge | 1 | 2 | 3 | 4 | 5 | ||
| Total retinal layer | 172.14 ┬▒ 7.28 | 167.29 ┬▒ 8.60 | 158.88 ┬▒ 9.48 | 151.40 ┬▒ 8.98 | 146.38 ┬▒ 9.69 | 141.45 ┬▒ 8.96 | <0.001 |
| Inner retinal layer | 127.19 ┬▒ 5.06 | 122.69 ┬▒ 7.16 | 118.79 ┬▒ 6.74 | 113.19 ┬▒ 7.55 | 109.69 ┬▒ 7.93 | 106.62 ┬▒ 8.29 | <0.001 |
| Outer retinal layer | 44.95 ┬▒ 6.50 | 44.60 ┬▒ 4.91 | 40.10 ┬▒ 6.04 | 38.21 ┬▒ 6.85 | 36.69 ┬▒ 7.39 | 34.83 ┬▒ 7.39 | <0.001 |
| Choroid | 78.44 ┬▒ 27.71 | 96.22 ┬▒ 20.31 | 104.33 ┬▒ 16.23 | 112.02 ┬▒ 18.39 | 116.24 ┬▒ 16.97 | 115.40 ┬▒ 15.24 | <0.001 |
Table┬Ā2.
Inner retinal layer thickness at a distance from the optic nerve head edge
| Layer thickness (╬╝m) |
Distance from the ONH edge (mm) |
p-value* | |||||
|---|---|---|---|---|---|---|---|
| 0 | 1 | 2 | 3 | 4 | 5 | ||
| GCC | 52.27 ┬▒ 4.64 | 49.22 ┬▒ 7.22 | 48.53 ┬▒ 8.59 | 45.93 ┬▒ 9.27 | 45.38 ┬▒ 8.51 | 44.91 ┬▒ 9.09 | <0.001 |
| GCL | 20.07 ┬▒ 6.69 | 18.31 ┬▒ 5.00 | 17.31 ┬▒ 4.75 | 16.58 ┬▒ 4.56 | 16.13 ┬▒ 5.27 | 15.53 ┬▒ 5.59 | 0.001 |
| INL | 13.78 ┬▒ 2.44 | 13.84 ┬▒ 2.44 | 13.16 ┬▒ 2.50 | 12.71 ┬▒ 2.67 | 12.51 ┬▒ 3.56 | 11.78 ┬▒ 2.73 | 0.002 |
| ONL | 39.62 ┬▒ 5.06 | 32.69 ┬▒ 5.31 | 28.79 ┬▒ 6.40 | 24.69 ┬▒ 6.65 | 22.50 ┬▒ 6.57 | 19.90 ┬▒ 6.56 | <0.001 |
REFERENCES
1) Kim CH, Jin SY, Lee YH, Chang YS. Analysis of macular layer thickness measured using spectral domain optical coherence tomography in Korean subjects. J Korean Ophthalmol Soc 2016;57:264-75.

2) Gupta P, Sidhartha E, Tham YC, et al. Determinants of macular thickness using spectral domain optical coherence tomography in healthy eyes: the Singapore Chinese Eye study. Invest Ophthalmol Vis Sci 2013;54:7968-76.


3) Kim MH, Jeon CY, Baek SK, et al. The thickness of each retinal layer and visual acuity after vitrectomy in idiopathic epiretinal membrane. J Korean Ophthalmol Soc 2017;58:420-9.

4) Ko TH, Fujimoto JG, Schuman JS, et al. Comparison of ultrahighand standard-resolution optical coherence tomography for imaging macular pathology. Ophthalmology 2005;112:1922.e1-15.


5) Sayanagi K, Sharma S, Kaiser PK. Comparison of retinal thickness measurements between three-dimensional and radial scans on spectral-domain optical coherence tomography. Am J Ophthalmol 2009;148:431-8.


6) Badar├│ E, Novais E, Prodocimo LM, Sallum JM. Spectral-domain optical coherence tomography for macular edema. The Scientific World Journal 2014;2014:191847.



7) Ferguson LR, Grover S, Dominguez JM 2nd, et al. Retinal thickness measurement obtained with spectral domain optical coherence tomography assisted optical biopsy accurately correlates with ex vivo histology. PLoS One 2014;9:e111203.



8) Carpenter CL, Kim AY, Kashani AH. Normative retinal thicknesses in common animal models of eye disease using spectral domain optical coherence tomography. Adv Exp Med Biol 2018;1074:157-66.


9) Alkin Z, Kashani AH, L├│pez-Jaime GR, et al. Quantitative analysis of retinal structures using spectral domain optical coherence tomography in normal rabbits. Curr Eye Res 2013;38:299-304.


10) Ruggeri M, Wehbe H, Jiao S, et al. In vivo three-dimensional high-resolution imaging of rodent retina with spectral-domain optical coherence tomography. Invest Ophthalmol Vis Sci 2007;48:1808-14.


11) Muraoka Y, Ikeda HO, Nakano N, et al. Real-time imaging of rabbit retina with retinal degeneration by using spectral-domain optical coherence tomography. PLoS One 2012;7:e36135.



12) Penha FM, Rodrigues EB, Maia M, et al. Retinal and ocular toxicity in ocular application of drugs and chemicals--part I: animal models and toxicity assays. Ophthalmic Res 2010;44:82-104.


13) Del Amo EM, Urtti A. Rabbit as an animal model for intravitreal pharmacokinetics: clinical predictability and quality of the published data. Exp Eye Res 2015;137:111-24.


14) Chen S, Popp NA, Chan CC. Animal models of age-related macular degeneration and their translatability into the clinic. Expert Rev Ophthalmol 2014;9:285-95.



15) Bartuma H, Petrus-Reurer S, Aronsson M, et al. In vivo imaging of subretinal bleb-induced outer retinal degeneration in the rabbit. Invest Ophthalmol Vis Sci 2015;56:2423-30.


16) Lavaud A, Soukup P, Martin L, et al. Spectral domain optical coherence tomography in awake rabbits allows identification of the visual streak, a comparison with histology. Transl Vis Sci Technol 2020;9:13.

17) Cicinelli MV, Marchese A, Bandello F, Coppola M. Inner retinal layer and outer retinal layer findings after macular hole surgery assessed by means of optical coherence tomography. J Ophthalmol 2019;2019:3821479.



18) Bhagat PR, Deshpande KV, Natu B. Utility of ganglion cell complex analysis in early diagnosis and monitoring of glaucoma using a different spectral domain optical coherence tomography. J Curr Glaucoma Pract 2014;8:101-6.


19) Anraku A, Ishida K, Enomoto N, et al. Association between optic nerve head microcirculation and macular ganglion cell complex thickness in eyes with untreated normal tension glaucoma and a hemifield defect. J Ophthalmol 2017;2017:3608396.



20) Arepalli S, Srivastava SK, Hu M, et al. Assessment of inner and outer retinal layer metrics on the Cirrus HD-OCT Platform in normal eyes. PLoS One 2018;13:e0203324.



21) Vaney DI, Hughes A. The rabbit optic nerve: fibre diameter spectrum, fibre count, and comparison with a retinal ganglion cell count. J Comp Neurol 1976;170:241-51.


22) Oyster CW, Takahashi ES, Hurst DC. Density, soma size, and regional distribution of rabbit retinal ganglion cells. J Neurosci 1981;1:1331-46.



23) Juliusson B, Bergstr├Čm A, R├Čhlich P, et al. Complementary cone fields of the rabbit retina. Invest Ophthalmol Vis Sci 1994;35:811-8.

24) Hirata M, Tsujikawa A, Matsumoto A, et al. Macular choroidal thickness and volume in normal subjects measured by swept-source optical coherence tomography. Invest Ophthalmol Vis Sci 2011;52:4971-8.


25) De Schaepdrijver L, Simoens P, Lauwers H, De Geest JP. Retinal vascular patterns in domestic animals. Res Vet Sci 1989;47:34-42.


26) Ninomiya H, Inomata T, Kanemaki N. Microvascular architecture of the rabbit eye: a scanning electron microscopic study of vascular corrosion casts. J Vet Med Sci 2008;70:887-92.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




