 |
 |
| J Korean Ophthalmol Soc > Volume 62(3); 2021 > Article |
|
국문초록
대상과 방법
2018년 4월부터 2020년 1월까지 내원한 환자 중 빛간섭단층촬영 및 형광안저혈관조영술을 통해 나이관련황반변성에 동반된 맥락막신생혈관을 진단받았으나 치료받은 적 없는 59명의 63안을 대상으로 하였다. 삼출성 나이관련황반변성에 동반된 맥락막신생혈관은 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술에서 황반부의 과형광 및 후기의 누출 소견을 보이는 경우로 정의하였고, 빛간섭단층촬영에서 나타난 맥락막신생혈관의 위치에 따라 1형 및 2형으로 분류하였으며 이를 빛간섭단층혈관조영술의 자동 및 수동분할 결과와 비교하였다.
결과
1형 맥락막신생혈관은 45안, 2형 맥락막신생혈관은 18안이었다. 빛간섭단층혈관조영술의 자동분할에서 맥락막신생혈관 1형은 45안 중 29안, 2형은 18안 중 17안에서 확인되었고 수동분할을 수행하면 1형은 45안 중 41안, 2형은 18안에서 신생혈관이 확인되었다. 빛간섭단층혈관조영술에서 자동분할만 시행하면 1형 맥락막신생혈관 진단의 민감도는 64.44%, 수동분할을 수행하면 91.11%였고(p<0.001), 2형 맥락막신생혈관의 진단에서 자동분할만 시행하면 민감도는 94.44%, 수동분할도 수행한 경우 100%였다(p=1.000).
ABSTRACT
Purpose
To report the availability of optical coherence tomography angiography (OCTA) when diagnosing type 1 and type 2 choroidal neovascularization (CNV) associated with age-related macular degeneration.
Methods
We conducted a retrospective chart review of 63 eyes of 59 patients who visited the outpatient clinic from April 2018 to January 2020 with treatment-naïve type 1/2 CNV associated with age-related macular degeneration. The CNV was diagnosed through fluorescein angiography and indocyanine green angiography on the appearance of hyperfluorescence and leakage at the late phase. The CNV type was classified by location using OCT. These results were compared with those of automatic and manual segmentations via OCTA.
Results
Of the 63 eyes, 45 eyes showed type 1 CNV and 18 eyes indicated type 2 CNV. Using the automatic segmented display of OCTA, type 1 CNV was identified in 29 of 45 eyes and type 2 CNV was confirmed in 17 of 18 eyes. In addition, when manual segmentation was performed, type 1 CNV was found in 41 of 45 eyes and type 2 CNV in 18 of 18 eyes. The sensitivity of diagnosis of type 1 CNV using only automatic segmentation in OCTA was 64.44%; the sensitivity increased to 91.11% when additional manual segmentation was performed (p < 0.001). For type 2 CNV, the sensitivity was 94.44% using automatic segmentation in OCTA and 100% with additional manual segmentation (p = 1.000).
지금까지 맥락막신생혈관은 형광안저혈관조영술(fluorescein angiography)과 인도시아닌그린형광안저혈관조영술(indocyanine green angiography)을 통해 진단하고 위치에 따른 신생혈관의 분류는 빛간섭단층촬영술을 이용하였는데[1,2] 최근에는 빛간섭단층혈관조영술을 이용하면 맥락막신생혈관의 진단과 분류가 모두 가능하다고 알려져 있다[3,4]. 조영제를 이용한 형광안저혈관조영술의 경우 약제 유발 과민반응 및 침습적인 검사 방법으로 인한 합병증의 가능성이 존재하여 신생혈관의 치료 반응을 평가하기 위해 수차례 검사를 시행하기 어렵다는 단점이 있으며[5,6], 검사에 필요한 소요시간이 길고 형광고임과 형광물질의 누출, 염색 등으로 인해 신생혈관의 미세구조 경계를 정확히 파악하기 쉽지 않다[7,8].
반면 빛간섭단층혈관조영술은 비침습적인 검사 방법으로 망막 및 맥락막을 층별로 구획하여 혈관 구조를 보여주기 때문에 병변의 위치와 범위를 알 수 있으며 3차원 영상도 제공한다[9,10]. 특히, 삼출성 나이관련황반변성에 동반된 1형 맥락막신생혈관의 경우 망막색소상피세포층 아래에 존재하기 때문에 기존의 형광안저혈관조영술에서는 망막색소상피세포층에 가려지므로 검출하기 위해 많은 양의 형광물질이 필요하다[11]. 따라서 층별로 구획된 영상을 제공하는 빛간섭단층혈관조영술은 1형 맥락막신생혈관을 진단하는데 특히 유용한 방법이 될 수 있다. 본 연구에서는 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술에서 진단된 1형 및 2형 맥락막신생혈관에 대해 빛간섭단층혈관조영술을 시행하였으며, 자동분할 화면과 수동분할 화면에서 각각 신생혈관의 존재 여부를 확인하였고, 최종적으로 빛간섭단층혈관조영술이 1형 및 2형 맥락막신생혈관의 진단에 도움이 되는지 확인하고자 하였다.
본 연구는 2018년 4월부터 2020년 1월까지 본원에 내원한 환자 중 형광안저혈관조영술 및 인도시아닌그린형광안저혈관조영술, 빛간섭단층촬영을 통해 나이관련황반변성에 동반된 맥락막신생혈관을 진단받았으나 상기 질환에 대해 치료받은 과거력이 없는 59명의 63안을 대상으로 하였으며 의무기록을 통한 후향적 연구를 진행하였다. 본 연구는 상업적 이해관계가 없으며, 본원 임상연구심의위원회(Institutional review board, IRB)의 승인을 받아 진행하였고(승인 번호: SVEC 202003-004-01) 헬싱키선언(Declaration of Helsinki)을 준수하였다.
모든 환자는 나이관련황반변성에 동반된 맥락막신생혈관으로 처음 진단할 당시에 최대교정시력, 안압검사, 굴절검사, 안저검사, 형광안저혈관조영술, 인도시아닌그린형광 안저혈관조영술 및 빛간섭단층촬영과 빛간섭단층혈관조영술을 시행하였다. 최대교정시력은 Snellen 시력표를 이용하여 측정하였으며 logMAR로 변환하였다. 고도근시(6디옵터 이상) 환자, 시력에 영향을 줄 수 있는 다른 질환이나 병태를 동반한 경우 본 연구에서 제외하였으며, 이전에 유리체망막 수술을 시행 받았거나 나이관련황반변성으로 진단받고 안구내 주사 또는 레이저치료를 시행 받은 경우 역시 연구 대상에서 제외하였다.
삼출성 나이관련황반변성에 동반된 맥락막신생혈관은 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술에서 황반부의 맥락막신생혈관, 망막하 삼출물과 출혈, 망막색소상피박리를 시사하는 과형광 및 후기의 누출 소견을 보이는 경우로 정의하였고, 빛간섭단층촬영에서 나타난 맥락막신생혈관의 위치에 따라 1형 및 2형으로 분류하였다[12]. 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술에 의한 맥락막신생혈관의 분류 결과를 모르는 상태로 다른 검사자에 의해 빛간섭단층혈관조영술에서 맥락막신생혈관이 존재하는지 확인한 후에 함께 제시되는 빛간섭단층촬영에서 맥락막신생혈관의 위치를 확인하여 1형 및 2형을 분류하였으며, 이를 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술로 맥락막신생혈관을 분류한 결과와 비교하였다. 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술, 빛간섭단층촬영 및 빛간섭단층혈관조영술의 검사 결과는 위에 제시한 방법에 따라 각각 두 명의 검사자가 평가하여 일치된 경우를 연구 대상에 포함하였고 병태 생리에 차이를 보인다고 알려져 있는 결절맥락막혈관병증 및 망막혈관종성증식은 제외하였다.
빛간섭단층혈관조영술은 한 명의 숙련된 검사자에 의해 시행되었으며 870 nm의 파장을 광원으로 이용하여 초당 85,000개의 A-scan을 조사하는 Spectralis OCT2 (spectral domain optical coherence tomography [SD-OCT]; Heidelberg engineering, Heidelberg, Germany) 기기가 이용되었다. 스캔을 통해 얻어진 신호는 Full-spectrum probabilistic approach 알고리즘을 이용하여 이미지로 표현되었고 본 연구에서는 황반을 중심으로 하는 3 × 3 mm 영역을 촬영하였다.
빛간섭단층혈광조영술 자동분할의 경우 스캔된 이미지를 내장된 소프트웨어를 통해 표층혈관총(superficial vascular complex)과 심층혈관총(deep vascular complex), 무혈관망막복합체(avascular complex), 맥락막모세혈관층(choriocapillaris)이 자동으로 구분되었으며, 표층혈관총은 내경계막부터 내망상층/내핵층 경계의 위쪽 17 µm에 해당하는 부분 사이의 영역으로 정의되었고, 심층혈관총은 내망상층/내핵층 경계로부터 위쪽 17 µm에 해당하는 부분부터 외망상층 사이의 영역을 포함하였다. 무혈관망막복합체는 외망상층 아래에서 브루크막(Bruch's membrane)까지의 영역으로 맥락막모세혈관층은 브루크막 아래의 영역으로 정의하였다.
맥락막신생혈관 진단을 위한 빛간섭단층혈관조영술의 수동분할은 Farecki et al [13]이 제시한 방법을 사용하였다. 자동분할 방식을 통해 정의된 맥락막모세혈관층 및 외망막층에서 분할 수준을 수동적으로 조정하여 맥락막신생혈관의 존재 여부를 확인하였고 신생혈관이 존재하는 경우, 신생혈관망이 가장 크게, 경계가 잘 구분되는 형태를 보이는 위치를 확인하였다. 빛간섭단층혈관조영술 시행 중 주시가 잘 되지 않거나 안구의 움직임과 관련된 오류(motion artifact), 눈 깜빡임과 관련된 오류(blinking artifact)가 심한 경우는 제외되었으며 측정된 이미지의 signal strength index가 40 dB 이상인 경우만을 대상으로 하였다.
대상 환자는 총 59명의 63안으로 첫 내원 당시, 빛간섭단층촬영 및 형광안저혈관조영술, 인도시아닌그린형광안저혈관조영술을 통해 진단된 1형 맥락막신생혈관 환자 41명의 45안과 2형 맥락막신생혈관으로 진단된 18명의 18안으로 구성되었다. 평균 연령은 70.85 ± 10.63세였으며, 39명이 남자, 24명이 여자였다. 1형 맥락막신생혈관 환자의 평균 연령은 68.69 ± 10.24세였고 2형 맥락막신생혈관 환자의 경우 76.28 ± 9.88세로 확인되어 두 환자군 간에 통계적으로 유의한 차이가 있었다(p=0.009). 첫 내원 당시 최대교정시력은 1형 맥락막신생혈관의 경우 0.27 ± 0.28 logMAR scale, 2형 맥락막신생혈관은 0.82 ± 0.43 logMAR scale로 측정되어 두 환자군 사이에 통계적으로 유의한 차이가 있었다(p<0.001) (Table 1).
1형 맥락막신생혈관으로 진단된 45안 중 29안은 첫 내원 시 시행한 빛간섭단층혈관조영술에서 내장된 프로그램을 이용한 자동분할 화면을 통해 맥락막신생혈관이 확인되었으며, 2형 맥락막신생혈관의 경우 18안 중 17안에서 자동 분할 화면을 통해 맥락막신생혈관을 확인하였다. 또한 연구 대상이 되는 63안에 대하여 빛간섭단층혈관조영술의 망막층별 수동분할을 수행하였고, 1형 맥락막신생혈관은 45안 중에서 41안, 2형 맥락막신생혈관은 18안 모두 맥락막신생혈관의 존재를 확인할 수 있었다.
빛간섭단층혈관조영술의 자동분할 화면에서 1형 및 2형 맥락막신생혈관을 확인할 수 있었던 경우에는 안저촬영 및 형광안저혈관조영술과 인도시아닌그린형광안저혈관조영술, 빛간섭단층촬영을 통해 진단된 맥락막신생혈관과 상응하는 위치의 무혈관복합체 망막층에서 신생혈관이 확인되었다(Fig. 1). 자동분할 화면에서 맥락막신생혈관이 확인되지 않았던 경우는 1형 맥락막신생혈관에서 16안이었으며 그 중에 12안에서 수동분할을 통해 신생혈관이 확인되었고(Fig. 2), 2형 맥락막신생혈관에서는 1안만이 자동분할 화면에서 맥락막신생혈관이 불분명하였지만 수동분할 화면에서 신생혈관이 확인되었다(Table 2). 자동분할 화면에서 맥락막신생혈관이 확인되지 않은 17안에 대한 자동분할과 수동분할 화면을 비교해보았을 때, 맥락막신생혈관의 크기가 작은 경우, 다발성 혹은 크고 넓은 망막색소상피박리 또는 망막하삼출물이 맥락막신생혈관과 같은 위치에 존재하는 경우가 대부분이었으며 특히 1형 맥락막신생혈관 16안 중 4안은 수동분할 방식으로도 명확한 신생혈관을 특정하기 어려웠다.
빛간섭단층혈관조영술의 분할 방법에 따른 맥락막신생혈관의 진단 민감도를 구해보면, 1형 맥락막신생혈관의 경우 빛간섭단층혈관조영술의 자동분할 화면을 통해 진단할 경우 64.44%의 민감도를 보였으며 수동분할을 추가로 수행한 경우 91.11%였다(p<0.001). 2형 맥락막신생혈관의 진단에서 자동분할만 시행한 경우 민감도는 94.44%이고 수동분할을 추가로 수행한 경우 민감도는 100%였다(p=1.000, Table 3).
빛간섭단층혈관조영술(optical coherence tomographyangiography)은 비침습적으로 적혈구의 움직임을 감지하여 혈관의 구조를 시각화하는 방식으로 고해상도의 망막 및 맥락막의 혈관 구조를 보여주는 검사이다[14]. 중심오목을 중심으로 하는 3 × 3 mm 영역의 혈관 밀도 및 중심오목무혈관부위(foveal avascular zone) 면적과 형태 변화 등을 측정하여 여러 망막 질환의 진단과 경과 확인에 이용하고 있다[15,16]. 맥락막신생혈관은 빛간섭단층혈관조영술에서 주로 외망막층 및 맥락막모세혈관층에서 높은 혈류와 공급혈관을 동반한 잘 형성된 혈관망의 형태로 관찰되는 것으로 알려져 있다[17,18]. 이러한 맥락막신생혈관을 진단하고 분류하기 위해 표준 검사로 이용되고 있는 형광안저혈관조영술은 신생혈관 부위에서 형광물질의 유출을 보인다는 점이 빛간섭단층혈관조영술과 가장 큰 차이라고 할 수 있으며 형광물질의 유출은 맥락막신생혈관의 활성도를 나타내는 지표로 이용될 수 있다[19]. 하지만 다른 관점에서 보면 형광물질의 누출로 신생혈관의 구조를 가리는 현상이 나타날 수 있기 때문에 이 점은 1형 맥락막신생혈관과 같은 잠복 신생혈관의 미세혈관 구조를 파악하고 크기나 모양의 변화 및 병변의 위치를 확인하는 데 빛간섭단층혈관조영술이 더 용이하다는 것을 의미하기도 한다[20,21].
빛간섭단층혈관조영술에서 1형 맥락막신생혈관에 대한 초기 연구는 형광안저혈관조영술에서 확인하기 어려웠던 신생혈관의 성장 형태를 “부채꼴 산호(sea fan)”, “해파리(medusa)”, “실타래(tangle)” 그리고 “고사목(dead tree)” 등의 모양으로 분류하는 내용이 주를 이루었다[22,23]. 그 외에도 맥락막신생혈관의 평균 면적을 구하거나 신생혈관 내부 혈관 밀도 비율 등을 정량적으로 분석하여 신생혈관 활성도와 연관성을 확인하려는 연구도 있었는데, 평균 맥락막신생혈관 면적은 신생혈관 활성도와 통계학적으로 유의한 연관성을 보였으나 신생혈관밀도의 비율은 유의하지 않은 것으로 나타났다[24,15]. Xu et al [25]은 1형 맥락막신생혈관을 기존의 형태학적 분류에 더하여 신생혈관의 핵심혈관이 성숙한 정도나 분지혈관의 분포 등도 포함시켜 분류하였고 신생혈관 성장의 예후 지표로서 이를 이용할 수 있음을 확인하였다.
1형 맥락막신생혈관은 빛간섭단층혈관조영술에서 혈관 경계가 불분명하고 2형 맥락막신생혈관에 비해 크기가 더 작은 것으로 알려져 있으며 외망막층까지 확장되는 2형 맥락막신생혈관에 비해 확인이 어렵다는 특징이 있다[15]. 또한 삼출성 나이관련황반변성에 동반된 맥락막신생혈관의 경우 정상 망막 및 맥락막에 비해 망막부종이나 삼출물, 출혈, 연속성이 손상된 망막층 등의 병변이 동반될 수 있기 때문에 이는 더욱 맥락막신생혈관의 확인을 어렵게 하는 요인이 된다[18,12]. 따라서 맥락막신생혈관의 빛간섭단층혈관조영술에 대한 기존의 연구들은 자동분할이 아닌 수동분할까지 수행하여 검사의 민감도 및 특이도를 확인하는 경우가 많았다[26,27].
빛간섭단층혈관조영술에서 망막층을 자동분할하는 알고리즘은 건강한 눈을 기준으로 하기에 정상적인 망막층의 구조를 변화시키는 질병이 발생할 경우 이러한 알고리즘은 각각의 망막층을 정상적으로 구별하지 못하고 하나의 층으로 인식하거나 전혀 다른 층으로 오인하는 오류를 범하게 된다. 특히 맥락막신생혈관에 동반되는 망막색소상피박리, 망막출혈, 망막하액, 망막내액 등이 심할수록 이러한 망막층의 구별이 어려워지며 이는 자연히 자동분할의 오류를 초래하게 되어 빛간섭단층혈관조영술검사에서 맥락막신생혈관의 진단을 어렵게 만드는 주요 원인이 된다. 이러한 문제를 해결하고자 각각의 빛간섭단층혈관조영술 제조사마다 정확한 분할 알고리즘에 대하여 연구를 꾸준히 시행하고 있고 이를 지속적인 소프트웨어 업데이트를 통해 자동 분할의 정확도를 향상시키고자 노력하고 있지만 아직까지 망막층의 구조가 변형되는 병적인 상황에서는 완벽한 자동 분할이 쉽지 않은 실정이다[28]. 따라서 모든 제조사들은 이를 보완하고자 해당 소프트웨어에서 다양한 수동분할의 기능을 제공한다. 물론 이러한 기능을 사용하고자 하는 경우 각각의 프로그램에서 volume scan을 불러오고 망막층의 분할을 직접 수정하고 확인하는 데 상당한 시간과 노력이 소요되는 것이 사실이나, 자동분할에서 놓칠 수 있는 맥락막신생혈관을 새롭게 찾아낼 수 있으므로 수동분할에 대한 숙지가 필요할 것으로 생각된다.
빛간섭단층혈관조영술의 수동분할은 맥락막신생혈관의 진단뿐만 아니라 다른 망막질환의 진단에서도 유용한 방법이 될 수 있는데, 당뇨망막병증에서 망막중심오목 무혈관 부위의 면적을 비교하거나[29], 중심장액맥락망막병증에서 발생한 맥락막신생혈관의 확인에도 유용한 것으로 알려져 있다[30]. 또한 망막질환이 없는 건강한 성인을 대상으로 망막중심오목 무혈관 부위를 분석한 연구에서도 자동분할만 시행한 것보다 수동분할을 시행하였을 때 더 정확한 결과를 보였다는 보고도 있다[31].
하지만 빛간섭단층혈관조영술은 중심오목을 중심으로 하는 2 × 2 mm부터 12 × 12 mm까지의 제한된 영역에 대한 정보를 제공할 수 있다고 알려져 있으며 아직까지는 3 × 3 mm 영역에 한해 고해상도의 영상을 얻을 수 있어 형광안저혈관조영술보다 좁은 범위의 영역만을 확인할 수 있다[32]. 또한 짧은 검사 시간을 통해 특정 시점의 혈류에 대한 정보를 수집하기 때문에 형광안저혈관조영술과는 다른 종류의 오류(artifact)가 발생할 가능성이 있다. 예를 들어 피험자의 움직임이나 눈 깜박임으로 인한 오류(motion artifact), 망막의 큰 혈관에 의해 깊은 층 망막에 생기는 그림자 오류(shadow artifact), 망막색소상피박리 병변의 경계에서 발생하는 흰 잡음 오류(white noise artifact), 미세혈관류나 섬유성 맥락막신생혈관 내부의 느린 혈류로 인해 혈관 구조가 검출되지 않는 오류 등이 있다[33]. 따라서 빛간섭단층혈관조영술에서 얻은 정보는 이와 같은 오류가 발생할 가능성을 염두에 두고 해석할 필요가 있다.
빛간섭단층혈관조영술의 자동분할 방식은 내장된 소프트웨어를 이용하여 외망막층의 혈관조영상에서 내망막층의 혈관조영상과 오류(artifacts)를 제거한 자동화 알고리즘을 통해 신생혈관을 확인할 수 있으며 대부분의 맥락막신생혈관은 자동분할 방식으로 검출이 가능하다고 알려져 있다[34,24]. 따라서 실제 임상에서는 대부분 자동분할 방식으로 제공된 영상을 통해 맥락막신생혈관의 존재를 확인한다. 하지만 빛간섭단층혈관조영술에서 자동분할 방식의 정확성은 망막층의 연속성이 유지되는 상황에서 유효하기 때문에 삼출성 나이관련황반변성과 같이 망막층의 연속성이 손상된 질환에서는 오류가 발생할 가능성이 있다[28]. 이를 보완하기 위한 빛간섭단층혈관조영술의 수동분할은 자동분할 방식을 통해 정의된 망막 및 맥락막의 각 층이 해부학적으로 정확한지 확인하고 이를 수정할 수 있으며, 분할 수준을 수동적으로 조정하여 병변의 존재 여부를 확인하는 방식으로 병변의 검출률을 높이기 위해 제한적으로 시행되고 있다[17]. 잠복 신생혈관의 특성을 가지는 1형 맥락막신생혈관은 빛간섭단층혈관조영술의 자동분할 방식을 이용할 경우 다른 유형의 맥락막신생혈관에 비해 검출률이 낮은 것으로 알려져 있기 때문에[13], 자동분할만 시행하는 것보다 수동분할을 추가로 시행하는 것이 진단에 유용할 수 있다.
본 연구에서 결절맥락막혈관병증과 망막혈관종성증식은 전형적인 삼출성 나이관련황반변성과 병태생리에 차이가 있다고 알려져 연구 대상에서 제외되었는데, 결절맥락막혈관병증의 경우 스펙트럼영역 빛간섭단층촬영(SD-OCT)에서 방사상으로 가지를 치는 선형의 혈관(branching vascular network)과 동반된 결절로 구성되는 이상혈관구조가 발견되었으며[35], 깊이증강모드 빛간섭단층촬영(enhanced depth imaging OCT)에서는 맥락막의 비후와 구조적인 변화가 확인되어 맥락막의 두께 감소가 특징인 전형적인 삼출성 나이관련황반변성과 병태생리에서 차이가 있을 것으로 생각된다[36-38]. 또 망막혈관종성증식은 Yannuzzi et al [39]에 따르면 깊은 망막층뿐만 아니라 맥락막에서도 처음에 신생혈관이 발생한다는 것이 밝혀져 서로 다른 두 곳의 신생혈관 병소를 가진다는 점에서 전형적인 삼출성 나이관련황반변성에 동반된 맥락막신생혈관과 병태생리에 차이를 보인다. 따라서 본 연구에서는 비슷한 병태생리를 보이는 삼출성 나이 관련황반변성에 동반된 1형과 2형의 맥락막신생혈관을 대상으로 연구를 진행하였다.
임상에서 맥락막신생혈관을 진단할 때 빛간섭단층혈관조영술의 수동분할을 추가로 시행하는 것이 자동분할만 이용하는 것에 비해 실제로 유용한지 확인한 연구는 없었기에 1형과 2형 맥락막신생혈관을 대상으로 이를 확인하고자하였고, 2형 맥락막신생혈관은 자동분할과 수동분할에서 진단의 민감도가 통계적으로 유의한 차이가 없었으나 1형 맥락막신생혈관의 진단에서는 수동분할이 자동분할에 비해 유용한 방법임을 확인하였다.
본 연구 대상 중에 빛간섭단층혈관조영술의 자동분할 방식으로 맥락막신생혈관이 확인되지 않았던 경우를 보면, 1형 맥락막신생혈관의 경우 대부분 신생혈관의 크기가 작고 주위에 망막하액이나 망막색소상피박리가 동반되어 있었으며 2형 맥락막신생혈관의 경우에는 망막내액과 망막하액의 양이 많아서 맥락막신생혈관이 확인되지 않았다. 수동분할을 추가로 시행하였을 때 대부분 신생혈관의 확인이 가능하였으나 망막색소상피박리의 범위가 3 × 3 mm를 넘어서면서 박리 높이가 높았던 경우와 형광안저혈관조영술에서 확인된 맥락막신생혈관의 크기가 매우 작으면서 신생혈관의 위치에 망막하 삼출물이 넓게 분포했던 경우에는 수동분할로도 신생혈관이 명확하게 확인되지 않았다. de Carlo et al [26]에 따르면 주시가 잘 되지 않거나 망막하 출혈이나 삼출물, 망막색소상피박리가 큰 경우에는 맥락막신생혈관, 특히 1형의 경우 빛간섭단층혈관조영술에서 검출이 어렵다고 알려져 있어 본 연구의 결과와 상응하는 것을 확인할 수 있었다. 따라서 위의 경우를 제외하면 나이관련황반변성에 동반된 맥락막신생혈관에서 진단을 위해 형광물질을 이용한 망막혈관조영술을 시행하기 어렵거나 여러 차례 검사가 필요한 경우에는 빛간섭단층혈관조영술을 수행하는 것이 임상적으로 유용함을 확인할 수 있었다. 하지만 연구의 대상이 63안으로 많지 않았기에 수동분할로도 맥락막신생혈관이 확인되지 않았던 증례를 더 수집하여 이에 대한 후속 연구가 필요할 것으로 생각되며, 각 유형별 맥락막신생혈관의 경과 확인 또는 치료 효과 판정에도 유효하게 사용할 수 있는지에 대한 추가 연구도 필요하다.
Figure 1.
Representative images of two subtypes of choroidal neovascularization (CNV) with exudative age-related macular degeneration. Fundus photograph (A, E), fluorescein and indocyanine green angiography (B, F), optical coherence tomography (C, G) and optical coherence tomography angiography (OCTA) images (D, H) of type 1 CNV (A-D) and type 2 CNV (E-H). CNV in OCTA was indicated by yellow dot circles.
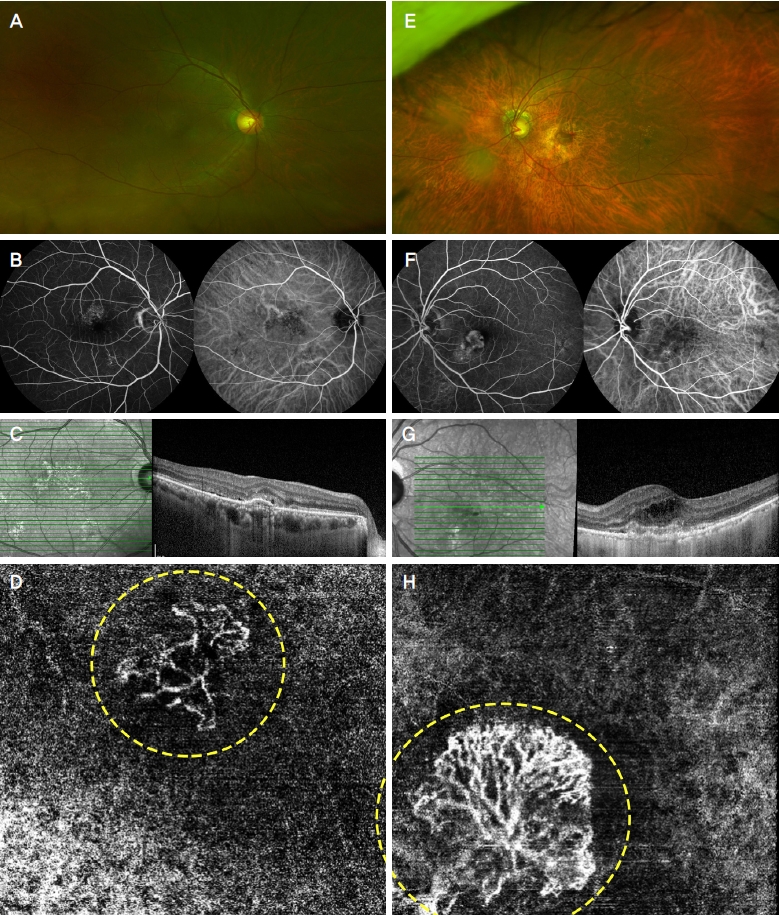
Figure 2.
Case of ambiguous detection of choroidal neovascularization (CNV) on automated segmentation, but well identification on manual segmentation in optical coherence tomography angiography. Fundus photograph (A), fluorescein and Indocyanine green angiography (B), optical coherence tomography (C) and images of automated segmentation (D) and manual segmentation (E) in optical coherence tomography angiography (OCTA). CNV on manual segmentation in OCTA was indicated by yellow dot circle.
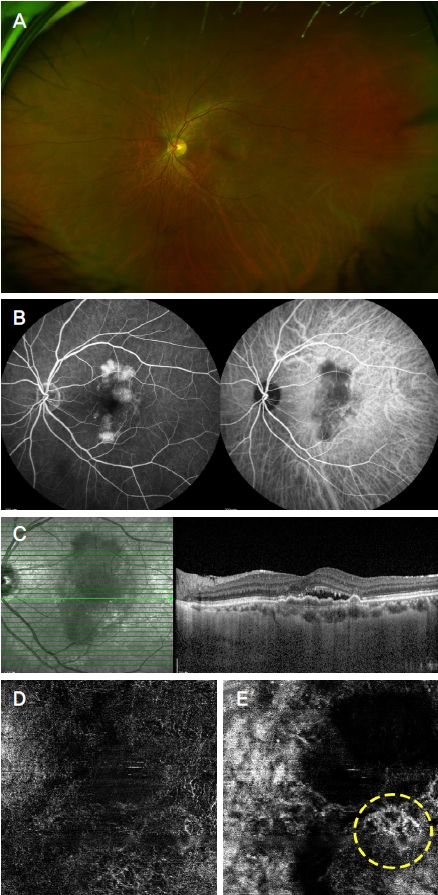
Table 1.
Demographic data of patients with type 1 or 2 choroidal neovascularization
| Type 1 CNV (n = 45) | Type 2 CNV (n = 18) | p-value* | |
|---|---|---|---|
| Age (years) | 68.69 ± 10.24 | 76.28 ± 9.88 | 0.009 |
| Sex (M:F) | 29:16 | 10:8 | 0.515 |
| Mean BCVA (logMAR) | 0.27 ± 0.28 | 0.82 ± 0.43 | <0.001 |
Table 2.
Numerical value of detected CNV by two methods of segmentation in OCTA
| Type 1 CNV (n = 45) | Type 2 CNV (n = 18) | |
|---|---|---|
| AS in OCTA | 29 | 17 |
| MS in OCTA | 41 | 18 |
Table 3.
Comparisons of sensitivity of diagnosing type 1 and 2 CNV between two methods in OCTA
| Sensitivity after AS in OCTA (%) | Sensitivity after MS in OCTA (%) | p-value* | |
|---|---|---|---|
| Type 1 CNV | 64.44 | 91.11 | <0.001 |
| Type 2 CNV | 94.44 | 100 | 1.000 |
REFERENCES
1) Do DV, Gower EW, Cassard SD, et al. Detection of new-onset choroidal neovascularization using optical coherence tomography: the AMD DOC Study. Ophthalmology 2012;119:771-8.


3) Jia Y, Bailey ST, Wilson DJ, et al. Quantitative optical coherence tomography angiography of choroidal neovascularization in age-related macular degeneration. Ophthalmology 2014;121:1435-44.



4) Coscas GJ, Lupidi M, Coscas F, et al. Optical coherence tomography angiography versus traditional multimodal imaging in assessing the activity of exudative age-related macular degeneration: a new diagnostic challenge. Retina 2015;35:2219-28.

5) Stanga PE, Lim JI, Hamilton P. Indocyanine green angiography in chorioretinal diseases: indications and interpretation: an evidence-based update. Ophthalmology 2003;110:15-21.


6) Lopez-Saez MP, Ordoqui E, Tornero P, et al. Fluorescein-induced allergic reaction. Ann Allergy Asthma Immunol 1998;81:428-30.


7) Novotny HR, Alvis DL. A method of photographing fluorescence in circulating blood in the human retina. Circulation 1961;24:82-6.


8) Yannuzzi LA, Slakter JS, Sorenson JA, et al. Digital indocyanine green videoangiography and choroidal neovascularization. Retina 1992;12:191-223.


9) Spaide RF, Klancnik JM Jr, Cooney MJ. Retinal vascular layers imaged by fluorescein angiography and optical coherence tomography angiography. JAMA Ophthalmol 2015;133:45-50.


10) Wang RK, Jacques SL, Ma Z, et al. Three dimensional optical angiography. Opt Express 2007;15:4083-97.


11) Bressler NM, Bressler SB. Neovascular (exudative or “wet”) age-related macular degeneration. In: Ryan SJ, Sadda SR, Hinton DR, Retina 5th ed. Vol. 3. Philadelphia: Saunders Elsevier, 2013;1183-212.
12) Seddon JM, Sharma S, Adelman RA. Evaluation of the clinical age-related maculopathy staging system. Ophthalmology 2006;113:260-6.


13) Farecki ML, Gutfleisch M, Faatz H, et al. Characteristics of type 1 and 2 CNV in exudative AMD in OCT-Angiography. Graefes Arch Clin Exp Ophthalmol 2017;255:913-21.


14) Makita S, Hong Y, Yamanari M, et al. Optical coherence angiography. Opt Express 2006;14:7821-40.


15) Ji BJ, Kim HC. Foveal microvascular changes based on optical coherence tomography angiography in mild nonproliferative diabetic retinopathy. J Korean Ophthalmol Soc 2016;57:1723-30.

16) Kuehlewein L, An L, Durbin MK, Sadda SR. Imaging areas of retinal nonperfusion in ischemic branch retinal vein occlusion with swept-source OCT microangiography. Ophthalmic Surg Lasers Imaging Retina 2015;46:249-52.


17) Kuehlewein L, Bansal M, Lenis TL, et al. Optical coherence tomography angiography of type 1 neovascularization in age-related macular degeneration. Am J Ophthalmol 2015;160:739-48.e2.


18) Jia Y, Bailey ST, Wilson DJ, et al. Quantitative optical coherence tomography angiography of choroidal neovascularization in agerelated macular degeneration. Ophthalmology 2014;121:1435-44.


19) Conrath J, Giorgi R, Raccah D, Ridings B. Foveal avascular zone in diabetic retinopathy: quantitative vs qualitative assessment. Eye (Lond) 2005;19:322-6.


20) Novais EA, Adhi M, Moult EM, et al. Choroidal neovascularization analyzed on ultrahigh-speed swept-source optical coherence tomography angiography compared to spectral-domain optical coherence tomography angiography. Am J Ophthalmol 2016;164:80-8.



21) Inoue M, Jung JJ, Balaratnasingam C, et al. A comparison between optical coherence tomography angiography and fluorescein angiography for the imaging of type 1 neovascularization. Invest Ophthalmol Vis Sci 2016;57:314-23.

22) Sulzbacher F, Pollreisz A, Kaider A, et al. Identification and clinical role of choroidal neovascularization characteristics based on optical coherence tomography angiography. Acta Ophthalmol 2017;95:414-20.


23) Carnevali A, Sacconi R, Querques L, et al. Natural history of treatment-naïve quiescent choroidal neovascularization in age-related macular degeneration using OCT angiography. Ophthalmol Retina 2018;2:922-30.


24) Faridi A, Jia Y, Gao SS, et al. Sensitivity and specificity of OCT angiography to detect choroidal neovascularization. Ophthalmol Retina 2017;1:294-303.



25) Xu D, Dávila JP, Rahimi M, et al. Long-term progression of type 1 neovascularization in age-related macular degeneration using optical coherence tomography angiography. Am J Ophthalmol 2018;187:10-20.


26) de Carlo TE, Bonini Filho MA, Chin AT, et al. Spectral-domain optical coherence tomography angiography of choroidal neovascularization. Ophthalmology 2015;122:1228-38.


27) Souedan V, Souied EH, Caillaux V, et al. Sensitivity and specificity of optical coherence tomography angiography (OCT-A) for detection of choroidal neovascularization in real-life practice and varying retinal expertise level. Int Ophthalmol 2018;38:1051-60.


28) Spaide RF, Curcio CA. Evaluation of segmentation of the superficial and deep vascular layers of the retina by optical coherence tomography angiography instruments in normal eyes. JAMA Ophthalmol 2017 135:259.‐62.


29) Park JJ, Soetikno BT, Fawzi AA. Characterization of the middle capillary plexus using optical coherence tomography angiography in healthy and diabetic eyes. Retina 2016;36:2039-50.



30) Bonini Filho MA, de Carlo TE, Ferrara D, et al. Association of choroidal neovascularization and central serous chorioretinopathy with optical coherence tomography angiography. JAMA Ophthalmol 2015;133:899-906.



31) Rommel F, Siegfried F, Kurz M, et al. Impact of correct anatomical slab segmentation on foveal avascular zone measurements by optical coherence tomography angiography in healthy adults. J Curr Ophthalmol 2018;30:156-60.



32) Matsunaga D, Yi J, Puliafito CA, Kashani AH. OCT angiography in healthy human subjects. Ophthalmic Surg Lasers Imaging Retina 2014;45:510-5.


33) de Carlo TE, Romano A, Waheed NK, Duker JS. A review of optical coherence tomography angiography (OCTA). Int J Retina Vitreous 2015 Apr 15 . doi: 10.1186/s40942-015-0005-8.

34) Liu L, Gao SS, Bailey ST, et al. Automated choroidal neovascularization detection algorithm for optical coherence tomography angiography. Biomed Opt Express 2015;6:3564-76.



35) Khan S, Engelbert M, Imamura Y, Freund KB. Polypoidal choroidal vasculopathy: simultaneous indocyanine green angiography and eye-tracked spectral domain optical coherence tomography fi ndings. Retina 2012;32:1057-68.

36) Kim SW, Oh J, Kwon SS, et al. Comparison of choroidal thickness among patients with healthy eyes, early age-related maculopathy, neovascular age-related macular degeneration, central serous chorioretinopathy, and polypoidal choroidal vasculopathy. Retina 2011;31:1904-11.


37) Koizumi H, Yamagishi T, Yamazaki T, et al. Subfoveal choroidal thickness in typical age-related macular degeneration and polypoidal choroidal vasculopathy. Graefes Arch Clin Exp Ophthalmol 2011;249:1123-8.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,543 View
- 101 Download
- Related articles
-
Diagnostic Availability of Blind Spot Mapping for Ocular Torsion.2016 June;57(6)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



