 |
 |
| J Korean Ophthalmol Soc > Volume 62(3); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļé£ņ╣śņä▒ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņŚÉņä£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ĒÜ©Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
ņŖżĒģīļĪ£ņØ┤ļō£ņÖĆ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļĪ£ ņĪ░ņĀłļÉśņ¦Ć ņĢŖņĢä ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļĪ£ ņ╣śļŻīĒĢ£ ļ╣äĻ░ÉņŚ╝ņä▒ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ ĒÖśņ×ÉņØś ņØśļ¼┤ ĻĖ░ļĪØņØä ĒøäĒ¢źņĀüņ£╝ļĪ£ ļČäņäØĒĢśņśĆļŗż. ļéśņØ┤, ņä▒ļ│ä, Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä, ņĀäņŗĀņ¦łĒÖśĻ│╝ņØś ņŚ░Ļ┤Ćņä▒ ļō▒ņØä ĒżĒĢ©ĒĢ£ ĒÖśņ×ÉņØś ļ│æļĀźņØä ļČäņäØĒĢśņśĆļŗż. ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģ Ēøä ņ×¼ļ░£ ņŚåņØ┤ ņ£Āņ¦ĆļÉśļŖö ĻĖ░Ļ░äĻ│╝ ņŗ£ļĀź ļ│ĆĒÖö, ņ×äĒöīļ×ĆĒŖĖ Ēł¼ņŚ¼ Ēܤņłśļź╝ ļČäņäØĒĢśņśĆĻ│Ā, ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖņÖĆ Ļ┤ĆļĀ©ĒĢ£ ņĢłņĢĢņāüņŖ╣ņŚÉ ļīĆĒĢ┤ ļČäņäØĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
5ļ¬ģ 7ņĢłņØ┤ ĒżĒĢ©ļÉśņŚłļŗż. ĒÅēĻĘĀ ļéśņØ┤ļŖö 73.2 ┬▒ 12.5ņäĖ(59-92ņäĖ)ņśĆļŗż. 7ņĢł ļ¬©ļæÉņŚÉņä£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ļ¦źļØĮļ¦ēņŻ╝ļ”äņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż. 5ļ¬ģ ļ¬©ļæÉņŚÉņä£ ņ┤łĻĖ░ņŚÉļŖö Ļ│ĀņÜ®ļ¤ē ņĀäņŗĀ ņŖżĒģīļĪ£ņØ┤ļō£ļĪ£ ņĪ░ņĀłĒĢśņśĆĻ│Ā, ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ņČöĻ░ĆĒĢśņśĆļŗż. ņ×”ņØĆ ņ×¼ļ░£Ļ│╝ ņĢĮņĀ£ ļČĆņ×æņÜ®ņ£╝ļĪ£ ņĪ░ņĀłņØ┤ ņøÉĒÖ£ĒĢśņ¦Ć ņĢŖņĢä ĒÅēĻĘĀ 8.2Ļ░£ņøö(3-27Ļ░£ņøö) Ēøä ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņØä Ļ▓░ņĀĢĒĢśņśĆļŗż. Ēł¼ņŚ¼ Ēøä 7ņĢł ļ¬©ļæÉņŚÉņä£ ņĄ£ņåī 2Ļ░£ņøö ņØ┤ņāü(2-5Ļ░£ņøö) Ļ│Ąļ¦ēņŚ╝ņØĆ ņל ņĪ░ņĀłļÉśņŚłļŗż. 7ņĢłņŚÉņä£ ņ┤Ø 15ĒÜī(ĒÅēĻĘĀ 2.1ĒÜī)ļź╝ ņŻ╝ņ×ģĒĢśņśĆĻ│Ā, 1ĒÜīņŚÉņä£ ņØ╝ņŗ£ņĀü ņĢłņĢĢņāüņŖ╣ņØ┤ ļ░£ņāØĒĢ£ Ļ▓ā ņÖĖ ĒĢ®ļ│æņ”ØņØĆ ļ░£ņāØĒĢśņ¦Ć ņĢŖņĢśļŗż.
ABSTRACT
Purpose
To report the effect of an intravitreal dexamethasone implant on refractory posterior scleritis.
Methods
The medical records of patients treated with an intravitreal dexamethasone implant for non-infectious refractory posterior scleritis were retrospectively reviewed, including age, sex, duration of follow-up, and presence of associated systemic diseases. The duration until relapse, changes in visual acuity, number of implants, and side effects associated with the implant were also analyzed.
Results
Seven eyes from five patients were included. The mean age was 73.2 ┬▒ 12.5 years (59-92 years). Although all patients had been treated with high-dose systemic steroid, and immunosuppressants were added, the posterior scleritis was poorly controlled. The duration from the diagnosis to the first dexamethasone implant was a mean of 8.2 months (3-27 months). The scleritis was well controlled in all eyes until at least 2 months (2-5 months) after inserting the implant. An average of 2.1 (total of 15 times in the seven eyes) implants were inserted. No complications related to the implant were observed other than a temporary increase in intraocular pressure in one eye.
Ļ│Ąļ¦ēņŚ╝ņØĆ Ļ│Ąļ¦ēņØä ņ╣©ļ▓öĒĢśļŖö ņŚ╝ņ”Øņ¦łĒÖśņØ┤ļŗż. ĒåĄņ”ØĻ│╝ ņČ®Ēśł, Ļ▓░ļ¦ēļČĆņóģņØä ļÅÖļ░śĒĢśļ®░, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņŚÉņä£ Ļ│Ąļ¦ēĒśłĻ┤ĆņØś ĒÖĢņןĻ│╝ Ļ│Ąļ¦ēļČĆņóģņØ┤ Ļ┤Ćņ░░ļÉĀ ļĢī ņØśņŗ¼ĒĢĀ ņłś ņ׳ļŗż. Ļ│Ąļ¦ēņŚ╝ņØĆ ņøÉņØĖņŚÉ ļö░ļØ╝ Ļ░ÉņŚ╝ņä▒Ļ│╝ ļ╣äĻ░ÉņŚ╝ņä▒ņØĆ ļŗżņŗ£ ņĀäņŗĀņ¦łĒÖśĻ│╝ ņŚ░Ļ┤ĆļÉśņ¢┤ ļéśĒāĆļéśļŖö Ļ▓ĮņÜ░ņÖĆ ņĀäņŗĀņ¦łĒÖśĻ│╝ņØś ņŚ░Ļ┤Ćņä▒ņØä ņ░Šņ¦Ć ļ¬╗ĒĢśļŖö Ļ▓ĮņÜ░ļĪ£ ļéśļłī ņłś ņ׳ļŗż. ļśÉĒĢ£ ņ╣©ļ▓öļÉ£ Ļ│Ąļ¦ēņØś ļ▓öņ£äņŚÉ ļö░ļØ╝ ņĀäļČĆĻ│Ąļ¦ēņŚ╝, ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņ£╝ļĪ£ ĻĄ¼ļČäĒĢĀ ņłś ņ׳ļŗż[1]. ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØĆ ļ¦źļØĮļ¦ēņŻ╝ļ”ä, ņŗ£ņŗĀĻ▓ĮļČĆņóģ, ļ¦źļØĮļ¦ēņé╝ņČ£, ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼ ļō▒ņØ┤ Ļ┤Ćņ░░ļÉśļ®░, ņĀäņ▓┤ Ļ│Ąļ¦ēņŚ╝ ņżæ ļé«ņØĆ ļ╣äņ£©ņØä ņ░©ņ¦ĆĒĢ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśņŚłļŗż[2,3]. ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØĆ ĒÖ®ļ░śņ╣©ļ▓öņØ┤ ĒØöĒĢśņŚ¼ ņżæņŗ¼ ņŗ£ļĀźņĀĆĒĢś ņ£äĒŚśņØ┤ ļåÆĻ│Ā, ņĀÉņĢłņĢĮļ¦īņ£╝ļĪ£ļŖö ņĪ░ņĀłļÉśņ¦Ć ņĢŖļŖöļŗż[3]. ņĀäņŗĀ ņŖżĒģīļĪ£ņØ┤ļō£ ļ░Å ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ĒżĒĢ©ĒĢ£ ņןĻĖ░Ļ░ä ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢ£ Ļ▓ĮņÜ░Ļ░Ć ļ¦ÄņĢä[3], ĒĢ®ļ│æņ”ØĻ│╝ ņ╣śļŻī ĒÜ©ļŖź ņé¼ņØ┤ņØś ĻĘĀĒśĢņØ┤ ņżæņÜöĒĢśļŗż[4].
ļ╣äĻ░ÉņŚ╝ņä▒ Ļ│Ąļ¦ēņŚ╝ņØ┤ ĒøäĻĘ╣ļČĆļź╝ ņ╣©ļ▓öĒĢ£ Ļ▓ĮņÜ░ļŖö ņĀäņŗĀ ņŖżĒģīļĪ£ņØ┤ļō£ņÖĆ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£Ļ░Ć 1ņ░© ņäĀĒāØ ņĢĮņĀ£ņØ┤ļŗż. ĒĢśņ¦Ćļ¦ī ņ×¼ļ░£ Ēś╣ņØĆ ņĢĮņĀ£ ļČĆņ×æņÜ®ņ£╝ļĪ£ 1ņ░© ņĢĮņĀ£ļ¦īņ£╝ļĪ£ ņĪ░ņĀłņØ┤ ņ¢┤ļĀżņÜ┤ Ļ▓ĮņÜ░Ļ░Ć ļ¦Äļŗż. ņĀĆņ×ÉļōżņØĆ ļé£ņ╣śņä▒ ņ”ØļĪĆļōżņŚÉņä£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ 0.7 mg (Ozurdex┬«; Allergan, Irvine, CA, USA)ņØä ņé¼ņÜ®ĒĢśņśĆĻ│Ā, ņÜ░ņłśĒĢ£ Ļ▓ĮĻ│╝ļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. 1ņ░© ņĢĮņĀ£ļĪ£ ņĪ░ņĀłļÉśņ¦Ć ņĢŖļŖö ļ╣äĻ░ÉņŚ╝ņä▒ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņŚÉņä£ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļź╝ ņ╣śļŻī ļīĆņĢłņ£╝ļĪ£ ņĀ£ņĢłĒĢśĻ│Āņ×É ĒĢ£ļŗż.
2013ļģä 1ņøöļČĆĒä░ 2020ļģä 1ņøöĻ╣īņ¦Ć ļ│ĖņøÉ ņĢłĻ│╝ņŚÉņä£ ļ╣äĻ░ÉņŚ╝ņä▒ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ ĒÖśņ×Éļōż ņżæ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņé¼ļź╝ Ēł¼ņŚ¼ ļ░øņØĆ ĒÖśņ×ÉļōżņØś ņØśļ¼┤ĻĖ░ļĪØņØä ĒøäĒ¢źņĀüņ£╝ļĪ£ ļČäņäØĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĒŚ¼ņŗ▒ĒéżņäĀņ¢Ė(Declaration of Helsinki)ņØä ņżĆņłśĒĢśņŚ¼ ļ│ĖņøÉņØś ņ×äņāüņŚ░ĻĄ¼ņ£żļ”¼ņŗ¼ņØśņ£äņøÉĒÜī(Institutional Review Board, IRB)ņØś ņŖ╣ņØĖ(ņŖ╣ņØĖ ļ▓łĒśĖ:2003-005-088)ņØä ļ░øņĢśļŗż.
ļ¼Ėņ¦äņØä ĒåĄĒĢ┤ ĒåĄņ”ØņØä ĒÖĢņØĖĒĢśņśĆĻ│Ā, ņäĖĻĘ╣ļō▒Ļ▓Ćņé¼ņŚÉņä£ Ļ▓░ļ¦ē ņČ®Ēśł ļ░Å ļČĆņóģ, Ļ│Ąļ¦ē ĒśłĻ┤ĆņØś ĒÖĢņןĻ│╝ ļČĆņóģņØä Ļ┤Ćņ░░ĒĢśņŚ¼ Ļ│Ąļ¦ēņŚ╝ņØä ņ¦äļŗ©ĒĢśņśĆļŗż. ņĢłņ┤łņØīĒīīĻ▓Ćņé¼ņŚÉņä£ T-signņØ┤ Ļ┤Ćņ░░ļÉśļŖö Ļ▓ĮņÜ░ ĒøäļČĆļź╝ ņ╣©ļ▓öĒĢ£ Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ĒĢśņŚ¼ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņ£╝ļĪ£ ņ¦äļŗ©ĒĢśņśĆļŗż. Ļ░£ĒÜīņČ®, ĒåĪņåīĒöīļØ╝ņ”łļ¦ł, ļ¦żļÅģ, Ļ▓░ĒĢĄ ļō▒ņØĆ ĒśłņĢĪĻ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ĒÖĢņØĖĒĢśņśĆĻ│Ā, ņŖżĒģīļĪ£ņØ┤ļō£ņŚÉ ļīĆĒĢ£ ļ░śņØæ ļ░Å ļ│æņØś ņ¦äĒ¢ē ņ¢æņāüņŚÉ ĻĘ╝Ļ▒░ĒĢśņŚ¼ ļ╣äĻ░ÉņŚ╝ņä▒ņ£╝ļĪ£ ĒīÉļŗ©ĒĢśņśĆļŗż. ņĢłņĀĆĻ▓Ćņé¼ ļ░Å ĒśĢĻ┤æņĢłņĀĆĒśłĻ┤ĆņĪ░ņśüņŚÉņä£ ļ¦Øļ¦ēņŚ╝ Ēś╣ņØĆ ļ¦Øļ¦ēĒśłĻ┤ĆņŚ╝ņØ┤ Ļ┤Ćņ░░ļÉśļŖö Ļ▓ĮņÜ░ļŖö ņĀ£ņÖĖĒĢśņśĆļŗż. ņ╣śļŻī Ēøä Ļ│Ąļ¦ēņŚ╝ņØś ņ×¼ļ░£ņØĆ ĒåĄņ”Ø, ņäĖĻĘ╣ļō▒Ļ▓Ćņé¼, ņĢłņĀĆĻ▓Ćņé¼, ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(DRI OCT Triton; Topcon Medical Systems, Tokyo, Japan)ņ£╝ļĪ£ ĒÅēĻ░ĆļÉśņŚłļŗż.
ļéśņØ┤, ņä▒ļ│ä, ņ¦łļ│æņØś ļ░£ņāØ ņŗ£ņĀÉ, ņ┤łĻĖ░ ņ”Øņāü, Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä, ņĀäņŗĀņ¦łĒÖśĻ│╝ņØś ņŚ░Ļ┤Ćņä▒ ļō▒ņØä ĒżĒĢ©ĒĢ£ ĒÖśņ×ÉņØś ļ│æļĀźņØä ļČäņäØĒĢśņśĆļŗż. ņé¼ņÜ®ļÉ£ ņŖżĒģīļĪ£ņØ┤ļō£ņÖĆ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ņØś ņóģļźśņÖĆ ņÜ®ļ¤ē, ĒĢ®ļ│æņ”Ø ļ░£ņāØ ņŚ¼ļČĆļź╝ ļČäņäØĒĢśņśĆļŗż. ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģ Ēøä ņ×¼ļ░£ ņŚåņØ┤ ņ£Āņ¦ĆļÉśļŖö ĻĖ░Ļ░äĻ│╝ ņ×äĒöīļ×ĆĒŖĖ Ēł¼ņŚ¼ Ēܤņłśļź╝ ļČäņäØĒĢśņśĆĻ│Ā, ņ╣śļŻī ņĀä ĒøäņØś ņŗ£ļĀźļ│ĆĒÖöļź╝ logarithm of the minimum angle of resolution (logMAR) ņŗ£ļĀźņ£╝ļĪ£ ļ│ĆĒÖśĒĢśņŚ¼ ļČäņäØĒĢśņśĆļŗż. ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖņÖĆ Ļ┤ĆļĀ©ĒĢ£ ņĢłņĢĢņāüņŖ╣Ļ│╝ ļ░▒ļé┤ņן ļ░£ņāØņŚÉ ļīĆĒĢ┤ ļČäņäØĒĢśņśĆļŗż.
ĒøäļČĆļź╝ ņ╣©ļ▓öĒĢ£ Ļ│Ąļ¦ēņŚ╝ņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ Ēøä ņ┤łĻĖ░ ņ╣śļŻīļĪ£ Ibuprofen 400 mg 3ĒÜī/ņØ╝ ļ░Å kgļŗ╣ 1 mgņØś Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ļź╝ ļ│ĄņÜ®ĒĢśņśĆĻ│Ā, ņØ┤Ēøä Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ļź╝ ņ▓£ņ▓£Ē׳ Ļ░Éļ¤ēĒĢśņśĆļŗż. ņĪ░ņĀłņØ┤ ņČ®ļČäĒĢśņ¦Ć ņĢŖļŗżĻ│Ā ĒīÉļŗ©ļÉśļŖö Ļ▓ĮņÜ░ ļ®öĒåĀĒŖĖļĀēņäĖņØ┤ĒŖĖ 7.5-10 mg/ņŻ╝, Ēś╣ņØĆ ņé¼ņØ┤Ēü┤ļĪ£ņŖżĒżļ”░ 200 mg/ņØ╝ņØä ņČöĻ░ĆĒĢśņśĆļŗż. ņĀäņŗĀ ņŖżĒģīļĪ£ņØ┤ļō£ņÖĆ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ ņ╣śļŻīņŚÉļÅä Ļ│Ąļ¦ēņŚ╝ņØ┤ ĒśĖņĀäļÉśņ¦Ć ņĢŖĻ▒░ļéś ĒĢ®ļ│æņ”ØņØ┤ ļ░£ņāØĒĢśņŚ¼ ņ╣śļŻīĻ░Ć ņ¢┤ļĀżņÜ┤ Ļ▓ĮņÜ░, ņĀäņŗĀ ņŖżĒģīļĪ£ņØ┤ļō£ ļ░Å ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ Ļ▓ĮĻ░É ņ╣śļŻī ņżæ ņ×¼ļ░£ĒĢśļŖö Ļ▓ĮņÜ░ņŚÉ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż.
ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņé¼ļŖö ĒżļÅäļ¦ēņŚ╝ ņ╣śļŻīņŚÉ ņżĆĒĢśņŚ¼ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņĀÉņĢłļ¦łņĘ© Ēøä 5% povidone iodineņ£╝ļĪ£ ļłł ņŻ╝ņ£äņÖĆ Ļ▓░ļ¦ēļéŁņØä ņåīļÅģĒĢśĻ│Ā Ļ░£Ļ▓ĆĻĖ░ļĪ£ ņĢłĻ▓ĆņØä ļ▓īļ”░ Ēøä ņĢĮļ¼╝ņØ┤ Ēāæņ×¼ļÉ£ 22Ļ▓īņØ┤ņ¦Ć ņŻ╝ņ×ģĻĖ░ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņłśņĀĢņ▓┤ ņĢłņŚÉņä£ļŖö Ļ░üļ¦ēņ£żļČĆļĪ£ļČĆĒä░ 4 mm, ņØĖĻ│ĄņłśņĀĢņ▓┤ ņĢłņŚÉņä£ļŖö 3 mm ļ¢©ņ¢┤ņ¦ä ņāüņØ┤ņĖĪ ļČĆņ£ä ņä¼ļ¬©ņ▓┤ ĒÅēļ®┤ļČĆļĪ£ ņéĮņ×ģĒĢśņśĆļŗż. Ļ│Ąļ¦ēņŚ╝ņ£╝ļĪ£ ņØĖĒĢ£ ļ░£ņĀüņØ┤ļéś Ļ│Ąļ¦ē ņ¢ćņĢäņ¦ÉņØ┤ ļ│┤ņØ┤ļŖö Ļ││ņØĆ Ēö╝ĒĢśņŚ¼ ņŻ╝ņ×ģĒĢśņśĆļŗż.
5ļ¬ģ 7ņĢł(ļé©ņä▒ 1ļ¬ģ, ņŚ¼ņä▒ 4ļ¬ģ)ņØ┤ ĒżĒĢ©ļÉśņŚłĻ│Ā, ĒÅēĻĘĀ ļéśņØ┤ļŖö 73.2ņäĖ(59-92ņäĖ)ņśĆļŗż. 1ļ¬ģņØĆ ļźśļ¦łĒŗ░ņŖż Ļ┤ĆņĀłņŚ╝ņØ┤ ņ¦äļŗ©ļÉśņŚłĻ│Ā, 4ļ¬ģņØĆ Ļ│Ąļ¦ēņŚ╝Ļ│╝ Ļ┤ĆļĀ©ļÉ£ ņĀäņŗĀņ¦łĒÖśņØ┤ ĒÖĢņØĖļÉśņ¦Ć ņĢŖņĢśļŗż. 3ļ¬ģņØĆ ņ¢æņĢłņŚÉ Ļ│Ąļ¦ēņŚ╝ņØ┤ ļ░£ņāØĒĢśņśĆĻ│Ā, 2ļ¬ģņØĆ ļŗ©ņĢłņŚÉ ļ░£ņāØĒĢśņśĆļŗż. ņ¢æņĢłņŚÉ Ļ│Ąļ¦ēņŚ╝ņØ┤ ļ░£ņāØĒĢ£ 3ļ¬ģ ņżæ 2ļ¬ģņØĆ ņ¢æņĢł ļ¬©ļæÉ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņé¼ļĪ£ ņ╣śļŻīĒĢśņśĆĻ│Ā, 1ļ¬ģņØĆ ņŗ£ļĀźņØ┤ ņóŗņØĆ ņóīņĢłņŚÉļ¦ī ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļź╝ ņé¼ņÜ®ĒĢśņśĆĻĖ░ņŚÉ ņóīņĢłņØ┤ ļīĆņāüņŚÉ ĒżĒĢ©ļÉśņŚłļŗż.
5ļ¬ģ 7ņĢł ļ¬©ļæÉ ņ▓½ ļé┤ņøÉņŚÉņä£ ņČ®Ēśł ļ░Å ĒåĄņ”ØņØä ĒśĖņåīĒĢśņśĆļŗż. 7ņĢł ņżæ 4ņĢłņŚÉņä£ ņĀäļ░® ņŚ╝ņ”Ø ņäĖĒżĻ░Ć ĒÖĢņØĖļÉśņŚłļŗż. 1ņĢłņØĆ +3, 3ņĢłņØĆ +1ņØś ņŚ╝ņ”Ø ņäĖĒżĻ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż. 7ņĢł ļ¬©ļæÉ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü ļ░Å ņĢłņĀĆĻ▓Ćņé¼ņŚÉņä£ ļ¦źļØĮļ¦ēņŻ╝ļ”äņØ┤ ĒÖĢņØĖļÉśņŚłļŗż. Ļ▓ĮĒĢ£ ņ£Āļ”¼ņ▓┤ ĒØÉļ”╝ņØ┤ 2ņĢłņŚÉņä£ Ļ┤Ćņ░░ļÉśņŚłļŗż. ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ Ēł¼ņŚ¼ ņĀä Ļ▓ĮĻĄ¼ ņĀ£ņĀ£ļ¦īņ£╝ļĪ£ ņ╣śļŻīĒ¢łļŹś ĒÅēĻĘĀ 8.2Ļ░£ņøö(3-27Ļ░£ņøö) ļÅÖņĢł, ĒÅēĻĘĀ 2.25ĒÜī ņ×¼ļ░£ĒĢśņśĆļŗż. 4ļ¬ģ(80%)ņŚÉņä£ ņĢĮņĀ£ ļČĆņ×æņÜ®ņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Table 1).
ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņłĀņØĆ ĒÅēĻĘĀ 2.1ĒÜī(2-3ĒÜī, ņ┤Ø 15ĒÜī) ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, Ēł¼ņŚ¼ ņĀä ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ĒÅēĻĘĀ logMAR 0.75 ┬▒ 0.47 (0.4-1.4), ļ¦łņ¦Ćļ¦ē ļ░®ļ¼ĖņŚÉņä£ ņĖĪņĀĢĒĢ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ĒÅēĻĘĀ LogMAR 0.38 ┬▒ 0.35 (0-1.2)ņśĆļŗż. ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņłĀ Ēøä 7ņĢł ļ¬©ļæÉņŚÉņä£ ņ×¼ļ░£ņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤, ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļź╝ ņ×¼ņŻ╝ņ×ģĒĢśņśĆļŗż. ņ▓½ ņŻ╝ņ×ģ Ēøä ņ×¼ļ░£ņØ┤ Ļ┤Ćņ░░ļÉśĻĖ░Ļ╣īņ¦ĆņØś ĒÅēĻĘĀ ĻĖ░Ļ░äņØĆ 3.4Ļ░£ņøö(2-5Ļ░£ņøö)ņØ┤ņŚłļŗż(Table 2). 7ņĢłņŚÉņä£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņ▓½ Ēł¼ņŚ¼ Ēøä ĒÅēĻĘĀ 18.4Ļ░£ņøö(5-42Ļ░£ņøö), ļ¦łņ¦Ćļ¦ē ņŻ╝ņé¼ Ēøä ĒÅēĻĘĀ 12Ļ░£ņøö(2-38Ļ░£ņøö)ņØä Ļ┤Ćņ░░ ņżæņØ┤Ļ│Ā, 7ņĢł ļ¬©ļæÉņŚÉņä£ Ļ▓ĮĻĄ¼ņĀ£ņĀ£ ņŚåņØ┤ ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśĻ│Ā ņ׳ļŗż. ņĀäņ▓┤ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØĆ ĒÅēĻĘĀ 31.5Ļ░£ņøöņØ┤ņŚłļŗż(7-68Ļ░£ņøö).
1ņĢłņŚÉņä£ ņ▓½ ņŻ╝ņ×ģ Ēøä ņØ╝ņŗ£ņĀü ņĢłņĢĢņāüņŖ╣ņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤ ņĢłņĢĢĒĢśĻ░ĢņĀ£ļĪ£ ņĪ░ņĀłĒĢśņśĆļŗż. ņØ┤Ēøä ņČöĻ░Ć ņŻ╝ņé¼ņŚÉņä£ļŖö ņĢłņĢĢņāüņŖ╣ņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. 7ņĢł ņżæ 3ņĢłņØĆ ļ░▒ļé┤ņןņłśņłĀņØ┤ ņŗ£Ē¢ēļÉ£ ņāüĒā£ņśĆĻ│Ā, ļéśļ©Ėņ¦Ć 4ņĢł ņżæ 3ņĢłņØĆ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģ Ēøä ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, 1ņĢłņØĆ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ņżæ ņØśļ»Ė ņ׳ļŖö ļ░▒ļé┤ņן ļ│ĆĒÖöĻ░Ć ĒÖĢņØĖļÉśņ¦Ć ņĢŖņĢśļŗż.
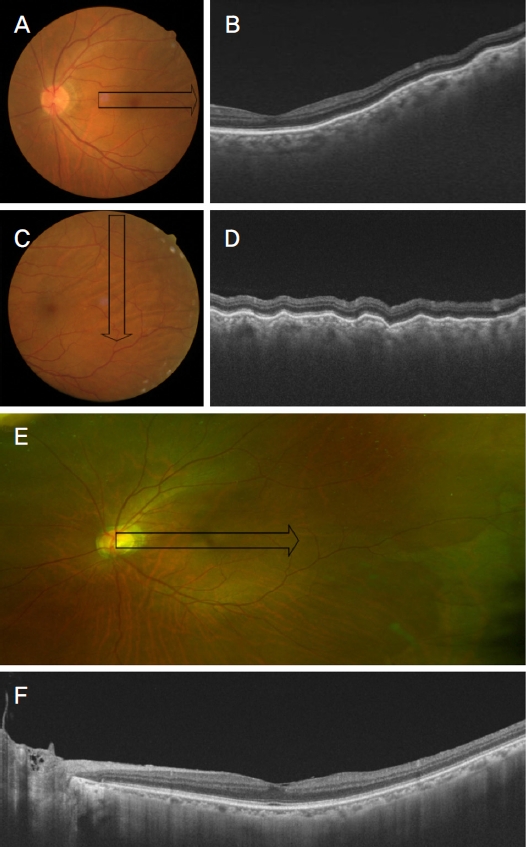
Ļ░äļÅģņä▒, ļ╣łĒśł, Ēśłļŗ╣ņĪ░ņĀł ņןņĢĀ ļō▒ņ£╝ļĪ£ ņČ®ļČäĒĢ£ ņÜ®ļ¤ēņØś ņĢĮņĀ£ ņé¼ņÜ®ņØ┤ ņ¢┤ļĀżņøī, Ļ│Ąļ¦ēņŚ╝ņØ┤ ņĪ░ņĀłļÉśņ¦Ć ņĢŖņĢśļŗż(Fig. 1). ļ░£ļ│æ 4Ļ░£ņøö Ēøä ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļź╝ ņéĮņ×ģĒĢśņśĆĻ│Ā Ļ│Ąļ¦ēņŚ╝ņØĆ ņĪ░ņĀłļÉśņŚłļŗż. 4Ļ░£ņøö Ēøä ņ×¼ļ░£ĒĢśņŚ¼ 2ļ▓łņ¦Ė ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņØ┤Ēøä 4ļģäĻ░ä ņ×¼ļ░£ ņåīĻ▓¼ņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż.
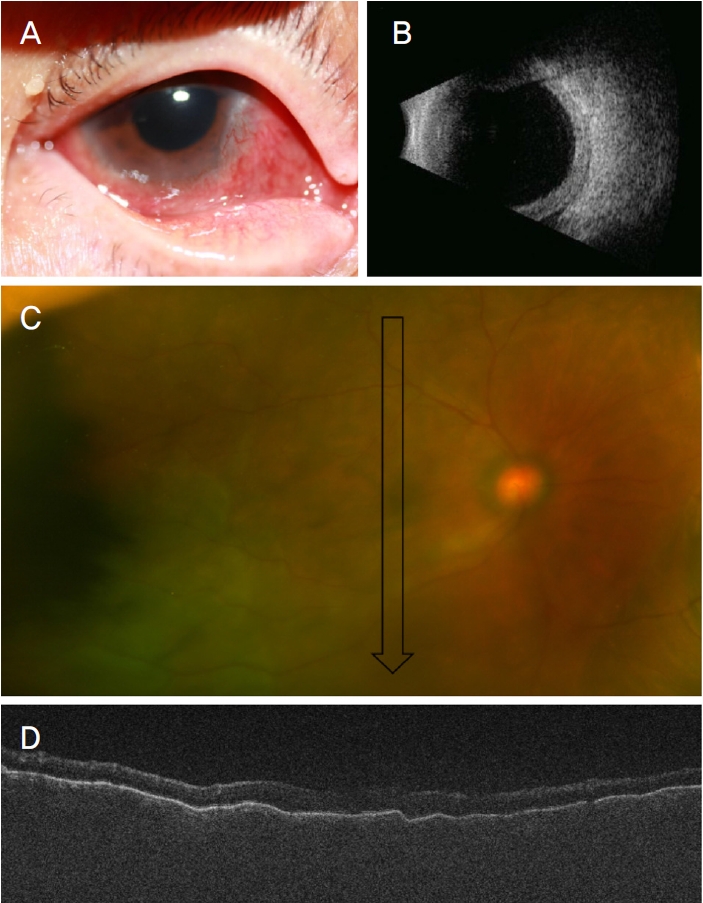
ĒāĆļ│æņøÉņŚÉņä£ Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ ļ░Å ņé¼ņØ┤Ēü┤ļĪ£ņŖżĒżļ”░ ņĀ£ņĀ£ļĪ£ ņĪ░ņĀłļÉśņ¦Ć ņĢŖņĢä ņĀäņøÉļÉ£ ĒÖśņ×ÉņśĆļŗż. ņ┤łĻĖ░ Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ ņé¼ņÜ®ņ£╝ļĪ£ Ļ│Ąļ¦ēņŚ╝ņØĆ ņĪ░ņĀłļÉśņŚłņ£╝ļéś ņ┐Āņŗ▒ņ”ØĒøäĻĄ░Ļ│╝ ļ╣łĒśłņØ┤ ļÅÖļ░śļÉśņ¢┤, ņŖżĒģīļĪ£ņØ┤ļō£ Ļ░Éļ¤ē Ēøä ņ£Āņ¦Ć ņÜ®ļ¤ēņŚÉņä£ ņ×¼ļ░£ĒĢśņśĆļŗż. ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļź╝ ņéĮņ×ģĒĢśņśĆĻ│Ā ĒĢ£ ļŗ¼ ļÆż ļ¦źļØĮļ¦ēņŻ╝ļ”ä ņåīņŗżņØ┤ ĒÖĢņØĖļÉśņŚłļŗż(Fig. 2). ņ▓½ ņŻ╝ņé¼ 5Ļ░£ņøö ļÆż ļ¦źļØĮļ¦ēņŻ╝ļ”äņØ┤ ņĢģĒÖöļÉśļŖö ņ¢æņāüņØ┤ ļ│┤ņŚ¼ ļæÉ ļ▓łņ¦Ė ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ļæÉ ļ▓łņ¦Ė ņŻ╝ņé¼ Ēøä ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØĆ ņĪ░ņĀłļÉśņŚłĻ│Ā, ņØ┤Ēøä 18Ļ░£ņøö ļÅÖņĢł Ļ│Ąļ¦ēņŚ╝ Ļ┤ĆļĀ© ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņĢśĻ│Ā, ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśņŚłļŗż.
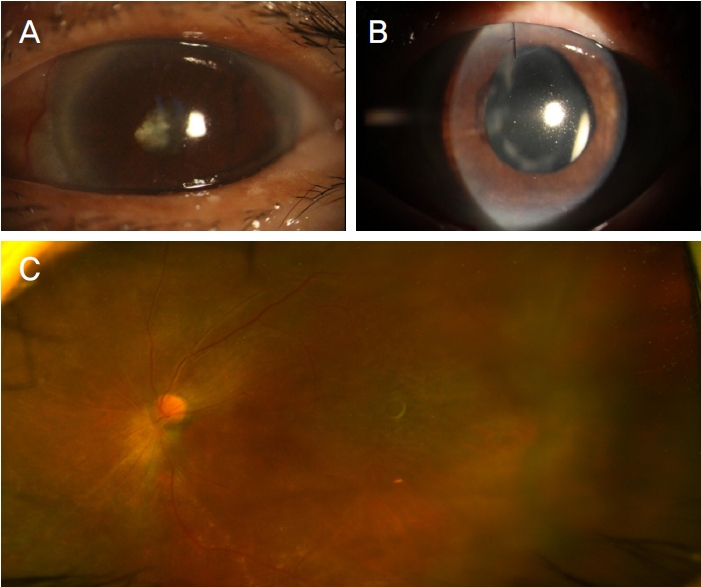
ņ£äņןĻ┤Ć ņןņĢĀļĪ£ ļ¬©ļōĀ ņóģļźśņØś Ļ▓ĮĻĄ¼ ņĢĮņĀ£ ļ│ĄņÜ®ņŚÉ ņ¢┤ļĀżņøĆņØä ĒśĖņåīĒĢśņśĆļŗż. ņ¢æņĢł Ļ│Ąļ¦ēņŚ╝ņØ┤ ņĪ░ņĀłļÉśņ¦Ć ņĢŖĻ│Ā, ņØ┤Ēøä ņÜ░ņĢł ļ¦Øļ¦ē ļ░Ģļ”¼Ļ░Ć ļ░£ņāØĒĢśņŚ¼ Ļ│Ąļ¦ēļæÉļź┤ĻĖ░, ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀ, ņŗżļ”¼ņĮś ĻĖ░ļ”ä ņŻ╝ņ×ģņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņóīņĢłļÅä Ļ│Ąļ¦ēņŚ╝ņØ┤ ņĪ░ņĀłļÉśņ¦Ć ņĢŖņĢä ņóīņĢł ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖņŻ╝ņ×ģņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, Ļ│Ąļ¦ēņŚ╝ ņĪ░ņĀłņØä ĒÖĢņØĖĒĢ£ Ēøä ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż(Fig. 3). 40Ļ░£ņøö ļÅÖņĢł ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ 3ĒÜī ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ▓½ ņŻ╝ņé¼ 40Ļ░£ņøö Ēøä ļćīĒśłĻ┤Ćņ¦łĒÖśņ£╝ļĪ£ ņé¼ļ¦ØĒĢśņśĆļŗż.
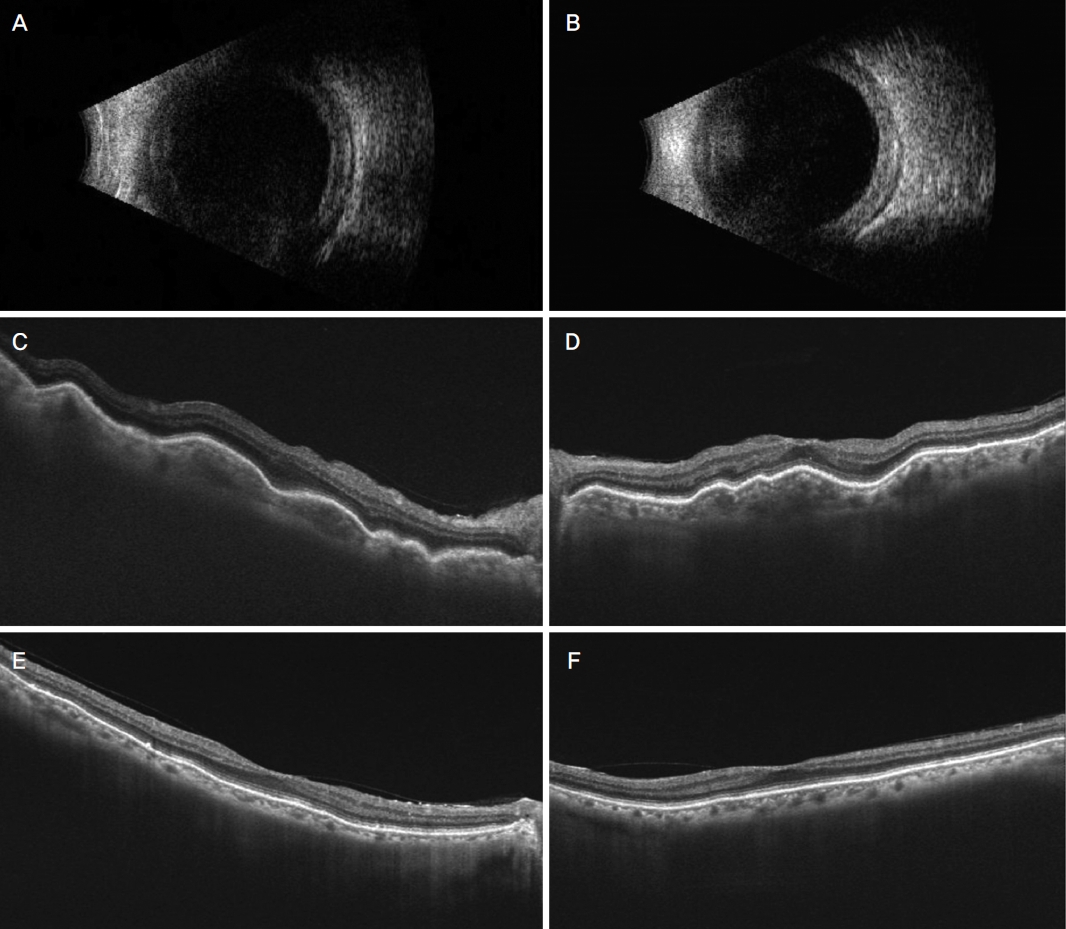
ņ£Āņ¦Ć ņÜ®ļ¤ēņŚÉņä£ ņ×¼ļ░£ĒĢśņŚ¼ ņĢĮņĀ£ Ļ░Éļ¤ēņØ┤ ņ¢┤ļĀżņøĀĻ│Ā, ņ┐Āņŗ▒ņ”ØĒøäĻĄ░ ņØśņŗ¼ ņåīĻ▓¼ņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż. ņ¢æņĢł ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņ×ģ Ēøä ņ¢æņĢł ļ¬©ļæÉ ĒśĖņĀäļÉśņŚłļŗż. 2.5Ļ░£ņøö Ēøä ņ¢æņĢł ļ¬©ļæÉ ņ×¼ļ░£ ņåīĻ▓¼ņØ┤ ļ│┤ņŚ¼ ļæÉ ļ▓łņ¦Ė ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā ņŻ╝ņé¼ Ēøä 5Ļ░£ņøö ĒøäĻ╣īņ¦Ć ņČöĻ░Ć ņĢĮņĀ£ ņŚåņØ┤ ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśņŚłļŗż(Fig. 4).
ļźśļ¦łĒŗ░ņŖż Ļ┤ĆņĀłņŚ╝ņØä ļÅÖļ░śĒĢ£ ņ¢æņĢł ĒøäļČĆĻ│Ąļ¦ēņŚ╝ ĒÖśņ×ÉņśĆļŗż. Ļ│ĀņÜ®ļ¤ē ļŗ©ĻĖ░ ļČĆņŗĀĒö╝ņ¦łĒśĖļź┤ļ¬¼ ņé¼ņÜ® Ēøä ņĪ░ņĀłļÉśņŚłņ£╝ļéś ņ£Āņ¦Ć ņÜ®ļ¤ēņŚÉņä£ļŖö ņ×¼ļ░£ĒĢśņśĆļŗż(Fig. 5). ņóīņĢł ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ĒÜ©Ļ│╝Ļ░Ć ņÜ░ņłśĒĢśņŚ¼ 6ņŻ╝ Ēøä ņÜ░ņĢłļÅä ņŻ╝ņé¼ĒĢśņśĆļŗż. ņ¢æņĢł ļ¬©ļæÉ ņ▓½ ņŻ╝ņé¼ 3Ļ░£ņøö ĒøäņŚÉ ļæÉ ļ▓łņ¦Ė ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ļæÉ ļ▓łņ¦Ė ņŻ╝ņé¼ Ēøä 2Ļ░£ņøöĻ╣īņ¦Ć Ļ│Ąļ¦ēņŚ╝ņØĆ ņĪ░ņĀłļÉśņ¢┤ ņĢłņĀĢĒÖöļÉ£ ņāüĒā£ļĪ£ ņ£Āņ¦ĆļÉśĻ│Ā ņ׳ļŗż.
ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņéĮņ×ģļ¼╝ņØĆ ņłśņÜ®ņä▒ ļČĆņŗĀĒö╝ņ¦łĒśĖļź┤ļ¬¼ņØĖ ļŹ▒ņé¼ļ®öĒāĆņåÉņØä ņĀĆņÜ®ļ¤ēņ£╝ļĪ£ ņłśĻ░£ņøö ļÅÖņĢł ņä£ņä£Ē׳ ļ░®ņČ£ĒĢśļŖö ņāØļČäĒĢ┤ņä▒ ņéĮņ×ģļ¼╝ļĪ£, ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒŖĖļ”¼ņĢöņŗ£ļåĆļĪĀņŚÉ ļ╣äĒĢ┤ ļŹö ņśżļ×£ ĻĖ░Ļ░ä ņ×æņÜ®ĒĢ£ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż[5]. ļŹ▒ņé¼ļ®öĒāĆņåÉņØĆ Ļ░ĢļĀźĒĢ£ ĒĢŁņŚ╝ņ”Ø ĒÜ©Ļ│╝ļź╝ Ļ░Ćņ¦ĆĻ│Ā ņ׳ņ¢┤ ļ╣äĻ░ÉņŚ╝ņä▒ ņżæĻ░äĒżļÅäļ¦ēņŚ╝, ĒøäļČĆĒżļÅäļ¦ēņŚ╝ņØś ņ╣śļŻīņĀ£ļĪ£ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż. ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņłĀņØĆ ĻĄŁņåīņĀüņ£╝ļĪ£ ņŖżĒģīļĪ£ņØ┤ļō£ ļåŹļÅäļź╝ ļåÆĻ▓ī ņ£Āņ¦ĆĒĢĀ ņłś ņ׳ņ¢┤ ņŖżĒģīļĪ£ņØ┤ļō£ļź╝ ĒżĒĢ©ĒĢ£ ĒĢŁņŚ╝ņ”ØņĀ£ņØś ņĀäņŗĀ ņé¼ņÜ® ņÜ®ļ¤ēņØä ņżäņØ╝ ņłś ņ׳ņ£╝ļ®░, ņĢĮĒÜ©ļŖö ņĄ£ļīĆ 6Ļ░£ņøö ņ¦ĆņåŹļÉĀ ņłś ņ׳ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż[6].
ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØś ņ╣śļŻīļŖö ĒøäļČĆĒżļÅäļ¦ēņŚ╝Ļ│╝ Ēü¼Ļ▓ī ļŗżļź┤ņ¦Ć ņĢŖņĢä ĒøäļČĆĒżļÅäļ¦ēņŚ╝ņŚÉ ĒÜ©Ļ│╝ņĀüņØĖ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņłĀņØ┤ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņŚÉļÅä ĒÜ©Ļ│╝ņĀüņØ╝ Ļ▓āņØ┤ļØ╝ ņśłņāüĒĢĀ ņłś ņ׳ļŗż. ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņŚÉņä£ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņ×ģņŚÉ Ļ┤ĆĒĢ£ ļ¼ĖĒŚīņØĆ Dubey et al [7]ņØś ņ”ØļĪĆ ļ│┤Ļ│ĀĻ░Ć ņ£ĀņØ╝ĒĢśļŗż. ĒøäļČĆĻ│Ąļ¦ēņŚ╝ ņ╣śļŻīļź╝ ņ£äĒĢ┤ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ņé¼ņÜ®ĒĢśņśĆņ£╝ļéś, ĒÅÉņŚÉ ĻĖ░ĒÜī Ļ░ÉņŚ╝ņØ┤ ļ░£ņāØĒĢśņŚ¼ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņéĮņ×ģņłĀņØä ņŗ£Ē¢ēĒĢ£ Ēøä ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØ┤ ņä▒Ļ│ĄņĀüņ£╝ļĪ£ ņĪ░ņĀłļÉśņŚłļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.
ļŹ▒ņé¼ļ®öĒāĆņåÉ ņéĮņ×ģņØś ļīĆĒæ£ņĀü ļČĆņ×æņÜ®ņØĆ ļ░▒ļé┤ņןĻ│╝ ņĢłņĢĢņāüņŖ╣ņØ┤ļŗż[5]. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņŻ╝ņé¼ņÖĆ Ļ┤ĆļĀ©ĒĢśņŚ¼ 15ĒÜī ņŻ╝ņé¼ ņżæ 1ĒÜīņŚÉņä£ ņØ╝ņŗ£ņĀü ņĢłņĢĢņāüņŖ╣ņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤ ņĢłņĢĢĒĢśĻ░ĢņĀ£ļź╝ ņØ╝ņŗ£ņĀüņ£╝ļĪ£ ņé¼ņÜ®ĒĢśņśĆĻ│Ā, Ļ░ÖņØĆ ļłłņØś 2ņ░© ņŻ╝ņé¼ ĒøäņŚÉļŖö ņĢłņĢĢņāüņŖ╣ņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ļÉ£ ĒÖśņ×ÉļōżņØĆ Ļ│ĀļĀ╣ņØ┤ņ¢┤ņä£ ļ░▒ļé┤ņן ņ£Āļ░£ņØĆ ņżæņÜöĒĢ£ ĒĢ®ļ│æņ”Øņ£╝ļĪ£ Ļ│ĀļĀżļÉśņ¦ĆļŖö ņĢŖņĢśļŗż. ļ░▒ļé┤ņןņłśņłĀņØ┤ ņŗ£Ē¢ēļÉśņ¦Ć ņĢŖņØĆ 4ņĢł ņżæ 3ņĢłņŚÉņä£ļŖö ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņĀäļČĆĒä░ ņāüļŗ╣ĒĢ£ ļ░▒ļé┤ņן ļ│ĆĒÖöĻ░Ć Ļ┤Ćņ░░ļÉśņ¢┤ ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ļéśļ©Ėņ¦Ć 1ņĢłņØĆ ņØśļ»Ė ņ׳ļŖö ļ░▒ļé┤ņן ņ¦äĒ¢ēņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż.
ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØĆ ņĢłņĀĆĻ▓Ćņé¼ ļ░Å ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ļ¦źļØĮļ¦ēņŻ╝ļ”äņØ┤ Ļ┤Ćņ░░ļÉśļŖö Ļ▓āņØ┤ ĒŖ╣ņ¦ĢņĀüņØ┤ļ®░, ņĢłņ┤łņØīĒīīņŚÉņä£ T-signņØä ļ│┤ņØ╝ ļĢī ņ¦äļŗ©ĒĢĀ ņłś ņ׳ļŗż[2,3]. ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ļÉ£ 5ļ¬ģ 7ņĢłņŚÉņä£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ļÜ£ļĀĘĒĢ£ ļ¦źļØĮļ¦ēņŻ╝ļ”äņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłĻ│Ā, ņĀüņĀłĒĢ£ ņ╣śļŻī ĒøäņŚÉļŖö ļ¦źļØĮļ¦ēņŻ╝ļ”äņØ┤ ņåīņŗżļÉśļŖö Ļ▓āņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. ņĢłņ┤łņØīĒīīļŖö ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØś ņ¦äļŗ©ņŚÉļŖö ņ£ĀņÜ®ĒĢśņ¦Ćļ¦ī ņ╣śļŻī ļ░śņØæņØä ļ»ĖņäĖĒĢśĻ▓ī ĒÅēĻ░ĆĒĢśļŖö Ļ▓āņØĆ ņĀ£ĒĢ£ņĀüņØ┤ļØ╝ļŖö ļ│┤Ļ│ĀņŚÉ ļö░ļØ╝[2], ņ¦äļŗ© Ēøä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņŚÉļŖö ĒÖ£ņÜ®ĒĢśņ¦Ć ņĢŖņĢśļŗż. ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ 7ņĢł ļ¬©ļæÉņŚÉņä£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ļ¦źļØĮļ¦ēņŻ╝ļ”äņØ┤ ĒÖĢņØĖļÉśņŚłļŗż. ļśÉĒĢ£ ņ×äĒöīļ×ĆĒŖĖ Ēøä ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØś ĒśĖņĀäĻ│╝ ņ×¼ļ░£ ņåīĻ▓¼ ņŚŁņŗ£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ĒåĄĒĢ┤ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØĆ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØä ņ¦äļŗ©ĒĢśĻ│Ā Ļ▓ĮĻ│╝ļź╝ Ļ┤Ćņ░░ĒĢśļŖö ļŹ░ ņ£ĀņÜ®ĒĢśļŗżĻ│Ā ņāØĻ░üļÉ£ļŗż.
McCluskey et al [2]ņØś ņŚ░ĻĄ¼ņŚÉņä£ ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņŚÉņä£ ņŗ£ļĀźņĀĆĒĢśļŖö ņĢĮ 50.3%ņŚÉņä£ ļ░£ņāØĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņĢłņĀäņłśņ¦Ć ņØ┤ĒĢśņØś ņŗ£ļĀźņĀĆĒĢśĻ░Ć ņĢĮ 10.2%ņŚÉņä£ ļ░£ņāØĒĢśņśĆĻ│Ā, ĒŖ╣Ē׳ 50ņäĖ ņØ┤ņāüņØś ĒÖśņ×ÉņŚÉņä£ ņŗ£ļĀźņĀĆĒĢś ņ£äĒŚśņØ┤ ļåÆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ļÉ£ ĒÖśņ×ÉņØś ĒÅēĻĘĀņŚ░ļĀ╣ņØĆ 77ņäĖ(59-92ņäĖ)ļĪ£ ļ╣äĻĄÉņĀü Ļ│ĀļĀ╣ņØ┤ņŚłĻ│Ā, ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņŻ╝ņé¼ ņĀä ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź(logMAR)ņØś ĒÅēĻĘĀņØĆ 0.75ņśĆĻ│Ā, ņĄ£ņóģ ļ░®ļ¼Ė ļŗ╣ņŗ£ņØś ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź(logMAR)ņØś ĒÅēĻĘĀņØĆ 0.38ņØ┤ņŚłļŗż. ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØś Ļ▓ĮņÜ░ ņĢĮ 28-44% ņĀĢļÅäņŚÉņä£ ņĀäņŗĀņ¦łĒÖśņØ┤ ņŚ░Ļ┤ĆļÉ£ Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłĻ│Ā[2,8] ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 5ļ¬ģ ņżæ 1ļ¬ģ(20%)ņŚÉņä£ ļźśļ¦łĒŗ░ņŖż Ļ┤ĆņĀłņŚ╝ņØ┤ ļÅÖļ░śļÉśņŚłļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ Ļ▓ĮĻĄ¼ ņĢĮņĀ£ņØś ļČĆņ×æņÜ® ļ░Å ņ×”ņØĆ ņ×¼ļ░£ļĪ£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņéĮņ×ģņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. Ļ▓ĮĻĄ¼ ņĢĮņĀ£ļĪ£ ņĪ░ņĀłņØ┤ ņ¢┤ļĀżņÜ┤ Ļ▓ĮņÜ░ ņé¼ņÜ®ļÉĀ ņłś ņ׳ļŖö ļŗżņ¢æĒĢ£ ņāØļ¼╝ĒĢÖņĀü ņĀ£ņĀ£Ļ░Ć ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŗż. Tumor necrosis factor-╬▒ņØś ļŗ©ņØ╝ Ēü┤ļĪĀ ĒĢŁņ▓┤ņØĖ infliximab [9,10]ņØä ņØ┤ņÜ®ĒĢ£ ņ╣śļŻīĻ░Ć ļīĆĒæ£ņĀüņØ┤ļ®░, rituximab [11], Tofacitinib [12], Anakinra [13] ļō▒ņØ┤ ņé¼ņÜ®ļÉ£ ņ”ØļĪĆļōżņØ┤ ļ│┤Ļ│ĀļÉśņŚłļŗż. ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖļŖö ņāØļ¼╝ĒĢÖņĀü ņĀ£ņĀ£ņŚÉ ļ╣äĒĢ┤ ņĀäņŗĀļČĆņ×æņÜ® ņ£äĒŚśņØ┤ ņĀüĻ│Ā ņāüļīĆņĀüņ£╝ļĪ£ Ļ░ĆĻ▓®ņØ┤ ņĀĆļĀ┤ĒĢśļŗżļŖö ņןņĀÉņØ┤ ņ׳ļŗż.
Lavric et al [14]ņØĆ 114ņ”ØļĪĆņØś ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņŚÉ ļīĆĒĢ┤ ļČäņäØĒĢśņśĆĻ│Ā, ņ╣śļŻī ņŗ£ņ×æ Ēøä ĒÅēĻĘĀ 210ņØ╝ ņĀĢļÅäņŚÉ Ļ┤ĆĒĢ┤Ļ░Ć ņØ┤ļŻ©ņ¢┤ņĪīļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆĻ│Ā, ņØ┤ ņżæ 36.6%ņŚÉņä£ļŖö ņØ┤Ēøä ņ×¼ļ░£ļÉśņŚłļŗżĻ│Ā ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 3ļ¬ģ 3ņĢłņØś Ļ▓ĮņÜ░ Ļ┤ĆĒĢ┤Ļ░Ć ņØ┤ļŻ©ņ¢┤ņ¦ä Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉśļ®░, ņØ┤Ēøä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ļÅÖņĢł ņ×¼ļ░£ņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. 2ļ¬ģ 4ņĢłņØś Ļ▓ĮņÜ░ņŚÉļŖö Ļ┤ĆĒĢ┤Ļ░Ć ņØ┤ļŻ©ņ¢┤ņ¦Ćņ¦Ć ņĢŖņØĆ Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ĒøäĒ¢źņĀüņØ┤ļ®░, ļŗ©ņØ╝ ĻĖ░Ļ┤ĆņØś 5ļ¬ģ 7ņĢłņØä ļīĆņāüņ£╝ļĪ£ ĒĢ£ ļīĆņĪ░ĻĄ░ņØ┤ ņŚåļŖö ņŚ░ĻĄ¼ņśĆĻĖ░ņŚÉ ņČöĻ░Ć ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢ£ Ļ▓Ćņ”ØņØ┤ ĒĢäņÜöĒĢśļŗż. ļśÉĒĢ£ ņ╣śļŻī Ēøä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņŚÉņä£ ņĢłņ┤łņØīĒīīĻ▓Ćņé¼Ļ░Ć ņØ┤ļŻ©ņ¢┤ņ¦Ćņ¦Ć ņĢŖņØĆ ņĀÉņØĆ ņĀ£ĒĢ£ņĀÉņØ┤ļŗż. ĒĢśņ¦Ćļ¦ī ļō£ļ¼Ė ņ¦łĒÖśņ£╝ļĪ£ ņĢīļĀżņ¦ä ĒøäļČĆĻ│Ąļ¦ēņŚ╝ ĒÖśņ×Éļōż ņżæ ĻĖ░ņĪ┤ ņ╣śļŻī ļ░®ļ▓Ģņ£╝ļĪ£ ņĪ░ņĀłļÉśņ¦Ć ņĢŖņØĆ ĒÖśņ×ÉļōżņØä ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆĻĖ░ņŚÉ ņŚ░ĻĄ¼ņØś ņØśņØśĻ░Ć ņ׳ļŗżĻ│Ā ņāØĻ░üĒĢ£ļŗż.
ĒøäļČĆĻ│Ąļ¦ēņŚ╝ņØś ņØ╝ņ░© ņ╣śļŻīļŖö Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ņÖĆ Ļ▓ĮņÜ░ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ņØ┤ļŗż. ĒĢśņ¦Ćļ¦ī ņØ╝ņ░© ņ╣śļŻīļĪ£ ņĪ░ņĀłļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░ ļŹ▒ņé¼ļ®öĒāĆņåÉ ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņłĀņØĆ ņ£ĀņÜ®ĒĢ£ ņ╣śļŻī ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳ļŗż.
Figure┬Ā1.
Ocular images of the left eye of patient 1. Fundus photo images (A, C) and corresponding scanning plane images of optical coherence tomography (B, D) before implant insertion. Fundus photos (A, C) and optical coherence tomography (B, D) images show choroid folds related with uncontrolled posterior scleritis. Fundus photo (E) and optical coherence tomography (F) images after the dexamethasone implant show the well-controlled scleritis. Black arrows indicate the scanning area of optical coherence tomography.
Figure┬Ā2.
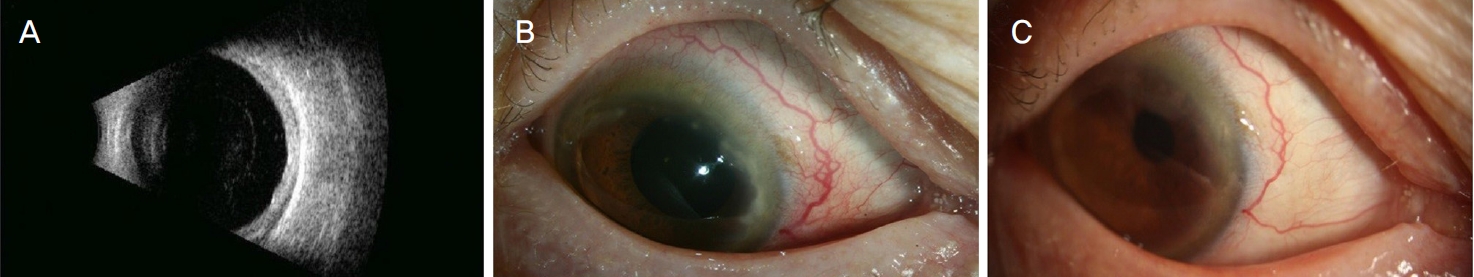
Ocular images of right eye of patient 2. Anterior photo (A) shows the diffuse scleritis accompanied with episcleral vessel engorgement and chemosis. Ultrasonography (B) shows sub-tenon fluid accumulation with thickened sclera. Wide fundus photo (C) and optical coherence tomography (D) show the choroid folds. Black arrows indicate the scanning area of optical coherence tomography.
Figure┬Ā3.
Ocular images of left eye of patient 3. Anterior photo (A) shows severe cataract, posterior synechiae and scleritis in the left eye. Anterior photo (B) and wide fundus photo (C) after cataract surgery and dexamethasone implant show well located intraocular lens and well controlled scleritis.
Figure┬Ā4.
Ultrasonography and optical coherence tomography images of patient 4. Ultrasonography in the right eye (A) and in the left eye (B) before the implant show sub-tenon fluid accumulation with thickened sclera. Optical coherence tomography images in the right eye (C) and in the left eye (D) show choroid folds related with the uncontrolled scleritis. After dexamethasone implant, choroid folds nearly disappear in optical coherence tomography images in the right eye (E) and in the left eye (F).
Figure┬Ā5.
Ultrasonography (A) and anterior photos (B, C) in left eye of patient 5. Ultrasonography (A) before the implant shows thickened sclera with sub-tenon fluid collection. A photo (B) before the implant shows edematous sclera with vessel engorgement. At two months after dexamethasone implant, there is no inflammation sign in a photo (C).
Table┬Ā1.
Demography and previous medication
Table┬Ā2.
Effect, duration, and complication of dexamethasone implant
REFERENCES
1) Ramenaden ER, Raiji VR. Clinical characteristics and visual outcomes in infectious scleritis: a review. Clin Ophthalmol 2013;7:2113-22.


2) McCluskey PJ, Watson PG, Lightman S, et al. Posterior scleritis: clinical features, systemic associations, and outcome in a large series of patients. Ophthalmology 1999;106:2380-6.


3) Gonzalez-Gonzalez LA, Molina-Prat N, Doctor P, et al. Clinical features and presentation of posterior scleritis: a report of 31 cases. Ocul Immunol Inflamm 2014;22:203-7.


4) Corti M, Palmero D, Eiguchi K. Respiratory infections in immunocompromised patients. Curr Opin Pulm Med 2009;15:209-17.


5) Hunter RS, Lobo AM. Dexamethasone intravitreal implant for the treatment of noninfectious uveitis. Clin Ophthalmol 2011;5:1613-21.


6) Tomkins-Netzer O, Taylor SRJ, Bar A, et al. Treatment with repeat dexamethasone implants results in long-term disease control in eyes with noninfectious uveitis. Ophthalmology 2014;121:1649-54.


7) Dubey N, Minija CK, Shanmugam MP. Intravitreal dexamethasone implant in a case of recurrent posterior scleritis. J Vitreoretin Dis 2017;1:84-7.

8) Akpek EK, Thorne JE, Qazi FA, et al. Evaluation of patients with scleritis for systemic disease. Ophthalmology 2004;111:501-6.


9) Murphy CC, Ayliffe WH, Booth A, et al. Tumor necrosis factor ╬▒ blockade with infliximab for refractory uveitis and scleritis. Ophthalmology 2004;111:352-6.


10) Kim DH, Wee WR, Lee JH, Kim MK. A case report of intractable scleritis effectively treated with infliximab. J Korean Ophthalmol Soc 2008;49:1690-5.

11) de Fidelix TS, Vieira LA, de Freitas D, Trevisani VF. Biologic therapy for refractory scleritis: a new treatment perspective. Int Ophthalmol 2015;35:903-12.


12) Paley MA, Karacal H, Rao PK, et al. Tofacitinib for refractory uveitis and scleritis. Am J Ophthalmol Case Rep 2019;13:53-5.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




