 |
 |
| J Korean Ophthalmol Soc > Volume 62(2); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉņŚÉņä£ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī(non-damaging retinal laser therapy) ĒÜ©Ļ│╝ļź╝ ļČäņäØĒĢśĻ│Āņ×É ĒĢśņśĆļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
2016ļģä 11ņøöļČĆĒä░ 2018ļģä 2ņøöĻ╣īņ¦Ć ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīļź╝ ļ░øņØĆ ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉļōżņØä ļīĆņāüņ£╝ļĪ£ ĒøäĒ¢źņĀü ņŚ░ĻĄ¼ļź╝ ņŗżņŗ£ĒĢśņśĆļŗż. 2ĒÜī ņØ┤ņāü ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀņØä ņŗ£Ē¢ē ļ░øņĢśņ£╝ļéś ņŗ£ļĀźĒśĖņĀäņØ┤ ļÉśņ¦Ć ņĢŖĻ│Ā ļ¦Øļ¦ēĒĢśņĢĪņØ┤ Ļ░ÉņåīļÉśņ¦Ć ņĢŖņĢśļŹś ĒÖśņ×ÉļōżņŚÉĻ▓ī ļ╣äņåÉņāü ļĀłņØ┤ņĀĆ ņ╣śļŻīļź╝ ņŗ£Ē¢ē, ņĄ£ņåī 6Ļ░£ņøö ņØ┤ņāü ņČöņĀü Ļ┤Ćņ░░ Ļ░ĆļŖźĒĢśņśĆļŹś Ļ▓ĮņÜ░ļź╝ ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆĻ│Ā, ņ╣śļŻī ņĀäĒøäļĪ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź ļ░Å ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ņØ┤ņÜ®ĒĢ£ ĒÖ®ļ░śņØś ļæÉĻ╗ś ļ│ĆĒÖöļĪ£ ļ¦Øļ¦ēĒĢśņĢĪņØś ņ¢æņØä ņĖĪņĀĢĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
ņ┤Ø 18ļ¬ģ(ļé©ņ×É 11ļ¬ģ, ņŚ¼ņ×É 7ļ¬ģ)ņØś ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉļōżņØ┤ ļČäņäØņŚÉ ĒżĒĢ©ļÉśņŚłņ£╝ļ®░, ĒÖśņ×ÉļōżņØś ļéśņØ┤ļŖö ĒÅēĻĘĀ 54.6 ┬▒ 13.19ņäĖ, ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī ņØ┤Ēøä ņČöņĀü Ļ┤Ćņ░░ ĻĖ░Ļ░äņØĆ ĒÅēĻĘĀ 9.75 ┬▒ 3.20Ļ░£ņøöņØ┤ņŚłļŗż. ļĀłņØ┤ņĀĆ ņĀäĒøäņØś ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗ś(nm)ļŖö ĒÅēĻĘĀ 375ņŚÉņä£ 246ņ£╝ļĪ£ Ļ░ÉņåīĒĢśņśĆĻ│Ā(p<0.001), ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ĒÅēĻĘĀ 0.48ņŚÉņä£ 0.40ņ£╝ļĪ£ ĒśĖņĀäļÉśņŚłļŗż(p=0.028). ļĀłņØ┤ņĀĆ ņØ┤Ēøä ļ¦Øļ¦ēĒĢśņĢĪņØ┤ ņÖäņĀä ņåīņŗżļÉ£ ĒÖśņ×ÉļŖö 10ļ¬ģ(ļé©ņ×É 5ļ¬ģ, ņŚ¼ņ×É 5ļ¬ģ)ņ£╝ļĪ£ ņÖäņĀä ņåīņŗżļźĀņØĆ 55.56%ņśĆļŗż. ļĀłņØ┤ņĀĆ ņ╣śļŻī Ēøä ĒÖ®ļ░śļČĆņŚÉ ĒŖ╣ļ│äĒĢ£ ņØ┤ņāü ņåīĻ▓¼ņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż.
Ļ▓░ļĪĀ
ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×ÉņŻ╝ņ×ģņłĀ ņŗ£Ē¢ē ĒøäņŚÉļÅä ĒśĖņĀäļÉśņ¦Ć ņĢŖļŖö ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉņŚÉņä£ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīļŖö ļ╣äĻĄÉņĀü ņĢłņĀäĒĢśļ®░ ļ¦Øļ¦ēĒĢśņĢĪņØä Ļ░Éņåīņŗ£ĒéżļŖö ļŹ░ ĒÜ©Ļ│╝ņĀüņØĖ ņ╣śļŻīļ▓Ģņ£╝ļĪ£ Ļ│ĀļĀżļÉĀ ņłś ņ׳ļŗż.
ABSTRACT
Purpose
This study analyzed the effects of non-damaging retinal laser therapy (NRT) in patients with chronic central serous chorioretinopathy.
Methods
A retrospective study was conducted on patients with chronic central serous chorioretinopathy who were undergoing follow-up with NRT from November 2016 to February 2018. NRT was performed in patients who underwent intravitreal anti-vascular endothelial growth factor (anti-VEGF) injection at least two times with no improvement in visual acuity and a reduced amount of subretinal fluid. Before and after treatment, logMAR best-corrected visual acuity (BCVA) evaluation and subretinal fluid (SRF) according to thickness measurements of the macula determined from optical coherence tomography imagery were performed over a period of at least 6 months.
Results
Eighteen eyes of 18 patients (11 male and 7 female) with chronic central serous retinopathy were treated with NRT. The mean age of patients was 54.6 ┬▒ 13.19 years old and the mean duration of follow-up was 9.75 ┬▒ 3.20 months. The central macular thickness decreased from 375 to 246 nm (p < 0.001) and BCVA improved from 0.48 to 0.40 (p = 0.028). SRF completely resolved in 55.56% of the patients after NRT.
ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņØĆ ļ¦Øļ¦ēņāēņåīņāüĒö╝ņĖĄņØś ļ│æņĀü ļ│ĆĒÖöņÖĆ ņØ┤ņŚÉ ļÅÖļ░śļÉ£ ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼ļź╝ ĒŖ╣ņ¦Ģņ£╝ļĪ£ ĒĢśļŖö ņ¦łļ│æņ£╝ļĪ£[1], ļīĆļČĆļČäņØś Ļ▓ĮņÜ░ 3Ļ░£ņøö ņØ┤ļé┤ ņ×ÉņŚ░ ĒśĖņĀäļÉśĻ│Ā ņóŗņØĆ ņŗ£ļĀźņśłĒøäļź╝ ļ│┤ņØ┤ņ¦Ćļ¦ī, ņĢĮ 5%ņØś ĒÖśņ×ÉļŖö ļ¦īņä▒ņ£╝ļĪ£ ņ¦äĒ¢ēĒĢ£ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳Ļ│Ā[2], ņØ┤ Ļ▓ĮņÜ░ ĒÖ®ļ░śļČĆ ļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ņ¦ĆņåŹļÉśĻ▒░ļéś ņ×”ņØĆ ņ×¼ļ░£ņØä ļ│┤ņØ┤ļ®┤ņä£ ļ¦Øļ¦ēņāēņåīņāüĒö╝ņ£äņČĢ, ņŗ£ņäĖĒż ņÖĖņĀłņØś ļ│ĆĒÖö, ļ¦Øļ¦ēĒĢśņé╝ņČ£, ļ¦Øļ¦ēĒĢśņä¼ņ£Āņ”Ø, ļéŁĒżĒÖ®ļ░śļ│Ćņä▒ ļ░Å ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ļō▒ņØś ĒĢ®ļ│æņ”Øņ£╝ļĪ£ ņŗ£ļĀźņĀĆĒĢś, ņśüĻĄ¼ņĀü ņżæņŗ¼ņĢöņĀÉņØä Ļ░ĆņĀĖņś¼ ņłś ņ׳ļŗż[2,3]. 6Ļ░£ņøö ņØ┤ņāü Ļ░ÉĻ░üņŗĀĻ▓Įļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ņ¦ĆņåŹ ļśÉļŖö ņ×¼ļ░£ĒĢśņŚ¼ ņ”ØņāüņØś ĒśĖņĀäņØ┤ ņŚåņØä Ļ▓ĮņÜ░ ņČöĻ░ĆņĀü ĒĢ®ļ│æņ”ØņØä ņśłļ░®ĒĢśĻĖ░ ņ£äĒĢ┤ ļ│┤ļŗż ņĀüĻĘ╣ņĀüņØĖ ņ╣śļŻīĻ░Ć ĻČīņןļÉ£ļŗż[4,5]. ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņØś ļ│æļ”¼ĻĖ░ņĀäņØĆ ļ¬ģĒÖĢĒĢśĻ▓ī ļ░ØĒśĆņ¦Ćņ¦Ć ņĢŖņĢśņ¦Ćļ¦ī, ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś Ēł¼Ļ│╝ņä▒ ņ”ØĻ░ĆņÖĆ ļ¦Øļ¦ēņāēņåīņāüĒö╝(retinal pigment epithelium, RPE)ņØś ĒÄīĒöä ĻĖ░ļŖźĻ│╝ ļ░®ņ¢┤ļ▓Į ĻĖ░ļŖź ņĀĆĒĢśļĪ£ ņØĖĒĢ┤ ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼ ļ░Å ļ¦Øļ¦ēņāēņåīņāüĒö╝ļ░Ģļ”¼Ļ░Ć ņ£Āļ░£ļÉśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĪīļŗż[5,6]. ņØ┤ļ¤¼ĒĢ£ ļ│æļ”¼ ĻĖ░ņĀäņŚÉ ņ░®ņĢłĒĢśņŚ¼, ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņØś ņ╣śļŻīļĪ£ Ļ┤æņŚŁĒĢÖ ņ╣śļŻī(photodynamic therapy)ņÖĆ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É(vascular endothelial growth factor, VEGF) ņŻ╝ņ×ģņłĀņØ┤ ļäÉļ”¼ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż[7,8]. Ļ░üĻ░üņØś ņ╣śļŻī ļ░®ļ▓ĢņØä ņĀüņĀłĒĢśĻ▓ī ļ│æĒ¢ēĒĢśņśĆņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā Ļ░ÉĻ░üņŗĀĻ▓Įļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ņ¦ĆņåŹļÉśļŖö Ļ▓ĮņÜ░ņŚÉļŖö ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīļź╝ Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ļŗż. ĻĖ░ņĪ┤ņØś ļ¦Øļ¦ē ļĀłņØ┤ņĀĆĻ┤æņØæĻ│ĀņłĀņØĆ ļ¦Øļ¦ēņØś ņāēņåīņāüĒö╝ņĖĄņŚÉ ņśüĻĄ¼ņĀüņØĖ ņåÉņāüņØä ņŻ╝ĻĖ░ ļĢīļ¼ĖņŚÉ ĒÖ®ļ░ś ņ¦łĒÖśņŚÉņä£ļŖö ņé¼ņÜ®ĒĢĀ ņłś ņŚåņŚłņ£╝ļéś[1,8,9] ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīļŖö ļ¦Øļ¦ē ņåÉņāüņØä ņĄ£ņåīĒÖöĒĢśĻĖ░ ņ£äĒĢ┤ ļĀłņØ┤ņĀĆ ņäĖĻĖ░ļź╝ Ļ░Éņåīņŗ£ĒéżĻ│Ā ņ¦¦ņØĆ ĒÄäņŖżļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŻ╝ļ│Ć ņŗĀĻ▓Įļ¦Øļ¦ēņĪ░ņ¦üņŚÉ ņåÉņāüņØä ņŻ╝ņ¦Ć ņĢŖņĢä ĒÖ®ļ░ś ņ¦łĒÖśņØä ņ╣śļŻīĒĢśļŖö ļŹ░ ņŗ£ļÅäĒĢ┤ ļ│╝ ņłś ņ׳ļŗż[10,11].
ņĢäņ¦üĻ╣īņ¦Ć Ļ│ĀņŗØņĀüņØĖ ņ╣śļŻīņŚÉļÅä ļ░śņØæĒĢśņ¦Ć ņĢŖļŖö ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉņŚÉņä£ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī ĒÜ©Ļ│╝ņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļŖö ņĢīļĀżņ¦ä ļ░öĻ░Ć ņŚåļŗż. ļö░ļØ╝ņä£ ņĀĆņ×ÉļōżņØĆ ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņŚÉ ļīĆĒĢ£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×ÉņŻ╝ņ×ģņłĀ ņØ┤ĒøäņŚÉļÅä ĒśĖņĀäļÉśņ¦Ć ņĢŖņØĆ ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢśņśĆļŗż.
2016ļģä 11ņøöļČĆĒä░ 2018ļģä 2ņøöĻ╣īņ¦Ć ļ│ĖņøÉņŚÉņä£ ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Øņ£╝ļĪ£ ņ¦äļŗ©ļ░øņØĆ 18ļ¬ģ 18ņĢłņØä ĒøäĒ¢źņĀüņ£╝ļĪ£ ļČäņäØĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĒŚ¼ņŗ▒ĒéżņäĀņ¢ĖņØä ņżĆņłśĒĢśņśĆĻ│Ā, ļ│ĖņøÉ ņŚ░ĻĄ¼ņ£żļ”¼ņŗ¼ņØśņ£äņøÉĒÜī(Institutional Review Board, IRB)ņØś ņŖ╣ņØĖ(ņŖ╣ņØĖ ļ▓łĒśĖ: 2020-423)ņØä ļ░øņĢä ņ¦äĒ¢ēĒĢśņśĆļŗż. ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņØś ņ¦äļŗ©ņØĆ ņĢłņĀĆĻ▓Ćņé¼ņŚÉņä£ ĒÖ®ļ░śļČĆņØś ņןņĢĪņä▒ ņ£ĄĻĖ░ļź╝ ļ│┤ņØ┤Ļ│Ā, ĒśĢĻ┤æņĢłņĀĆņĪ░ņśü ņåīĻ▓¼ņŚÉņä£ ļ│æļ│ĆļČĆņŚÉ ņŚ░Ļ┤ĆļÉ£ ĒśĢĻ┤æļłäņČ£ņØä ļ│┤ņØ┤ļ®┤ņä£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņåīĻ▓¼ņāü Ļ░ÉĻ░üņŗĀĻ▓Įļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ĒÖĢņØĖļÉśļŖö Ļ▓ĮņÜ░ļĪ£ ņĀĢņØśĒĢśņśĆļŗż[12].
ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Øņ£╝ļĪ£ ņ¦äļŗ©ļ░øņØĆ ĒÖśņ×É ņżæ ņ”ØņāüņØ┤ ņĄ£ņåī 6Ļ░£ņøö ņØ┤ņāü ņ¦ĆņåŹļÉśĻ│Ā, 2ĒÜī ņØ┤ņāü ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ļ▓Āļ░öņŗ£ņŻ╝ļ¦Ö(Bevacizumab, Avastin┬«; Genentech Inc., South SanFrancisco, CA, USA, 1.25 mg/0.05 mL) ņŻ╝ņ×ģņłĀņØä ņŗ£Ē¢ēļ░øņĢśņ£╝ļéś ĒśĖņĀäļÉśņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ļ¦ī ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ņŗ£ņ╝░ļŗż. ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ņŗ£ņłĀ ņĀä ņä▒ļ│ä, ļéśņØ┤, ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź(logarithm of the minimum angle of resolution, logMAR)ņØä ņĖĪņĀĢĒĢśņśĆĻ│Ā ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼, ņĢłņĀĆņ┤¼ņśü, Cirrus HD-OCT (Carl Zeiss Meditec, Inc., Dublin, CA, USA)ļź╝ ņØ┤ņÜ®ĒĢ£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ╣śļŻīļŖö ĒĢ£ ļ¬ģņØś ņłÖļĀ©ļÉ£ ņĢłĻ│╝ ņĀäļ¼ĖņØś(D.Y.L)ņŚÉ ņØśĒĢ┤ ņŗ£Ē¢ēļÉśņŚłņ£╝ļ®░ ņ╣śļŻī ĒÜ©Ļ│╝ ĒīÉņĀĢņØä ņ£äĒĢ┤ ņŗ£ņłĀ Ēøä 1Ļ░£ņøö, 3Ļ░£ņøö, 6Ļ░£ņøöņŚÉ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź, ņĢłņĀĆĻ▓Ćņé¼, ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ņŗ£Ē¢ēĒĢśņŚ¼ ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼ņÖĆ ļ¦Øļ¦ēņāēņåīņāüĒö╝ļ░Ģļ”¼ņØś ĒśĖņĀä ņŚ¼ļČĆ ļ░Å ĒĢ®ļ│æņ”Ø ļ░£ņāØ ņŚ¼ļČĆļź╝ ņĪ░ņé¼ĒĢśņśĆļŗż. ņŗ£ņłĀ Ēøä 6Ļ░£ņøöņŚÉ ņŗ£Ē¢ēĒĢ£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗śĻ░Ć Ļ░Ćņן ļåÆņØĆ ļČĆņ£äņØś ļåÆņØ┤ļź╝ ļ╣äĻĄÉĒĢśņŚ¼ ĻĘĖ ļåÆņØ┤Ļ░Ć 20% ņØ┤ņāü Ļ░ÉņåīĒĢ£ Ļ▓ĮņÜ░ņŚÉ ļČĆļČä ĒśĖņĀäņØ┤ļØ╝ ĒĢśņśĆĻ│Ā, ņÖäņĀäĒ׳ ņé¼ļØ╝ņĪīņØä Ļ▓ĮņÜ░ņŚÉļŖö ņÖäņĀä ņåīņŗżņØ┤ļØ╝ ņĀĢņØśĒĢśņśĆļŗż. ņ×¼ļ░£ņØĆ ņןņĢĪņä▒ ļ¦Øļ¦ēĒĢśņĢĪņØ┤ ņÖäņĀä ņåīņŗżļÉ£ Ēøä ļŗżņŗ£ ļ░£ņāØĒĢ£ Ļ▓ĮņÜ░ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.
ņ╣śļŻīļŖö Ēīīņן 577 nm PASCAL ļĀłņØ┤ņĀĆ(Topcon Medical Laser Systems, Livermore, CA, USA)ņØś ņŚöļō£ĒżņØĖĒŖĖ ļ¦żļŗłņ¦Ćļ©╝ĒŖĖ(Endpoint Management)ļź╝ ņé¼ņÜ®ĒĢśņśĆļŗż. ņŗ£ņłĀļ░®ļ▓ĢņØĆ ļ©╝ņĀĆ barely visible burn (ļĀłņØ┤ņĀĆ Ēøä 2ņ┤ł ņØ┤ļé┤ ĒÜīļ░▒ņāēņØś ņØæĻ│Āļ░śņØ┤ Ēؼļ»ĖĒĢśĻ▓ī ļ│┤ņØ┤ļŖö Ļ▓āņ£╝ļĪ£ ņĀĢņØś)ņØś titrationņØä ņāüņØ┤ņĖĪ ĒśłĻ┤ĆĻČü(superotemporal vascular arcade) ļśÉļŖö ĒĢśņØ┤ņĖĪ ĒśłĻ┤ĆĻČü(superotemporal vascular arcade)ņØś ĒśłĻ┤Ć ļ░öĻ╣źņŚÉ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ▓śņØī 150 mW, 15 msļĪ£ 200 ╬╝m Ēü¼ĻĖ░ņØś ĒĢśļéśņØś ņØæĻ│Āļ░śņ£╝ļĪ£ ĒģīņŖżĒŖĖĒĢśņŚ¼ ņ¦äĒĢ£ ĒÜīļ░▒ņāēņØ┤ ļ░öļĪ£ ļ│┤ņØ┤Ļ▒░ļéś ņŚÉļäłņ¦ĆĻ░Ć Ļ░ĢĒĢśļŗżĻ│Ā ĒīÉļŗ©ļÉśļ®┤ ņäĖĻĖ░ļź╝ 10 mwņö® ņżäņØ┤Ļ│Ā ņØæĻ│Āļ░śņŚÉ ņāēĻ╣ö ļ│ĆĒÖöĻ░Ć ņŚåņ£╝ļ®┤ ņäĖĻĖ░ļź╝ ņś¼ļ”¼ļŖö ņŗØņ£╝ļĪ£ ņĄ£ļīĆ 200 mwĻ╣īņ¦Ć ņ”ØĻ░Ćņŗ£ņ╝£ ļĀłņØ┤ņĀĆņØś ņäĖĻĖ░ļź╝ ņĀĢĒĢśņśĆļŗż. barely visible burn (100% ļĀłņØ┤ņĀĆ ņŚÉļäłņ¦Ć)ņØś ņäĖĻĖ░ļź╝ ņĀĢĒĢ£ ĒøäņŚÉļŖö Endpoint managementļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ 30%ņØś ņŚÉļäłņ¦Ćļź╝ ĒÖ®ļ░śļČĆņŚÉ ņĪ░ņé¼ĒĢśņśĆļŗż. ĒÖ®ļ░śļČĆ ļĀłņØ┤ņĀĆļŖö ņÜ░ņäĀ ņżæņŗ¼ņÖĆ ņ£äņŚÉņä£ 3 ├Ś 3 Ēī©Ēä┤, Spot diameter 200 ╬╝m, Spacing 0.25 diameterļĪ£ ņäżņĀĢĒĢśņŚ¼ ņĄ£ļīĆĒĢ£ ņżæņ▓®ļÉśņ¦Ć ņĢŖĻ▓ī ņŻ╝ņØśĒĢśļ®┤ņä£ ņżæņŗ¼ņŚÉņä£ ņŻ╝ļ│Ćņ£╝ļĪ£ ņé¼Ļ░üĒśĢ ļ¬©ņ¢æņ£╝ļĪ£ ņ¦äĒ¢ēĒĢśļ®┤ņä£ ĒśłĻ┤ĆĻČü ņØ┤ļé┤ļĪ£ ņĄ£ļīĆĒĢ£ ņ┤śņ┤śĒĢśĻ▓ī ņĪ░ņé¼ĒĢśņśĆļŗż. ļ¦łņ¦Ćļ¦ēņŚÉļŖö ņżæņŗ¼ ņśżļ¬®ņŚÉ 2 ├Ś 2 Ēī©Ēä┤ņ£╝ļĪ£ 1ĒÜī ļśÉļŖö 2ĒÜī ļĀłņØ┤ņĀĆļź╝ ņĪ░ņé¼ĒĢśņśĆļŗż(Fig. 1). ņ╣śļŻī ĒøäņŚÉļÅä ļ¦Øļ¦ēĒĢśņĢĪņØ┤ ļé©ņØĆ Ļ▓ĮņÜ░ ņ×¼ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆļŖöļŹ░ ļ¦Øļ¦ēņåÉņāüņØś Ļ░ĆļŖźņä▒ņØä ņĄ£ņåīĒÖöĒĢśĻĖ░ ņ£äĒĢ┤ 2Ļ░£ņøö ņØ┤ņāüņØś Ļ░äĻ▓®ņØä ļæÉĻ│Ā ņŗ£Ē¢ēĒĢśņśĆĻ│Ā ņ╣śļŻī ļ░®ļ▓ĢņØĆ ļÅÖņØ╝ĒĢśņśĆļŗż. 2ĒÜīņØś ļĀłņØ┤ņĀĆ ņ╣śļŻīņŚÉļÅä ņ╣śļŻī ļ░śņØæņØ┤ ņĀäĒśĆ ņŚåļŖö Ļ▓ĮņÜ░ ļŹö ņØ┤ņāü ņ╣śļŻīĒĢśņ¦Ć ņĢŖņĢśļŗż.
ĒåĄĻ│äļČäņäØņØĆ SPSS (Version 18.0; IBM Corp., Armonk, NY, USA) ĒöäļĪ£ĻĘĖļשņØä ņé¼ņÜ®ĒĢśņśĆļŗż. ņ╣śļŻī ņĀäĒøäņØś ņŗ£ļĀź, ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗ś ļ╣äĻĄÉļŖö Wilcoxon Signed-Rank, ļĀłņØ┤ņĀĆ ņ╣śļŻī Ēøä ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ņÖäņĀä ņåīņŗżļÉśļŖöļŹ░ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö ņØĖņ×ÉļŖö Mann-Whitney testņÖĆ FisherŌĆÖs exact testļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņäØĒĢśņśĆņ£╝ļ®░, p<0.05ņØĖ Ļ▓ĮņÜ░ ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.
ļé©ņä▒ 11ņĢł, ņŚ¼ņä▒ 7ņĢłņ£╝ļĪ£ ņ┤Ø 18ņĢłņØ┤ ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ļÉśņŚłļŗż. ĒÖśņ×ÉļōżņØĆ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī ņĀäĻ╣īņ¦Ć ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀņØä ĒÅēĻĘĀ ņ╣śļŻīļź╝ 3.1ĒÜī ļ░øņĢśĻ│Ā, ļĀłņØ┤ņĀĆ ņ╣śļŻīļŖö ĒÅēĻĘĀ 2.83 ┬▒ 0.83ĒÜī, ļĀłņØ┤ņĀĆ ņäĖĻĖ░ļŖö 140.32 ┬▒ 12.56 mW, Spot ņłśļŖö 458 ┬▒ 72.34ņśĆļŗż. ņ╣śļŻī Ēøä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØĆ ĒÅēĻĘĀ 9.75 ┬▒ 3.20Ļ░£ņøöņØ┤ņŚłļŗż(Table 1). ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī 6Ļ░£ņøö Ēøä ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź(logMAR)ņØĆ ĒÅēĻĘĀ 0.40 ┬▒ 0.31ļĪ£ ņ╣śļŻī ņĀä ĒÅēĻĘĀ 0.48 ┬▒ 0.29ņŚÉ ļ╣äĒĢ┤ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśĻ▓ī ĒśĖņĀäļÉśņŚłĻ│Ā(p=0.028), ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗ś ņŚŁņŗ£ ņ╣śļŻī ņĀä ĒÅēĻĘĀ 375.21 ┬▒ 36.42 nmņŚÉ ļ╣äĒĢ┤ ņ╣śļŻī 6Ļ░£ņøö Ēøä ĒÅēĻĘĀ 246.44 ┬▒ 41.88 nmļĪ£ ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśĻ▓ī Ļ░ÉņåīĒĢśņśĆļŗż(p<0.001) (Table 2).
ļĀłņØ┤ņĀĆ ņ╣śļŻī Ēøä 16ņĢłņŚÉņä£ ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼ņØś ņÖäņĀä ņåīņŗż ļśÉļŖö ļČĆļČä ĒśĖņĀäņØä Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłņ£╝ļéś 2ņĢłņŚÉņä£ļŖö ņ╣śļŻīņŚÉ ļ░śņØæĒĢśņ¦Ć ņĢŖĻ│Ā ĒśĖņĀäļÉśņ¦Ć ņĢŖņĢśļŗż. 16ņĢł ņżæ ņÖäņĀä ņåīņŗżņØĆ 8ļ¬ģņ£╝ļĪ£, ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī 6Ļ░£ņøö Ēøä ņÖäņĀä ņåīņŗżļźĀņØĆ 55.56%ļĪ£ ļ│┤ņśĆļŗż(Fig. 2). ļĀłņØ┤ņĀĆ ņ╣śļŻī Ēøä ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ņÖäņĀäĒ׳ ņåīņŗżļÉ£ ĒÖśņ×ÉņŚÉņä£ ĒÖ®ļ░śļČĆņŚÉ ņØæĻ│Āļ░śņØ┤ ļ░£ņāØĒĢśĻ▒░ļéś ĒÖ®ļ░śļČĆņŚÉ ņČ£Ēśł ļśÉļŖö ņé╝ņČ£ļ¼╝ ļō▒ņØś ļČĆņ×æņÜ®ņØ┤ ņāØĻĖ┤ ĒÖśņ×ÉļŖö ņŚåņŚłļŗż(Fig. 3).
ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻī Ēøä ņןņĢĪļ¦Øļ¦ēļ░Ģļ”¼Ļ░Ć ņÖäņĀä ņåīņŗżļÉśļŖöļŹ░ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö ņØĖņ×Éļź╝ ļČäņäØĒĢśĻĖ░ ņ£äĒĢ┤ ņÖäņĀä ņåīņŗżļÉ£ ĒÖśņ×ÉĻĄ░Ļ│╝ ĻĘĖļĀćņ¦Ć ņĢŖņØĆ ĒÖśņ×ÉĻĄ░ņØä ļČäņäØĒĢśņśĆņØä ļĢī, ņÖäņĀä ņåīņŗżĻĄ░ņŚÉņä£ņØś ĒÖśņ×É ņŚ░ļĀ╣ņØ┤ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśĻ▓ī ļé«ņĢśļŗż(p=0.043). ļśÉĒĢ£ ļĀłņØ┤ņĀĆ ņ╣śļŻī ņØ┤ņĀäņŚÉ ņŗ£Ē¢ēĒĢ£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀ ņØ┤Ēøä ļ░śņØæņØ┤ ņ׳ņŚłļŗżĻ░Ć ņ×¼ļ░£ĒĢśņśĆļŹś ĒÖśņ×ÉļōżņŚÉņä£ ļ░śņØæņØ┤ ņĀäĒśĆ ņŚåņŚłļŹś ĒÖśņ×Éļōżļ│┤ļŗż ļĀłņØ┤ņĀĆ ņ╣śļŻī ĒÜ©Ļ│╝Ļ░Ć ļŹö ļø░ņ¢┤ļé£ Ļ▓āņ£╝ļĪ£ ļéśņÖöļŗż(p=0.38). ļśÉĒĢ£ ļĀłņØ┤ņĀĆ ņ╣śļŻī ņĀä ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ļ¦Øļ¦ēĒĢśņĢĪņØś ļåÆņØ┤Ļ░Ć ļé«ņØäņłśļĪØ ņÖäņĀä ņåīņŗżņŚÉ ņ£Āļ”¼Ē¢łļŗż(p=0.030). ĻĘĖ ņÖĖ ļ¦Øļ¦ēņāēņåīņāüĒö╝ļ░Ģļ”¼ ņ£Āļ¼┤ ļō▒ ļŗżļźĖ ņÜöņØĖļōżņØĆ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż(Table 3).
ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņØĆ Ļ░ÉĻ░üņŗĀĻ▓Įļ¦Øļ¦ēņĖĄ ļ░æņŚÉ ņןņĢĪņØ┤ ņČĢņĀüļÉśļŖö Ļ▓āņØä ĒŖ╣ņ¦Ģņ£╝ļĪ£ ĒĢśļŖö ņ¦łĒÖśņ£╝ļĪ£ ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś Ļ│╝Ēł¼Ļ│╝ņä▒ņØ┤ ļ│æņØĖņ£╝ļĪ£ ņĢīļĀżņĀĖ ņÖöļŗż[13]. ņĢīļĀżņ¦ä ņ╣śļŻīļ▓Ģ ņżæ ĻĄŁņåī ļĀłņØ┤ņĀĆĻ┤æņØæĻ│ĀņłĀņØĆ ļłäņČ£ ļČĆņ£äņŚÉ Ļ┤æņØæĻ│ĀļÉ£ RPEĻ░Ć ņä¼ņ£ĀĒÖöļÉśņ¢┤ ĻĄŁņåī ļłäņČ£ņØä ļ¦ēņ£╝ļ®░ ņŻ╝ļ│ĆļČĆ RPEĻ░Ć ļ¦Øļ¦ēĒĢśņĢĪņØä ļ¦źļØĮļ¦ēļ¬©ņäĖĒśłĻ┤ĆņĖĄņ£╝ļĪ£ ļ░░ņČ£ĒĢśļŖö ņ×æņÜ®ņŚÉ ļÅäņøĆņØä ņżĆļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż[13]. ĒĢśņ¦Ćļ¦ī ļ¦źļØĮļ¦ēņŚÉ ĻĄŁĒĢ£ļÉ£ ņäĀĒāØņĀüņØĖ ņ╣śļŻīĻ░Ć ļČłĻ░ĆļŖźĒĢśļ®░ ļłäņČ£ņĀÉņØ┤ ņżæņŗ¼ņåīņÖĆņŚÉ ņ׳ļŖö Ļ▓ĮņÜ░ņŚÉļŖö ņ¦üņĀæ ļĀłņØ┤ņĀĆĻ┤æņØæĻ│ĀņłĀņØä ņŗ£Ē¢ēĒĢĀ ņłś ņŚåĻ│Ā ļĀłņØ┤ņĀĆ ņ╣śļŻīņŗ£ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ļ░£ņāØ ļ░Å ņżæņŗ¼ ņĢöņĀÉ ļō▒ ļ╣äĻ░ĆņŚŁņĀüņØĖ ņåÉņāüņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż[14]. Ļ┤æņŚŁĒĢÖ ņ╣śļŻīļŖö Ļ┤æĻ│╝ļ»╝ņĀ£ņØĖ verteporfinņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗ£Ē¢ēĒĢśļŖö Ļ┤æņØæĻ│ĀņłĀļĪ£ņä£ ļ¦źļØĮļ¦ēļ¬©ņäĖĒśłĻ┤ĆņØś ņłśņČĢņØä ņ£Āļ░£ĒĢśņŚ¼ ĒśłĻ┤ĆņØś Ēł¼Ļ│╝ņä▒ņØä ļé«ņČöĻ│Ā, ņåÉņāüļÉ£ RPEļź╝ ĒāłļØĮņŗ£ĒéżļŖö ļīĆņŗĀ ņĀĢņāü RPEļź╝ ņ×ÉļØ╝Ļ▓ī ĒĢ©ņ£╝ļĪ£ņŹ© ļ¦źļØĮļ¦ēņé╝ņČ£ņØä ņżäņØ┤Ļ│Ā ļ¦Øļ¦ēĒĢśņĢĪ Ļ░Éņåīļź╝ ņ£ĀļÅäĒĢśņŚ¼ ĒÜ©Ļ│╝ņĀüņØĖ ņ╣śļŻīļ▓Ģņ£╝ļĪ£ ņĢīļĀżņĪīļŗż[15]. ĻĘĖļ¤¼ļéś Ļ┤æņŚŁĒĢÖ ņ╣śļŻī ņŚŁņŗ£ RPEņØś ņ£äņČĢ, ļ¦źļØĮļ¦ēļ¬©ņäĖĒśłĻ┤ĆņØś ĒŚłĒśł ļ│ĆĒÖö, ņØ┤ņ░©ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ĒśĢņä▒ ļō▒ņØś ĒĢ®ļ│æņ”ØņØ┤ ļ│┤Ļ│ĀļÉśļ®┤ņä£[16,17] ņāłļĪ£ņÜ┤ ņ╣śļŻīļ▓ĢņØ┤ ņŚ░ĻĄ¼ļÉśņŚłĻ│Ā, Ēśäņ×¼ļŖö ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀņØ┤ ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś Ļ│╝Ēł¼Ļ│╝ņä▒ņØä ņ¢ĄņĀ£ĒĢśļŖö ĒÜ©Ļ│╝Ļ░Ć ņ׳ņ£╝ļ®┤ņä£ ļĀłņØ┤ņĀĆĻ┤æņØæĻ│ĀņłĀņØ┤ļéś Ļ┤æņŚŁĒĢÖ ņ╣śļŻīņŚÉ ļ╣äĒĢ┤ ļČĆņ×æņÜ®ņØś ņ£äĒŚśņØ┤ ņŚåņ¢┤ ļ╣äĻĄÉņĀü ņĢłņĀäĒĢśĻ▓ī ņŗ£ņłĀĒĢĀ ņłś ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśļ®┤ņä£ Ēśäņ×¼ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņØś ņŻ╝ļÉ£ ņ╣śļŻīļĪ£ ņØ┤ņÜ®ļÉśĻ│Ā ņ׳ļŗż[5,18].
ĻĘĖļ¤¼ļéś ļ¦īņä▒ņĀüņØĖ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉņŚÉņä£ ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŗ£ņłĀ ĒøäņŚÉļÅä ņ×¼ļ░£ņØ┤ ļ╣łļ▓łĒĢśĻ▒░ļéś ļ│æļ│ĆņØ┤ ņ¦ĆņåŹļÉĀ Ļ▓ĮņÜ░ ĒÖśņ×ÉņØś ļČłĒÄĖĻ░ÉĻ│╝ ņĀĢņŗØņĀüņØĖ Ļ│ĀĒåĄ, Ļ▓ĮņĀ£ņĀü ļČĆļŗ┤ņØä ņżä ņłś ņ׳ņ¢┤ ņØ┤ļ¤░ Ļ▓ĮņÜ░ ņŗ£ļÅäĒĢ┤ ļ│╝ ņłś ņ׳ļŖö ņ╣śļŻī ļ░®ļ▓Ģ ņżæ ĒĢśļéśĻ░Ć ĒÖ®ļ░śļČĆ ņé░ļ×Ć Ļ┤æņØæĻ│ĀņłĀ(macular scatter photocoagulation)ņØä ņØ┤ņÜ®ĒĢ£ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīļŗż. ĒÖ®ļ░śļČĆ ņé░ļ×Ć Ļ┤æņØæĻ│ĀņłĀņØś ņ×æņÜ®ĻĖ░ņĀäņØĆ ļ¬ģĒÖĢĒ׳ ļ░ØĒśĆņ¦Ćņ¦Ć ņĢŖņĢśņ£╝ļéś ņŚ┤ņČ®Ļ▓® ļŗ©ļ░▒ņ¦ł(heat shock protein, HSP)Ļ│╝ ļ░ĆņĀæĒĢ£ ņŚ░Ļ┤ĆņØ┤ ņ׳ņØä Ļ▓āņØ┤ļØ╝ ņāØĻ░üļÉ£ļŗż[10,19]. ņŚ┤ņČ®Ļ▓® ļŗ©ļ░▒ņ¦łņØĆ ņäĖĒżĻ░Ć Ļ│Āņś©ņØś ņŚ┤ņŚÉ ļģĖņČ£ļÉśņŚłņØä ļĢī ļ░£ĒśäļÉśļŖö ļŗ©ļ░▒ņ¦łļĪ£, ņŚ┤ņČ®Ļ▓®(heat shock) ļ┐Éļ¦īņØ┤ ņĢäļŗłļØ╝ Ļ▒░ņØś ļ¬©ļōĀ ņóģļźśņØś ņŖżĒŖĖļĀłņŖżĻ░Ć HSPņØś ļ░£ĒśäņØä ņ£ĀļÅäĒĢ©ņ£╝ļĪ£, HSPņØś ļ░£ĒśäņØĆ ņŖżĒŖĖļĀłņŖżņŚÉ ļģĖņČ£ļÉ£ ņäĖĒżņŚÉņä£ ļ│┤ņØ┤ļŖö ņØ╝ļ░śņĀüņØĖ ĒśäņāüņØ┤ļØ╝Ļ│Ā ĒĢĀ ņłś ņ׳ļŗż[20]. ņŚ¼ļ¤¼ ņóģļźśņØś ņŖżĒŖĖļĀłņŖżļŖö ņäĖĒż ļé┤ ĒÖśĻ▓ĮņØś ļ│ĆĒÖöļź╝ ņØ╝ņ£╝ņ╝£ ļŗ©ļ░▒ņ¦łĻ│╝ DNAņŚÉ ņåÉņāüņØä ņØ╝ņ£╝Ēé¼ ņłś ņ׳ļŖöļŹ░, ņåÉņāüļÉ£ ņäĖĒżļŖö ņŚŁņäżņĀüņ£╝ļĪ£ ņä£ļĪ£ ļŗżļźĖ ļæÉ Ļ░Ćņ¦Ć ļ░śņØæņØä ļ│┤ņØ╝ ņłś ņ׳ļŗż. ņ▓½ ļ▓łņ¦ĖļŖö ņäĖĒżņ×Éļ®Ėņé¼(apoptosis)ņØ┤ļŗż. ņØ┤ļŖö ņäĖĒż ņé¼ļ®ĖņØś ĒĢ£ ļ░®ņŗØņ£╝ļĪ£ņä£, ņåÉņāüļÉ£ ņäĖĒżļź╝ ņĀ£Ļ▒░ĒĢśņŚ¼ ņŚ╝ņ”ØņØä ļ░®ņ¦ĆĒĢ£ļŗż. ļæÉ ļ▓łņ¦ĖļŖö ņŖżĒŖĖļĀłņŖż ļ░śņØæ(stress response)ņØ┤ļŗż. ņØ┤ļź╝ ĒåĄĒĢ┤ ņäĖĒżļŖö ņ×ÉņŗĀņØś ņåÉņāüņØä ļ░®ņ¦ĆĒĢśĻ│Ā ĒÜīļ│ĄņØä ņ┤ēņ¦äņŗ£ņ╝£ ņāØņĪ┤ņØä ļÅĢļŖöļŗż[21]. ļ¦ÄņØĆ HSPļŖö ņäĖĒż ļé┤ņŚÉņä£ molecular chaperonesņ£╝ļĪ£ ĒÖ£ļÅÖĒĢśņŚ¼ ļŗ©ļ░▒ņ¦łņØś ņØæņ¦æ(aggregation)ņØä ļ░®ņ¦ĆĒĢśĻ│Ā, ņåÉņāüļÉ£ ļŗ©ļ░▒ņ¦łņØś ņłśļ”¼ņŚÉ Ļ┤ĆņŚ¼ĒĢ£ļŗż. ņØ┤Ļ▓āņØĆ ņäĖĒż ļé┤ņŚÉ ņĪ┤ņ×¼ĒĢśļŖö ļŗżņ¢æĒĢ£ ļŗ©ļ░▒ņ¦łņØś ņ¦æļŗ©ņ£╝ļĪ£, ļŗżļźĖ ļŗ©ļ░▒ņ¦łļōżņØ┤ ņØæņ¦æļÉśļŖö Ļ▓āņØä ļ░®ņ¦ĆĒĢśĻ│Ā, ņØæņ¦æĻ┤┤(aggregate)ļź╝ ņÜ®ĒĢ┤ņŗ£Ēéżļ®░, ļŗ©ļ░▒ņ¦ł ĻĄ¼ņĪ░ ĒśĢņä▒ņØä ļÅĢĻ▒░ļéś(folding), ļ│ĆĒśĢļÉ£ ļŗ©ļ░▒ņ¦łņØś ĻĄ¼ņĪ░ļź╝ ļ░öļĪ£ņ×ĪĻ│Ā(refolding), ņåÉņāüļÉ£ ļŗ©ļ░▒ņ¦łņØä ļČäĒĢ┤(degradation)ĒĢśĻ▒░ļéś, ņŗ¼Ļ░üĒĢ£ ņåÉņāüņØś Ļ▓ĮņÜ░, ņåÉņāüļÉ£ ļŗ©ļ░▒ņ¦łņØä ļ│┤ļŗż Ēü░ ņØæņ¦æĻ┤┤ļĪ£ Ļ▓®ļ”¼(sequestration) ņŗ£ĒéżļŖö ņŚŁĒĢĀņØä ļŗ┤ļŗ╣ĒĢ£ļŗż. Ļ▓░ĻĄŁ ņäĖĒżļŖö molecular chaperonesņØś ĒÖ£ļÅÖņØä ĒåĄĒĢśņŚ¼ ļŗ©ļ░▒ņ¦łņØś ĒĢ®ņä▒, ļ│ĆĒśĢ, ņØ┤ļÅÖ ĻĘĖļ”¼Ļ│Ā ļČäĒĢ┤ ļō▒ ņĀä Ļ│╝ņĀĢņØä ņĪ░ņĀłĒĢ£ļŗż[22]. ņØ┤ Ļ░ĆņäżņØä ĒåĄĒĢ┤, ļ¦Øļ¦ēņØś ļĀłņØ┤ņĀĆ ņÜöļ▓ĢņØĆ HSP ļ░£ĒśäņØś ņŚŁņ╣śĻ░Æ ņØ┤ņāü, RPEņŚÉ ņŚ┤ņåÉņāüņØä ņŻ╝ļŖö ņŚÉļäłņ¦Ć ļ»Ėļ¦īņŚÉņä£ ņĪ░ņĀłļÉśņ¢┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ņāØĻ░üļÉ£ļŗż. ņĢīļĀżņ¦ä ņĢīĻ│Āļ”¼ņ”śņŚÉ ļö░ļØ╝ ĒÅēĻĘĀ ņäĖĻĖ░ 150 mW, ņŗ£Ļ░ä 15 msļĪ£ Titration Ēøä ņ╣śļŻīņŗ£ņŚÉļŖö 30%ņØś ņŚÉļäłņ¦ĆļĪ£ ņäżņĀĢĒĢśņśĆļŗż[10,23]. ļśÉĒĢ£ ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ļåÆņØ┤ĻĖ░ ņ£äĒĢ┤ ņĄ£ļīĆĒĢ£ ļäōņØĆ ļ▓öņ£äņØś ļ│æļ│ĆņŚÉ ļĀłņØ┤ņĀĆļź╝ ņĪ░ņé¼ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ļŗżĻ│Ā ĒīÉļŗ©ĒĢśņŚ¼ 3 ├Ś 3 Ēī©Ēä┤, Spot diameter 200 ╬╝m, Spacing 0.25 diameterļĪ£ ņäżņĀĢĒĢśņŚ¼ ĒÖ®ļ░śļČĆņŚÉ ļĀłņØ┤ņĀĆļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż[10]. ņØ┤ļ¤░ Ļ│Āļ░ĆļÅä Ēī©Ēä┤ņØĆ ļĀłņØ┤ņĀĆ ņĪ░ņé¼ ņśüņŚŁņØś 50% ļ®┤ņĀüņŚÉ ĒĢ┤ļŗ╣ĒĢ£ļŗż. ļśÉĒĢ£ optical coherence tomographyņŚÉ ņØśĒĢ┤ ĒÖĢņØĖļÉ£ ļ¦Øļ¦ēĒĢśņĢĪ ļČĆņ£ä ļ┐Éļ¦ī ņĢäļŗłļØ╝ fluorescence angiography Ļ▓Ćņé¼ņāü Ļ│╝ĒśĢĻ┤æņ£╝ļĪ£ ļ¦īņä▒ RPE ņåÉņāüņØ┤ ņØśņŗ¼ļÉśļŖö ļČĆņ£äļÅä ņ╣śļŻī ļ▓öņ£äņŚÉ ĒżĒĢ©ņŗ£ņ╝░ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļĀłņØ┤ņĀĆ ņ╣śļŻī 6Ļ░£ņøö Ēøä ņÖäņĀä ņåīņŗżļźĀņØĆ 55.56%ļĪ£ ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ Ē¢łļŹś Lavinsky and Palanker [10]ņØś ņØ┤ņĀä ņŚ░ĻĄ¼ņŚÉņä£ņØś 75%ļ│┤ļŗżļŖö ļŗżņåī ļé«ņĢśņ£╝ļéś, ļ│Ė ņŚ░ĻĄ¼ļŖö ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀņØä ņŗ£Ē¢ēļ░øņĢśņ£╝ļéś ĒśĖņĀäņØ┤ ņŚåņŚłļŹś ĒÖśņ×ÉļōżņØä ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆņØīņØä Ļ░ÉņĢłĒĢśļ®┤ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆĻ░Ć ņóŗņØĆ ĒÜ©Ļ│╝ļź╝ ļ│┤ņśĆņØīņØä ņĢī ņłś ņ׳ļŗż. ļ¦Øļ¦ēĒĢśņĢĪ ņÖäņĀä ņåīņŗżņŚÉ ņśüĒ¢źņØä ļ»Ėņ│żļŹś ņØĖņ×Éļōż ņżæ Ļ│ĀļĀ╣ņØ┤ ļÉĀņłśļĪØ RPE ņäĖĒżņØś ļģĖĒÖöĻ░Ć Ļ┤ĆĻ│äņ׳ļŗżĻ│Ā ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż. ļģĖĒÖöņÖĆ Ļ┤ĆĻ│äļÉśņ¢┤ ņØ╝ņ¢┤ļéśļŖö ņäĖĒż ļé┤ņØś ņŻ╝ņÜö ļ│ĆĒÖö ņżæ ĒĢśļéśļŖö ņŚ┤ņČ®Ļ▓® ļ░śņØæĻ│╝ ubiquitin-proteosome degradation system (UPS)ņØś ĻĖēĻ▓®ĒĢ£ Ļ░Éņåī ĒśäņāüņØ┤ļŗż. ļ╣äņĀĢņāüņĀüņØĖ ĒÅ┤ļ”¼ĒÄ®Ēŗ░ļō£ļź╝ ņ”ØĻ░Ćņŗ£ĒéżļŖö ņŚ¼ļ¤¼ ņÜöņØĖļōżņØĆ ņäĖĒżņØś ļģĖĒÖö ĒöäļĪ£ĻĘĖļשņØä ņ┤ēņ¦äņŗ£ĒéżĻ│Ā, ļģĖĒÖöļŖö ļŗżņŗ£ UPSņÖĆ chaperone systemņØä ņ¢ĄņĀ£ņŗ£ņ╝£, ņäĖĒżĻ░Ć ļ╣äņĀĢņāüņĀüņØĖ ļŗ©ļ░▒ņ¦łņØä ņ▓śļ”¼ĒĢĀ ņłś ņŚåļÅäļĪØ ļ¦īļōĀļŗż[24]. ņ”ē RPE ņäĖĒżņØś ļģĖĒÖöļĪ£ ņØĖĒĢ┤ ņŚ┤ņČ®Ļ▓® ļ░śņØæņØ┤ Ļ░ÉņåīĒĢśļ®┤ņä£ ļĀłņØ┤ņĀĆ ĒÜ©Ļ│╝ ņŚŁņŗ£ Ļ░ÉņåīĒĢ£ Ļ▓āņØ┤ļØ╝Ļ│Ā ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż. ļ¦Øļ¦ēĒĢśņĢĪņØś ļåÆņØ┤Ļ░Ć ļåÆņØäņłśļĪØ ļ░░ņČ£ĒĢ┤ņĢ╝ ĒĢśļŖö ņןņĢĪļ¤ēņØ┤ ļ¦ÄĻ│Ā, ļĀłņØ┤ņĀĆĻ░Ć RPEņŚÉ ļŗ┐ĻĖ░ļÅä ņ¢┤ļĀżņøīņĀĖ ņÖäņĀä ņåīņŗżņØ┤ ņ¢┤ļĀĄļŗżĻ│Ā ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż. ņØ┤ņĀäņŚÉ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀņØä ņŗ£Ē¢ēļ░øņĢśņØä ļĢī ļ░śņØæņØ┤ ņ׳ņŚłļŗżļŖö Ļ▓āņØĆ, ĻĘĖņŚÉ ļ░śņØæĒĢĀ ņĀĢņāü RPE ņäĖĒżĻ░Ć ļé©ņĢäņ׳ļŖö ņāüĒā£ļØ╝Ļ│Ā ņāØĻ░üĒĢĀ ņłś ņ׳Ļ│Ā ļö░ļØ╝ņä£ ļĀłņØ┤ņĀĆ ņ╣śļŻīņŚÉņä£ļÅä ļŹö ĒÜ©Ļ│╝Ļ░Ć Ēü┤ ņłś ņ׳ļŗżĻ│Ā ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ĒøäĒ¢źņĀü ņŚ░ĻĄ¼ļĪ£ņä£ ļ¬ć Ļ░Ćņ¦Ć ņĀ£ĒĢ£ņĀÉņØ┤ ņ׳ļŗż. ņ▓½ņ¦ĖļĪ£, ĒÖśņ×É ņłśĻ░Ć ņĀüĻ│Ā Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØ┤ ņ¦¦ņĢä ņ╣śļŻīņØś ņĢłņĀäņä▒ņØä ĒīÉļŗ©ĒĢśĻĖ░ņŚÉļŖö ļČĆņĪ▒ĒĢśĻ│Ā ņןĻĖ░ņĀüņØĖ ņśłĒøä ļ╣äĻĄÉĻ░Ć ļČłĻ░ĆļŖźĒĢśļŗżļŖö ņĀÉņØ┤ļŗż. ņČöĒøä ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒÖśņ×É ņłśņÖĆ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØä ļŖśļĀż ļ╣äĻĄÉ ļČäņäØĒĢśļŖö Ļ▓āņØ┤ ĒĢäņÜöĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ļæśņ¦Ė, Ļ░ü ĒÖśņ×ÉļōżņØś ļ░£ļ│æ ņŗ£ņĀÉĻ│╝ ņ╣śļŻī ņŗ£ņĀÉ ļśÉĒĢ£ ņä£ļĪ£ ļŗ¼ļØ╝ ņ¦łļ│æņØś ņØ┤ĒÖś ĻĖ░Ļ░äņØ┤ ņ╣śļŻī ĒÜ©Ļ│╝ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źļÅä ņĢī ņłś ņŚåņŚłļŗż. ņģŗņ¦Ė, ļ│Ė ņŚ░ĻĄ¼ļŖö ļīĆņĪ░ĻĄ░ ņŚåņØ┤ ņ╣śļŻīĻĄ░ļ¦ī ĒżĒĢ©ĒĢśĻ│Ā ņ׳ņ¢┤ ļĀłņØ┤ņĀĆ ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ĒīÉļ│äĒĢśļŖö ļŹ░ ņĀ£ĒĢ£ņĀÉņØ┤ ņ׳ļŗż. ļ╣äļĪØ ĻĖēņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņŚÉ ļ╣äĒĢ┤ ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”ØņŚÉņä£ļŖö ļ¦Øļ¦ēĒĢśņĢĪņØś ņ×ÉņŚ░ Ļ┤ĆĒĢ┤ ļ╣äņ£©ņØ┤ ļé«ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ņ¦Ćļ¦ī[25], ļ¦Øļ¦ēĒĢśņĢĪņØś ņåīņŗżņØ┤ ļ╣äņåÉņāüļ¦Øļ¦ēļĀłņØ┤ņĀĆ ņ╣śļŻīņØś ĒÜ©Ļ│╝ ņÖĖņŚÉ ņ×ÉņŚ░ Ļ┤ĆĒĢ┤ņŚÉ ņØśĒĢ£ Ļ▓āņØ╝ Ļ░ĆļŖźņä▒ļÅä ņÖäņĀäĒ׳ ļ░░ņĀ£ĒĢĀ ņłś ņŚåļŗż.
ĻĘĖļ¤¼ļéś ļ│Ė ņŚ░ĻĄ¼ņØś ņØśļ»ĖļŖö ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉņŚÉņä£ Ēśäņ×¼ Ļ░Ćņן Ļ│ĀņŗØņĀüņØĖ ņ╣śļŻīļĪ£ ņĢīļĀżņ¦ä ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀņŚÉļÅä ņ×¼ļ░£ĒĢśĻ▒░ļéś ĒśĖņĀäņØ┤ ņŚåļŖö Ļ▓ĮņÜ░ ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīļĪ£ ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗śņÖĆ ņŗ£ļĀźņØä ĒśĖņĀäņŗ£ĒéżĻ│Ā, ļ¦Øļ¦ēĒĢśņĢĪņØä Ļ░Éņåīņŗ£Ēé¼ ņłś ņ׳ļŗżļŖö Ļ▓āņØ┤ļŗż. ļ╣äņåÉņāü ļ¦Øļ¦ē ļĀłņØ┤ņĀĆ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ņĢłņĀäņä▒ņØĆ ņØ┤ļ»Ė Wood et al [26]ņØś ņŚ░ĻĄ¼ņŚÉņä£ ĒÜ©Ļ│╝ņÖĆ ņĢłņĀäņä▒ņØä ņ×ģņ”ØĒĢśņśĆĻ│Ā, ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļÅä ļ¦Øļ¦ēņØś ņØ┤ņ░©ņĀüņØĖ ņåÉņāüņØ┤ļéś ļŗżļźĖ ļĀłņØ┤ņĀĆ Ļ┤ĆļĀ© ĒĢ®ļ│æņ”ØņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. Ļ▓░ļĪĀņĀüņ£╝ļĪ£ ļ╣äņåÉņāüļ¦Øļ¦ēļĀłņØ┤ņĀĆ ņ╣śļŻīļŖö ņØ┤ņĀäņŚÉ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņäĖĒż ņä▒ņןņØĖņ×É ņŻ╝ņ×ģņłĀ ĒøäņŚÉļÅä ĒśĖņĀä ņŚåļŖö ļ¦īņä▒ ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ĒÖśņ×ÉņŚÉĻ▓ī ņČöĻ░ĆņĀüņØĖ ņ╣śļŻī ļ░®ļ▓Ģņ£╝ļĪ£ Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ļŗż.
NOTES
Figure┬Ā1.
Schematic image of Non-damaging retinal laser therapy procedure. (A) Titration is performed at inferotemporal vascular arcade outside (black arrow). (B) Treatment is performed going around from parafovea using Endpoint management (30% energy), 3 ├Ś 3 patterns and 0.25 diameter spacing between the laser spots. (C) Treatment is extended to periphery until it covors total treatment area (about 3-4 cycles). (D) Finally fovea is treated using 2 ├Ś 2 patterned laser with 30% endpoint management.

Figure┬Ā2.
Optical coherence tomography images of chronic central serous chorioretinopathy patients taken before non-damaging retinal laser therapy (NRT) (left) and after 6 month of NRT (right). (A) Central macular thickness decreased, subretinal fluid completely resolved. (B) Central macular thickness decreased, subretinal fluid partially resolved. (C) Central macular thickness and subretinal fluid didnŌĆÖt decrease.
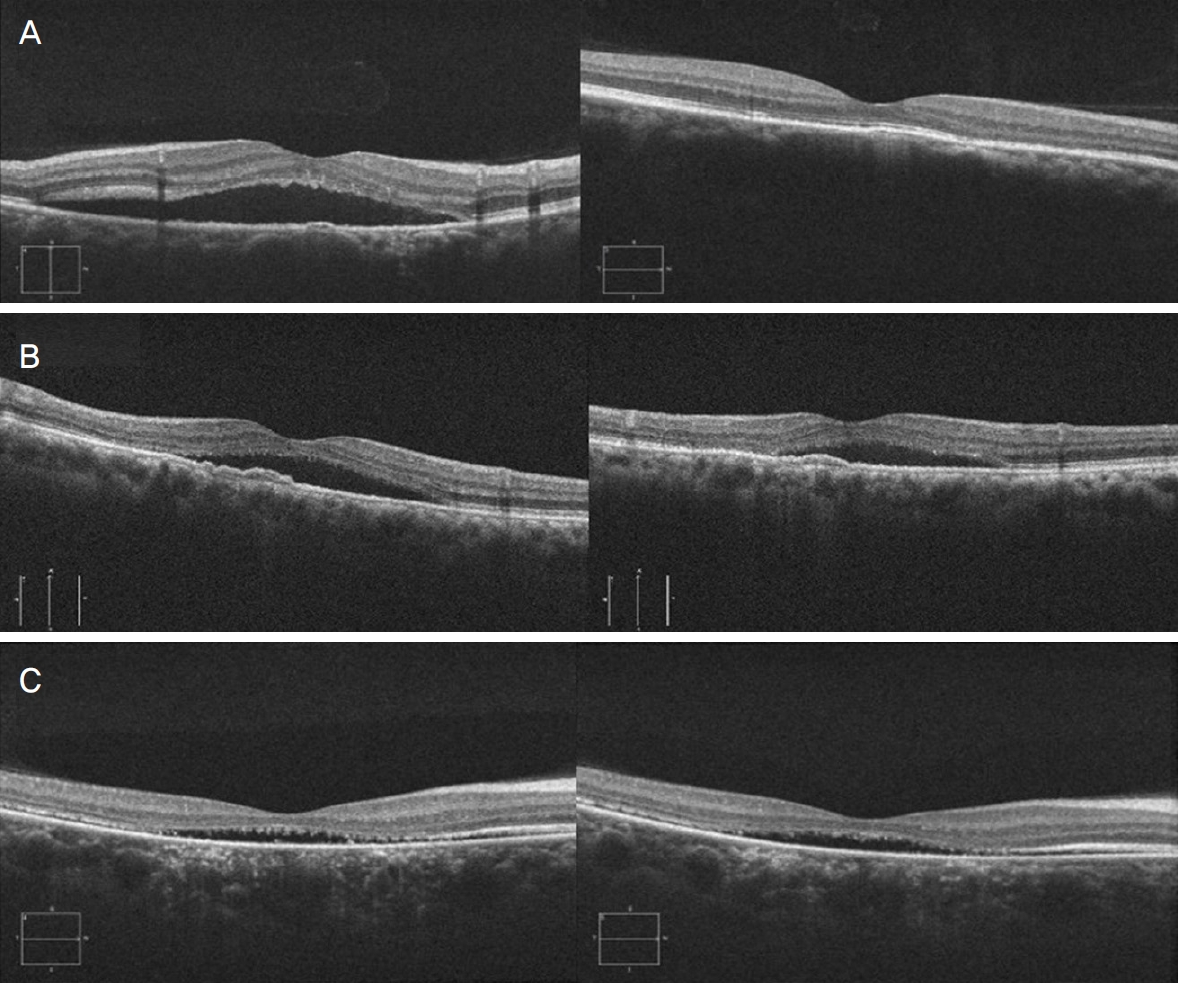
Figure┬Ā3.
Fundus photos (A, B) and optical coherence tomography images (C, D) of chronic central serous chorioretinopathy patient taken before non-damaging retinal laser therapy (NRT) (left) and after 6 month of NRT (right). Subretinal fluid completely resolved and there is no specific lesions or scar changes after NRT (left).
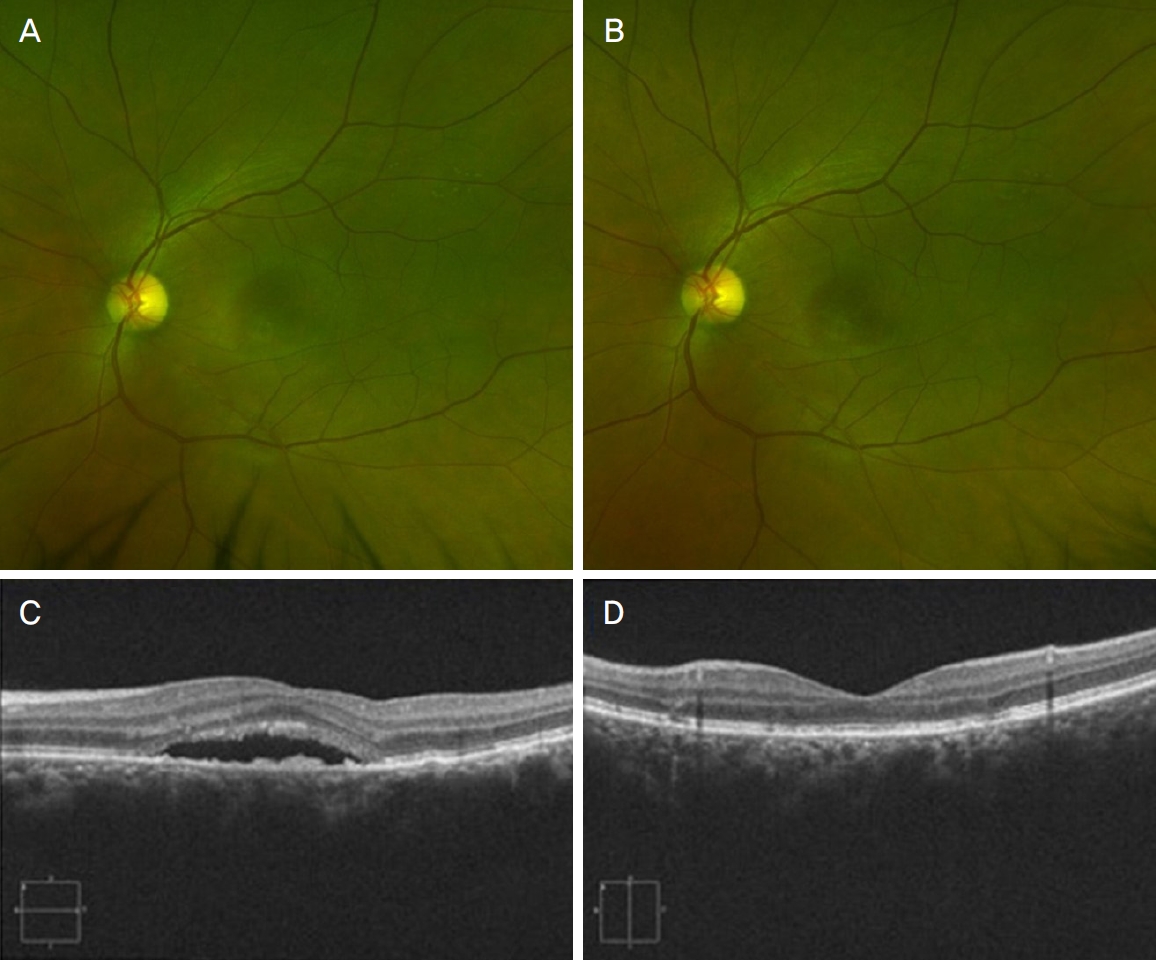
Table┬Ā1.
Clinical characteristics of patients
Table┬Ā2.
Main outcomes
| Variable | Pre NRT | Post NRT | p-value* |
|---|---|---|---|
| CRT (nm) | 375.21 ┬▒ 36.42 | 246.44 ┬▒ 41.88 | <0.001 |
| BCVA (logMAR) | 0.48 ┬▒ 0.29 | 0.40 ┬▒ 0.31 | 0.028 |
| SRF (+) | 18 | 8 | - |
| Complete resolution (%) | - | 55.56 | - |
Table┬Ā3.
Factors associated with SRF resolution
| Variable | Post NRT SRF (+) (n = 8) | Post NRT SRF (-) (n = 10) | p-value |
|---|---|---|---|
| Age (years) | 61.55 ┬▒ 11.64 | 49.76 ┬▒ 13.32 | 0.043* |
| Sex (M/F) | 5/3 | 6/4 | 0.702ŌĆĀ |
| Number of pre IVBe injections | 3.18 ┬▒ 1.39 | 3.01 ┬▒ 2.25 | 0.764* |
| Number of NRT | 2.96 ┬▒ 0.85 | 2.80 ┬▒ 0.93 | 0.610* |
| Previous PED (+/-) | 3/5 | 3/7 | 0.436ŌĆĀ |
| Response to prev IVBe (relapsed/refractory) | 2/6 (25/75) | 6/4 (60/40) | 0.038ŌĆĀ |
| Height of SRF (nm) | 191.61 ┬▒ 13.44 | 145.33 ┬▒ 18.37 | 0.030* |
REFERENCES
1) Yeo YD, Kim JH, Kim YC, Kim KS. Photodynamic therapy and focal laser photocoagulation in chronic central serous chorioretinopathy. J Korean Ophthalmol Soc 2016;57:56-62.

2) Ross A, Ross AH, Mohamed Q. Review and update of central serous chorioretinopathy. Curr Opin Ophthalmol 2011;22:166-73.


3) Oh IS, Jang JH. Outer retinal layers alterations in chronic central serous chorioretinopathy: spectral domain-OCT and fundus autofluorescence findings. J Korean Ophthalmol Soc 2016;57:763-71.

4) Iida T, Yannuzzi LA, Spaide RF, et al. Cystoid macular degeneration in chronic central serous chorioretinopathy. Retina 2003;23:1-7.


5) Koh KM, Kim JY, Kim JW, Choi MJ. The efficacy of intravitreal bevacizumab injection in patients with acute central serous chorioretinopathy. J Korean Ophthalmol Soc 2012;53:781-5.

6) Manayath GJ, Ranjan R, Shah VS, et al. Central serous chorioretinopathy: current update on pathophysiology and multimodal imaging. Oman J Ophthalmol 2018;11:103-12.


7) Kim JA, Shin JY, Bae SH, et al. Comparison of choroidal hyperpermeability change after photodynamic therapy and ranibizumab for chronic central serous chorioretinopathy. J Korean Ophthalmol Soc 2015;56:205-12.

8) Kweon EY. Factors influencing the effect of the intravitreal bevacizumab injection in patients with central serous chorioretinopathy. J Korean Ophthalmol Soc 2014;55:391-5.

9) Verma L, Sinha R, Venkatesh P, Tewari HK. Comparative evaluation of diode laser versus argon laser photocoagulation in patients with central serous retinopathy: a pilot, randomized controlled trial [ISRCTN84128484]. BMC Ophthalmol 2004;4:15.



10) Lavinsky D, Palanker D. Nondamaging photothermal therapy for the retina: initial clinical experience with chronic central serous retinopathy. Retina 2015;35:213-22.

11) Sramek C, Mackanos M, Spitler R, et al. Non-damaging retinal phototherapy: dynamic range of heat shock protein expression. Invest Ophthalmol Vis Sci 2011;52:1780-7.


12) Semeraro F, Morescalchi F, Russo A, et al. Central serous chorioretinopathy: pathogenesis and management. Clin Ophthalmol 2019;13:2341-52.


13) Ficker L, Vafidis G, While A, Leaver P. Long-term follow-up of a prospective trial of argon laser photocoagulation in the treatment of central serous retinopathy. Br J Ophthalmol 1988;72:829-34.



14) Burumcek E, Mudun A, Karacorlu S, Arslan MO. Laser photocoagulation for persistent central serous retinopathy: results of long-term follow-up. Ophthalmology 1997;104:616-22.


15) Yannuzzi LA, Slakter JS, Gross NE, et al. Indocyanine green angiography-guided photodynamic therapy for treatment of chronic central serous chorioretinopathy: a pilot study. 2003. Retina 2012;32 Suppl 1:288-98.
16) Tzekov R, Lin T, Zhang KM, et al. Ocular changes after photodynamic therapy. Invest Ophthalmol Vis Sci 2006;47:377-85.


17) Colucciello M. Choroidal neovascularization complicating photodynamic therapy for central serous retinopathy. Retina 2006;26:239-42.


18) Schaal KB, Hoeh AE, Scheuerle A, et al. Intravitreal bevacizumab for treatment of chronic central serous chorioretinopathy. Eur J Ophthalmol 2009;19:613-7.


19) Caballero S, Kent DL, Sengupta N, et al. Bone Marrow-Derived cell recruitment to the neurosensory retina and retinal pigment epithelial cell layer following subthreshold retinal phototherapy. Invest Ophthalmol Vis Sci 2017;58:5164-76.



20) Zininga T, Ramatsui L, Shonhai A. Heat shock proteins as immunomodulants. Molecules 2018;23:2846.



21) Beere HM. "The stress of dying": the role of heat shock proteins in the regulation of apoptosis. J Cell sci 2004;117(Pt 13):2641-51.


22) Voellmy R, Boellmann F. Chaperone regulation of the heat shock protein response. Adv Exp Med Biol 2007;594:89-99.


23) Lavinsky D, Sramek C, Wang J, et al. Subvisible retinal laser therapy: titration algorithm and tissue response. Retina 2014;34:87-97.

24) Meriin AB, Sherman MY. Role of molecular chaperones in neurodegenerative disorders. Int J Hyperthermia 2005;21:403-19.


-
METRICS

-
- 1 Crossref
- 0 Scopus
- 2,847 View
- 100 Download
- Related articles




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



