 |
 |
| J Korean Ophthalmol Soc > Volume 61(11); 2020 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
Ļ░üļ¦ēņ▓£Ļ│Ą ņØ┤Ēøä ņłśņ░©ļĪĆ ņ¢æļ¦ēņØ┤ņŗØņłĀņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā Ļ░üļ¦ēņØś ņ£ĪņĢäņóģņØ┤ ļ░śļ│ĄņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśļŖö ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņĖĄĒīÉņØ┤ņŗØņłĀņØś ĒÜ©Ļ│╝ļź╝ ņ”ØļĪĆ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”ØļĪĆņÜöņĢĮ
17ļģä ņĀä ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ņØ┤ ļ░£ļ│æĒĢ£ 46ņäĖ ļé©ņ×É ĒÖśņ×ÉĻ░Ć Ļ░üļ¦ēņ▓£Ļ│Ą Ēøä ņłśņ░©ļĪĆ ņ¢æļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ē ļ░øņĢśņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā Ļ░üļ¦ēņ£ĪņĢäņóģņØ┤ 4ņ░©ļĪĆ ļ░śļ│Ą ļ░£ņāØĒĢśņśĆļŗż. 2Ļ░£ņøö ņĀäļČĆĒä░ Ļ░üļ¦ēņ£ĪņĢäņóģņØ┤ ļśÉ ļŗżņŗ£ ņ×¼ļ░£ĒĢśņśĆĻ│Ā ņØ┤Ēøä ļ╣ĀļźĖ ņåŹļÅäļĪ£ ņä▒ņןĒĢśņśĆļŗż. ņĀäņŗĀļ¦łņĘ©ĒĢś Ļ░üļ¦ēņ£ĪņĢäņóģņØä ņĀ£Ļ▒░ĒĢ£ Ēøä 4.0 mm ņ¦üĻ▓ĮņØś ņøÉĒśĢņ£╝ļĪ£ ņĀłņĀ£ĒĢ£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ ņé¼ļ×ī Ļ░üļ¦ē(Halo; Eversight Inc., Palo Alto, CA, USA)ņØä ņ£ĪņĢäņóģ ņĀłņĀ£ļČĆņŚÉ ņĖĄĒīÉ ņØ┤ņŗØĒĢśņśĆĻ│Ā, ņØ┤ņŗØ Ļ░üļ¦ē Ēæ£ļ®┤ņŚÉ ļÅÖņØ╝ Ēü¼ĻĖ░ņØś ņ¢æļ¦ēņØä ņØ┤ņŗØĒĢśņśĆļŗż. ņłśņłĀ 1ļŗ¼ Ēøä ņØ╝ņŗ£ņĀüņ£╝ļĪ£ ņłśņłĀ ļČĆņ£ä ņŚ╝ņ”Ø ņ╣©ņ£ż ņåīĻ▓¼ņØä ļ│┤ņśĆņ£╝ļéś ĒĢŁņāØņĀ£ ņ╣śļŻī Ēøä ĒśĖņĀäļÉśņŚłņ£╝ļ®░, ņłśņłĀ Ēøä 8Ļ░£ņøöĻ░ä Ļ░üļ¦ēņ£ĪņĢäņóģ ņ×¼ļ░£, ņłśņłĀ ļČĆņ£ä ņ£ĄĒĢ┤ ļ░Å ņČöĻ░Ć Ļ░ÉņŚ╝ ņŚåņØ┤ ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśņŚłļŗż.
ABSTRACT
Purpose
We describe a patient with Stevens-Johnson syndrome who exhibited recurrent anterior corneal granulomas after corneal perforation (despite multiple amniotic membrane [AM] transplantations); the patient was successfully treated by lamellar grafting of an acellular, preserved human cornea.
Case summary
Corneal granulomas developed four times in a 46-year-old man who had been diagnosed with Stevens-Johnson syndrome 17 years priorly and who had undergone multiple AM transplantations after corneal perforation. A corneal granulomatous mass recurred 2 months prior to presentation in our clinic; it rapidly increased in size. With the patient under general anesthesia, the corneal mass was excised and a 4.0-mm-diameter, acellular preserved human cornea (Halo; Eversight Inc., Palo Alto, CA, USA) was grafted. A similarly sized AM was placed over the grafted cornea. Although the engrafted cornea exhibited stromal infiltration 1 month after surgery, the keratitis improved following brief antibiotic treatment. At 8 months postoperatively, the wound was stable; no granuloma recurrence, no graft melting, and no suspected microbial keratitis were observed in the region of the graft.
ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░(Stevens-Johnson syndrome)Ļ│╝ ļ│┤ļŗż ņżæņ”ØņØś ĒśĢĒā£ņØĖ ļÅģņä▒Ēæ£Ēö╝Ļ┤┤ņé¼(toxic epidermal necrolysis)ļŖö ņĢłĻĄ¼ ļ░Å ĻĄ¼Ļ░Ģ ļō▒ņØś ņĀÉļ¦ēĻ│╝ Ēö╝ļČĆļź╝ ņ╣©ļ▓öĒĢśļŖö ļ¦żņÜ░ ļō£ļ¼╝ņ¦Ćļ¦ī ņŗ¼Ļ░üĒĢ£ ņ×ÉĻ░Ćļ®┤ņŚŁņä▒ņØś ņłśĒż, ļ¼╝ņ¦æņä▒ ņ¦łĒÖśņØ┤ļŗż[1]. ņĢĮ 50%ņŚÉņä£ ĻĖēņä▒ĻĖ░ ļĢī ņĢłĻĄ¼ļź╝ ņ╣©ļ▓öĒĢśņŚ¼ Ļ░Ćņä▒ļ¦ēĻ▓░ļ¦ēņŚ╝ ļ░Å ņÖĖņĢłļČĆ ņāüĒö╝Ļ▓░ņåÉņØä ņ£Āļ░£ĒĢśļŖöļŹ░, ņØ┤ļĢī ņżæņ”Ø ņÖĖņĢłļČĆ ĒĢ®ļ│æņ”Ø(severe ocular complication)ņØä Ļ▓ĮĒŚśĒĢ£ ĒÖśņ×É ņżæ ņāüļŗ╣ņłśļŖö ņżæņ”Ø ņĢłĻĄ¼Ļ▒┤ņĪ░ņ”Ø, Ļ░üļ¦ēņŚ╝, ņ¦ĆņåŹ ņāüĒö╝Ļ▓░ņåÉ, Ļ░üļ¦ēĻČżņ¢æ, ļ░śĒØöĻ▓░ļ¦ēņŚ╝, Ļ▓ĆĻĄ¼ņ£Āņ░®, ņĢłĻĄ¼ Ēæ£ļ®┤ Ļ░üņ¦łĒÖö ļ░Å Ļ▓░ļ¦ēļéŁ ļŗ©ņČĢ ļō▒ņØś ļ¦īņä▒ ĒĢ®ļ│æņ”ØĻ│╝ ņØ┤ļĪ£ ņØĖĒĢ£ ņŗ£ļĀźņåīņŗżņØä Ļ▓ĮĒŚśĒĢśĻ▓ī ļÉ£ļŗż[2,3]. ļśÉĒĢ£ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ņŚÉņä£ Ļ▓░ļ¦ē ņäĖĻĘĀņ┤ØņØś ļ│ĆĒÖöņÖĆ ņŚ░Ļ┤ĆļÉśņ¢┤ Ļ░ÉņŚ╝Ļ░üļ¦ēņŚ╝ņØś ļ╣łļÅäĻ░Ć ņ”ØĻ░ĆĒĢśļŖöļŹ░[4] ņØ┤ļŖö Ļ▓░Ļ│╝ņĀüņ£╝ļĪ£ Ļ░üļ¦ēņØś ĻČżņ¢æņØä Ļ▒░ņ│É ņ▓£Ļ│ĄņØä ņ┤łļלĒĢĀ ņłś ņ׳ļŗż[5].
ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ņŚÉņä£ Ļ░üļ¦ēņØś ĻČżņ¢æ, ņ£ĄĒĢ┤(melting) ļ░Å ņ▓£Ļ│Ą ļ░£ņāØņØĆ ņāüļīĆņĀüņ£╝ļĪ£ ņל ņĢīļĀżņĪīņ£╝ļéś ļ░śļ│ĄņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśļŖö Ļ░üļ¦ēņ£ĪņĢäņóģņŚÉ ļīĆĒĢ┤ņä£ļŖö ņØ┤ņĀ£Ļ╣īņ¦Ć ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåņŚłļŗż. ļéśņĢäĻ░Ć ņØ┤ļ¤¼ĒĢ£ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ņŚÉņä£ņØś ņ×¼ļ░£ņä▒ Ļ░üļ¦ēņ£ĪņĢäņóģ ļ│æļ│ĆņŚÉņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņłśņłĀņĀü ņ╣śļŻī ņŚŁņŗ£ ņĢīļĀżņ¦ä ļ░ö ņŚåņŚłļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ Ļ░üļ¦ēņ▓£Ļ│Ą Ēøä ņłśņ░©ļĪĆ ņ¢æļ¦ēņØ┤ņŗØņłĀņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ļÅÖņØ╝ļČĆņ£äņŚÉņä£ ņ×¼ļ░£ĒĢśļŖö Ļ░üļ¦ēņ£ĪņĢäņóģņØä ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņĖĄĒīÉņØ┤ņŗØņłĀņØä ĒåĄĒĢ┤ ņ╣śļŻīĒĢśņśĆĻĖ░ņŚÉ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
46ņäĖ ļé©ņ×É ĒÖśņ×ÉĻ░Ć Ļ│╝Ļ▒░ļĀźņāü 17ļģä ņĀä ļ»ĖņāüņØś ņĢĮļ¼╝ ļ│ĄņÜ® Ēøä ļ░£ņāØĒĢ£ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ļ░£ļ│æ ņ¦üĒøä 5ļģäĻ░ä ņÜ░ņĢłņØś ņ×ÉĻ░Ćņ£żļČĆĻ▓░ļ¦ēņØ┤ņŗØņłĀ, ņŗ¼ļČĆĒæ£ņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀ(deep anterior lamellar keratoplasty), ļŗżņĖĄņØś(multi-layered) ņśüĻĄ¼ņ¢æļ¦ēņØ┤ņŗØņłĀ ļ░Å ļ░░ņ¢æņĮöņĀÉļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ē ļ░øņĢśļŗż.
ņØ┤Ēøä 2ņ░©ļĪĆ Ļ░üļ¦ēĻČżņ¢æ ņ▓£Ļ│ĄņØ┤ ļ░£ņāØĒĢśņŚ¼ ļ¦żĒÜī ņłśļ│ĄņĀü ļŗżņĖĄņśüĻĄ¼ņ¢æļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļéś ļÅÖņØ╝ ļČĆņ£äņŚÉņä£ Ļ░üļ¦ēĻČżņ¢æ ļ░Å Ļ░üļ¦ēņ£ĪņĢäņóģņØ┤ 4ņ░©ļĪĆ ļ░śļ│Ą ļ░£ņāØĒĢśņśĆļŗż. ņĄ£ņ┤ł ņ▓£Ļ│Ą ļŗ╣ņŗ£ 0.8 mm ņ¦üĻ▓ĮņØś Ļ░üļ¦ēĻČżņ¢æņ▓£Ļ│ĄņØ┤ ļ░£ņāØĒĢśņŚ¼ ņ”ēņŗ£ ļŗżņĖĄ ņśüĻĄ¼ņ¢æļ¦ēņØ┤ņŗØņłĀ ļ░Å ņĀäļ░® ņ×¼Ļ▒┤ņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļéś 3.5Ļ░£ņøö Ēøä ņ¢æļ¦ē ņ£ĄĒĢ┤ ļ░Å Ļ░üļ¦ēĻČżņ¢æņØ┤ ļ░£ņāØĒĢśņśĆļŗż. ņØ┤Ēøä Ļ░ÖņØĆ ņ×Éļ”¼ņŚÉņä£ ņ£ĪņĢäņóģņØ┤ ļ░£ņāØĒĢśņŚ¼ 2ĒÜī ļŗ©ņł£ ņĀłņĀ£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļéś ļæÉ ļ▓ł ļ¬©ļæÉ ņĀłņĀ£ 2-3Ļ░£ņøö ļé┤ Ļ░üļ¦ēņ£ĪņĢäņóģņØ┤ ņ×¼ļ░£ĒĢśņśĆņ£╝ļ®░, ļæÉ ļ▓łņ¦Ė ņ×¼ļ░£ Ēøä ņ£ĪņĢäņóģ ņĀłņĀ£ ļ░Å ļŗżņĖĄ ņśüĻĄ¼ņ¢æļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļéś 1-2ņŻ╝ ļÆżļČĆĒä░ Ļ░üļ¦ēņØś ņāüĒö╝Ļ▓░ņåÉņØ┤ ņ×¼ļ░£ĒĢśĻ│Ā ņ¢æļ¦ēņØś ņ£ĄĒĢ┤ ņåīĻ▓¼ņØä ļ│┤ņśĆļŗż. ņØ┤Ēøä ļ│┤ņĪ┤ņĀü ņ╣śļŻī ņżæ Ļ░üļ¦ēĻČżņ¢æņ▓£Ļ│ĄņØ┤ ņ×¼ļ░£ĒĢśņŚ¼ ļŗżņĖĄ ņśüĻĄ¼ņ¢æļ¦ēņØ┤ņŗØņłĀņØä ņ×¼ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ņłśņłĀ 3Ļ░£ņøö Ēøä ņØ┤ņŗØ Ēæ£ļ®┤ņØś ņŗ¼ĒĢ£ ņāüĒö╝Ļ▓░ņåÉņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż.
ņØ┤Ēøä 15Ļ░£ņøö ļ¦īņŚÉ ņ×¼ļ░®ļ¼ĖĒĢ£ ņÖĖļלņŚÉņä£ ņÜ░ņĢł Ļ░üļ¦ē Ēæ£ļ®┤ņŚÉ ĻČżņ¢æņä▒ ļ│æļ│ĆņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤(Fig. 1A) ņĀÉņĢł ĒĢŁņāØņĀ£ Ēł¼ņŚ¼ ļ░Å ļ│┤ņĪ┤ņĀü ņ╣śļŻī Ēøä ĒśĖņĀäļÉśņŚłņ£╝ļéś, 3Ļ░£ņøö ņØ┤Ēøä ļ░®ļ¼Ė ņŗ£ ĒØĪņé¼ Ļ░üļ¦ēņŗżņ¦ł ņåŹņŚÉņä£ļČĆĒä░ ļÅīņČ£ļÉśļ®┤ņä£ ļ╣ĀņĀĖļéśņśżļŖö ĒśĢņāüņØś Ļ░üļ¦ēņ£ĪņĢäņóģņä▒ ņóģĻ┤┤Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłĻ│Ā(Fig. 1B) ļłł Ļ╣£ļ╣Īņ×ä ņŗ£ ņØ┤ļ¼╝Ļ░ÉņØä ĒśĖņåīĒĢśņśĆļŗż. ņĀÉņĢł ĒĢŁņāØņĀ£, ņĀÉņĢł ņŖżĒģīļĪ£ņØ┤ļō£, ņĀÉņĢł 0.1% ņé¼ņØ┤Ēü┤ļĪ£ņŖżĒżļ”░ Ēł¼ņĢĮņŚÉļÅä ļ╣ĀļźĖ ņåŹļÅäļĪ£ ņä▒ņןĒĢśņŚ¼(Fig. 1C) ņłśņłĀ ņ¦üņĀäņŚÉļŖö ņןĻ▓Į 4 mm, ļŗ©Ļ▓Į 3 mm Ēü¼ĻĖ░ļĪ£ ļ╣äļīĆĒĢ┤ņĪīļŗż(Fig. 1D). Ļ░üļ¦ēņ£ĄĒĢ┤ ļśÉļŖö Ļ░ÉņŚ╝ņä▒ ĻČżņ¢æņ£╝ļĪ£ ņØĖĒĢ£ ņŗ¼ĒĢ£ ņŚ╝ņ”Ø, Ēś╣ņŗ£ ļ¬©ļź╝ ņóģĻ┤┤ ĒøäļČĆņØś ļ»ĖņäĖ ņ▓£Ļ│Ąņ£╝ļĪ£ ņØĖĒĢ£ ņØ┤ņ░©ņĀüņØĖ ņŚ╝ņ”Øņ£╝ļĪ£ ņØĖĒĢ£ ĒÖöļåŹņä▒ ņ£ĪņĢäņóģ ļ░£ņāØ, ņØ┤ņĀä ņ£ĪņĢäņóģņä▒ ņóģĻ┤┤ņØś ļČłņČ®ļČäĒĢ£ ņĀ£Ļ▒░ņŚÉ ņØśĒĢ£ ņ×¼ļ░£ ļō▒ņØś ļŗżņ¢æĒĢ£ Ļ░ĆļŖźņä▒ņØä ņŚ╝ļæÉņŚÉ ļæÉĻ│Ā ļ│æņåī ļ░Å ņŻ╝ļ│ĆļČĆ ņĪ░ņ¦üņØä ņČ®ļČäĒ׳ ņĀ£Ļ▒░ĒĢ£ Ēøä ņ¢æļ¦ēļ│┤ļŗż Ēø©ņö¼ ļæÉĻ║╝ņÜ┤ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ ņé¼ļ×ī Ļ░üļ¦ē(sterile full-sized and split thickness cornea, Halo; Eversight Inc., Palo Alto, CA, USA)ņØä ņØ┤ņÜ®ĒĢ£ ņĖĄĒīÉņØ┤ņŗØņłĀņØä Ļ│äĒÜŹĒĢśņśĆļŗż.
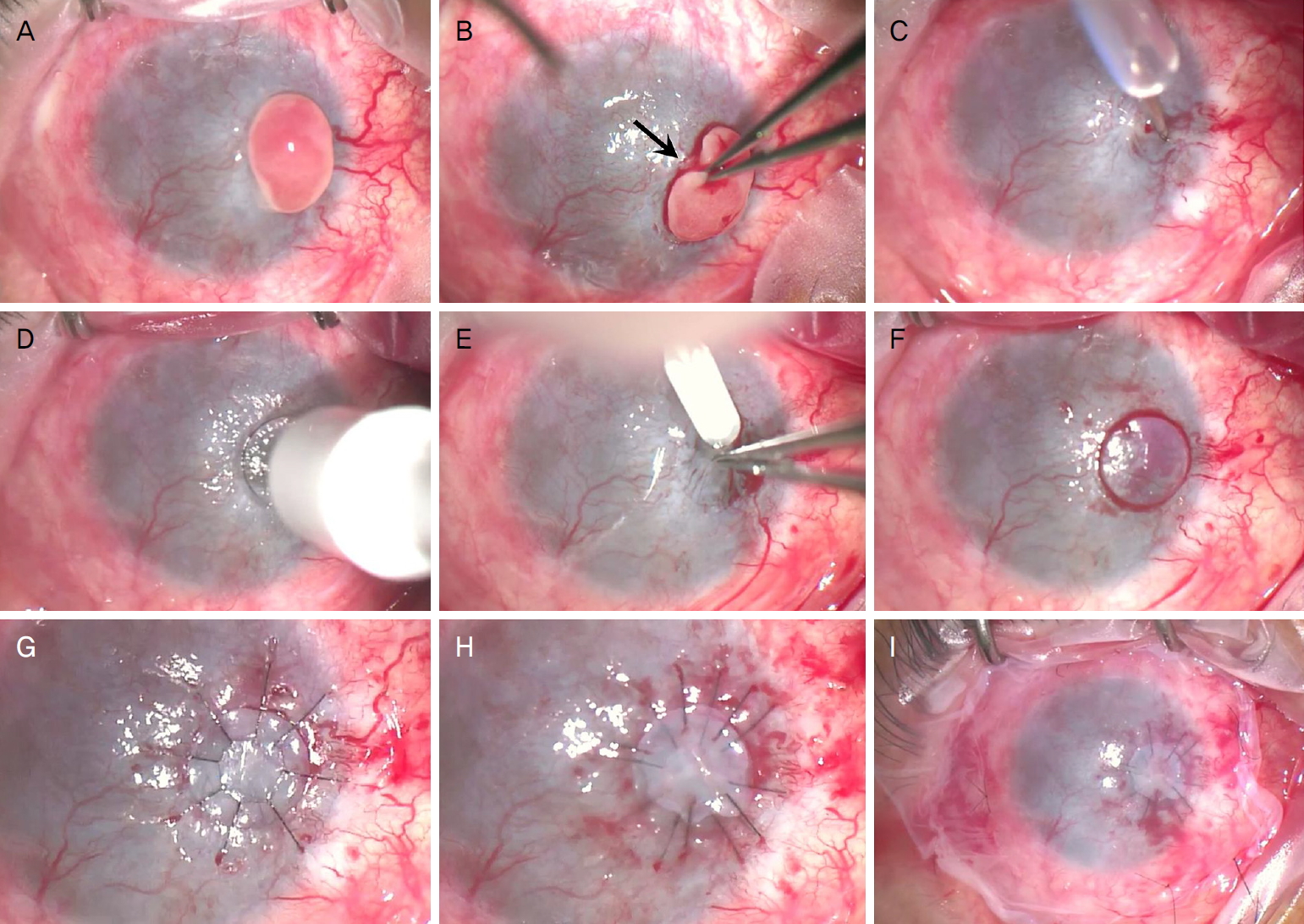
ņłśņłĀņØĆ ņĀäņŗĀļ¦łņĘ©ĒĢśņŚÉ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņÜ░ņĢł ņ£ĀĻ▓Įņä▒ ņóģĻ┤┤(Fig. 2A, B)ļź╝ ņĀłņĀ£ĒĢśĻ│Ā ĻĖ░ņĀĆņØś ņśüņ¢æ ĒśłĻ┤ĆļōżņØä ņĀäĻĖ░ ņåīņ×æĒĢ£ Ēøä(Fig. 2C), ņóģĻ┤┤ņØś ļ¬®(stalk)ņØä ņżæņŗ¼ņŚÉ ļæÉĻ│Ā 4.0 mm ņ¦üĻ▓ĮņØś ņøÉĒśĢ Ēö╝ļČĆ ņāØĻ▓Ć ĒÄĆņ╣ś(Stiefel Laboratories, Research Triangle Park, Durham, NC, USA)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņĀĆ Ļ░üļ¦ēĻĖ░ņ¦łņØä ņĖĄĒīÉ ņĀłņĀ£ĒĢśņśĆļŗż(Fig. 2D, E). ņØ┤Ēøä ļ¼┤ņäĖĒż ņé¼ļ×ī ļ│┤ņĪ┤Ļ░üļ¦ē(sterile full-sized and split thickness cornea, Halo, Eversight, Ann Arbor, MI, USA)ņØä 4.0 mm ņ¦üĻ▓ĮņØś ņøÉĒśĢņ£╝ļĪ£ ņĀłņĀ£ĒĢśņŚ¼ 10-0 ļéśņØ╝ļĪĀ ļ┤ēĒĢ®ņé¼ļĪ£ Ļ│ĀņĀĢ ļ┤ēĒĢ®ĒĢśņśĆļŗż(Fig. 2F, G). ņØ┤ņŗØ Ļ░üļ¦ēĒÄĖ ņ£äļĪ£ ņāüĒö╝ĒÖöļź╝ ļÅäļ¬©ĒĢśĻĖ░ ņ£äĒĢ┤ ļÅÖĻ▓░ ņ¢æļ¦ē(MS-Amnion; MSBIO, Seongnam, Korea)ņØä ņØ┤ņŗØĻ░üļ¦ēĒÄĖĻ│╝ ļÅÖņØ╝ Ēü¼ĻĖ░ņØĖ 4.0 mm ņøÉĒśĢņ£╝ļĪ£ ņĀłņĀ£ĒĢ£ Ēøä ĻĖ░ņĀĆļ¦ēņØ┤ ņ£äļĪ£ ņśżĻ▓ī ĒĢśņŚ¼ ņśüĻĄ¼ ņ¢æļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā(Fig. 2H), Ļ░üļ¦ēņØ┤ ļŗż ļŹ«ņØ┤ļÅäļĪØ ĻĖ░ņĀĆļ¦ēņØ┤ ņĢäļלļĪ£ ņśżļÅäļĪØ ĒĢśņŚ¼ ņ×äņŗ£ ņ¢æļ¦ēļŹ¦ļīÉņłĀņØä ņŗ£Ē¢ēĒĢ£ Ēøä ņłśņłĀņØä ņóģļŻīĒĢśņśĆļŗż(Fig. 2I). ņĀłņĀ£ ņóģĻ┤┤ņØś ļ│æļ”¼ņĪ░ņ¦üĻ▓Ćņé¼ņāü ņ£ĪņĢäņóģņØä ļÅÖļ░śĒĢ£ ļ¦īņä▒ĻĖ░ ĒÖ£ļÅÖ ņŚ╝ņ”ØņåīĻ▓¼ņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 3).
ņłśņłĀ 1Ļ░£ņøö Ēøä ņłśņłĀ ļČĆņ£äņŚÉņä£ ņŚ╝ņ”Ø ņ╣©ņ£żņØä ļÅÖļ░śĒĢ£ Ļ░ÉņŚ╝ņä▒ Ļ░üļ¦ēņŚ╝ ņČöņĀĢ ņåīĻ▓¼ņØ┤ ļ░£ņāØĒĢśņśĆņ£╝ļéś ņ░░Ļ│╝ ļ░░ņ¢æĻ▓Ćņé¼ņāü ņØīņä▒ņØ┤ņŚłĻ│Ā Ļ▓ĮĒŚśņĀü ņĀÉņĢł ĒĢŁĻĘĀņĀ£ ļ░Å ĒĢŁņ¦äĻĘĀņĀ£ļĪ£ņä£ 2.5% vancomycin, 5% ceftazidime, 1% voriconazole Ēł¼ņĢĮ Ēøä ĒśĖņĀäļÉśņŚłļŗż. ņØ┤Ēøä ņĀÉņĢł ĒĢŁņāØņĀ£ņÖĆ ņĀÉņĢł 0.1% ņé¼ņØ┤Ēü┤ļĪ£ņŖżĒżļ”░ Ēł¼ņĢĮĒĢśļ®┤ņä£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśņśĆņ£╝ļ®░ ņłśņłĀ 8Ļ░£ņøö Ēøä Ļ░üļ¦ēņØś ņ£ĪņĢäņóģ ņ×¼ļ░£, ņłśņłĀ ļČĆņ£ä ņ£ĄĒĢ┤ ļ░Å ņČöĻ░Ć Ļ░ÉņŚ╝ ņŚåņØ┤ ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśņŚłļŗż(Fig. 4).
Ļ▓░ļ¦ē ņ£ĪņĢäņóģņØĆ ļłłĻ║╝ĒÆĆņä▒ĒśĢņłĀ, ņØĄņāüĒÄĖņĀłņĀ£ņłĀ, ņĮ®ļŗżļלļü╝ ņĀłĻ░£, ņĢłņÖĆ ļé┤ hydroxyapatite ņ×äĒöīļ×ĆĒŖĖ ņéĮņ×ģņłĀ, ņé¼ņŗ£ņłśņłĀ ļō▒ņØś ļŗżņ¢æĒĢ£ ņłśņłĀ ņØ┤ĒøäņŚÉ ņóģņóģ ļ░£ņāØĒĢ£ļŗż[6-8]. ņØ┤ņŚÉ ļ░śĒĢ┤ Ļ░üļ¦ēņŚÉņä£ ļ░£ņāØĒĢ£ ņ£ĪņĢäņóģņØĆ Ļ▓░ļ¦ēņŚÉ ļ╣äĒĢ┤ ĻĘĖ ļ│┤Ļ│ĀĻ░Ć ĒśäņĀĆĒ׳ ļō£ļ¼╝ļŗż[9-11]. ĻĘĖņżæ Ferry [6]ņØĆ 1989ļģä 100ļĪĆņØś Ļ░üļ¦ēņ£ĪņĢäņóģņØä ĒżĒĢ©ĒĢ£ Ļ░Ćņן ļ¦ÄņØĆ ņłśņØś ņ”ØļĪĆļź╝ ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļéś ņāüļŗ╣ņłśļŖö ļŗżļלļü╝ Ēś╣ņØĆ ņĢłĻĄ¼ ļ░Å ņĢłĻĄ¼ ļČĆņåŹĻĖ░ ņłśņłĀ ņØ┤ĒøäņŚÉ ļ░£ņāØĒĢśņśĆĻ│Ā, Cameron and Mahmood [11]ņØ┤ ļ│┤Ļ│ĀĒĢ£ 14ļ¬ģņØś ņ”ØļĪĆļōżņØĆ ņĢłĻĄ¼Ļ▒┤ņĪ░ņ”Ø, ņåŹļłłņŹ╣ļłłņ░īļ”äņ”Ø, ņĢīņ╣╝ļ”¼ ĒÖöĒĢÖ ĒÖöņāü, ņĢłļ░śĒØöņ£Āņé¼ņ▓£Ēżņ░Į(ocular cicatricial pemphigoid), ļģ╣ļé┤ņן ņĢłņĢĮ ņĀÉņĢł, ņĢłņÖĆ ļ░®ņé¼ņäĀ ņ╣śļŻī, ņÖĖņĢłļČĆ Ļ░ÉņŚ╝ņä▒ ĻČżņ¢æ ĒÖśņ×ÉļōżļĪ£ņä£, ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ļ░£ņāØĒĢ£ Ļ░üļ¦ēņ£ĪņĢäņóģņØĆ ņØ┤ņĀ£Ļ╗Å ĻĄŁļé┤ņÖĖņŚÉņä£ ļ│┤Ļ│ĀļÉ£ ļ░ö ņŚåņŚłļŗż.
ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ļ¦īņä▒ĻĖ░ņŚÉņä£ļŖö ņĢłĻĄ¼ Ēæ£ļ®┤ ņĢłņĀĢĒÖöļź╝ ļ¬®ņĀüņ£╝ļĪ£ ļłłļ¼╝ņĀÉĒÅÉņćä, ņĀÉļ¦ēņØ┤ņŗØ(mucous membrane graft), ņ¢æļ¦ēņØ┤ņŗØ, ĻĄ¼Ļ░ĢņĀÉļ¦ēņØ┤ņŗØ ļō▒ņØ┤ ņŗ£ļÅäļÉśļŖöļŹ░[3,12], ņØ┤ļŖö ļłłĻ║╝ĒÆĆ ņĢłņ¬Įļ®┤ņØś Ļ░üņ¦łĒÖöļÉ£ Ēæ£ļ®┤ņŚÉņä£ ĻĖ░ņØĖĒĢśļŖö ļ░śļ│ĄņĀüņØĖ ļ¦łņ░░ ņ×ÉĻĘ╣ņØ┤ Ļ░üļ¦ēņØś ņŚ╝ņ”Ø, ņŗĀņāØĒśłĻ┤Ć ĒśĢņä▒, ļ░śĒØöĒÖö ļ░Å ņ£żļČĆ ņżäĻĖ░ņäĖĒż Ļ▓░ĒĢŹņØä ņ┤łļלĒĢśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż[13]. Ļ░üļ¦ēņØś ņ£ĪņĢäņóģņØĆ Ļ▓░ļ¦ēņ£ĪņĢäņóģĻ│╝ ļ¦łņ░¼Ļ░Ćņ¦ĆļĪ£ ļŗżņłśņØś ĒśłĻ┤Ćņ£╝ļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳ņ£╝ļ®┤ņä£ ņŻ╝ļĪ£ ļ”╝ĒöäĻĄ¼ņÖĆ ĒśĢņ¦ł ņäĖĒż(plasma cell)ļĪ£ ĻĄ¼ņä▒ļÉ£ ņŚ╝ņ”ØņäĖĒżņØś ņ╣©ņ£żņØ┤ ĒŖ╣ņ¦ĢņĀüņØ┤ļ®░[11], ļ│Ė ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ņŚŁņŗ£ ņ¦ĆņåŹņĀüņØĖ ļ¦īņä▒ĻĖ░ ņŚ╝ņ”ØņØ┤ ļ░śļ│ĄņĀüņØĖ ņ£ĪņĢäņóģņØś ļ░£ņāØņŚÉ ņØ╝ņĪ░Ē¢łļŗżĻ│Ā ņČöņĀĢļÉ£ļŗż.
ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ļ░Å ļÅģņä▒Ēæ£Ēö╝Ļ┤┤ņé¼ ĒÖśņ×ÉļōżņŚÉņä£ Ļ░üļ¦ēĻČżņ¢æ, ņ£ĄĒĢ┤, ņ▓£Ļ│Ą ļō▒ņØ┤ ļ░£ņāØĒĢśņśĆņØä ļĢī ļŗ╣ņן ņĢłĻĄ¼ ļ│┤ņĀä(salvaging) ļ¬®ņĀüņ£╝ļĪ£ Ļ│╝Ļ▒░ ņĪ░ņ¦ü ņĀæĒĢ®ņĀ£ ņé¼ņÜ®, Gunderson Ļ▓░ļ¦ēĒö╝ĒīÉņłĀ, ņ╣śļŻīņĀü ņĀäņĖĄ Ļ░üļ¦ēņØ┤ņŗØņłĀ, ļÅÖņóģ Ļ░üļ¦ēņ£żļČĆņØ┤ņŗØņłĀ ļō▒ņØ┤ ņŗ£ļÅäļÉśņŚłļŗż[3]. ļ│Ė ņ”ØļĪĆņŚÉņä£ Ļ│╝Ļ▒░ ņłśņ░©ļĪĆ ņ¢æļ¦ēņØ┤ņŗØņłĀņØä Ē¢łņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ļ¦żļ▓ł ļÅÖņØ╝ĒĢ£ Ļ│╝Ļ▒░ ņłśņłĀ ļČĆņ£äņŚÉņä£ Ļ░üļ¦ēņ£ĪņĢäņóģņØ┤ ņ×¼ļ░£ĒĢśņśĆļŖöļŹ░, ņØ┤ļŖö ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ņØś ņ¦łļ│æĒŖ╣ņä▒ņāü ņŗ¼ĒĢ£ ņŚ╝ņ”ØņØ┤ ņśżļ×£ ĻĖ░Ļ░ä ņ¦ĆņåŹ ļ░Å ņłśņŗ£ ņĢģĒÖöļÉśļŖö ņāüĒÖ®ņŚÉņä£, ņØ┤ņŗØ ņ¢æļ¦ē Ēæ£ļ®┤ņ£╝ļĪ£ ņāüĒö╝ĒÖöĻ░Ć ņØ┤ļŻ©ņ¢┤ņ¦ĆĻ│Ā ņ¢æļ¦ēņØ┤ ņČ®ļČäĒ׳ ĻĖ░ņ¦łĒÖöļÉśĻĖ░ ņĀäņŚÉ ļ╣Āļź┤Ļ▓ī ņ£ĄĒĢ┤ļÉśņŚłĻĖ░ ļĢīļ¼ĖņØ╝ Ļ▓āņØ┤ļØ╝Ļ│Ā ņāØĻ░üļÉ£ļŗż. ņØ┤ļŖö ļ│Ė ņ”ØļĪĆņŚÉņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØ┤ņŗØĻ│╝ ļÅÖļ░śņØ┤ņŗØĒĢ£ ņ¢æļ¦ēņØ┤ ņØ┤ņŗØĒĢ£ ļ│┤ņĪ┤ Ļ░üļ¦ēĻ│╝ļŖö ļŗ¼ļ”¼ ņēĮĻ▓ī ņāØņ░®ĒĢśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņ┤łĻĖ░ņŚÉ ņØ╝ļČĆ ņ£ĄĒĢ┤ļÉśņŚłļŹś ņĀÉĻ│╝ļÅä ņāüĒåĄĒĢ£ļŗż. ļŗżņ¢æĒĢ£ ņøÉņØĖņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢ£ Ļ░üļ¦ē 30-90% Ļ╣ŖņØ┤ņØś Ļ░üļ¦ēĻČżņ¢æņŚÉņä£ ņśüĻĄ¼ņĀü ļŗżņĖĄņ¢æļ¦ēņØ┤ņŗØņØä ņŗ£Ē¢ēĒĢ£ ņØ┤ņĀä ņŚ░ĻĄ¼ņŚÉņä£, 11ņĢł ņżæ 7ņĢłņŚÉņä£ 12Ļ░£ņøö ĒøäņŚÉļÅä ņ¢æļ¦ēņØ┤ ļČĆļČäņĀüņ£╝ļĪ£ ļé©ņĢäņ׳ņŚłĻ│Ā, 9ņĢłņŚÉņä£ļŖö 12Ļ░£ņøöĻ╣īņ¦Ć Ļ░üļ¦ēĻČżņ¢æņØś ņ×¼ļ░£ ņŚåņØ┤ ņ£Āņ¦ĆļÉ£ ļ░ö ņ׳ļŗż[14]. ĒĢśņ¦Ćļ¦ī ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░ ļŗżņĖĄņ¢æļ¦ēņØ┤ņŗØ Ēøä 1-2ņŻ╝ļ¦īņŚÉļÅä ņ¢æļ¦ēņØ┤ ņ£ĄĒĢ┤ļÉśĻĖ░ ņŗ£ņ×æĒ¢łļŖöļŹ░, ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉ ņØ┤ņŗØĒĢ£ ņ¢æļ¦ē ņ£äļĪ£ ņāüĒö╝Ļ░Ć ņČ®ļČäĒ׳ ņ×¼ņāØļÉśĻĖ░ņŚÉ ņĢ×ņä£ ņĢłĻĄ¼ Ēæ£ļ®┤ņØś Ļ│╝ļÅäĒĢ£ ļ®┤ņŚŁ ņŚ╝ņ”Ø, ļ¦łņ░░ ļ░Å ļ»ĖņāüņØś Ļ░ÉņŚ╝ ļō▒ņŚÉ ņØśĒĢ┤ ļ╣Āļź┤Ļ▓ī ņ£ĄĒĢ┤ļÉ£ Ēøä ĒÜīļ│ĄļÉśņ¦Ć ļ¬╗ĒĢ£ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉļŖö Ļ▓░ļ¦ēņØś ņäĖĻĘĀņ┤ØņØ┤ ļ│ĆĒÖöļÉśĻ│Ā ļŗżņ¢æĒĢ£ ļ│æņĀü ņäĖĻĘĀņØś ļ▓łņŗØņØ┤ ņē¼ņÜ┤ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[4]. ļ│Ė ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ļ╣äļĪØ ņ£ĪņĢäņóģņØś ņ×¼ļ░£ ņĀä ĒåĄņāüņĀüņ£╝ļĪ£ ņŗ£Ē¢ēĒĢ£ Ļ▓░ļ¦ē ĻĄ¼ņäØ ņäĖĻĘĀļ░░ņ¢æņŚÉņä£ ņäĖĻĘĀņØ┤ Ļ▓ĆņČ£ļÉśņ¦ĆļŖö ņĢŖņĢśņ£╝ļéś, ĻĖ░ņĪ┤ ņ£ĪņĢäņóģ ņĪ░ņ¦üņØś ļČłņČ®ļČäĒĢ£ ņĀłņĀ£ Ēøä ņ×öņŚ¼ ņäĖĻĘĀņØ┤ ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņ”ØņŗØĒ¢łņØä ņłś ņ׳Ļ│Ā ņØ┤ļ»Ė ĒÖ®ĒÅÉĒÖöļÉ£ ņĢłĻĄ¼ Ēæ£ļ®┤ņŚÉņä£ņØś ļ¦īņä▒ ņŚ╝ņ”ØņØ┤ ļŹöĒĢ┤ņĀĖ ĒÖöļåŹņä▒ ņ£ĪņĢäņóģņØś ņ×¼ļ░£ļĪ£ ņØ┤ņ¢┤ņĪīņØä Ļ░ĆļŖźņä▒ņØ┤ ņ׳ļŗż. ņØ┤ņŚÉ ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņ£ĪņĢäņóģņØś ļ¬®(stalk)ņØä ĒżĒĢ©ĒĢśņŚ¼ ņŻ╝ļ│ĆļČĆ Ļ░üļ¦ēņØä ņČ®ļČäĒ׳ ņĀłņĀ£ĒĢśņśĆņ£╝ļ®░, ĻĘĖ Ēøä ļŗżņĖĄņ¢æļ¦ēļ│┤ļŗżļŖö ņØ┤ņŗØ Ēøä ņĢłņĀĢņä▒ņØ┤ ļ│┤ļŗż ļåÆņØä ļ¼┤ņäĖĒż Ļ░üļ¦ēņØä ņØ┤ņŗØĒĢ£ Ļ▓āņØ┤ Ļ░üļ¦ēņ£ĪņĢäņóģņØś ņ×¼ļ░£ ļ░®ņ¦ĆņŚÉ ņ£ĀĒÜ©ĒĢśĻ▓ī ņ×æņÜ®ĒĢ£ Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż.
ļ│Ė ņ”ØļĪĆņŚÉņä£ ņĀüņÜ®ĒĢ£ ļ│┤ņĪ┤ Ļ░üļ¦ēņØĆ ņĀäņ×ÉņäĀ ņĪ░ņé¼(electron beam irradiation, 15-21 KGy) Ēøä ļ¼┤ņäĖĒżĒÖö ņŗ£ņ╝░ĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ļĪĀņĀüņ£╝ļĪ£ Ļ▒░ļČĆ ļ░śņØæņØś ņ£äĒŚśņØä ņżäņØ╝ ņłś ņ׳Ļ│Ā, ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņØś ļ░░ņŚ┤ņØ┤ ĻĘ£ņ╣ÖņĀüņØĖ Ļ░üļ¦ē Ļ│Āņ£ĀņØś ĒŖ╣ņä▒ņāü ļ┤ēĒĢ® Ēøä ņĪ░ņ¦üņØś ļŖśņ¢┤ņ¦É ļ░Å ņ£ĄĒĢ┤ņŚÉ Ļ░ĢĒĢśļ®░, ņīĆ ņ£Āļל ņ×¼ņĪ░ĒĢ® ņé¼ļ×ī Ēśłņ▓Ł ņĢīļČĆļ»╝(rice derived recombinant human serum albumin) ņÜ®ņĢĪ ņåŹņŚÉņä£ ņāüņś© ļ│┤Ļ┤ĆļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ņé¼ņÜ®ņØ┤ ĒÄĖļ”¼ĒĢśļŗżļŖö ņןņĀÉņØ┤ ņ׳ļŗż. Ļ┤ĆļĀ© ņŚ░ĻĄ¼ļĪ£ņä£ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØ ņłśĒś£ņ×É ļīĆĻĖ░ ņżæ ĻĄÉļ¤ē ņÜöļ▓Ģ(bridging therapy)ņ£╝ļĪ£ņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņé¼ņÜ®ĒĢśņŚ¼ ņŗ¼ļČĆĒæ£ņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢ£ 1Ļ▒┤ņØś ņŚ░ĻĄ¼Ļ░Ć Ļ│╝Ļ▒░ ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ņ£╝ļéś[15], ņ¢æļ¦ēņØ┤ņŗØņłĀņŚÉļÅä ņ×¼ļ░£ĒĢśļŖö Ļ░üļ¦ēņ£ĪņĢäņóģņŚÉņä£ ņ£ĪņĢäņóģņØś ņ×¼ļ░£ ļ░®ņ¦Ćļź╝ ļ¬®ņĀüņ£╝ļĪ£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņĀüņÜ®ĒĢ£ Ļ▓āņØĆ ļ│Ė ņ”ØļĪĆ ļ│┤Ļ│ĀĻ░Ć ņĄ£ņ┤łņØ┤ļŗż.
ļ¼╝ļĪĀ ļ│Ė ļŗ©ņØ╝ ņ”ØļĪĆļź╝ ĒåĄĒĢ┤ņä£ Ļ░üļ¦ēņ£ĪņĢäņóģ ļō▒ ņŚ╝ņ”Øņä▒ ļ│æļ│ĆņØä ļÅÖļ░śĒĢ£ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņĖĄĒīÉņØ┤ņŗØņłĀņØś ņןĻĖ░ņĀü ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ĒÖĢļ”ĮĒĢĀ ņłś ņŚåĻ│Ā ļśÉĒĢ£ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ņ¦łļ│æ ĒŖ╣ņä▒ņāü ļÅÖļ░ś Ļ░ÉņŚ╝ ņ£äĒŚśņØä ĒĢŁņāü ņŚ╝ļæÉņŚÉ ļæÉņ¢┤ņĢ╝ ĒĢ£ļŗż. ĒĢśņ¦Ćļ¦ī, ļ┤ēĒĢ®ņØ┤ ņÜ®ņØ┤ĒĢśĻ│Ā ņ£ĄĒĢ┤ņŚÉ Ļ░ĢĒĢ£ Ļ░üļ¦ē ņĪ░ņ¦üņØś ĒŖ╣ņä▒ņāü Ļ░üļ¦ēņ£ĪņĢäņóģņØä ļÅÖļ░śĒĢśļŖö ļō▒ņØś ļ¦īņä▒ĻĖ░ ņŖżĒŗ░ļĖÉņŖż-ņĪ┤ņŖ©ņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ņĢłĻĄ¼ Ēæ£ļ®┤ņØś ņĢłņĀĢĒÖö ļ¬®ņĀüņ£╝ļĪ£ ņĀüņÜ® ņŗ£ ļśÉ ĒĢśļéśņØś ņ╣śļŻīņĀü ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳Ļ▓Āļŗż.
Figure┬Ā1.
Slit-lamp photographs of the corneal granulomatous mass before surgery in 46-year-old man who was previously diagnosed with Stevens-Johnson syndrome with severe ocular complications. (A) There was seen a corneal ulcer (inside the white dotted oval) at previously perforated and amniotic membrane-transplanted area without mass-like lesion no mass-like at 5 months before surgery. (B-D) Afterwards, the corneal granulomatous mass appeared at 3ŌĆÖo clock corneal mid-periphery. At 2 months before surgery, the reddish round mass appeared emanating from the corneal stroma (B). The mass enlarged gradually and rapidly at 1 month before surgery (C) and just before the surgery (D).

Figure┬Ā2.
Intraoperative photos (A, B). The pedunculated oval mass and its stalk (arrow, B) is noted before the excision (C-I). After the excision of the mass, the feeder vessels were electrocauterized (C). The mass-excised area was partially cut using 4.0 mm skin biopsy punch (D), then lamellar dissection of the underlying corneal tissue was done (E). The acellular preserved human cornea (F, G) and the cryopreserved human amniotic membrane (AM) (H) were cut into 4.0 mm circle and transplanted at the mass-excised area using 10-0 nylon sutures. Finally, temporary AM patch was performed (I).
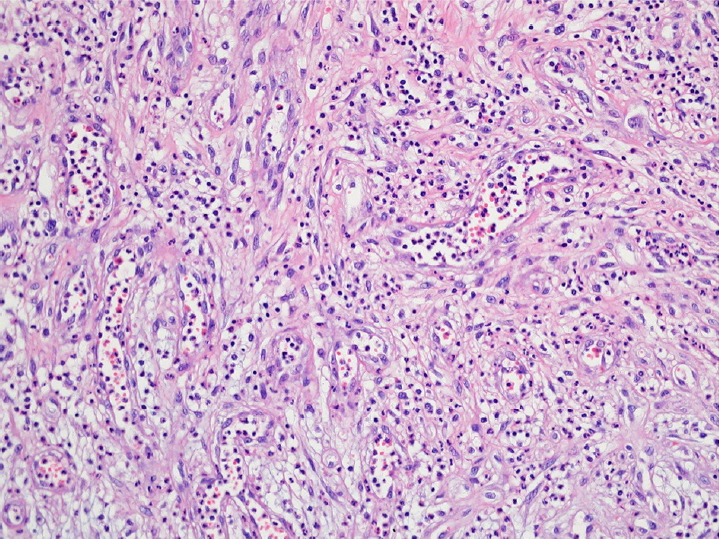
Figure┬Ā3.
The histologic appearance of corneal granuloma in this case. There is capillary proliferation in a lobular pattern, with chronic and active inflammatory cells (hematoxylin-eosin stain; original magnification, ├Ś100).
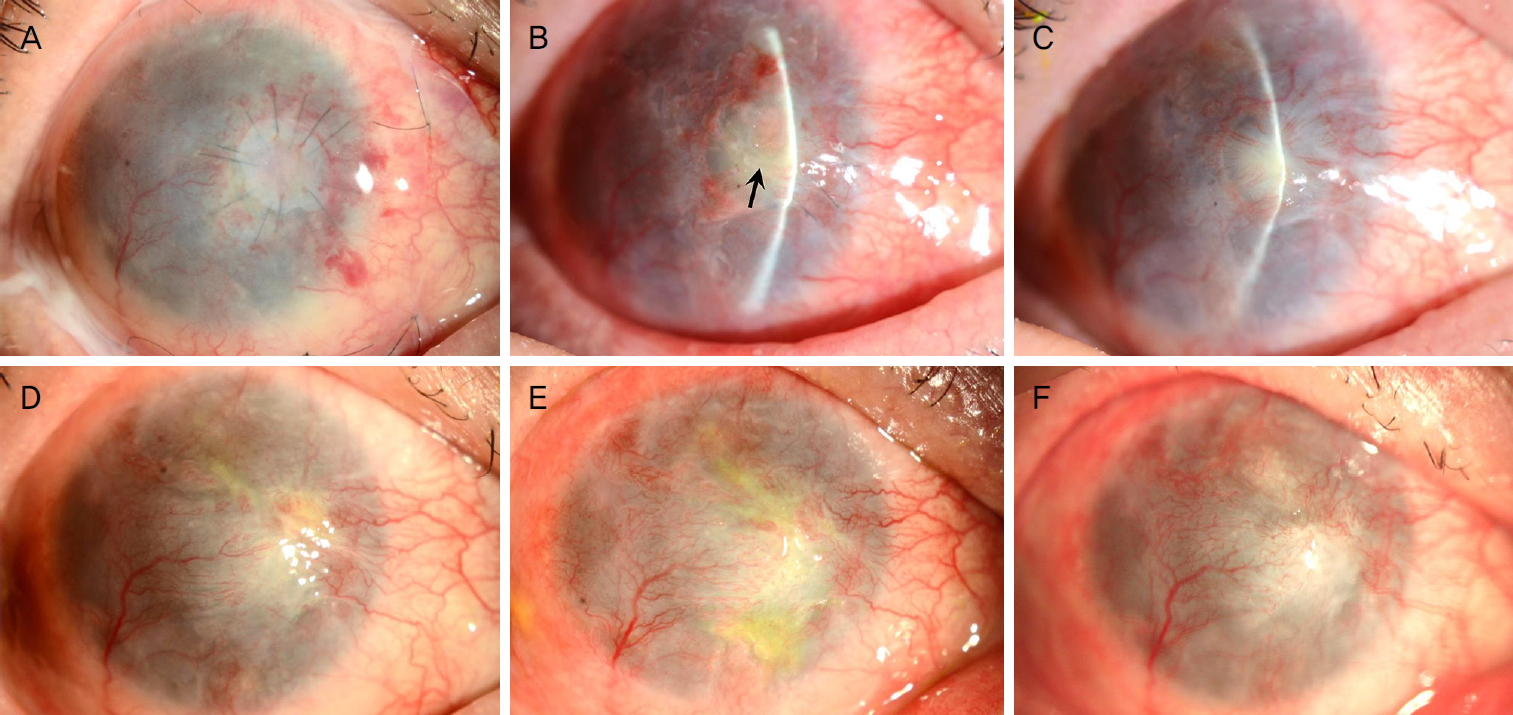
Figure┬Ā4.
The time-serial slit-lamp photographs over 8 months after surgery. (A) The engrafted preserved cornea and amniotic membrane is observed at 1 day after surgery. (B) At 1 month after surgery, the keratitis with corneal stromal infiltration is noted (arrow). (C) After the experimental topical antibiotics and antifungal combination therapy, the corneal infiltrative lesion improved at 2 months after surgery. (D-F) At 4 months (D), 6 months (E), and 8 months (F) after surgery, there was no recurrence of corneal granuloma, graft melting and the additional suspicious microbial keratitis at the graft area.
REFERENCES
1) Frey N, Jossi J, Bodmer M, et al. The Epidemiology of Stevens-Johnson syndrome and toxic epidermal necrolysis in the UK. J Invest Dermatol 2017;137:1240-7.


2) Sotozono C, Ang LP, Koizumi N, et al. New grading system for the evaluation of chronic ocular manifestations in patients with Stevens-Johnson syndrome. Ophthalmology 2007;114:1294-302.


3) Kohanim S, Palioura S, Saeed HN, et al. Acute and chronic ophthalmic involvement in Stevens-Johnson syndrome/toxic epidermal necrolysis - a comprehensive review and guide to therapy. II. Ophthalmic disease. Ocul Surf 2016;14:168-88.


4) Frizon L, Ara├║jo MC, Andrade L, et al. Evaluation of conjunctival bacterial flora in patients with Stevens-Johnson Syndrome. Clinics (Sao Paulo) 2014;69:168-72.



5) Sachdev R, Bansal S, Sinha R, et al. Bilateral microbial keratitis in highly active antiretroviral therapy-induced Stevens-Johnson syndrome and toxic epidermal necrolysis: a case series. Ocul Immunol Inflamm 2011;19:343-5.


6) Ferry AP. Pyogenic granulomas of the eye and ocular adnexa: a study of 100 cases. Trans Am Ophthalmol Soc 1989;87:327-47.


7) Lin CJ, Liao SL, Jou JR, et al. Complications of motility peg placement for porous hydroxyapatite orbital implants. Br J Ophthalmol 2002;86:394-6.



8) Espinoza GM, Lueder GT. Conjunctival pyogenic granulomas after strabismus surgery. Ophthalmology 2005;112:1283-6.


9) Googe JM, Mackman G, Peterson MR, et al. Pyogenic granulomas of the cornea. Surv Ophthalmol 1984;29:188-92.


10) Mietz H, Arnold G, Kirchhof B, Krieglstein GK. Pyogenic granuloma of the cornea: report of a case and review of the literature. Graefes Arch Clin Exp Ophthalmol 1996;234:131-6.


12) Iyer G, Pillai VS, Srinivasan B, et al. Mucous membrane grafting for lid margin keratinization in Stevens-Johnson syndrome: results. Cornea 2010;29:146-51.


13) Di Pascuale MA, Espana EM, Liu DT, et al. Correlation of corneal complications with eyelid cicatricial pathologies in patients with Stevens-Johnson syndrome and toxic epidermal necrolysis syndrome. Ophthalmology 2005;112:904-12.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




