지연성으로 증상이 발현된 수정체 내 덱사메타손 삽입물
Delayed Symptoms after Intralenticular Dexamethasone Implant
Article information
Abstract
목적
지연성으로 증상이 발현된 수정체 내 덱사메타손 삽입물(Ozurdex®; Allergan, Irvine, CA, USA) 1예를 경험하여 이를 보고하고자 한다.
증례요약
65세 남자 환자가 우안 비문증과 시력저하를 주소로 내원하였다. 세극등현미경검사상 경도의 수정체핵 혼탁과 수정체 내 덱사메타손 삽입물이 관찰되었다. 환자는 당뇨황반부종으로 수차례 유리체강내 혈관내피성장인자억제제 주사를 받았으며, 증상 발생 약 7주 전 덱사메타손 삽입물주입술을 받았다. 환자가 증상에 따른 불편감을 지속적으로 호소하여 수정체유화술과 후방인공수정체삽 입술을 시행하였다. 수술 후 증상은 호전되었다. 수술 1개월 후 낭포황반부종이 악화되어 유리체강내 트리암시놀론 아세토나이드(MaQaid®; Wakamoto Pharmaceutical Co., Ltd., Tokyo, Japan) 주사를 시행하였다. 유리체강내 주사 후 낭포황반부종은 점차 호전되는 양상을 보였다.
결론
수정체 내로 덱사메타손 삽입물을 주입하게 되는 경우는 매우 드물지만 시술 중 주의하여야 하며, 지연성으로도 수정체 내 덱사메타손 삽입물로 인한 증상이 발현될 수 있음을 인지할 필요가 있다. 따라서 면밀한 경과 관찰이 필요하며, 시력과 합병증에 따라 수술을 시행할 수 있다.
Trans Abstract
Purpose
To report a case of delayed symptoms after intralenticular dexamethasone implant (Ozurdex®; Allergan, Irvine, CA, USA).
Case summary
A 65-year-old male was referred for myodesopsia and decreased visual acuity. A dexamethasone implant was located in the crystalline lens, and the lens showed mild nucleus opacity. The patient had been treated with multiple intravitreal injections of anti-vascular endothelial growth factor and had received an injection of dexamethasone implant about seven weeks before symptom onset. Based on the symptoms, phacoemulsification was performed and an intraocular lens was placed within the capsular bag. After surgery, symptoms improved. One month after surgery, as cystoid macular edema worsened, the patient was treated with an intravitreal injection of triamcinolone acetonide (MaQaid®; Wakamoto Pharmaceutical Co., Ltd., Tokyo, Japan). After intravitreal injection, cystoid macular edema improved.
Conclusions
Intralenticular injection of the dexamethasone implant is very rare; however, great care should be taken during the procedure. It should be noted that the onset of symptoms by intralenticular dexamethasone implant may not occur immediately following the procedure. Thus, close follow-up is necessary, with the possibility of surgical intervention depending on visual acuity and underlying complications.
덱사메타손 삽입물(Ozurdex®; Allergan, Irvine, CA, USA)은 6개월까지 서서히 방출되는 700 μg의 덱사메타손을 포함하며, 직경 0.46 mm, 길이 6 mm, 무게 0.0012 g의 수용성 막대 모양 고체 고분자 물질이다[1]. 현재 당뇨망막병증과 망막분지정맥폐쇄 환자에서 황반부종이 있을 경우 치료제로 쓰이고 있으며, 트리암시놀론 아세토나이드보다 약물의 효과가 지속적으로 발현되고 안전한 장점이 있다[2-4]. 덱사메타손 삽입물의 합병증으로 고안압, 백내장, 안내염, 녹내장, 망막박리, 유리체출혈 등이 있으며, 매우 드물게 수정체 손상이 있을 수 있다[3,5]. 현재까지 덱사메타손 삽입물이 시술 중 수정체 손상을 일으켜 경과 관찰을 하거나 수술적 치료를 한 증례가 드물게 소개되었다[6-12]. 본 저자는 기존의 증례를 고찰하고, 지연성으로 증상이 발현된 수정체 내 덱사메타손 삽입물 1예를 보고하고자 한다.
증례보고
65세 남자 환자가 내원 3일 전 과음을 하였고, 다음날부터 발생한 우안 비문증과 시력저하를 주소로 내원하였다. 내원 당시 환자는 우안에 실과 같은 물체가 보인다고 하였고, 우안 나안시력은 안전수지 10 cm로 교정은 되지 않았다. 비접촉 안압계로 측정한 안압은 12.8 mmHg였다. 세극등현미경검사상 전방염증은 관찰되지 않았고, 경도의 수정체핵 혼탁과 수정체 내 덱사메타손 삽입물이 관찰되었다(Fig. 1A). 환자는 당뇨와 고혈압이 있었고 안저검사에서 양안에 증식당뇨망막병증이 관찰되었으며, 범망막광응고술을 시행한 레이저 반흔이 있었다. 과거력상 당뇨황반부종으로 수차례 유리체강내 혈관내피성장인자억제제 주사를 받았으며, 증상이 발생하기 약 7주 전 타병원에서 덱사메타손 삽입물주입술을 받았다. 샤임플러그검사법에서 수정체 내 덱사메타손 삽입물을 확인할 수 있었고(Fig. 1B), 빛간섭단층촬영에서 경도의 미만성 황반부종이 있었다(Fig. 2).
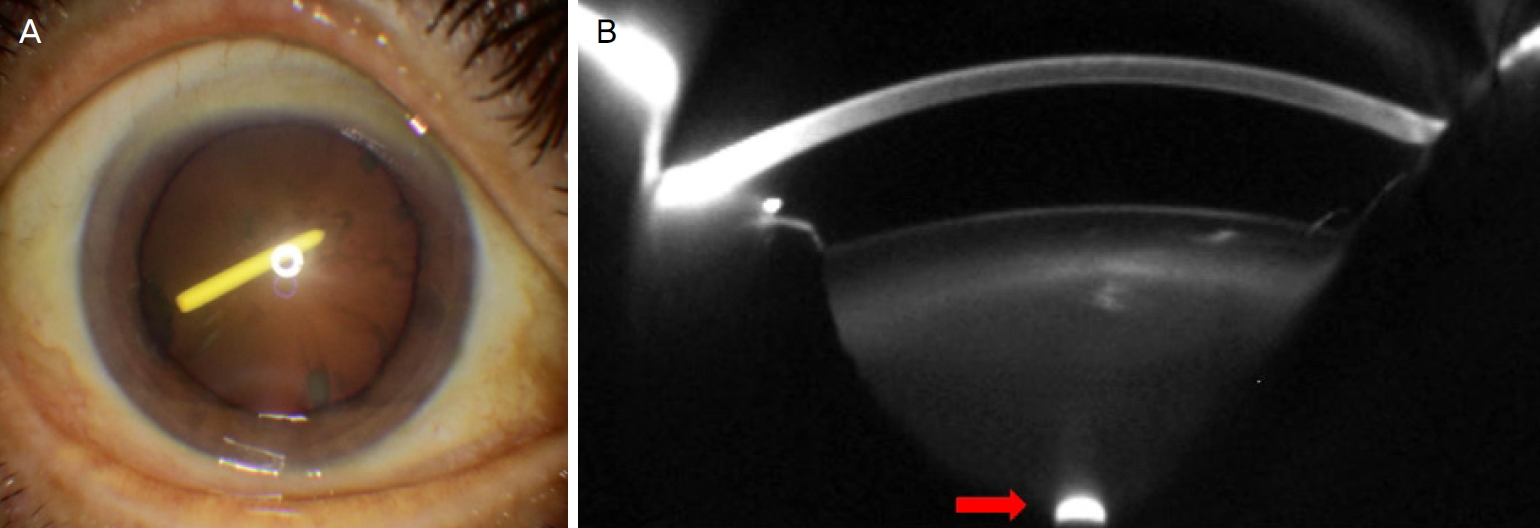
Slit lamp photograph and Pentacam scan before surgery. (A) Slit lamp photograph shows dexamethasone implant located in the crystalline lens and obliquely oriented involving the visual axis. (B) Pentacam scan of crystalline lens shows intralenticular dexamethasone implant (arrow).
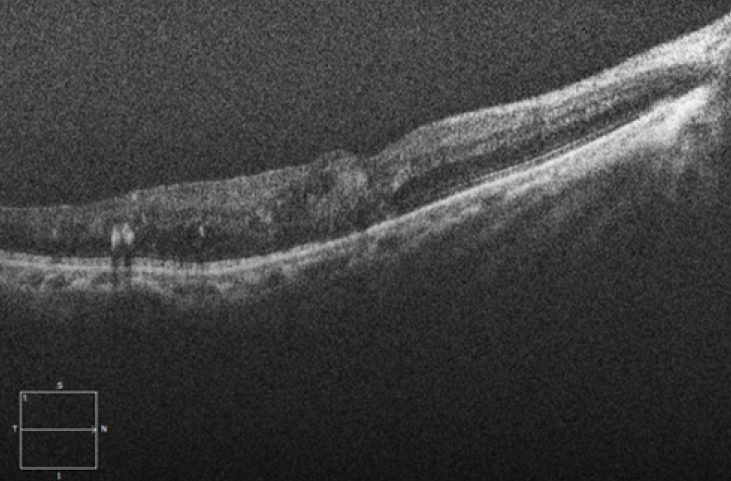
Optical coherence tomography of the right eye on the first visit. Optical coherence tomography shows diffuse retinal thickening and intraretinal fluid.
경과 관찰 중 환자가 증상에 따른 불편감을 지속적으로 호소하여 증상 발생 약 7주 후 수정체유화술 및 후방인공수정체삽입술을 시행하였다. 수술 시 수력분층술만 시행한 후 수정체유화술로 수정체내핵을 제거하였다. 이후 수정체외핵과 덱사메타손 삽입물, 피질을 제거하였고 덱사메타손 삽입물로 인한 후낭파열 부위를 관찰할 수 있었다(Fig. 3A). 점탄물질을 주입한 뒤 후낭파열 부위를 포함하여 후낭연속낭원형절개를 시행하였다. 후방인공수정체를 삽입하고 후낭파열의 확장이나 전방내 유리체가 없음을 확인한 후 수술을 마무리하였다.
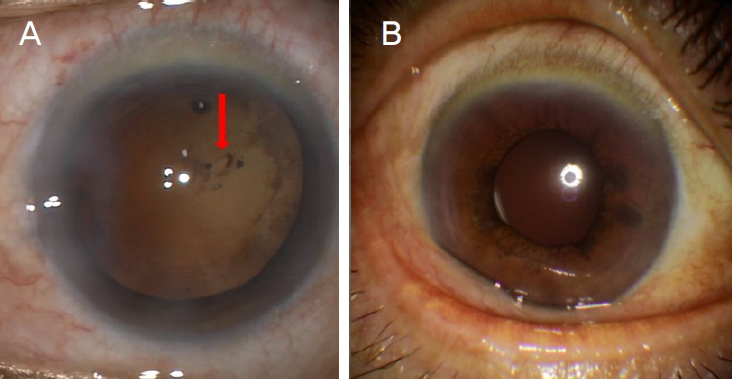
Intraoperative photograph and postoperative slit lamp photograph. (A) Intraoperative photograph shows posterior capsular rupture (arrow) after phacoemulsification. (B) Postoperative slit lamp photograph of the right eye shows well-positioned intraocular lens.
수술 다음날 내원 시 우안 비문증은 소실되었으며, 나안시력은 0.15, 비접촉 안압계로 측정한 안압은 9.2 mmHg였고, 인공수정체 위치 이상은 없었다(Fig. 3B). 수술 1개월 후 내원하였을 때 우안 나안시력은 0.03, 비접촉 안압계로 측정한 안압은 16.0 mmHg였다. 빛간섭단층촬영에서 낭포황반부종이 수술 전보다 악화된 것을 확인할 수 있었다(Fig. 4A, B). 이에 유리체강내 트리암시놀론 아세토나이드(MaQaid®; Wakamoto Pharmaceutical Co., Ltd., Tokyo, Japan) 주사를 시행하였다. 주사 1개월과 2개월 후 경과 관찰을 하였고, 낭포황반부종은 점차 호전되는 양상을 보였다(Fig. 4C, D).
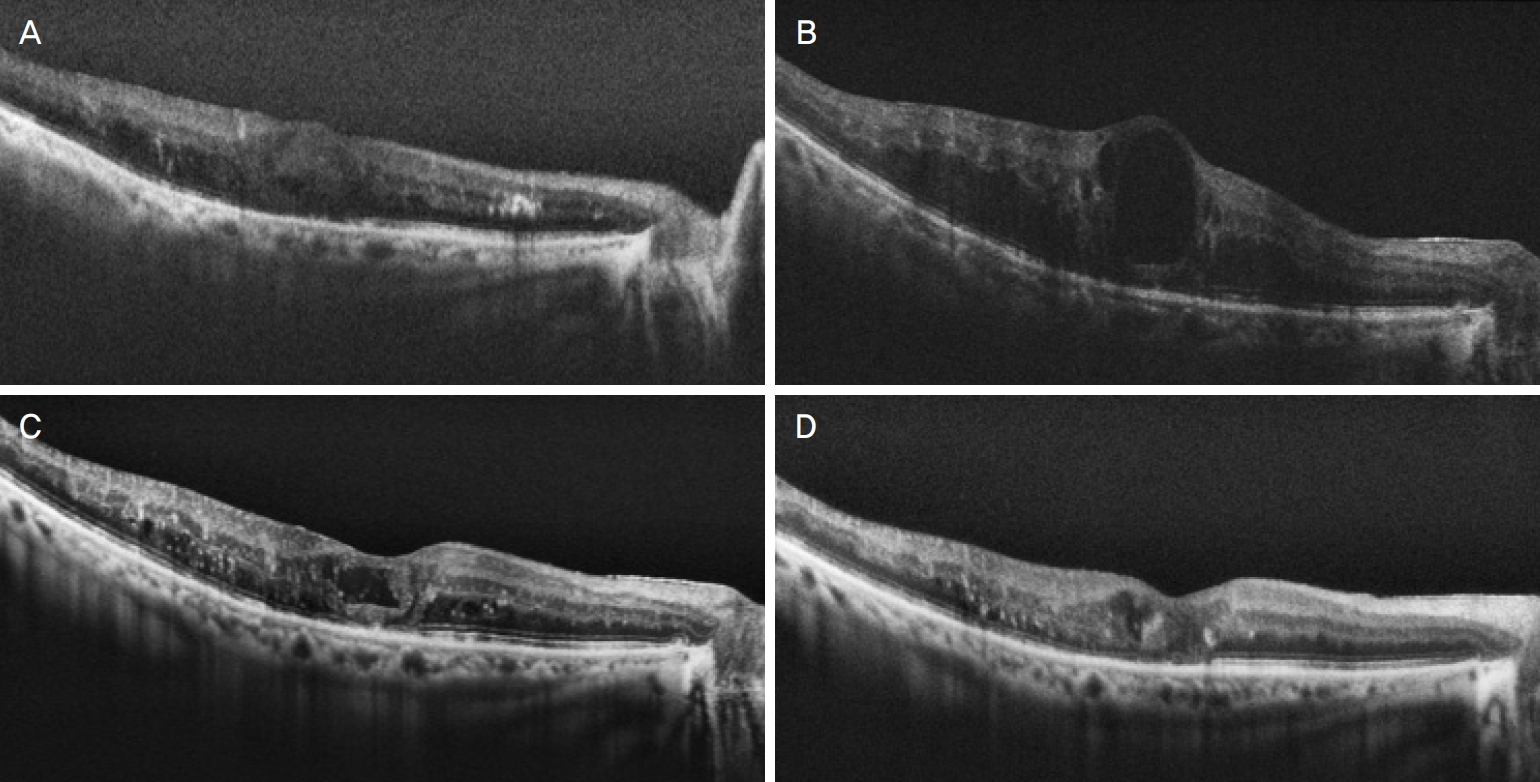
Optical coherence tomography on the day of surgery and during the follow-up period. (A) Optical coherence tomography shows diffuse retinal thickening and intraretinal fluid on the day of surgery. (B) Optical coherence tomography about one month following surgical removal of dexamethsone implant shows the cystoid macular edema with intraretinal fluid. (C) There is improvement in intraretinal fluid one month after intravitreal triamcinolone acetonide (MaQaid®) injection. (D) Further resolution of cystoid macular edema two months after intravitreal triamcinolone acetonide (MaQaid®) injection was observed.
고 찰
유리체강내 주사 중 수정체 손상은 매우 드문 합병증이며, 다기관 사례 연구에서 약 0.009%로 보고되었다[13]. 시술 중 미숙한 주입술이나 환자의 머리 움직임 등에 의해 수정체 내로 덱사메타손 삽입물이 주입되게 된다[9].
Baskan et al [6]은 망막중심정맥폐쇄로 인한 망막부종 환자에서 수정체 내로 덱사메타손 삽입물이 주입된 지 14개월 후 덱사메타손 삽입물의 모양이 유지되고 황반부종은 호전되지 않은 증례를 보고하였다. 그들은 덱사메타손 삽입물과 유리체 간에 불충분한 접촉으로 인해 치료적 효과가 만족스럽게 나타나지 않았다고 분석하였다. Coca-Robinot et al [7]은 수정체 내로 덱사메타손 삽입물이 주입된 후 안압상승이 발생한 두 증례를 보고하였고, 이러한 합병증을 막기 위해 가능한 빨리 수술을 해야 한다고 주장하였다.
Chhabra et al [8]은 수정체 내로 덱사메타손 삽입물이 주입된 후 3개월 동안 중심망막두께가 현저히 호전되었으나 백내장 진행으로 수술을 하게 된 증례를 보고하였다. Poornachandra et al [9]은 수정체 내로 덱사메타손 삽입물이 주입된 후 10개월이 지났으나 중심망막두께가 호전된 상태를 유지하고, 백내장도 진행되지 않은 증례를 보고하였다. Regan et al [10]은 당뇨황반부종 환자에서 수정체 내로 덱사메타손 삽입물이 주입되고 1년 동안 황반부종이 호전된 상태로 유지되었으며, 백내장수술 2개월 후까지 황반부종이 악화되지 않은 증례를 보고하였다. Clemente-Tomás et al [11]은 망막분지정맥폐쇄에 동반된 황반부종 환자에서 수정체 내로 덱사메타손 삽입물이 주입되고 약 18개월 후 백내장의 급속한 진행으로 수정체유화술 및 인공수정체삽입술을 시행한 증례를 보고하였다. 이 증례에서 약 18개월 동안 경과 관찰 중 백내장의 진행으로 인한 시력저하는 있었지만 빛간섭단층촬영을 통해 측정한 중심망막두께는 수정체 내에 삽입물이 위치한 상태에서도 계속 정상을 유지하였다. 그들은 덱사메타손 삽입물이 후낭파열 부위를 통해 유리체와 접촉하고 있어 치료 효과를 나타냈을 것이라고 분석하였다. 따라서 전안부 염증이 없고, 안압이 정상 범위 내에 있고, 삽입물이 시축에 영향을 주지 않고, 백내장이 진행하지 않는다면 경과 관찰을 할 수 있다고 하였다[11]. 백내장수술 후 황반부종에 대해 Baker et al [14]은 당뇨황반부종 치료 병력이 있는 환자에서 백내장수술 후 4주에는 13%, 16주에는 25%까지 황반부종이 발생함을 보고하였다.
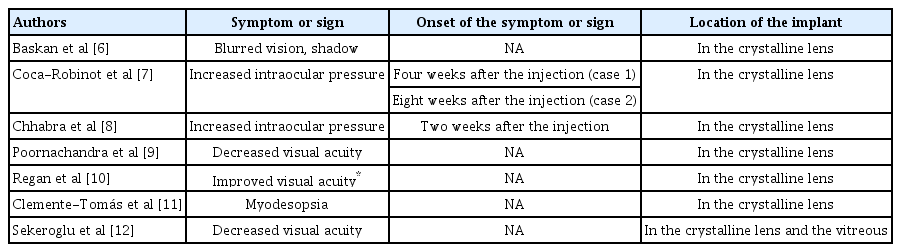
본 증례에서는 덱사메타손 삽입물이 시축을 가리고 있었고, 환자가 시력저하로 인한 불편감을 호소하여 증상이 발생한 지 약 7주 후에 수술을 하게 되었다. 수술 전 경도의 미만성 황반부종이 있었고 약 7주간 비슷한 상태를 유지하였으나 수술 1개월 후 급격히 황반부종이 악화되었다. 이는 Clemente-Tomás et al [11]의 가설대로 수술 전까지 유리체와 접촉된 상태로 효과를 발휘하던 수정체 내 덱사메타손 삽입물이 수술로 제거되면서 황반부종이 악화되었거나, 백내장수술 자체로 인하여 황반부종이 악화되었을 가능성이 있다. 환자는 덱사메타손 삽입물 주입술 후 약 7주 동안 없었던 비문증과 시력저하가 갑자기 나타났다. 백내장수술과 함께 덱사메타손 삽입물을 제거한 후 비문증은 소실되었고 시력은 향상되었기 때문에 지연성으로 환자의 증상이 발현된 것으로 보인다. 따라서 본 증례에서는 앞서 보고된 증례와 비교할 때 덱사메타손 삽입물 주입술 후 지연성으로 환자가 증상을 호소하였다는 점에서 차이가 있다. 국내에서 지연성으로 증상이 발현된 수정체 내 덱사메타손 삽입물에 대한 보고는 본 증례가 처음이다. Sekeroglu et al [12]은 덱사메타손 삽입물의 일부가 수정체 내에 위치하고 일부는 유리체강 내에 위치한 증례를 보고하였다(Table 1). 본 증례에서도 이와 같이 덱사메타손 삽입물의 일부가 수정체에 들어간 후 서서히 중심부로 이동하여 시축을 가리면서 증상이 지연성으로 발현되었을 것으로 추정한다.
결론적으로 덱사메타손 삽입물주입술 중 수정체 내로 덱사메타손 삽입물을 주입하게 되는 경우는 매우 드물지만 시술 중 주의하여야 하며, 지연성으로도 수정체 내 덱사메타손 삽입물로 인한 증상이 발현될 수 있음을 인지할 필요가 있다. 시력저하나 합병증을 동반하지 않는다면 치료적 효과를 기대할 수 있기 때문에 경과 관찰을 할 수 있다. 하지만 환자가 시력저하로 인한 불편감을 호소하거나 백내장, 안압상승, 염증과 같은 합병증이 발생한다면 수술이 필요하다.
Notes
Conflict of Interest
The authors have no conflicts to disclose.
References
Biography
조영채 / Yeong Chae Jo
메리놀병원 안과
Department of Ophthalmology, Maryknoll Medical Center