 |
 |
| J Korean Ophthalmol Soc > Volume 61(8); 2020 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļ░▒ļé┤ņןņĢłņŚÉņä£ ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻĖ░Ļ│äņØĖ ArgosņÖĆ ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁĻĖ░Ļ│äņØĖ IOL Master┬« 500ņØś ņāØņ▓┤Ļ│äņĖĪņ╣śļź╝ ļ╣äĻĄÉĒĢśĻ│Ā, ļ░▒ļé┤ņןņłśņłĀ Ēøä ĻĄ┤ņĀłļĀź ņśłņĖĪņØś ņĀĢĒÖĢņä▒ņØä ļ╣äĻĄÉĒĢ┤ļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
ļ░▒ļé┤ņןņłśņłĀņØä ņ£äĒĢ£ Ļ▓Ćņé¼ļź╝ ļ░øņØĆ 221ņĢłņØä ļīĆņāüņ£╝ļĪ£ ArgosņÖĆ IOL Master┬« 500ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĢłņČĢņןĻĖĖņØ┤(axial length), ņĀäļ░®Ļ╣ŖņØ┤(anterior chamber depth, ACD), Ļ░üļ¦ēĻĄ┤ņĀłļźĀ(K)ņØä ņĖĪņĀĢĒĢśņŚ¼ ļ╣äĻĄÉĒĢśņśĆļŗż. ņłśņłĀ ĒĢ£ ļŗ¼ Ēøä ņŗżņĀ£ ĻĄ┤ņĀłļĀźĻ│╝ ņśłņĖĪĻĄ┤ņĀłļĀźņØä ņØ┤ņÜ®ĒĢ£ ņĀłļīĆĻĄ┤ņĀłņśżņ░©ļź╝ ĻĄ¼ĒĢśņŚ¼ ņłĀ Ēøä ĻĄ┤ņĀł ņśłņĖĪņØś ņĀĢĒÖĢļÅäļź╝ ļ╣äĻĄÉĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
221ņĢł ņżæ 13ņĢłņØĆ IOL Master┬« 500ņ£╝ļĪ£ ņĖĪņĀĢņØ┤ ļÉśņ¦Ć ņĢŖņĢśņ£╝ļéś, ArgosļĪ£ļŖö ņāØņ▓┤Ļ│äņĖĪņØ┤ Ļ░ĆļŖźĒĢśņśĆņ£╝ļ®░, ļæÉ ņןļ╣ä ļ¬©ļæÉņŚÉņä£ ņĖĪņĀĢņØ┤ ļČłĻ░ĆĒĢ£ Ļ▓ĮņÜ░ļŖö 1ņĢłņØ┤ņŚłļŗż. ņĖĪņĀĢņØ┤ ļČłĻ░ĆĒ¢łļŹś 14ņĢłņØä ņĀ£ņÖĖĒĢ£ 207ņĢłņŚÉņä£ ļæÉ ņןļ╣äļĪ£ ņĖĪņĀĢĒĢ£ ņāØņ▓┤Ļ│äņĖĪĻ░ÆļōżņØĆ ĻĖēļé┤ņāüĻ┤ĆĻ│äņłś(intraclass correlation coefficient, ICC) ļ░Å Bland-Altman plotņŚÉņä£ ļåÆņØĆ ņØ╝ņ╣śļÅäļź╝ ļ│┤ņśĆļŗż(ICC AXL=0.999, ACD=0.975, K=0.978). ņĢłņČĢņןĻĖĖņØ┤ ļ░Å ņĀäļ░®Ļ╣ŖņØ┤ļŖö ArgosļĪ£ ņĖĪņĀĢĒĢ£ Ļ▓ĮņÜ░Ļ░Ć IOL Master┬« 500ņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ Ļ▓ĮņÜ░ļ│┤ļŗż ņ£ĀņØśĒĢśĻ▓ī ĻĖĖņŚłņ£╝ļéś(p=0.005, p=0.000) Ļ░üļ¦ēĻĄ┤ņĀłļźĀņØĆ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż(p=0.647). ļæÉ ņןļ╣äņØś ņłśņłĀ Ēøä ĻĄ┤ņĀłļĀź ņśłņĖĪņŚÉ ļīĆĒĢ£ ņĀłļīĆĻĄ┤ņĀłņśżņ░©ļŖö ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż(p=0.087).
ABSTRACT
Purpose
To compare the ocular biometry and postoperative refractive outcomes using two devices; the swept-source optical coherence tomography biometer (Argos) versus the partial coherence interferometer (IOL Master® 500, Carl Zeiss Meditec AG, Jena, Germany).
Methods
The axial length (AL), anterior chamber depth (ACD) and keratometry (K) in 221 cataract eyes were measured with Argos and IOL Master® 500. One month after surgery, refraction of the respective eyes was conducted and the mean absolute error (MAE) calculated for analysis of the refractive outcomes.
Results
Measurement was not possible in 13 eyes with the IOL Master® 500 but was possible with Argos. Measurement was not possible in one eye with either biometer. Agreement in measured ocular biometry between the two devices by intraclass correlation coefficient (ICC) and Bland-Altman plot (ICC AXL = 0.999, ACD = 0.975, K = 0.978) was excellent. The AL and ACD measured with Argos were significantly longer than measured with IOL Master® 500 (p = 0.005, p = 0.000). The MAE showed no significant difference between the Argos and IOL Master® 500 (p = 0.087).
ļŗżņ┤łņĀÉņØĖĻ│ĄņłśņĀĢņ▓┤ ļ░Å ļé£ņŗ£ĻĄÉņĀĢņØĖĻ│ĄņłśņĀĢņ▓┤ ļō▒ņØ┤ ļīĆņżæĒÖöļÉśļ®┤ņä£ ļ░▒ļé┤ņןņłśņłĀņØĆ ļŗ©ņł£ĒĢ£ ļ░▒ļé┤ņןņØś ņĀ£Ļ▒░Ļ░Ć ņĢäļŗī ĻĄ┤ņĀłĻĄÉņĀĢ ņłśņłĀļĪ£ņä£ ļ░øņĢäļōżņŚ¼ņ¦ĆĻ│Ā ņ׳ņ£╝ļ®░, ņØ┤ņŚÉ ļö░ļØ╝ ļŹö ņĀĢĒÖĢĒĢ£ ņāØņ▓┤Ļ│äņĖĪņØä ņ£äĒĢ£ ņāłļĪ£ņÜ┤ ņĖĪņĀĢ ļ░®ļ▓Ģ ļ░Å ņןļ╣äļōżņØś Ļ┤Ćņŗ¼ļÅäĻ░Ć ļåÆņĢäņ¦ĆĻ│Ā ņ׳ļŗż.
ņØĖĻ│ĄņłśņĀĢņ▓┤ņØś ļÅäņłś Ļ│äņé░ņØä ņ£äĒĢ┤ ĻĖ░ņĪ┤ņŚÉ ļäÉļ”¼ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖö ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁ(partial coherence interferometry)ņØś ņøÉļ”¼ļź╝ ņØ┤ņÜ®ĒĢ£ IOL Master┬« 500 (Carl Zeiss, Jena, Germany)ņØĆ 780 nm ĒīīņןņØś ņĀüņÖĖņäĀ Ļ┤æņäĀņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĢłņČĢņן ĻĖĖņØ┤, Ļ░üļ¦ēĻĄ┤ņĀłļźĀ, ņĀäļ░® Ļ╣ŖņØ┤ ļō▒ņØś ņāØņ▓┤ņĀĢļ│┤ļź╝ Ļ│äņĖĪĒĢśĻ│Ā, ņØ┤ļź╝ ĻĖ░ļ░śņ£╝ļĪ£ ĒĢśņŚ¼ ņØĖĻ│ĄņłśņĀĢņ▓┤ ļÅäņłśļź╝ Ļ│äņé░ĒĢ£ļŗż[1,2]. ņĄ£ĻĘ╝ ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│ä(swept source optical coherence tomography)ņŚÉ ĻĖ░ļ░śĒĢ£ ņןļ╣äļōżņØ┤ ņåīĻ░£ļÉśņ¢┤ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖöļŹ░, ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļŖö 1,050 nmļīĆ(70 nm bandwidth)ņØś Ēīīņן ņśüņŚŁņØä ņØ┤ņÜ®ĒĢ©ņ£╝ļĪ£ņŹ© ļåÆņØĆ Ēł¼Ļ│╝ņä▒ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĢłĻĄ¼ ĒøäļČĆ ĻĄ¼ņĪ░ļ¼╝ņŚÉ ļīĆĒĢ£ ļŹö ņĀĢĒÖĢĒĢ£ ņĀĢļ│┤ļź╝ ņ¢╗Ļ│Ā ļ¦żņ¦łĒś╝Ēāüņ£╝ļĪ£ ņØĖĒĢ£ ņé░ļ×ĆņŚÉ ņśüĒ¢źņØä ļŹ£ ļ░øļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[3,4]. Argos (Suntec, Inc., Nagoya, Japan)ļŖö ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äņŚÉ ĻĖ░ļ░śĒĢ£ ņןļ╣äļĪ£ņä£ ņĢłņČĢņןņØś ĻĖĖņØ┤ļź╝ Ļ░ü ļČäņĀłņŚÉ ļČĆĒĢ®ĒĢśļŖö ĻĄ┤ņĀłņ¦Ćņłś(refractive index)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņĀłņØś ĻĖĖņØ┤ļź╝ ņĖĪņĀĢĒĢśĻ│Ā Ļ░üĻ░üņØś ĻĖĖņØ┤ļź╝ ļŹöĒĢśļŖö ļ░®ņŗØņ£╝ļĪ£ Ļ│äņé░ĒĢśņŚ¼ ņĀĢĒÖĢņä▒ņØä ļåÆņØ┤Ļ│Ā ņ׳ņ£╝ļ®░, ņØ┤ņŚÉ ļö░ļØ╝ Barrett universal formula ļō▒ ņĄ£ĻĘ╝ ļ░£Ēæ£ļÉ£ ņŚ¼ļ¤¼ Ļ░Ćņ¦Ć 4ņäĖļīĆ ņØĖĻ│ĄņłśņĀĢņ▓┤ Ļ│äņé░ņŗØņØä ņé¼ņÜ®ĒĢĀ ņłś ņ׳ļŖö ņןņĀÉņØ┤ ņ׳ļŖö ņןļ╣äļĪ£ ņåīĻ░£ļÉ£ ļ░ö ņ׳ļŗż[5].
ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ IOL Master┬« 700 (Carl Zeiss) [6,7], OA-2000 (Tomey, Nagoya, Japan) [8], Argos [4,5] ļō▒Ļ│╝ ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁ ņøÉļ”¼ļź╝ ņØ┤ņÜ®ĒĢ£ IOL Master┬« 500ņØś ņāØņ▓┤Ļ│äņĖĪĻ░ÆņØä ļ╣äĻĄÉĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż. ļŗżļ¦ī, ņĢäņ¦ü ĻĄŁļé┤ņŚÉļŖö ArgosņÖĆ IOL Master┬« 500ņØś ņāØņ▓┤Ļ│äņĖĪĻ░ÆņØä ļ╣äĻĄÉĒĢśĻ│Ā ņłśņłĀ Ēøä ĻĄ┤ņĀłļĀź ņśłņĖĪņØś ņĀĢĒÖĢļÅäļź╝ ļ╣äĻĄÉĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ļ│┤Ļ│ĀļÉ£ ļ░ö ņŚåļŗż. ņØ┤ņŚÉ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ArgosņÖĆ IOL Master┬« 500ņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņן ĻĖĖņØ┤, ņĀäļ░®Ļ╣ŖņØ┤, Ļ░üļ¦ēĻ│ĪļźĀņØś ņØ╝ņ╣śļÅäļź╝ ļČäņäØĒĢśĻ│Ā, ņĢäņÜĖļ¤¼ ņłśņłĀ Ēøä ņŗżņĀ£ĻĄ┤ņĀłļĀźĻ│╝ ņśłņĖĪĻĄ┤ņĀłļĀźņØś ņ░©ņØ┤ņŚÉ ļīĆĒĢ£ ļæÉ ņןļ╣ä Ļ░äņØś ņĀĢĒÖĢļÅäļź╝ ļ╣äĻĄÉĒĢśĻ│Āņ×É ĒĢśņśĆļŗż.
2018ļģä 4ņøöĻ│╝ 2018ļģä 10ņøöņŚÉ ņĀ£ņŻ╝ļīĆĒĢÖļ│æņøÉ ņĢłĻ│╝ņŚÉ ļé┤ņøÉĒĢ£ ĒÖśņ×É ņżæ ļ░▒ļé┤ņןņłśņłĀņØä ņøÉĒĢśņŚ¼ ļ░▒ļé┤ņןņłśņłĀņØä ņ£äĒĢ£ ņĢłĻĄ¼ ņāØņ▓┤ Ļ▓Ćņé¼ ņ¦äĒ¢ēņŚÉ ļÅÖņØśĒĢśņśĆļŹś ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ĒøäĒ¢źņĀü ņØśļ¼┤ĻĖ░ļĪØ ļČäņäØņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ļ░▒ļé┤ņןņłśņłĀņØä ņ£äĒĢ£ ņØ╝ļ░śĻ▓Ćņé¼ ņżæ ņāØņ▓┤Ļ│äņĖĪņØä ņ£äĒĢ£ Ļ▓Ćņé¼ļĪ£ IOL Master┬« 500Ļ│╝ Argosļź╝ Ļ░ÖņØĆ ļéĀ ļÅÖņØ╝ĒĢ£ ņĪ░Ļ▒┤ņ£╝ļĪ£ ņ┤¼ņśüĒĢśņśĆĻ│Ā, ņ¢æņĢł ļ¬©ļæÉ Ļ▓Ćņé¼ĒĢśņśĆļŗż. ņØ┤ņĀäņŚÉ ļ░▒ļé┤ņןņłśņłĀņØä ļ░øņØĆ ĒÖśņ×Éļéś Ļ░üļ¦ēĒś╝ĒāüņØ┤ ņŗ¼ĒĢ£ Ļ▓ĮņÜ░, ļ╣øņØ┤ Ļ▒░ņØś ĒåĄĻ│╝ĒĢśņ¦Ć ļ¬╗ĒĢśļ”¼ļØ╝ ĒīÉļŗ©ļÉśļŖö ņŗ¼ĒĢ£ Ļ│╝ņłÖ ļ░▒ļé┤ņןņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░, ļśÉļŖö ļ¦Øļ¦ē ņ¦łĒÖśņØä Ļ░¢Ļ│Ā ņ׳ļŖö Ļ▓ĮņÜ░ļŖö ļīĆņāüņŚÉņä£ ņĀ£ņÖĖĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĒŚ¼ņŗ▒ĒéżņäĀņ¢ĖņØä ņżĆņłśĒĢśņśĆņ£╝ļ®░, ņĀ£ņŻ╝ļīĆĒĢÖļ│æņøÉ ņØśĒĢÖņŚ░ĻĄ¼ņŗ¼ņØśņ£äņøÉĒÜī(Institutional Review Board, IRB)ņØś ņŖ╣ņØĖĒĢśņŚÉ ņ¦äĒ¢ēļÉśņŚłļŗż(ņŖ╣ņØĖ ļ▓łĒśĖ: 2019-09-006).
ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ņä▒ļ│ä, ņŚ░ļĀ╣, Ļ│╝Ļ▒░ļĀźņØä ņĪ░ņé¼ĒĢśĻ│Ā, the Lens Opacities Classification System (LOCS) III [9]ņŚÉ ļö░ļźĖ ļ░▒ļé┤ņן ņĀĢļÅäļź╝ ņĪ░ņé¼ĒĢśņśĆļŗż. ļæÉ ņןļ╣äņØś ļ╣äĻĄÉļź╝ ņ£äĒĢ£ ņāØņ▓┤Ļ│äņĖĪņØĆ ņĢłņČĢņןĻĖĖņØ┤(axial length, AL), ņĀäļ░®Ļ╣ŖņØ┤(anterior chamber depth, ACD), ĒÅēĻĘĀ Ļ░üļ¦ēĻ│ĪļźĀ(Keratometry, K)ņØä ņØ┤ņÜ®ĒĢśņśĆĻ│Ā, ņØ┤ļōżņØś ņØ╝ņ╣śļÅäļź╝ ļČäņäØĒĢśņśĆļŗż. ņØ┤Ēøä ņŗżņĀ£ļĪ£ ļ░▒ļé┤ņןņłśņłĀņØä ņ¦äĒ¢ēĒĢ£ ĒÖśņ×Éļōż ņżæ ņłśņłĀ Ēøä 1Ļ░£ņøöņ¦Ė ĻĄ┤ņĀłĻ▓Ćņé¼ļź╝ ņ¦äĒ¢ēĒĢśņŚ¼ ĻĄ¼ļ®┤(spherical)Ļ░ÆņŚÉ ņøÉņŻ╝(cylindrical)Ļ░ÆņØś ņĀłļ░śņØä ļŹöĒĢ£ ņŗżņĀ£ ĻĄ┤ņĀłņśżņ░©(refractive error, RE)ļź╝ ĻĄ¼ĒĢśĻ│Ā, ļæÉ ņןļ╣äņØś ņśłņĖĪĻĄ┤ņĀłņśżņ░©ņÖĆ ņŗżņĀ£ĻĄ┤ņĀłņśżņ░© ņ░©ņØ┤ņØś ņĀłļīĆĻ░Æ(ņĀłļīĆņśżņ░© = |real RE - predictive RE|)ņØś ĒÅēĻĘĀ(mean absolute error, MAE)ņØä Ļ░üĻ░ü ĻĄ¼ĒĢśņŚ¼ ļ╣äĻĄÉĒĢśņśĆļŗż. ņśłņĖĪ ĻĄ┤ņĀłĻ░ÆņØĆ Haigis Ļ│ĄņŗØĻ│╝ Tecnis┬« ZCB00 (AMO, Santa Ana, CA, USA)ņØä ĻĖ░ņżĆņ£╝ļĪ£ Ļ│äņé░ĒĢśņśĆļŖöļŹ░, ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀäļ░®Ļ╣ŖņØ┤ļź╝ ļæÉ ņןļ╣äņØś Ļ│äņĖĪ ļ╣äĻĄÉĻ░Æņ£╝ļĪ£ ņØ┤ņÜ®ĒĢśņśĆĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ļź╝ ļ░śņśüĒĢśļŖö Haigis Ļ│ĄņŗØņØä ņśłņĖĪ ĻĄ┤ņĀłĻ░ÆņØä ĻĄ¼ĒĢśļŖö ļŹ░ ņØ┤ņÜ®ĒĢśņśĆĻ│Ā, ņĢłĻĄ¼ņØś ĒŖ╣ņłśņä▒ņŚÉ ņØśĒĢ┤ ņŗżņĀ£ ņłśņłĀņŚÉ ļŗżļźĖ Ļ│ĄņŗØĻ░ÆņØä ņ░ĖĻ│ĀĒĢśņŚ¼ ņłśņłĀĒĢśņśĆļŹöļØ╝ļÅä ņłśņłĀ Ēøä ĻĄ┤ņĀłļĀźņØä ņśłņĖĪĒĢ£ Ļ░ÆņØĆ ļÅÖņØ╝ĒĢśĻ▓ī Haigis Ļ│ĄņŗØņØä ņØ┤ņÜ®ĒĢ£ Ļ░Æņ£╝ļĪ£ ļ╣äĻĄÉĒĢśņśĆļŗż.
ĒåĄĻ│äļČäņäØņØĆ SPSS statistics ver. 18.0 (SPSS Inc., Chicago, IL, USA)ņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, ĻĖēļé┤ņāüĻ┤ĆĻ│äņłś(intraclass correlation coefficient, ICC)ņÖĆ Bland-Altman plotņØä ĻĄ¼ĒĢśņŚ¼ ņØ╝ņ╣śļÅäļź╝ ļČäņäØĒĢśņśĆļŗż. Ļ░ü Ļ│äņĖĪĻ░ÆņØ┤ ļæÉ ņןļ╣äņŚÉņä£ ņ░©ņØ┤Ļ░Ć ņ׳ļŖöņ¦ĆņŚÉ ļīĆĒĢ┤ ļīĆņØæĒæ£ļ│Ė t-Ļ▓ĆņĀĢņØä ņØ┤ņÜ®ĒĢśņśĆĻ│Ā, Ļ│äņĖĪĻ░ÆņØś Ļ▓ĮĒ¢źņä▒ņŚÉ ļīĆĒĢ┤ņä£ļŖö Pearson ņāüĻ┤ĆĻ│äņłśļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż. ņśłņĖĪĻ░Æ ņĀłļīĆņśżņ░©ņØś ĒÅēĻĘĀ(MAE)ņØś ļ╣äĻĄÉļŖö Ļ░ü ņןļ╣äņŚÉņä£ ņśłņĖĪĒĢ£ Ļ░ÆņØś ņśżņ░©Ļ░Ć ņ¢┤ļŖÉ ņןļ╣äņŚÉņä£ ļŹö 0ņŚÉ Ļ░ĆĻ╣īņÜ┤ņ¦Ćļź╝ Ļ▓ĆņĀĢĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ļÅģļ”ĮĒæ£ļ│Ė t-Ļ▓ĆņĀĢņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. ĒåĄĻ│äņĀü ņ£ĀņØśņłśņżĆņØĆ 0.05ļĪ£ ĒĢśņśĆļŗż.
ņ┤Ø 129ļ¬ģ 221ņĢłņŚÉ ļīĆĒĢ┤ ļČäņäØĒĢśņśĆļŗż. ļīĆņāüņØś ĒÅēĻĘĀ ņŚ░ļĀ╣ņØĆ 68.9 ┬▒ 12.1ņäĖņØ┤Ļ│Ā, ļé©ņ×É 58ļ¬ģ, ņŚ¼ņ×É 71ļ¬ģņØ┤ņŚłļŗż. 221ņĢł ņżæ ArgosņŚÉņä£ ņĖĪņĀĢņØ┤ Ļ░ĆļŖźĒ¢łņ¦Ćļ¦ī IOL Master┬« 500ņŚÉņä£ļŖö ņĖĪņĀĢņØ┤ ļÉśņ¦Ć ņĢŖņĢśļŹś ļłłņØĆ 13ņĢłņØ┤ņŚłņ£╝ļéś, IOL Master┬« 500ņŚÉņä£ ņĖĪņĀĢņØ┤ Ļ░ĆļŖźĒ¢łņ£╝ļéś ArgosņŚÉņä£ ņĖĪņĀĢņØ┤ ļÉśņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ļŖö ņŚåņŚłļŗż. ļæÉ ņןļ╣äņŚÉņä£ ļ¬©ļæÉ ņĖĪņĀĢņØ┤ ļÉśņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ļŖö 1ņĢłņØ┤ņŚłļŗż(Table 1).
ļæÉ ņןļ╣ä ļ¬©ļæÉ ņĖĪņĀĢņØ┤ Ļ░ĆļŖźĒ¢łļŹś 207ņĢłņØś ņĢłņČĢņןņØś ĻĖĖņØ┤ņØś ĒÅēĻĘĀņØĆ ArgosņŚÉņä£ 23.86 ┬▒ 1.32 mm, IOL Master┬« 500ņŚÉņä£ 23.84 ┬▒ 1.35 mmļĪ£ ņ£ĀņØśĒĢśĻ▓ī ArgosņŚÉņä£ ĒÅēĻĘĀ 0.02 mmĻ░Ćļ¤ē ļŹö ĻĖĖĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż(p=0.005). ņĀäļ░®Ļ╣ŖņØ┤ņØś ĒÅēĻĘĀņØĆ ArgosņŚÉņä£ 3.29 ┬▒ 0.45 mm, IOL Master┬« 500ņŚÉņä£ 3.20 ┬▒ 0.45 mmļĪ£ ņ£ĀņØśĒĢśĻ▓ī ArgosņŚÉņä£ ļŹö ĻĖĖĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż(p=0.000). Ļ░üļ¦ēĻĄ┤ņĀłļźĀņØś ĒÅēĻĘĀņØĆ ArgosņŚÉņä£ 43.72 ┬▒ 1.42 diopters (D), IOL Master┬« 500ņŚÉņä£ 43.74 ┬▒ 1.49 DļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(p=0.647) (Table 2).
ļæÉ ņןļ╣äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪņØś ĻĖēļé┤ņāüĻ┤ĆĻ│äņłśļŖö ņĢłņČĢņןĻĖĖņØ┤ 0.999, ņĀäļ░®Ļ╣ŖņØ┤ 0.975, Ļ░üļ¦ēĻ│ĪļźĀ 0.978ņØ┤ņŚłĻ│Ā(Table 2), Bland-Altman plotņŚÉņä£ļÅä Ļ│äņĖĪĻ░ÆļōżņØś ļåÆņØĆ ņØ╝ņ╣śļÅäļź╝ ļ│┤ņśĆļŗż(Fig. 1-3). ĒŖ╣ņ¦ĢņĀüņ£╝ļĪ£ ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć ņ¦¦ņØäņłśļĪØ ArgosļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć IOL Master┬« 500ņŚÉņä£ ņĖĪņĀĢĒĢ£ Ļ▓āļ│┤ļŗż ļŹö ĻĖĖĻ▓ī ņĖĪņĀĢļÉśņŚłļŗżļŖö Ļ▓āņØĖļŹ░(ņāüĻ┤ĆĻ│äņłś: -0.411, p=0.000), ņäĀĒśĢĒÜīĻĘĆņŗØņØĆ Y=-0.019X +0.468 (╔ø=0.468, p=0.000; ├¤=-0.019, p=0.000)ņ£╝ļĪ£, ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć 24.63 mm ļ»Ėļ¦īņØ╝ ļĢīļŖö ArgosĻ░Ć ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØ┤ IOL Master┬« 500ņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןļ│┤ļŗż ņĢĮĻ░ä ĻĖĖĻ▓ī ņĖĪņĀĢļÉśĻ│Ā, 24.63 mm ņØ┤ņāüņØ╝ ļĢīļŖö ArgosņŚÉņä£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØ┤ IOL master 500ņŚÉņä£ ņĖĪņĀĢĒĢ£ Ļ▓āļ│┤ļŗż ņĢĮĻ░ä ņ¦¦Ļ▓ī ņĖĪņĀĢļÉśļŖö Ļ▓ĮĒ¢źņØ┤ ņ׳ņŚłļŗż(Fig. 1). ņŗżņĀ£ļĪ£ ļ░▒ļé┤ņןņłśņłĀņØä ņ¦äĒ¢ēĒĢ£ Ļ▓ĮņÜ░ ņżæ Tecnis┬« ZCB00 (AMO)ņØä ņéĮņ×ģĒĢ£ ļłłņØ┤ 126ņĢłņ£╝ļĪ£ MAEļŖö ArgosņŚÉņä£ 0.531 ┬▒ 0.524 D, IOL Master┬« 500ņŚÉņä£ 0.477 ┬▒ 0.450 DņśĆĻ│Ā, ļæÉ Ļ░Æ Ļ░äņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(p=0.087).
ņĢłņČĢņןĻĖĖņØ┤ņØś ĒÜŹļōØļźĀ(acquisition rate)ņØĆ ArgosņŚÉņä£ 99.5% (220ņĢł/221ņĢł), IOL Master┬« 500ņŚÉņä£ 94.1% (208ņĢł/221ņĢł)ņØ┤ņŚłļŗż. ņĢłņČĢņןņØś ĻĖĖņØ┤, ņĀäļ░®Ļ╣ŖņØ┤, Ļ░üļ¦ēĻ│ĪļźĀĻ░ÆņØĆ ļ¬©ļæÉ ļæÉ ņןļ╣äņŚÉņä£ ļåÆņØĆ ņØ╝ņ╣śņ£©ņØä ļ│┤ņśĆņ£╝ļéś ņĢłņČĢņןņØś ĻĖĖņØ┤ļŖö ļ»ĖņäĖĒĢ£ ņ░©ņØ┤ņ¦Ćļ¦ī ArgosņŚÉņä£ ņĖĪņĀĢĒĢ£ Ļ░ÆņØ┤ ņ£ĀņØśļ»ĖĒĢśĻ▓ī ļŹö ĻĖĖņŚłĻ│Ā, ņĀäļ░®Ļ╣ŖņØ┤ ļśÉĒĢ£ ArgosņŚÉņä£ ņĖĪņĀĢĒĢ£ Ļ░ÆņØ┤ IOL Master┬« 500ņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ Ļ░Æļ│┤ļŗż ņ£ĀņØśļ»ĖĒĢśĻ▓ī ĻĖĖĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż. Ļ░üļ¦ēĻ│ĪļźĀņØĆ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż. ĒŖ╣Ē׳ ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć 24.63 mmļ│┤ļŗż ĻĖĖņłśļĪØ ArgosņŚÉņä£ ņĖĪņĀĢļÉ£ ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć IOL Master┬« 500ņŚÉņä£ ņĖĪņĀĢļÉ£ Ļ░ÆņŚÉ ļ╣äĒĢ┤ ļŹö ņ¦¦Ļ▓ī ņĖĪņĀĢļÉśļŖö Ļ▓ĮĒ¢źņØ┤ ņ׳ņŚłļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĒÖśņ×ÉļōżņØś ĒÅēĻĘĀ ņĢłņČĢņןņØĆ 23.85 mmļĪ£, ļæÉ ņןļ╣äņØś ņĢłņČĢņן ņĖĪņĀĢņ╣śņØś ļČäĻĖ░ņĀÉņØ┤ ļÉśļŖö 24.63 mmļ│┤ļŗż ļŗżņåī ņ¦¦ņĢśĻĖ░ ļĢīļ¼ĖņŚÉ, ArgosļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØś ĒÅēĻĘĀ ĻĖĖņØ┤Ļ░Ć IOL Master┬« 500ņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØś ĒÅēĻĘĀ ĻĖĖņØ┤ļ│┤ļŗż 0.02 mm ĻĖĖĻ▓ī ņĖĪņĀĢļÉ£ Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ņłśņłĀ Ēøä 1Ļ░£ņøöņ¦ĖņŚÉ ņĖĪņĀĢĒĢ£ ĻĄ┤ņĀłļĀźĻ│╝ ņłśņłĀ ņĀäņŚÉ ņśłņĖĪĒĢ£ ĻĄ┤ņĀłļĀź ņ░©ņØ┤ņØś ĒÅēĻĘĀņØä ļ╣äĻĄÉĒ¢łņØä ļĢī ArgosļĪ£ ņśłņĖĪĒĢ£ Ļ░ÆņØ┤ IOL Master┬« 500ņ£╝ļĪ£ ņśłņĖĪĒĢ£ Ļ░ÆĻ│╝ ņŗżņĀ£ Ļ░ÆĻ│╝ņØś ņśżņ░©ļŖö ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż.
ņāØņ▓┤Ļ│äņĖĪ, ĒŖ╣Ē׳ ņĢłņČĢņןĻĖĖņØ┤ņØś ĒÜŹļōØļźĀņØĆ ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņןļ╣äņŚÉņä£ 92.5-100%, ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņןļ╣äņŚÉņä£ 64-87.3%ļĪ£ ļŗżņ¢æĒĢśĻ▓ī ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ņ£╝ļ®░[4,5,8,10], ņ░©ņØ┤Ļ░Ć Ēü░ ņØ┤ņ£ĀļŖö ļīĆņāüņØś ņäĀņĀĢ ļ░Å ņĀ£ņÖĖ ņĪ░Ļ▒┤ņØ┤ Ļ░ü ņŚ░ĻĄ¼ļ¦łļŗż ļŗżļź┤ĻĖ░ ļĢīļ¼ĖņØĖļŹ░, ņØ┤ļ¤░ ņØ┤ņ£Āļź╝ Ļ░ÉņĢłĒĢśļŹöļØ╝ļÅä ļīĆņ▓┤ņĀüņ£╝ļĪ£ ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņןļ╣äņŚÉņä£ ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņןļ╣äļ│┤ļŗż ņøöļō▒Ē׳ ļåÆĻ▓ī ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳Ļ│Ā, ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļśÉĒĢ£ Argosļź╝ ņØ┤ņÜ®Ē¢łņØä ļĢī ĒÜŹļōØļźĀņØ┤ ļåÆņĢśļŗż. ļæÉ ņןļ╣ä ļ¬©ļæÉņŚÉņä£ Ļ░ÆņØä ņ¢╗ļŖö ļŹ░ ņŗżĒī©ĒĢ£ 1ņĢłņØś Ļ▓ĮņÜ░ ņłśņĀĢņ▓┤Ļ▓ēņ¦łĻ│╝ ĒĢĄņØ┤ ļ¬©ļæÉ LOCS III [9] ĻĖ░ņżĆņ£╝ļĪ£ 4ļŗ©Ļ│ä ņØ┤ņāüņØś ņŗ¼ĒĢ£ ļ░▒ļé┤ņן ņāüĒā£ņśĆļŗż. ArgosņŚÉņä£ļŖö Ļ░ÆņØä ņ¢╗ļŖö ļŹ░ņŚÉ ņä▒Ļ│ĄĒĢśņśĆņ£╝ļéś IOL Master┬« 500ņŚÉņä£ļŖö ņŗżĒī©Ē¢łļŹś 13ņĢłņØä ņé┤ĒÄ┤ļ│┤ļ®┤ ĒøäļéŁĒĢś ļ░Å ņĀäļéŁĒĢśļ░▒ļé┤ņןņØ┤ ņŗ¼Ē¢łļŹś Ļ▓ĮņÜ░Ļ░Ć 10ņĢłņØ┤ņŚłĻ│Ā, ļéśļ©Ėņ¦Ć 3ņĢłņØĆ Ļ▓ēņ¦ł ļśÉļŖö ĒĢĄ ļ░▒ļé┤ņןņØ┤ LOSC III ĻĖ░ņżĆ 3ļŗ©Ļ│ä ņØ┤ņāüņØś ņŗ¼ĒĢ£ ļ░▒ļé┤ņןņØ┤ņŚłļŗż. Ļ░üļ¦ēĒś╝Ēāü, ļ░▒ļé┤ņן, ņ£Āļ”¼ņ▓┤Ēś╝Ēāü ļō▒ņØś ļ¦żņ▓┤ Ēś╝ĒāüņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ņŚÉļÅä 1,050 nm ĒīīņןļīĆļź╝ ņØ┤ņÜ®ĒĢ£ ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļŖö ĻĖ░ņĪ┤ņØś 800 nm ĒīīņןļīĆļź╝ ņØ┤ņÜ®ĒĢ£ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(frequency domain optical coherence tomography)ļ│┤ļŗż ļŹö ņÜ░ņłśĒĢ£ Ēł¼Ļ│╝ņä▒Ļ│╝ ņśüņāüņØś ņ¦łņØä ņĀ£Ļ│ĄĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[11]. ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│ä, ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁĻ│ä, ņĀĆĻ░äņäŁņä▒ļ░śņé¼Ļ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪņןļ╣äļź╝ ļ╣äĻĄÉĒĢ£ Shammas et al [4]ņØś ņŚ░ĻĄ¼ņŚÉļÅä Ļ│╝ņłÖļ░▒ļé┤ņן(white cataract)ņØä Ļ░Ćņ¦ä ļæÉ ņ”ØļĪĆņŚÉņä£ļŖö ņäĖ ņןļ╣ä ļ¬©ļæÉ ņĖĪņĀĢ ļČłĻ░ĆĒĢśņśĆņ¦Ćļ¦ī, 5ļŗ©Ļ│äņØś ĒĢĄļ░▒ļé┤ņןĻ│╝ ĒøäļéŁĒĢśļ░▒ļé┤ņןņØ┤ ļÅÖļ░śļÉ£ ņ”ØļĪĆļōżĻ│╝ 4ļŗ©Ļ│äņØś ņłśņĀĢņ▓┤Ļ▓ēņ¦łļ│ĆĒÖöņÖĆ 3ļŗ©Ļ│äņØś ĒøäļéŁĒĢśļ░▒ļé┤ņןņØ┤ ļÅÖļ░śļÉ£ ļ¬ć Ļ░£ņØś ņ”ØļĪĆņŚÉņä£ ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁĻ│ä ļ░Å ņĀĆĻ░äņäŁņä▒ļ░śņé¼Ļ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪņןļ╣äļŖö ņĢłņČĢņןĻĖĖņØ┤ļź╝ ņĖĪņĀĢĒĢĀ ņłś ņŚåņŚłĻ│Ā, ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪņןļ╣äļŖö ņĢłņČĢņןņØä ņĖĪņĀĢĒĢĀ ņłś ņ׳ņŚłļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.
IOL Master┬« 700, OA-2000, Argos ļō▒ņØś ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪņןļ╣äņÖĆ ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ IOL Master┬« 500ņØś ņāØņ▓┤Ļ│äņĖĪĻ░ÆļōżņØś ņØ╝ņ╣śņ£©ņØĆ ļ¦żņÜ░ ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż[4-8]. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļÅä ļæÉ ņןļ╣äņŚÉņä£ ņĖĪņĀĢĒĢ£ ņāØņ▓┤Ļ│äņĖĪĻ░ÆļōżņØĆ ļ¬©ļæÉ ļåÆņØĆ ņØ╝ņ╣śņ£©ņØä ļ│┤ņśĆņ¦Ćļ¦ī, ļīĆņØæ Ēæ£ļ│Ėņ£╝ļĪ£ ĒÅēĻĘĀņØä ļ╣äĻĄÉĒĢśņśĆņØä ļĢī ņĢłņČĢņןņØś ĻĖĖņØ┤ņÖĆ ņĀäļ░®Ļ╣ŖņØ┤ļŖö ArgosņŚÉņä£ ļŹö ĻĖĖĻ▓ī ņĖĪņĀĢļÉśļŖö Ļ▓░Ļ│╝ļź╝ ņ¢╗ņŚłļŗż. ļśÉ, ĒŖ╣ņ¦ĢņĀüņ£╝ļĪ£ ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć ĻĖĖņłśļĪØ ArgosņŚÉņä£ ņĖĪņĀĢĒĢ£ Ļ░ÆņØ┤ IOL Master┬« 500ļ│┤ļŗż ņ×æĻ▓ī ņĖĪņĀĢņØ┤ ļÉśņŚłļŗż. ņØ┤Ļ▓āņØĆ Higashiyama et al [5]ņØ┤ ļ│┤Ļ│ĀĒĢ£ ļé┤ņÜ®Ļ│╝ ņØ╝ņ╣śĒĢśļŖö ļČĆļČäņ£╝ļĪ£ ņ¦¦ņØĆ ņĢłņČĢņן ĻĘĖļŻ╣(Short AL)Ļ│╝ ņżæĻ░ä ņĢłņČĢņן ĻĘĖļŻ╣(Intermediate AL) ĻĘĖļ”¼Ļ│Ā ĻĖ┤ ņĢłņČĢņן ĻĘĖļŻ╣(Long AL)ņØä ļéśļłäņ¢┤ ņĢłņČĢņן ĻĖĖņØ┤ļź╝ ļ╣äĻĄÉĒ¢łņØä ļĢī Short ALņŚÉņä£ļŖö ArgosļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØś ĒÅēĻĘĀĻ░ÆņØ┤ ļŹö ĻĖĖņŚłņ£╝ļéś, Long ALņŚÉņä£ļŖö ArgosļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņČĢņןņØś ĒÅēĻĘĀĻ░ÆņØ┤ ļŹö ņ¦¦ņĢśļŗż. ArgosļŖö ļäż ļČäņĀł(segment)ņØś ļČäņĀłĻĄ┤ņĀłņ¦Ć ņłś(segmental refractive index)ļź╝ Ļ░üĻ░ü ņĀüņÜ®ĒĢśņŚ¼ ĻĖĖņØ┤ļź╝ ĻĄ¼ĒĢśņŚ¼ ļŹöĒĢśļŖö ļ░®ņŗØņ£╝ļĪ£ ņĢłņČĢņן ĻĖĖņØ┤ļź╝ ņĖĪņĀĢĒĢśņ¦Ćļ¦ī IOL Matser┬« 500ņØĆ ĒĢśļéśņØś ĻĄ┤ņĀłņ¦Ćņłś(single refractive index)ļź╝ ņØ┤ņÜ®ĒĢ£ļŗż. ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņä▒ņØĖņØś ņĢłņČĢņןņØś ĻĖĖņØ┤ņØś ņ░©ņØ┤ļŖö ļīĆļČĆļČä ņ£Āļ”¼ņ▓┤Ļ░ĢņØś ĻĖĖņØ┤ņŚÉņä£ ņ░©ņØ┤Ļ░Ć ļé£ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż[12]. ņ”ē, ņ£Āļ”¼ņ▓┤Ļ░ĢņŚÉ ņĀüņÜ®ļÉśļŖö ĻĄ┤ņĀłņ¦ĆņłśņÖĆ IOL Master┬« 500ņØś ļŗ©ņØ╝ ĻĄ┤ņĀłņ¦Ćņłś ņ░©ņØ┤ņŚÉ ņØśĒĢ┤ ņĢłņČĢņןņØś ĻĖĖņØ┤Ļ░Ć ĻĖĖņ¢┤ņ¦łņłśļĪØ ArgosņŚÉņä£ ņĖĪņĀĢĒĢ£ ĻĖĖņØ┤ļ│┤ļŗż IOL Master┬« 500ņŚÉņä£ ņĖĪņĀĢĒĢ£ ĻĖĖņØ┤Ļ░Ć ļŹö ĻĖĖņ¢┤ņ¦ĆĻ▓ī ļÉśļŖö Ļ▓░Ļ│╝Ļ░Ć ļéśņś© Ļ▓āņØ┤ļØ╝ ņČöņĀĢļÉ£ļŗż. ĻĘĖļ¤¼ļéś ņØ┤ļ¤¼ĒĢ£ Ļ▓░Ļ│╝ļŖö Ļ▓░ĻĄŁ ļæÉ ņןļ╣ä ņżæ ĒĢśļéśņØś ņĢłņČĢņןĻĖĖņØ┤ ņĖĪņĀĢ Ļ▓░Ļ│╝ņØś ņŗĀļó░ļÅäĻ░Ć ļ¢©ņ¢┤ņ¦ĆļŖö Ļ▓āņØä ņØśļ»ĖĒĢśĻ│Ā ņØ┤ļ¤¼ĒĢ£ ņøÉņØĖņŚÉ ļīĆĒĢ£ ĒøäņåŹņŚ░ĻĄ¼ ļ░Å ļ│┤ņÖäņØ┤ ĒĢäņÜöĒĢĀ Ļ▓āņØ┤ļŗż.
ņĀäļ░®Ļ╣ŖņØ┤ļź╝ ņĖĪņĀĢĒĢśļŖö ļ░®ļ▓ĢņŚÉ ņ׳ņ¢┤ IOL Master┬« 500ņØĆ ļČĆļČäĻ▓░ĒĢ®Ļ░äņäŁņØä ņØ┤ņÜ®ĒĢśļŖö Ļ▓āņØ┤ ņĢäļŗī Ļ░üļ¦ēĻ│╝ ņłśņĀĢņ▓┤ņØś ņäĖĻĘ╣ņĪ░ļ¬ģ(lateral slit-illumination)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņāżņ×äĒöīļ¤¼ĻĘĖ ņøÉļ”¼(scheimpflug principle)ļĪ£ ņĀäļ░®Ļ╣ŖņØ┤ļź╝ ņĖĪņĀĢĒĢśļŖö ļ░®ņŗØņØä ņĘ©ĒĢśĻ│Ā ņ׳ļŗż[13]. Akman et al [6]Ļ│╝ Yoo et al [10]ņØś ņŚ░ĻĄ¼ņŚÉņä£ IOL Master┬« 700ņØś ņøÉļ”¼ļŖö ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü ĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĀäļ░®Ļ╣ŖņØ┤ņØś ļŗ©ļ®┤ ņśüņāüņØä ļČäņäØĒĢśļŖö Ļ▓āņ£╝ļĪ£, 1,050 nm ĻĖ┤ Ēīīņן ļĀłņØ┤ņĀĆļź╝ ņé¼ņÜ®ĒĢśļ®░, 6Ļ░£ņØś 0┬░, 30┬░, 60┬░, 90┬░, 120┬░, 150┬░ņØś ĒÜīņĀä ļŗ©ļ®┤ļōżņŚÉņä£ņØś ņĖĪņĀĢņ╣śļź╝ ņ¢╗ĻĖ░ņŚÉ ņĀäļ░®Ļ╣ŖņØ┤Ļ░Ć IOL Master┬« 500ļĪ£ ņĖĪņĀĢĒĢ£ Ļ▓āļ│┤ļŗż ņ£ĀņØśĒĢśĻ▓ī ļŹö ņ¦¦Ļ▓ī ņĖĪņĀĢļÉśņŚłņØīņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. Omoto et al [14]ņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö ArgosņÖĆ IOL Master┬« 700ņØś ņāØņ▓┤Ļ│äņĖĪĻ░ÆĻ│╝ ņłśņłĀ Ēøä ĻĄ┤ņĀłļĀźņØś ņśłņĖĪ ņśżņ░©ļź╝ ļ╣äĻĄÉĒĢśņśĆļŖöļŹ░, ArgosļĪ£ ņĖĪņĀĢĒĢ£ ņĀäļ░®Ļ╣ŖņØ┤Ļ░Ć IOL Master┬« 700ļ│┤ļŗż ņ£ĀņØśĒĢśĻ▓ī ĻĖĖĻ▓ī ņĖĪņĀĢļÉśļŖö Ļ▓āņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņ£äņŚÉņä£ ņ¢ĖĻĖēĒĢ£ ļ░öņÖĆ Ļ░ÖņØ┤ ArgosļŖö ļČäņĀłĻĄ┤ņĀłņ¦Ćņłśļź╝ ņé¼ņÜ®ĒĢśļŖö ļ░śļ®┤ IOL Master┬« 700ņØĆ ļŗ╣ļ¤ēĻĄ┤ņĀłņ¦Ćņłś(equivalent refractive index)ļź╝ ņé¼ņÜ®ĒĢ£ļŗż[14]. Ļ▓░ĻĄŁ ņĀäļ░®Ļ╣ŖņØ┤ņØś ņ░©ņØ┤ļŖö ņĖĪņĀĢļ░®ņŗØĻ│╝ ĻĄ┤ņĀłņ¦ĆņłśņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņČöņĖĪĒĢĀ ņłś ņ׳Ļ│Ā, ArgosņŚÉņä£ļŖö IOL Master┬« 500ņØ┤ļéś 700ļ│┤ļŗż ĻĖĖĻ▓ī ņĖĪņĀĢļÉśĻ│Ā ņ׳ļŗżĻ│Ā ĒīÉļŗ©ĒĢ┤ ļ│╝ ņłś ņ׳ļŗż. ļśÉĒĢ£, ņ£ä ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņżæĻ░äņĢłņČĢņןĻĘĖļŻ╣(Medium ALs; 22.00ŌēżAL<26.00 mm)Ļ│╝ ĻĖ┤ņĢłņČĢņןĻĘĖļŻ╣(Long ALs; ALŌēź26.00 mm)ņ£╝ļĪ£ ļéśļłäņ¢┤ Haigis, HofferQ, SKR/T, Barrett Universal II Ļ│ĄņŗØņŚÉ ļö░ļźĖ ļæÉ ņןļ╣äņØś ņĀłļīĆņśżņ░© ļ░Å ņĀłļīĆņśżņ░©ņØś ĒÅēĻĘĀņØä ļ╣äĻĄÉĒĢśņśĆļŖöļŹ░, ļ¬©ļōĀ Ļ│ĄņŗØņŚÉņä£ ņĀłļīĆņśżņ░©Ļ░ÆņØĆ IOL Master┬« 700Ļ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ArgosņŚÉņä£ ņ£ĀņØśĒĢśĻ▓ī(p<0.001), 0ņŚÉ Ļ░ĆĻ╣īņÜ┤ Ļ░ÆņØä Ļ░ĆņĪīĻ│Ā, ĒŖ╣Ē׳ Long ALsņŚÉņä£ ņĀłļīĆņśżņ░©ņØś ĒÅēĻĘĀ(MAE)ņØĆ HofferQņÖĆ SRK/T Ļ│ĄņŗØĒĢśņŚÉ ņ£ĀņØśĒĢśĻ▓ī ArgosņŚÉņä£ ļŹö ņ×æņĢśļŗż. ņØ┤Ļ▓ā ļśÉĒĢ£ ļČäņĀłĻĄ┤ņĀłņ¦ĆņłśņÖĆ ļŗ╣ļ¤ēĻĄ┤ņĀłņ¦ĆņłśņŚÉ ļö░ļØ╝ ņ£Āļ░£ļÉśļŖö ņ░©ņØ┤ņŚÉ ņØśĒĢ£ Ļ▓░Ļ│╝ļĪ£ ĒĢ┤ņäØĒĢ┤ ļ│╝ ņłś ņ׳Ļ│Ā, ArgosĻ░Ć Ļ▓Įņ¤üļĀź ņ׳ļŖö ņłśņłĀ Ēøä ĻĄ┤ņĀłļĀź ņśłņĖĪņØä ņĀ£Ļ│ĄĒĢśĻ│Ā ņ׳ņØīņØä ļ│╝ ņłś ņ׳ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĒīīņןĻ░Ćļ│Ć ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪĻĖ░(Argos)ļŖö ĻĖ░ņĪ┤ ļČĆļČäĻ▓░ĒĢ® Ļ░äņäŁĻ│äļź╝ ņØ┤ņÜ®ĒĢ£ ņāØņ▓┤Ļ│äņĖĪĻĖ░ļ│┤ļŗż ņĪ░ĻĖł ļŹö ņÜ░ņłśĒĢ£ ĒÜŹļōØļźĀ(99.5% vs. 94.1%)ļź╝ ļ│┤ņśĆļŗż. ļæÉ ņןļ╣äļĪ£ ņĖĪņĀĢĒĢ£ ņāØņ▓┤Ļ│äņĖĪĻ░ÆļōżņØĆ ņä£ļĪ£ ļåÆņØĆ ņØ╝ņ╣śļÅäļź╝ ļ│┤ņśĆĻ│Ā, ļśÉĒĢ£ ĒåĄĻ│äņĀüņ£╝ļĪ£ ļÅÖļō▒ĒĢśļ®░ ņÜ░ņłśĒĢ£ ņłśņłĀ Ēøä ĻĄ┤ņĀłņśłņĖĪļĀźņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. ĻĘĖļ¤¼ļéś ņĢłņČĢņןņØś ĻĖĖņØ┤ņŚÉ ļö░ļØ╝ ļ»ĖņäĖĒĢśņ¦Ćļ¦ī ņ£ĀņØśļ»ĖĒĢ£ ņ░©ņØ┤Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłĻĖ░ņŚÉ, ņČöĒøä ļŹö ļ¦ÄņØĆ ĒÖśņ×ÉĻĄ░ņØä ļīĆņāüņ£╝ļĪ£ ĒĢ£ ņäĖļČäĒÖöļÉ£ ņČöĻ░Ć ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢśĻ▓Āņ£╝ļ®░, ņØ┤ļź╝ ĒåĄĒĢ┤ ņĪ░ĻĖł ļŹö ņĀĢĒÖĢĒĢ£ ņłśņłĀ Ēøä ĻĄ┤ņĀłļĀź ņśłņĖĪņØ┤ Ļ░ĆļŖźĒĢ┤ņ¦ł Ļ▓āņ£╝ļĪ£ ĻĖ░ļīĆĒĢ£ļŗż.
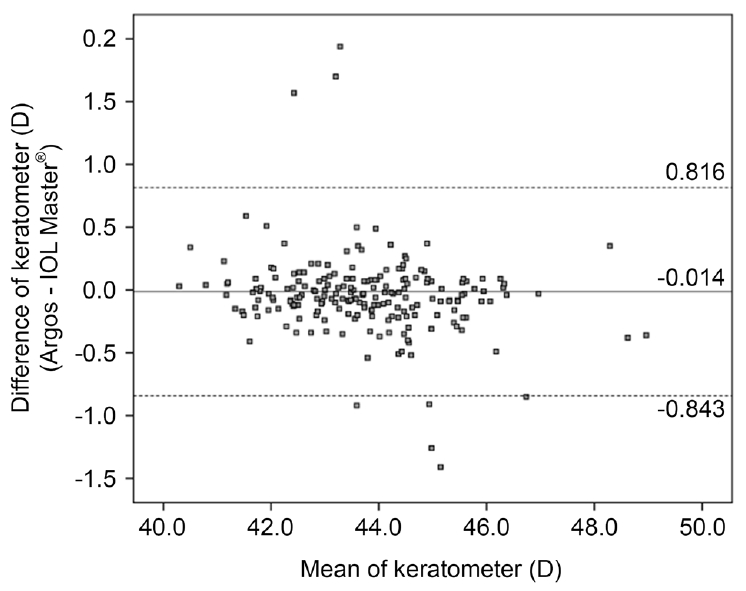
Figure┬Ā1.
Bland-Altman plot of axial length (AL) using Argos and IOL Master┬« 500 (Carl Zeiss Meditec AG, Jena, Germany). The solid line indicates the mean difference (0.012 mm). The dashed lines indicate the 95% limits of agreement (-0.109 mm, 0.134 mm). There was a significant negative correlation between the mean AL of the two biometers and the difference of AL (r = -0.412, p = 0.000). Bold line indicates Y = -0.019X+0.468, ╔ø=0.468 (p = 0.000), ├¤ = -0.019 (p = 0.000) by linear regression analysis. The ALs measured by Argos which was less than 24.63 mm (*) tended to be longer than ALs measured by IOL Master┬« 500.
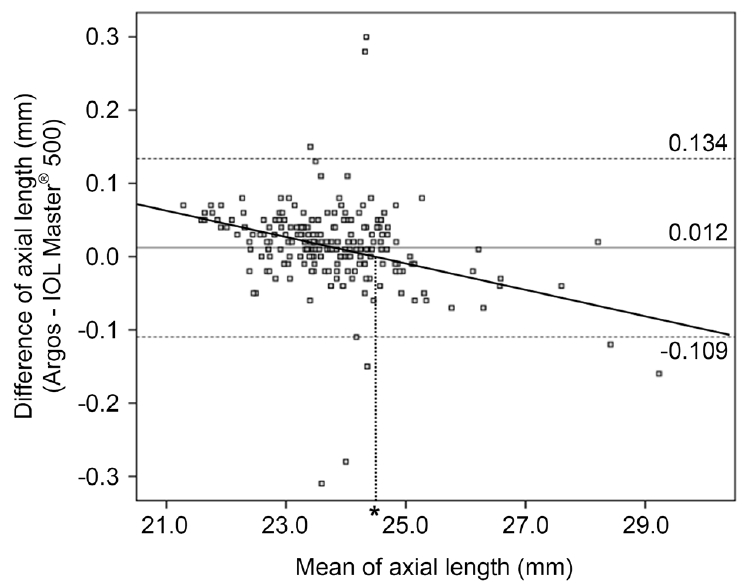
Figure┬Ā2.
Bland-Altman plot of anterior chamber depth using Argos and IOL Master® 500. The solid line indicates the mean difference (0.090 mm). The dashed lines indicate the 95% limits of agreement (-0.189 mm, 0.369 mm).
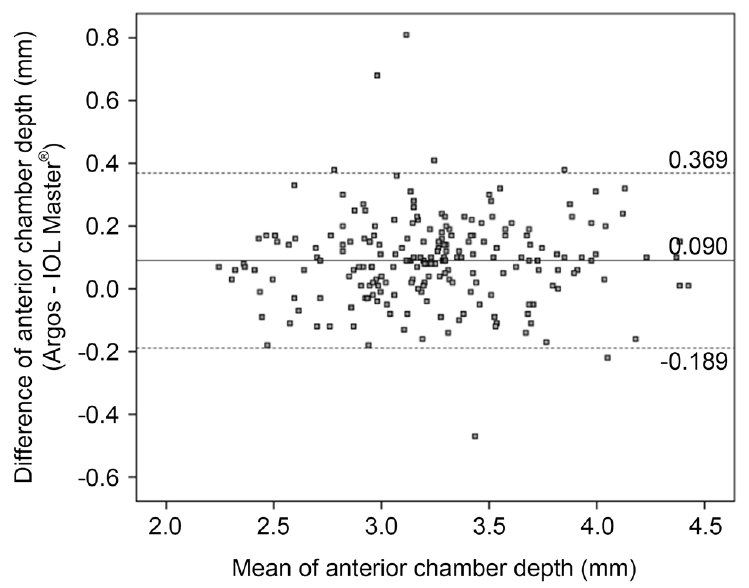
Figure┬Ā3.
Bland-Altman plot of keratometer using Argos and IOL Master® 500. The solid line indicates the mean difference (-0.014 diopters [D]). The dashed lines indicate the 95% limits of agreement (-0.843 D, 0.816 D).
Table┬Ā1.
Acquisition rate of Argos and IOL Master® 500
|
IOL Master® 500 |
Total | ||
|---|---|---|---|
| Success | Fail | ||
| Argos (n) | |||
| ŌĆāSuccess | 207 | 13 | 220 (99.5) |
| ŌĆāFail | 0 | 1 | 1 (0.5) |
| Total | 208 (94.1) | 13 (5.9) | 221 |
Table┬Ā2.
The comparison of values between Argos and IOL Master® 500
| Value | p-value* | ICC | |
|---|---|---|---|
| AL (mm) | |||
| ŌĆāArgos | 23.86 ┬▒ 1.32 | 0.005 | 0.999 |
| ŌĆāIOL Master┬« 500 | 23.84 ┬▒ 1.35 | ||
| ACD (mm) | |||
| ŌĆāArgos | 3.29 ┬▒ 0.45 | 0.000 | 0.975 |
| ŌĆāIOL Master┬« 500 | 3.20 ┬▒ 0.45 | ||
| K (D) | |||
| ŌĆāArgos | 43.72 ┬▒ 1.42 | 0.647 | 0.978 |
| ŌĆāIOL Master┬« 500 | 43.74 ┬▒ 1.49 |
REFERENCES
1) Drexler W, Findl O, Menapace R, et al. Partial coherence interferometry: a novel approach to biometry in cataract surgery. Am J Ophthalmol 1998;126:524-34.


2) Lam AK, Chan R, Pang PC. The repeatability and accuracy of axial length and anterior chamber depth measurements from the IOLMaster. Ophthalmic Physiol Opt 2001;21:477-83.


3) Povazay B, Hermann B, Unterhuber A, et al. Three-dimensional optical coherence tomography at 1050 nm versus 800 nm in retinal pathologies: enhanced performance and choroidal penetration in cataract patients. J Biomed Opt 2007;12:041211.


4) Shammas HJ, Ortiz S, Shammas MC, et al. Biometry measurements using a new large-coherence-length swept-source optical coherence tomographer. J Cataract Refract Surg 2016;42:50-61.


5) Higashiyama T, Mori H, Nakajima F, Ohji M. Comparison of a new biometer using swept-source optical coherence tomography and a conventional biometer using partial coherence interferometry. PLoS One 2018;13:e0196401.



6) Akman A, Asena L, G├╝ng├Čr SG. Evaluation and comparison of the new swept source OCT-based IOLMaster 700 with the IOLMaster 500. Br J Ophthalmol 2016;100:1201-5.


7) Yang JY, Kim HK, Kim SS. Axial length measurements: comparison of a new swept-source optical coherence tomography-based biometer and partial coherence interferometry in myopia. J Cataract Refract Surg 2017;43:328-32.


8) McAlinden C, Wang Q, Gao R, et al. Axial length measurement failure rates with biometers using swept-source optical coherence tomography compared to partial-coherence interferometry and optical low-coherence interferometry. Am J Ophthalmol 2017;173:64-9.


9) Gali HE, Sella R, Afshari NA. Cataract grading systems: a review of past and present. Curr Opin Ophthalmol 2019;30:13-8.


10) Yoo TK, Choi MJ, Lee HK, et al. Comparison of ocular biometry and refractive outcomes using IOL Master 700, IOL Master 500, and ultrasound. J Korean Ophthalmol Soc 2017;58:523-9.

11) Unterhuber A, Povazay B, Hermann B, et al. In vivo retinal optical coherence tomography at 1040 nm - enhanced penetration into the choroid. Opt Express 2005;13:3252-8.


12) Kim SY, Cho SY, Yang JW, et al. The correlation of differences in the ocular component values with the degree of myopic anisometropia. Korean J Ophthalmol 2013;27:44-7.







 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




