수정체 제거 및 인공수정체삽입술 후 발생하는 인공수정체 탈구는 가장 심각한 합병증 중 하나로 드물지 않게 발생하며, 후방 인공수정체 탈구의 빈도는 0.2-2.8%로 보고되었다[
1,
2]. 인공수정체 탈구는 모양체소대 약화와 낭의 수축으로 인해 발생하며, 위험인자로 노화, 고도근시, 포도막염, 외상, 이전의 유리체수술, 망막색소변성, 당뇨, 아토피 피부염, 녹내장, 결체조직 질환이 있다[
3,
4].
인공수정체 탈구가 발생할 경우 기존 인공수정체를 그대로 사용하여 재고정하는 방법과 새로운 인공수정체로 교환하는 방법이 있다. 인공수정체를 고정하는 방법에 따라 인공수정체 공막봉합고정술, 무봉합 인공수정체 공막내고정술 또는 인공수정체 홍채고정술을 선택할 수 있다[
5-
7].
인공수정체 공막봉합고정술은 Malbran et al [
8]이 1986년에 처음 발표한 이후 다양한 수술법이 소개되고 있다. 인공수정체 공막봉합고정술의 경우 봉합사와 관련된 다양한 합병증이 있을 수 있다. 이에 Gabor and Pavlidis [
6]는 공막터널을 만들어 인공수정체의 지지부를 공막내에 고정하는 방법을 처음으로 소개하였으며, 이후 Agarwal et al [
7]은 공막피판을 만든 후 섬유소 접착제를 이용하여 인공수정체의 지지부와 공막피판을 부착하는 방법을 소개하였다. 이외에도 변형된 다양한 수술법이 소개되었다[
9-
18].
현재까지 새로운 수술 방법의 소개와 수술 결과에 대한 보고는 다양하게 이루어졌으나 기존의 인공수정체를 이용하여 공막고정술을 시행하는 방법과 무봉합 공막내고정술을 이용한 인공수정체교환술에 대한 비교 연구는 부족하다. 이에 저자들은 인공수정체 탈구 환자 중 기존의 인공수정체를 이용하여 재고정술을 시행한 군과 무봉합 공막내고정술을 이용한 인공수정체교환술을 시행한 군에 대한 의무기록을 후향적으로 분석하여 6개월 이상의 임상결과를 보고하고자 한다.
대상과 방법
2014년 1월 1일부터 2019년 4월 30일까지 인공수정체 탈구로 본원을 내원한 환자 중 기존 인공수정체 재고정술 또는 무봉합 공막내고정술을 이용한 인공수정체교환술을 시행하고 6개월 이상 경과 관찰이 가능한 환자 90명 91안을 대상으로 후향적 연구를 진행하였다. 본 연구는 본원 연구윤리심의위원회의 승인을 받았다(승인 번호: 2019-283).
수술 전 환자는 최대교정시력과 안압측정, 자동각막굴절력계(KR-8800, Topcon, Tokyo, Japan)를 사용한 구면렌즈 대응치 및 난시값 측정, 세극등현미경검사, 안저검사, 안축장검사를 시행하였다. 수술 전 외상, 레이저치료를 포함한 과거력을 조사하였다. 수술 후 경과 관찰은 술 후 1, 3, 6개월째에 하였으며, 이후에는 3개월 간격으로 시행하였다. 안압상승, 저안압, 인공수정체 탈구, 지지부 미끄러짐, 지지부 부러짐, 광학부 동공포획, 낭포황반부종, 유리체출혈, 안내염, 망막박리를 포함한 경과 관찰 중 발생할 수 있는 합병증과 그에 대한 치료를 조사하였다. 수술 후 고안압은 25 mmHg 이상, 저안압은 6 mmHg 이하로 정의하였다. 산동 후 세극등현미경검사를 통해 인공수정체의 광학부 중심과 각막윤부를 기준으로 한 동공중심점의 떨어진 정도를 평가하여 두 지점의 차이가 1 mm 이상이고, 지지부의 위치 이상이 관찰될 때 지지부 미끄러짐이라고 정의하였다. 일측 또는 양측의 지지부가 고정된 위치에서 완전히 이탈하여 전방 또는 유리체강내에서 관찰되는 경우 인공수정체 탈구로 정의하였다. 지지부 미끄러짐과 인공수정체 탈구가 동시에 관찰되는 경우 인공수정체 탈구로 분류하였다.
모든 수술은 한 명의 술자(J. M. P)에 의해 시행되었으며, 이전에 유리체절제술을 받지 않은 환자는 유리체절제술을 함께 시행하였다. 기존의 인공수정체를 이용한 외부(Ab externo) 공막고정술의 술기는 일체형 인공수정체를 대상으로 다음과 같이 시행되었다. 2시와 8시 방향의 결막을 절개하여 공막을 노출시켰다. 각막윤부를 기저부로 한 삼각형의 부분층 공막피판(scleral flap)을 만들었다. 유리체절제기를 이용하여 전체 유리체절제술을 시행하였다. 눈속집게(GrieshaberⓇ Serrated Forceps, DSP, Alcon Inc., Schaffhausen, Switzerland)로 인공수정체를 잡은 후 유리체절제기로 인공수정체를 싸고 있는 낭과 피질을 제거하였다. 26게이지 바늘을 각막윤부에서 2.0 mm 떨어진 공막피판 아래의 공막을 통해 유리체강 내로 찌르고 반대편 공막피판 아래로는 10-0 doublearmed prolene (ProleneⓇ, Ethicon Inc., Somerville, NJ, USA)의 한쪽 바늘을 찔러 넣어 10-0 prolene의 바늘을 26게이지 바늘 속으로 단단히 끼운 후 26게이지 바늘이 들어간 공막쪽으로 빼내었다. 11시 방향에 2.8 mm 투명각막절개창을 낸 후 10-0 prolene을 각막절개창을 통해 빼내어 이등분하였다. 인공수정체의 한쪽 지지부를 각막절개창을 통해 빼낸 후 한쪽 10-0 prolene으로 고정하였다. 이후 반대쪽 지지부를 각막절개창을 통해 빼낸 후 반대쪽 10-0 prolene으로 고정하였다. 공막밖에 있는 봉합사를 잡아당겨 광학부가 중심에 위치한 것을 확인한 후 공막에 고정하였다. 10-0 ethilon (EthilonⓇ, Ethicon Inc.)으로 각막절개창을 봉합하였다. 이후 공막피판과 결막을 봉합하였다.
섬유소 접착제를 이용한 기존 인공수정체 공막내고정술의 술기는 삼체형의 인공수정체를 대상으로 다음과 같이 시행되었다. 2시와 8시 방향의 결막을 절개하여 공막을 노출시켰다. 각막윤부로부터 2 mm 떨어진 공막에 각막윤부와 평행하게 Stab knife (I-Knife
ⓇII, Alcon Inc., Fort Worth, TX, USA)를 이용하여 약 2 mm 길이로 긁어 고랑을 만들고 지지부가 놓일 수 있도록 하였다. 유리체절제기를 이용하여 전체 유리체절제술을 시행하였다. 눈속집게로 인공수정체를 잡은 후 유리체절제기로 인공수정체를 싸고 있는 낭과 피질을 제거하였다. 공막에 수직으로 25게이지 바늘로 구멍을 낸 다음 눈속집게를 통과시켜 인공수정체의 한쪽 지지부를 잡아 공막 밖으로 빼내었다. 반대편 인공수정체의 지지부도 같은 방법으로 빼내었다. 이후 26게이지 바늘을 이용하여 고랑의 끝부분에 각막윤부와 평행하게 약 2 mm 길이와 약 50% 공막두께의 공막터널을 만들었다. 맥퍼슨 집게(McPherson Tying Forceps Angled K5-5010, Katena Inc., Parsippany, NJ, USA)로 인공수정체의 지지부를 공막터널 내로 밀어 넣어 광학부가 안정적으로 중심에 위치하도록 하였다. 섬유소 접착제(Greenplast Q
Ⓡ, GC Pharma Corp., Yongin, Korea)를 이용하여 공막, 인공수정체 지지부, 결막을 고정하였다(
Fig. 1).
인공수정체 교환술은 다음과 같이 시행되었다. 탈구된 인공수정체의 재질에 따라 3.0 mm 또는 6.0 mm 투명각막절개창을 내었다. 인공수정체 절단기(Osher IOL Cutter [straight], Duckworth & Kent Ltd., Baldock, Hertfordshire, UK)로 기존 인공수정체를 자른 후 각막절개창을 통해 제거하였고, polymethyl methacrylate 재질일 경우 절단하지 않고 제거하였다. 새로운 인공수정체를 삽입한 후 10-0 ethilon으로 각막절개창을 봉합하였다. 새로운 인공수정체는 모두 삼체형 인공수정체인 MN60AC AcrySofⓇ (Alcon Inc.)를 사용하였다. 공막내고정술은 앞에서 언급한 방법과 같이 진행되었다.
기존 인공수정체로 외부(Ab externo) 공막고정술을 시행한 군(1군), 섬유소 접착제를 이용하여 기존 인공수정체로 공막내고정술을 시행한 군(2군), 공막내고정술을 이용한 인공수정체 교환술을 시행한 군(3군)으로 나누어 비교 분석하였다. 시력은 logarithm of the minimum angle of resolution (logMAR)로 변환하여 분석하였고, 수술 전과 수술 후 굴절률은 구면렌즈 대응치(spherical equivalent)로 비교하였다. 6개월 이상 경과관찰 중 발생한 합병증을 관찰하였다. 통계적인 분석은 SPSS 21.0 (IBM Corp., Armonk, NY, USA)을 사용하였다. 수술 전후 시간에 따른 측정값의 분석은 Wilcoxon signed-rank test를, 세 군 간의 비교에는 Kruskal-Wallis test, 두 군 간의 비교에는 Mann-Whitney U-test를 통계분석에 사용하였으며, 모든 경우 p<0.05일 때 통계적인 유의성이 있다고 인정하였다.
결 과
90명 91안의 환자가 연구 대상으로 포함되었다. 평균 연령은 61.1 ± 9.8세였으며, 남성 78명 79안, 여성 12명 12안이었다. 안축장은 1군에서 24.62 ± 1.73 mm, 2군에서 24.68 ± 1.77 mm, 3군에서 24.08 ± 1.43 mm였다. 야그레이저후낭절개술은 4안, 레이저홍채절개술은 3안에서 시행하였다. 외상의 과거력은 6안에서 있었고, 이전 인공수정체 탈구는 3군에서 6안, 2군에서 5안, 1군에서 4안 순으로 많았다. 이외에도 녹내장(8안), 거짓비늘증후군(1안), 망막박리(9안), 유리체출혈(1안)의 과거력이 있었으며, 세 군 간 유의한 차이는 없었다(모두
p>0.05) (
Table 1).
최대교정시력(logMAR)은 수술 전 1군에서 0.47 ± 0.60, 2군에서 0.57 ± 0.65, 3군에서 1.09 ± 0.81이었고, 수술 6개월 후 1군에서 0.10 ± 0.17, 2군에서 0.15 ± 0.29, 3군에서 0.31 ± 0.52로 향상되었다(각각,
p=0.001,
p<0.001,
p<0.001). 수술 전 세 군 간 최대교정시력은 유의한 차이가 있었으나(
p=0.010), 수술 6개월 후 세 군 간 유의한 차이가 없었다(
p=0.422). 수술 전과 수술 6개월 후 시력의 변화는 세 군간 유의한 차이가 있었다(
p=0.041) (
Table 2). 수술 전과 수술 후 시력의 변화에 대해 두 군 간 분석을 하였을 때, 1군과 2군 간에는 유의한 차이가 없었으나(
p=0.890), 1군과 3군 간, 2군과 3군 간에는 유의한 차이가 있었다(각각,
p=0.018,
p=0.046) (
Fig. 2).
구면렌즈 대응치(spherical equivalent)는 수술 전 1군에서 9.12 ± 3.60 diopters (D), 2군에서 9.24 ± 3.34 D, 3군에서 9.45 ± 4.25 D였고, 수술 6개월 후 1군에서 -1.26 ± 1.72 D, 2군에서 -1.32 ± 2.09 D, 3군에서 -0.17 ± 1.58 D로 근시화되었다(모두
p<0.001). 수술 전과 수술 후 구면렌즈 대응치의 변화는 세 군 간 유의한 차이가 없었다(
p=0.456) (
Table 3). 수술 6개월 후 구면렌즈 대응치에 대해 두 군 간 분석을 하였을 때, 1군과 2군 간에는 유의한 차이가 없었으나(
p=0.558), 1군과 3군 간, 2군과 3군 간에는 유의한 차이가 있었다(각각
p=0.004,
p=0.001) (
Fig. 3).
난시값(cylindrical power) 수술 전 1군에서 -1.03 ± 0.68 D, 2군에서 -1.22 ± 1.10 D, 3군에서 -1.18 ± 1.39 D였고, 수술 6개월 후 1군에서 -1.40 ± 0.95 D, 2군에서 -1.79 ± 1.43 D, 3군에서 -1.72 ± 1.18 D로 통계적으로 유의하게 변화되었다(각각
p=0.025,
p=0.007,
p=0.017) (
Table 4).
경과 관찰 기간 중 발생한 합병증으로 인공수정체 지지부 미끄러짐은 2군 중 6안, 3군 중 1안에서 발생하였으며, 이 중 1안은 인공수정체교환술을 시행하였고, 6안은 지지부를 공막터널 내로 재위치 시킨 다음 10-0 prolene으로 공막에 고정하였다. 인공수정체 탈구는 1군 중 2안, 2군 중 3안에서 발생하여 이 중 2안은 외부 공막고정술을 시행하였고, 3안은 인공수정체교환술을 시행하였다. 지지부 부러짐은 2군 중 1안에서 발생하여 인공수정체교환술을 시행하였다. 1안에서 광학부 동공포획이 있었고, 광학부를 밀어 넣어 재위치시켰다. 7안에서 술 후 일시적인 안압상승이 있었고, 점안용 베타차단제 및 탄산탈수효소억제제로 조절되었다. 1안에서 낭포황반부종이 있었고, 유리체강내 항혈관내피성장인자 주사 후 호전되었다. 1안에서 유리체출혈이 있었으며 재수술 후 호전되었다(
Table 5,
6). 합병증 중 각막 부전, 홍채 외상, 안내염, 망막열공, 망막박리는 없었다. 합병증 중 지지부 미끄러짐이 통계적으로 유의하게 2군에서 많이 발생하였다(
p=0.013) (
Table 5). 1군의 인공수정체 탈구(2안)과 3군의 지지부 미끄러짐(1안)의 빈도를 비교하였을 때 통계적으로 유의한 차이는 없었다(
p=0.537).
고 찰
인공수정체 공막고정술은 백내장수술 중 후낭파열이나 모양체소대 약화로 인공수정체를 후낭에 위치시킬 수 없을 경우, 무수정체안 또는 인공수정체 탈구의 경우에 시행하게 된다[
19]. 인공수정체 탈구로 인해 수술을 하게 되는 경우 기존 인공수정체의 종류, 지지부 모양, 손상 정도, 도수, 환자의 상태에 따라 기존 인공수정체를 공막에 재고정하거나 교환술을 시행한다[
7,
20].
Lewis [
21]는 삼각형의 공막피판을 만든 후 이곳으로 바늘을 통과시켜 봉합매듭을 만들고 공막피판으로 덮는 외부 공막고정술을 고안하였다. Chan [
22]은 모양체 주름부 공막절개창을 통해 일시적으로 탈구된 인공수정체의 지지부를 안구밖으로 노출시킨 후 봉합사로 고리를 만들고 다시 안구 내로 집어넣는 방법을 처음으로 고안하여 기존의 방법보다 안구 내에서 인공수정체를 조작하는 시간을 줄일 수 있었다. 그러나 이 방법은 관찰할 수 없는 홍채 뒤에서 인공수정체의 지지부를 조작하기 때문에 지지부의 손상 위험이 있어, Kokame et al [
23]은 탈구된 인공수정체를 홍채 앞쪽까지 위치시키고 투명각막절개창을 통해 지지부를 노출시키는 변형된 방법을 소개하였다. 본 연구에서 시행한 외부 공막고정술도 투명각막절개창을 낸 후 탈구된 인공수정체를 홍채 앞으로 위치시켜 지지부를 투명각막절개창을 통해 노출시켰다. 하지만 이 변형된 방법은 각막내피 손상, 각막 절개 필요성, 축동성 동공일 경우 인공수정체를 홍채 앞까지 조작하는 데 어려움이 있다는 단점이 있다[
23].
Gabor and Pavlidis [
6]가 소개한 공막터널을 만든 후 인공수정체의 지지부를 공막내에 고정하는 방법은 일체형 인공수정체에는 부적합하며 삼체형 인공수정체에 적합하다고하였다. 본 연구에서도 기존 인공수정체로 무봉합 공막내고정술을 시행한 모든 경우에서 삼체형 인공수정체였으며, 기존 인공수정체가 일체형 인공수정체인 경우 외부 공막고정술을 시행거나 새로운 삼체형 인공수정체로 무봉합 공막내고정술을 시행하였다. Agarwal et al [
7]은 지혈이나 인체 조직을 봉합하는 데 쓰이는 섬유소 접착제를 사용하여 인공 수정체의 지지부와 공막피판을 부착시켜 인공수정체를 안정적으로 위치시키는 방법을 소개하였다. 이 방법 또한 봉합사를 사용하지 않으므로 봉합사와 관련된 부작용이 없다는 장점이 있으나 공막피판을 만드는 과정이 추가적으로 필요하다. Ohta et al [
9]은 윤부에서 2 mm 떨어진 곳에 Y자 형태의 공막절개를 하고 공막터널에 지지부를 밀어 넣은 뒤 8-0 nylon으로 지지부를 공막에 고정하여 공막피판을 크게 만들 필요 없이 지지부의 안정성을 높일 수 있었으나 여전히 공막절개와 봉합 과정이 필요하고 봉합사와 관련된 합병증의 위험이 있었다. Zhang et al [
10]은 공막피판 없이 결막만 절개하여 윤부에서 1.5 mm 떨어진 공막에 약 50% 두께로 공막터널을 만들어 공막내 고정술을 시행하고 결막을 흡수성 봉합사로 봉합하였다.
Yamane et al [
11]은 27게이지 바늘에 인공수정체의 지지부를 끼워 넣어 양측 지지부를 동시에 공막 밖으로 노출시킨 후 공막터널에 지지부를 밀어 넣는 방법을 사용하였다. 이후 Yamane et al [
12]은 30게이지의 얇은 내벽의 바늘에 지지부를 끼워 넣어 공막 밖으로 노출시킨 후 지지부의 끝을 열소작기로 가열하는 방법으로 플랜지(flange)를 만들어 공막터널 내에 고정하는 변형된 방법을 소개하였다. 하지만 Yamane et al의 두 바늘을 이용한 방법은 후행지지부를 조작하는 동안 선행지지부의 바늘에 의해 망막이나 홍채, 모양체에 손상의 위험이 높다[
13]. Kelkar et al [
13]는 이러한 위험의 가능성을 줄이고자 한쪽 지지부의 끝을 플랜지로 만들어 공막터널 내에 고정한 후 후행지지부를 같은 방법으로 고정하였다. 하지만 플랜지를 만들기 위해 소작하는 과정에서 예상한 길이보다 지지부가 짧아지게 되면 수정하기 어렵고, 플랜지를 포함한 지지부가 공막터널 내로 미끄러져 들어갈 가능성이 있으며, 바늘을 안구내에 위치시킨 상태로 지지부를 바늘에 끼워 넣는 조작 과정에서 지지부의 손상, 출혈, 망막손상이 발생할 수 있다.
본 연구에서 시행된 무봉합 공막내고정술은 결막을 절개하고 26게이지 바늘을 이용하여 공막터널을 만들어 인공수정체의 지지부를 공막터널 내로 밀어 넣은 후 섬유소 접착제를 이용하여 공막, 인공수정체 지지부, 결막을 고정함으로써 비교적 간단하면서도 안내염을 포함한 봉합사와 관련된 합병증의 가능성을 줄일 수 있었다. 또한 공막피판을 만들지 않아 수술 시간을 단축시킬 수 있었고 공막피판으로 인한 난시와 공막위축과 같은 합병증의 위험을 낮출 수 있었다[
24]. 또한 양측 지지부가 놓일 위치에 대칭적으로 고랑과 공막터널을 만들어 인공수정체를 안정적으로 중심에 위치시킬 수 있었다.
수술 6개월 후 평균 최대교정시력은 이전의 재고정술이나 교환술을 시행한 연구[
25-
27]와 비슷하였고, 수술 전과 비교하여 유의하게 호전되었으며 수술 방법에 따른 차이가 없었다. 최대교정시력의 변화는 기존 인공수정체를 재고정한 군보다 인공수정체교환술을 시행한 군에서 컸는데 이는 군 간의 수술 전 초기 시력이 유의하게 달랐기 때문이다. 이는 수술 전 각막 상태, 전방세포, 잔여피질과 후낭, 탈구된 인공수정체의 위치와 같은 특성이 달랐기 때문으로 보인다.
Su et al [
28]은 봉합사로 공막고정술을 시행한 위치에 따라 구면렌즈 대응치 차이를 비교하였는데 각막윤부 2 mm 후방에 고정하였을 때 예측치보다 -1.35 ± -1.32 D, 각막윤부 3 mm 후방에 고정하였을 때 예측치보다 -0.43 ± -0.71 D 근시로 나타났다. 본 연구에서는 재고정술과 교환술 모두 각막윤부 2 mm 후방에 인공수정체의 지지부를 고정하였다. 구면렌즈 대응치는 수술 6개월 후 근시화되었으며 인공수정체교환술을 시행한 군보다 기존 인공수정체를 재고정한 군에서 유의하게 더 큰 근시값을 보였다. 이는 인공수정체교환술을 시행한 군과는 달리 기존 인공수정체를 사용한 군에서 목표 굴절률을 설정할 수 없었고, 후낭에 인공수정체가 위치해 있었을 때보다 기존 인공수정체로 외부 공막고정술이나 공막내고정술을 시행했을 때 인공수정체가 전방으로 이동하여 나타난 결과로 생각된다.
공막고정술 후 발생할 수 있는 합병증으로 각막부종, 고안압, 포도막 및 맥락막상강 출혈, 인공수정체 탈구, 지지부 미끄러짐 및 부러짐, 봉합부위 미란, 안내염, 낭포성 황반부종, 망막박리 등이 있다[
29-
31]. 본 연구의 인공수정체 탈구 또는 지지부 미끄러짐이 발생한 12안 중 9안이 삼체형의 기존 인공수정체로 공막내고정술을 시행한 군에서, 2안이 외부 공막고정술을 시행한 군에서, 1안이 인공수정체교환술을 시행한 군에서 발생하였다. 기존 인공수정체의 지지부가 부러질 정도의 손상은 없더라도 후방인공수정체 삽입술 후 일정 기간 동안 낭내에 위치해 있었기 때문에 탄성도가 저하되었을 가능성이 있고, 기존의 탈구된 삼체형 인공수정체는 공막내고정술을 위해 만들어진 인공수정체가 아니었기 때문에 새로운 인공수정체로 공막내고정술을 시행한 군과 비교하였을 때 재탈구의 빈도가 높았다고 생각된다. 또한 외부 공막고정술을 시행한 군에서는 일체형 인공수정체를 봉합사로 고정하였기 때문에 이와 같은 합병증이 적었던 것으로 생각된다. 지지부 미끄러짐 또한 일종의 부분 탈구로 생각할 수 있다. 1군의 인공수정체 탈구(2안)과 3군의 지지부 미끄러짐(1안)의 빈도를 비교하였을 때, 통계적으로 유의한 차이는 없었기 때문에 이러한 면에서 두 수술 방법의 안전성은 유의한 차이가 없다고 볼 수 있었다.
수술 결과뿐만 아니라 수술 방법에 따른 재료비 또한 고려해야 할 부분이다. 기존 인공수정체로 외부 공막고정술을 시행할 경우 봉합사에 대한 비용이 추가되고, 기존 인공수정체로 무봉합 공막내고정술을 시행할 경우 섬유소 접착제 비용이 추가된다. 또한 새로운 인공수정체로 무봉합 공막내고정술을 시행할 경우 인공수정체와 섬유소 접착제 비용이 추가된다. 봉합사보다 상대적으로 인공수정체와 섬유소 접착제의 비용이 부담될 수 있으므로 각 수술 방법의 결과와 더불어 환자의 경제적 상황을 고려하여 수술 방법을 결정하는 것이 필요하다.
본 연구의 한계점으로는 첫째, 후향적 연구로 각 군별 연구 대상자의 초기 특성이 달랐다. 둘째, 6개월 이상 경과 관찰이 가능한 경우만 연구에 포함시키고 수술 후 더 이상 내원하지 않았던 대상자들이 포함되지 않아 선택 편향이 있었다. 셋째, 수술 후 각막내피세포밀도를 측정하지 않아 평가 항목에 포함하지 못했다.
결론적으로 인공수정체가 탈구되었을 때 경우에 따라 수술 방법을 다르게 할 수 있다. 최종 최대교정시력은 탈구된 인공수정체를 이용하여 재고정술을 시행하는 것과 새로운 인공수정체로 공막내고정술을 이용하여 교환하는 것을 비교할 때 유의한 차이가 없었다. 재고정술을 시행하는 경우 더욱 근시화되는 경향이 있었기 때문에 재고정술이 교환술에 비해 비교적 간단하지만 수술 전 이에 대한 고려를 해야할 것으로 생각된다. 기존 삼체형 인공수정체로 공막내고정술을 시행할 경우 인공수정체 탈구 또는 지지부 미끄러짐의 위험이 높았기 때문에 탈구된 인공수정체가 삼체형일 경우 인공수정체교환술을 먼저 고려해 볼 수도 있다고 생각된다. 추후 장기적인 효과에 대한 비교 분석 및 고도근시 환자에서 인공수정체 공막고정술의 안정성에 대한 연구가 필요할 것으로 생각된다.
Figure 1.
The surgical procedure of sutureless intrascleral refixation of a dislocated intraocular lens. (A) The sclera is exposed and two points on sclera are marked at 2.0 mm posterior to the limbus (at 8 o’clock and 2 o’clock direction). (B) Two limbal parallel scleral grooves are made using a stab knife. (C) The haptic is grasped and pulled out through the scleral incision with 25-gauge intraocular forceps. (D) Two scleral tunnels are made using a 26-gauge needle. (E) The haptic is inserted into the scleral tunnel using McPherson forceps. (F, G) The sclera and conjunctiva are fixed using biological fibrin glue. (H) A centration of the intraocular lens is checked.
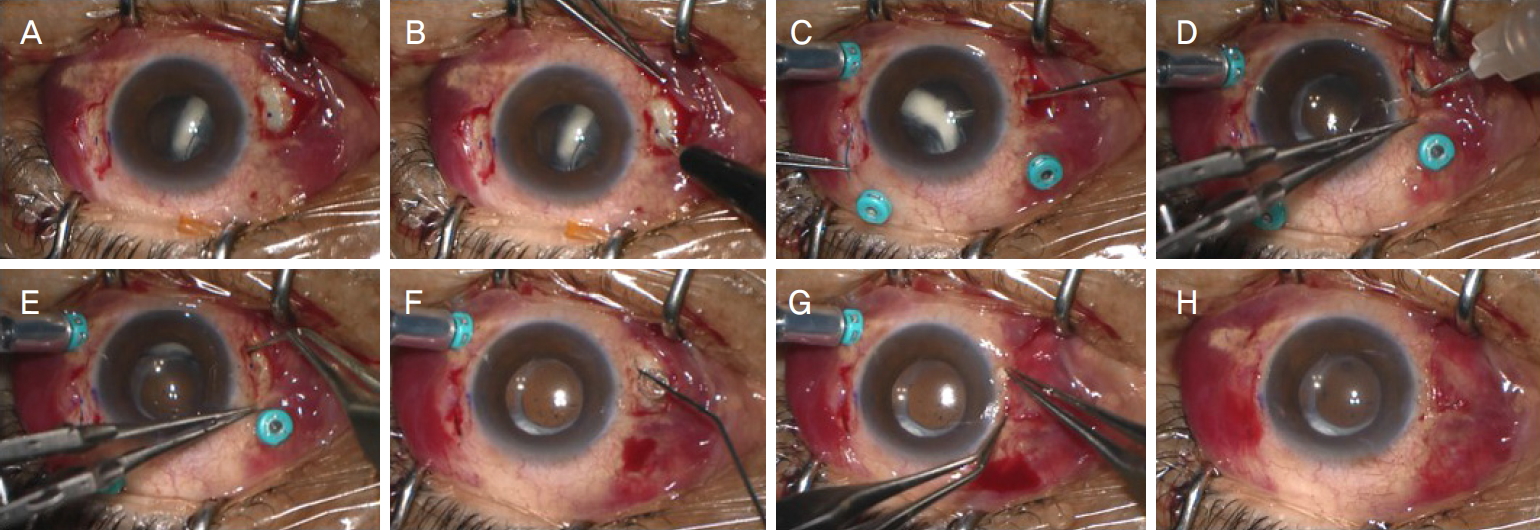
Figure 2.
Mean BCVA changes before and 6 months after surgery. The mean BCVA change was -0.37 ± 0.59 (Group 1), -0.42 ± 0.65 (Group 2), -0.78 ± 0.81 (Group 3). BCVA change: (Post-OP 6 months BCVA)-(Pre-OP BCVA); Group 1: ab externo scleral refixation; Group 2: intrascleral refixation; Group 3: exchange with intrascleral fixation. BCVA = best-corrected visual acuity; PostOP = postoperative; PreOP = preoperation. *Statistically significant (Mann-Whitney U-test).
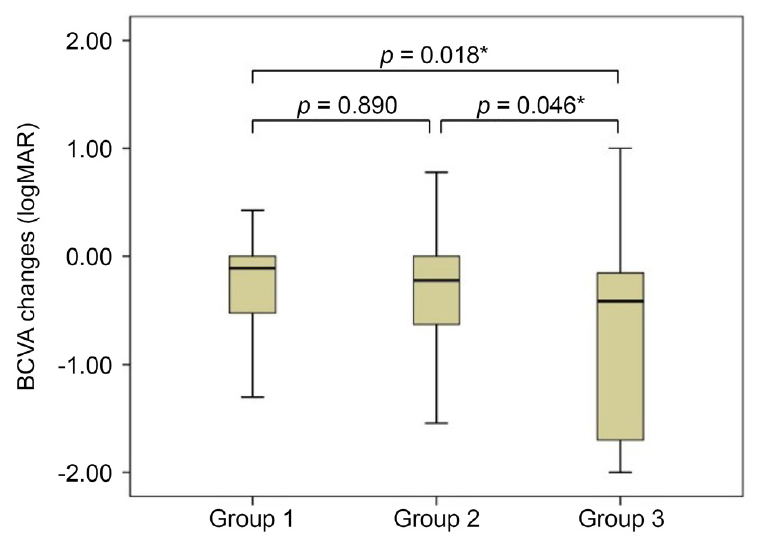
Figure 3.
Mean spherical equivalent 6 months after surgery. The mean spherical equivalent was -1.26 ± 1.72 D (Group 1), -1.32 ± 2.09 D (Group 2), -0.17 ± 1.58 D (Group 3). Group 1: ab externo scleral refixation; Group 2: intrascleral refixation; Group 3: exchange with intrascleral fixation. SE = spherical equivalent; D = diopters. *Statistically significant (Mann-Whitney U-test).

Table 1.
Baseline characteristics of patients with IOL refixation and exchange
|
Baseline characteristic |
Group 1 |
Group 2 |
Group 3 |
p-value*
|
|
Number of eyes (patients) |
29 (29) |
32 (31) |
30 (30) |
- |
|
Age (years) |
62.0 ± 8.8 |
60.7 ± 9.9 |
60.6 ± 10.9 |
0.860 |
|
Sex (male:female) |
25:4 |
29:2 |
24:6 |
0.280 |
|
Axial length (mm) |
24.62 ± 1.73 |
24.68 ± 1.77 |
24.08 ± 1.43 |
0.374 |
|
BCVA (logMAR) |
0.47 ± 0.60 |
0.57 ± 0.65 |
1.09 ± 0.81 |
0.010†
|
|
IOP (mmHg) |
18.0 ± 3.6 |
18.8 ± 5.4 |
16.4 ± 4.4 |
0.086 |
|
Refractive error (D, SE) |
9.12 ± 3.60 |
9.24 ± 3.34 |
9.45 ± 4.25 |
0.608 |
|
Cylindrical power (D) |
-1.03 ± 0.68 |
-1.22 ± 1.10 |
-1.18 ± 1.39 |
0.694 |
|
Ocular history |
|
|
|
|
|
Nd:YAG capsulotomy |
2 |
1 |
1 |
0.730 |
|
Laser peripheral iridotomy |
0 |
1 |
2 |
0.361 |
|
Trauma |
3 |
2 |
1 |
0.556 |
|
IOL dislocation |
4 |
5 |
6 |
0.805 |
|
Glaucoma |
1 |
3 |
4 |
0.407 |
|
Pseudoexfoliation syndrome |
0 |
0 |
1 |
0.362 |
|
Retinal detachment |
4 |
2 |
3 |
0.618 |
|
Vitreous hemorrhage |
0 |
1 |
0 |
0.398 |
Table 2.
Comparison of best-corrected visual acuity before and 6 months after surgery
|
Variable |
Group 1 |
Group 2 |
Group 3 |
p-value*
|
|
PreOP BCVA (logMAR) |
0.47 ± 0.60 |
0.57 ± 0.65 |
1.09 ± 0.81 |
0.010†
|
|
PostOP 6 months BCVA (logMAR) |
0.10 ± 0.17 |
0.15 ± 0.29 |
0.31 ± 0.52 |
0.422 |
|
p-value‡
|
0.001†
|
<0.001†
|
<0.001†
|
- |
|
BCVA change (logMAR) |
-0.37 ± 0.59 |
-0.42 ± 0.65 |
-0.78 ± 0.81 |
0.041†
|
Table 3.
Comparison of spherical equivalent before and 6 months after surgery
|
Variable |
Group 1 |
Group 2 |
Group 3 |
p-value*
|
|
PreOP SE (D) |
9.12 ± 3.60 |
9.24 ± 3.34 |
9.45 ± 4.25 |
0.608 |
|
PostOP 6 months SE (D) |
-1.26 ± 1.72 |
-1.32 ± 2.09 |
-0.17 ± 1.58 |
0.001†
|
|
p-value‡
|
<0.001†
|
<0.001†
|
<0.001†
|
- |
|
SE change (D) |
-10.38 ± 4.08 |
-10.56 ± 4.16 |
-9.62 ± 4.43 |
0.456 |
Table 4.
Comparison of cylindrical power before and 6 months after surgery
|
Variable |
Group 1 |
Group 2 |
Group 3 |
p-value*
|
|
PreOP Cyl (D) |
-1.03 ± 0.68 |
-1.22 ± 1.10 |
-1.18 ± 1.39 |
0.694 |
|
PostOP 6 months Cyl (D) |
-1.40 ± 0.95 |
-1.79 ± 1.43 |
-1.72 ± 1.18 |
0.576 |
|
p-value†
|
0.025‡
|
0.007‡
|
0.017‡
|
- |
|
Cyl change (D) |
-0.37 ± 0.76 |
-0.57 ± 1.41 |
-0.53 ± 1.57 |
0.452 |
Table 5.
Postoperative complications by surgical procedures
|
Complication (n) |
Group 1 |
Group 2 |
Group 3 |
p-value*
|
|
IOP elevation (7) |
2 (7) |
3 (9) |
2 (7) |
0.907 |
|
IOL dislocation (5) |
2 (7) |
3 (9) |
0 |
0.253 |
|
Haptic slippage (7) |
0 |
6 (19) |
1 (3) |
0.013†
|
|
Haptic breakage (1) |
0 |
1 (3) |
0 |
0.398 |
|
Optic capture (1) |
0 |
1 (3) |
0 |
0.398 |
|
Cystoid macular edema (1) |
0 |
0 |
1 (3) |
0.362 |
|
Vitreous hemorrhage (1) |
0 |
0 |
1 (3) |
0.362 |
Table 6.
Timing of postoperative complications and treatments
|
Case |
Sex/age |
Group |
Complication |
Timing |
Treatment |
|
1 |
M/64 |
1 |
IOL dislocation |
18 months |
IOL exchange |
|
2 |
M/63 |
1 |
IOL dislocation |
13 months |
IOL exchange |
|
3 |
M/41 |
1 |
IOP elevation |
1 week |
Beta-blocker, CAI |
|
4 |
M/57 |
1 |
IOP elevation |
1 week |
Beta-blocker, CAI |
|
5 |
M/72 |
2 |
IOP elevation |
15 months |
Beta-blocker, CAI |
|
6 |
M/68 |
2 |
IOP elevation |
1 day |
Beta-blocker, CAI |
|
7 |
M/56 |
2 |
IOP elevation |
1 week |
Beta-blocker, CAI |
|
8 |
M/73 |
2 |
IOL dislocation |
12 months |
Ab externo scleral refixation |
|
9 |
M/75 |
2 |
IOL dislocation |
9 months |
Ab externo scleral refixation |
|
10 |
M/49 |
2 |
IOL dislocation |
6 months |
IOL exchange |
|
11 |
M/55 |
2 |
Haptic slippage |
2 months |
Intrascleral refixation |
|
12 |
M/47 |
2 |
Haptic slippage |
1 month |
Intrascleral refixation |
|
13 |
M/65 |
2 |
Haptic slippage |
1 month |
Intrascleral refixation |
|
14 |
M/62 |
2 |
Haptic slippage |
6 months |
Intrascleral refixation |
|
15 |
M/56 |
2 |
Haptic slippage |
9 months |
Intrascleral refixation |
|
16 |
M/45 |
2 |
Haptic slippage |
2 weeks |
IOL exchange |
|
17 |
M/61 |
2 |
Optic capture |
1 week |
Reposition |
|
18 |
M/54 |
2 |
Haptic breakage |
2 weeks |
IOL exchange |
|
19 |
M/65 |
3 |
IOP elevation |
1 month |
Beta-blocker, CAI |
|
20 |
M/64 |
3 |
IOP elevation |
1 week |
Beta-blocker, CAI |
|
21 |
M/59 |
3 |
Haptic slippage |
24 months |
Intrascleral refixation |
|
22 |
F/76 |
3 |
Cystoid macular edema |
3 months |
Anti-VEGF |
|
23 |
M/45 |
3 |
Vitreous hemorrhage |
9 months |
Vitrectomy |
REFERENCES
1) Mello MO Jr, Scott IU, Smiddy WE, et al. Surgical management and outcomes of dislocated intraocular lenses. Ophthalmology 2000;107:62-7.


2) Gross JG, Kokame GT, Weinberg DV; Dislocated In-The-Bag Intraocular Lens Study Group. In-the-bag intraocular lens dislocation. Am J Ophthalmol 2004;137:630-5.


3) Jakobsson G, Zetterberg M, Lundström M, et al. Late dislocation of in-the-bag and out-of-the bag intraocular lenses: ocular and surgical characteristics and time to lens repositioning. J Cataract Refract Surg 2010;36:1637-44.


5) Gimbel HV, Condon GP, Kohnen T, et al. Late in-the-bag intraocular lens dislocation: incidence, prevention, and management. J Cataract Refract Surg 2005;31:2193-204.


6) Gabor SGB, Pavlidis MM. Sutureless intrascleral posterior chamber intraocular lens fixation. J Cataract Refract Surg 2007;33:1851-4.


7) Agarwal A, Kumar DA, Jacob S, et al. Fibrin glue-assisted sutureless posterior chamber intraocular lens implantation in eyes with deficient posterior capsules. J Cataract Refract Surg 2008;34:1433-8.


9) Ohta T, Toshida H, Murakami A. Simplified and safe method of sutureless intrascleral posterior chamber intraocular lens fixation: Y-fixation technique. J Cataract Refract Surg 2014;40:2-7.


10) Zhang Y, He F, Jiang J, et al. Modified technique for intrascleral fixation of posterior chamber intraocular lens without scleral flaps. J Cataract Refract Surg 2017;43:162-6.


11) Yamane S, Inoue M, Arakawa A, Kadonosono K. Sutureless 27-gauge needle-guided intrascleral intraocular lens implantation with lamellar scleral dissection. Ophthalmology 2014;121:61-6.


12) Yamane S, Sato S, Maruyama-Inoue M, Kadonosono K. Flanged intrascleral intraocular lens fixation with double-needle technique. Ophthalmology 2017;124:1136-42.


14) Can E. Flapless and sutureless intrascleral fixation of posterior chamber intraocular lens for correction of aphakia. J Cataract Refract Surg 2018;44:929-31.


16) Nudleman E, Yonekawa Y, Prenner JL. Sutureless transscleral fixation of secondary intraocular lenses. Curr Opin Ophthalmol 2018;29:210-6.


17) Yoshida N, Kojima T, Yokoyama S, et al. New surgical approach for intrascleral fixation using an intraocular lens with hook-shaped haptics. J Cataract Refract Surg 2018;44:129-33.


20) Ganekal S, Venkataratnam S, Dorairaj S, Jhanji V. Comparative evaluation of suture-assisted and fibrin glue-assisted scleral fixated intraocular lens implantation. J Refract Surg 2012;28:249-52.


21) Lewis JS. Ab externo sulcus fixation. Ophthalmic Surg 1991;22:692-5.


22) Chan CK. An improved technique for management of dislocated posterior chamber implants. Ophthalmology 1992;99:51-7.


23) Kokame GT, Atebara NH, Bennett MD. Modified technique of haptic externalization for scleral fixation of dislocated posterior chamber lens implants. Am J Ophthalmol 2001;131:129-31.


26) Kristianslund O, Råen M, Østern AE, Drolsum L. Late in-the-bag intraocular lens dislocation: a randomized clinical trial comparing lens repositioning and lens exchange. Ophthalmology 2017;124:151-9.


27) Dalby M, Kristianslund O, Drolsum L. Long-term outcomes after surgery for late in-the-bag intraocular lens dislocation: a randomized clinical trial. Am J Ophthalmol 2019;207:184-94.


28) Su D, Stephens JD, Obeid A, et al. Refractive outcomes after pars plana vitrectomy and scleral fixated intraocular lens with gore-tex suture. Ophthalmol Retina 2019;3:548-52.


29) Solomon K, Gussler JR, Gussler C, Van Meter WS. Incidence and management of complications of transsclerally sutured posterior chamber lenses. J Cataract Refract Surg 1993;19:488-93.


30) Scott IU, Flynn HW Jr, Feuer W. Endophthalmitis after secondary intraocular lens implantation. A case-report study. Ophthalmology 1995;102:1925-31.


31) Davies EC, Pineda R 2nd. Complications of scleral-fixated intraocular lenses. Semin Ophthalmol 2018;33:23-8.


Biography
조영채 / Yeong Chae Jo
메리놀병원 안과
Department of Ophthalmology, Maryknoll Medical Center










 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



