 |
 |
| J Korean Ophthalmol Soc > Volume 63(5); 2022 > Article |
|
국문초록
증례요약
타병원에서 양안 전층각막이식술을 받은 당뇨, 고혈압의 기저질환을 가진 74세 남자 환자가 우안 각막이식 거부반응으로 전층각막이식재수술을 시행받았다. 환자는 우안 말기 녹내장의 병력을 가지고 있었으며, 수술 전 나안시력 안전수지 30 cm에서 수술 25일 후 나안시력 0.02로 호전되었으나 각막상피결손이 처음 확인되었다. Herpes simplex virus 감염에 준해 치료하였으나 호전되지 않았고, 수술 35일 후 안내염 소견이 보여 전방세척술, 유리체절제술 및 유리체내 항생제 주사를 시행하였으며, 수술 중 시행한 세균 배양검사상 메티실린 내성 응고효소음성 포도상구균이 동정되었다. 치료 두 달 후 나안시력 0.06, 전방 및 유리체염증이 회복되었다.
ABSTRACT
Purpose
To report a case of subacute methicillin-resistant coagulase-negative Staphylococcus hominis endophthalmitis after re-operation for penetrating keratoplasty in a patient who had a penetrating keratoplasty rejection.
Case summary
A 74-year-old man with underlying diabetes and hypertension who underwent bilateral penetrating keratoplasty at another hospital underwent penetrating keratoplasty reoperation due to corneal transplant rejection in the right eye. He had a history of end-stage glaucoma in the right eye and the visual acuity was finger counting at 30 cm. About 25 days postoperatively, the corneal epithelial defect was first found. Treatment based on suspicion of herpes simplex virus infection did not result in improvement and endophthalmitis was suspected in the right eye about 35 days after surgery. Anterior chamber irrigation, pars planar vitrectomy, and intravitreal antibiotic injection were performed. Culture revealed methicillin-resistant coagulase negative Staphylococcus hominis. After 2 months of treatment, the anterior chamber and vitreous inflammation decreased and best corrected visual acuity in the right eye recovered to 0.06.
전층각막이식술은 수용 각막전층을 기증각막으로 대치하여 이식하는 술기로, 각막이식술 후 발생하는 안내염은 0.2-0.77%의 빈도로 발생하는 것으로 보고되고 있으며[1], 보통 수술 후 72시간 이내에 발생한다고 한다. 외인안내염의 원인으로는 안구 내 수술 후 발생하는 것이 가장 빈도가 높지만, 외상이나 안구 내 주사, 각막궤양수술 외에도 외인안내염의 원인이 될 수 있으며 면역저하된 기저질환을 갖고 있는 환자나 면역저하 상태가 잠복되어 있는 경우 내인안내염을 일으킬 수 있다. 전층각막이식술 후 발생한 안내염의 원인 미생물은 보고에 따라 다양한데, 세균이 75% 정도를 차지하며, 한 보고에 의하면 Streptococcus 및 Staphylococcus를 포함한 그람 양성균이 55%, Pseudomonas, Klebsiella, Serratia 등을 포함한 그람 음성균이 19%, 진균은 21% 정도를 차지한다[2]. 그람 양성의 혈장 응고효소 음성균(coagulase-negative)은 대표적인 피부상재균으로, 그중에서도 Staphylococcus epidermidis (S. epidermidis)와 Staphylococcus hominis (S. hominis)가 가장 많이 분포하고 있다. 이 증례는 전층각막이식술 후 메티실린 내성 응고효소음성 호미니스 포도상구균(methicilin resistant coagulase negative Staphylococcus hominis, MRCoNS hominis)에 의한 아급성 세균안내염이 발생한 국내 첫 보고로 이를 보고하고자 한다.
타병원에서 12년 전 우안 전층각막이식술, 2년 전 좌안 전층각막이식술을 받은 당뇨, 고혈압의 기저질환을 가진 74세 남자 환자가 우안 시력저하를 주소로 내원하였다. 약 20년 전 양안에 백내장수술을 받은 상태였고, 문진상 우안의 시력저하는 12년 전에 각막을 이식받은 후 1-2년부터 지속되었다고 하였다. 환자는 양안 말기 녹내장으로 안압하강제 Combigan® (Allergan Inc., Irvine, CA, USA)을 하루 2회 사용 중이었으며, 세극등현미경검사상 우안 각막이식편의 광범위한 혼탁 및 부종이 보여 각막혼탁으로 안저가 관찰되지 않았다(Fig. 1A). B스캔 초음파검사상 유리체의 염증 및 혼탁 소견은 발견되지 않았고(Fig. 1B), 내원 당시 최대 교정시력은 우안 안전수지 30 cm, 좌안 0.06, 양안 안압 18/19 mmHg였다. 우안 말기 녹내장과 과거 전층각막이식 수술력을 가지고 있는 고위험군 판단하에 환자의 동의를 받고 전층각막이식재수술을 시행하였다. 수술은 전신마취로 시행되었으며, 우안에 있던 기존 각막이식절편을 제거한 후 전층각막이식술을 시행하였다. 공여안은 25세 남성 환자의 수입 각막이었으며, 사망 한 시간 후 안구적출술 및 각공막 절제가 시행된 조직으로 확인되었다. 기존 각막이식절편 공여부에 묻은 잔존 봉합사를 포함하여, 기존 이식절편보다 크게 8.00 mm 크기로 이식절편을 제거하였으며, 이후 점탄 물질을 주입하여 전방을 유지하였다. 기증각막은 각막원형천공기(Barron Trephine, Katena Products Inc., Parsippany-Troy Hills, NJ, USA)를 통해 8.25 mm 크기로 절단되었으며, 10-0 나일론 봉합사를 사용하여 16개 단속봉합으로 이식편을 고정하고 치료용 렌즈를 삽입한 후 수술을 끝마쳤다. 또한, 공여자 각결막 조직에서 도말 및 배양검사를 시행하였다. 수술 다음 날 아침 중등도의 각막부종이 관찰되었으며 봉합 부위 유출 없이 긴장도를 유지하였고, 전방염증은 심하지 않았으며(1+) 안압은 우안 14 mmHg, 좌안 15 mmHg로 유지되었다. 수술 후 경구용 항생제와 경구용 스테로이드 32 mg을 복용하도록 하였고 안약은 국소 스테로이드 점안제(prednisolone acetate 1%)를 두 시간마다, 점안항생제(moxifloxacin 0.5%)를 하루 4번 점안 및 항생제 안연고(ofloxacin 3 mg/g)를 자기 전에 점안하도록 하였다.
수술 후 4일째 전방 내 염증 세포 trace였으며 경도의 데스메막주름과 각막기질부종이 있었으나 수술 직후에 비해 점차 감소하는 양상이었다. 각막상피는 추가적인 각막미란이나 결손이 없는 상태로 재상피화가 진행 중임을 확인하였고, 수술 중 시행한 배양검사에서는 균이 검출되지 않아 퇴원 후 경과 관찰하였다. 수술 25일 후 외래 내원 시 우안 나안시력 0.02로 수술 전에 비해 시력이 회복된 양상이었으나, 5시 방향 이식각막의 봉합 부위 주위로 약 1 × 1 mm2 크기의 각막상피결손이 처음 확인되었다(Fig. 2). Fluorescein paper로 염색한 후 관찰했을 때 각막기질로의 침윤이 관찰되었고, 경계는 명확한 양상이었다. 치료용 렌즈를 착용하도록 하고 국소 스테로이드 점안제(prednisolone acetate 1%), 점안항생제(moxifloxacin 0.5%) 하루 4번 점안 및 prednisolone 16 mg으로 복용량을 줄이면서 경과 관찰하였다. 각막상피결손 발견 5일 뒤 상피결손이 악화되는 양상으로, 5시 방향에 국한되었던 상피결손이 4시부터 6시 봉합부까지 확장되는 양상이었다. 명확한 가지모양(dendritic)의 병변은 아니었으나, 지도모양(geographic) 궤양의 가능성을 배제하기 어렵고, 헤르페스바이러스감염이 이식수술 후 공여자 각막상피결손의 흔한 원인 중 하나이므로 예방적으로 스테로이드 점안제(prednisolone 10 mg/mL) 하루 두 번으로 줄이고 ganciclovir 1.5 mg/g 안연고 하루 5회, prednisolone 16 mg 유지 및 valacyclovir 500 mg을 하루 3회 복용 추가하고 외래 내원하도록 하였다. 하지만 5일 뒤 악화된 우안 통증으로 내원하였으며, 5시 방향 상피결손은 보이지 않았으나 10시 방향 봉합 부위부터 하측으로 넓게 중심시야를 침범하는 각막상피결손이 새로 관찰되었으며(Fig. 3B), 전방 내 세포 4+, 전방축농이 보였고(Fig. 3A), B스캔 초음파 검사상에서도 유리체강 내 염증세포 침윤으로 인한 유리체 혼탁이 관찰되었다(Fig. 3C). 우안 안내염의 양상 의심하에 각막상피결손 부위 도말 및 배양검사를 시행하였다. 각막 점안마취 후 No.15 Bard-Parker knife (Bard-Parker Co., Danbury, CT, USA)로 병변의 가장자리 및 기저를 긁고 유리슬라이드에 도말 및 그람염색을 시행하였다. 또, 검체를 채취 한 면봉을 배지에 접종하고 배양을 시행하였다. 배양된 세균의 동정은 미생물자동분석기(VITEK system, BioMerieux-Co., Lyon, France)를 이용하였다. 입원 후 전방세척술로 전방축농 제거와 유착된 동공박리 및 성형술 및 23게이지 평면부 유리체절제술, 유리체내 항생제주입술(vancomycin 1.0 mg/ 0.1 mL, ceftazidime 2.0 mg/0.1 mL, amphotericin 0.1 mg/ 0.1 mL)을 시행하였다. 수술 중 획득한 전방수와 유리체내에서 도말 및 배양검사를 시행하였다. 전방검체는 30게이지 주사침으로 방수 약 0.2 mL를 채취하였으며, 유리체검체는 주입관의 연결 부위에 시린지를 연결하여 관류액이 들어가기 전 희석되지 않은 상태로 약 0.5 mL를 채취하였다. 수술 중 이측부 일부 이식봉합에 유출이 발생하여 각막이식편의 재봉합을 시행하였다. 수술 후 moxifloxacin 0.5% 점안액과 tobramycin 0.3% 점안액은 두 시간마다, prednisolone 10 mg/mL 점안액은 하루 4회, homatropine hydrobromide 20 mg 점안액은 하루 2회, vancomycin (2 g/day), ceftazidime (2 g/day)을 정맥 주사하였다. 이후 수술 전 실시한 각막상피결손 부위 도말 및 배양검사, 유리체절제술 중 시행한 균배양검사의 전방수와 유리체내 검체 모두에서 MRCoNS hominis가 동정되었으며, 입원 시 시행한 각막병변부 배양검사에서도 동일한 세균이 동정되었다. 항생제 감수성 결과 ciprofloxacin, erythromycin, clindamycin, linezolid, tetracycline, vancomycin 등의 항생제에는 감수성을 보였지만, penicillin, oxacillin, trimethoprim/sulfamethoxazole 등에는 내성을 나타냈다. 항생제 감수성 결과 확인 후 vancomycin 1.0 mg/0.1 mL 유리체강내 주사치료 및 Fortified vancomycin HCl 25 mg/mL 점안약, moxifloxacin 0.5% 점안약으로 변경하여 치료하였다. 유리체절제술 후 14일 뒤 전방 염증 1+ 및 안저 관찰 가능한 소견으로 회복되어 퇴원하였다. 치료 두 달 후 전방 및 유리체염증이 회복된 상태 유지 및 우안 나안시력 0.06으로 시력 회복되었다(Fig. 4).
전층각막이식수술 후 세균안내염의 발생률은 0.1-2.47%로 드물지만 발생하면 예후가 매우 불량한 것으로 알려져 있다[1,3,4]. 전층각막이식수술 후 발생한 안내염의 원인은 기증각막감염, 수술 중 전파, 수술 후 봉합 관련 합병증, 상처 벌어짐, 수술 후 각막염이 주요 원인이며 그 외에도 장기간 점안 스테로이드제 사용, 진균각막염, 외상, 각막의 얇아짐, 이전 수술 부위 근처에 발생한 각막염이 위험요인으로 보고되고 있다[5]. 이런 모든 감염은 고령과 당뇨 등 전신적으로 면역저하된 환자에서 더 증가될 수 있다[6]. 그중 봉합관련 문제가 전층각막이식 후 안내염 원인 중 약 42%로 높았고, 약 85.5%가 감염으로 인한 각막염 이후 안내염이 발생되었다고 보고되었다[6]. 감염의 원인은 그람 양성균이 가장 많이 보고되고 있으며, 그 원인균은 Streptococcus pneumoniae, Staphylococcus epidermidis, Pseudomonas aeruginosa, Staphylococcus aureus, Propionibacterium acnes 순으로 검출된 바 있다[7,8]. 또한, 각막이식의 실패를 초래하는 고위험군을 대상으로 한 국내 최근 연구 결과에서는[9] 이전 각막이 식력이 있거나, 각막이식 시행 횟수가 많을수록 이식실패 가능성이 높아지는 것으로 보았다.
본 증례는 전층각막이식재수술 약 25일 후 공여부에 발생한 각막상피결손과 각막염이 아급성 감염성 안내염으로 악화된 예이다. 시행한 균배양검사상 각막병변과 전방수, 유리체검체 모두에서 동일한 메티실린 내성 응고효소음성 호미니스 포도상구균이 검출되었다. 본 증례에서는 수술 시 공여부 조직에서 시행한 배양검사상 모두 음성이 확인되었고, 아급성으로 발생하였으므로 수술 전 기증각막 문제나 수술 중 전파된 병원감염의 가능성은 떨어진다. 수술 후 25일째부터 아급성으로 봉합사 주변 각막 부위에서 각막상피결손과 지속 악화되는 각막염이 확인되었고, 같은 원인균에 의한 감염안내염이 발생한 것으로 추정된다. 또, 각막이식 실패력, 스테로이드 점안제 사용과 더불어, 조절되지 않는 당뇨 병력과 고령의 나이에 의한 면역저하 상태가 항생제 내성균 감염 및 안내염 발생에 영향을 끼친 것으로 보인다[8].
이 증례에서 검출된 항생제 내성균은 MRCoNS hominis로, 면역력 저하된 환자에서 흔히 발견되는 항생제 내성균이다[10]. S. hominis는 그람 양성의 응고효소음성 포도상구균으로, S. epidermidis 다음으로 얼굴, 액와 등 신체에 가장 많이 분포하는 피부상재균이며, S. epidermidis, Bacillus subtilis와 함께 안구감염을 일으키는 균주 중 하나로 보고된 바 있다[11]. S. hominis는 대부분 penicillin, erythromycin, novobiocin에 잘 반응하는 것으로 보이지만, 메티실린뿐 아니라 aminoglycoside와 macrolide 계열의 여러 항생제에 저항성을 나타낼 수 있다. 한 국내 연구에 따르면[12], 전층각막 이식수술 후 이식편감염이 발생한 환자군에서 치료 실패의 흔한 원인은 기존의 이식 실패력, 이식 각막의 오랜 보존 기간, 진균각막염이었다. 또, 해당 연구에서 실시한 균배양 검사상 균이 검출된 15명(53.6%) 중 세균성 감염 9예, 진균성 감염 6예였으며, 그중 가장 흔한 세균성 원인은 Streptococcus 종이었고(6명, 40.0%), 그 외에도 Acinetobacter baumanii, Enterobacter cloaca, Klebsiella ornithinolytica가 1예씩 검출된 바 있다. 하지만 본 증례에서 검출된 항생제 내성 균주 감염에 의한 전층각막이식수술 후 안내염에 대한 논문은 국내에 보고되지 않았으며, 국외 보고에서 전층각막이식 후 발생한 안내염의 원인균이 S. hominis인 경우는 약 1.25%로 매우 낮았다[6].
이 논문의 주요 의의는 첫째, 전층각막이식수술 후 발생한 메티실린 내성 S. hominis 안내염의 최초 보고라는 점이다. 기존 국내 연구에서 각막이식 후 이식절편 감염 및 이식 실패의 위험요소를 분석한 바 있지만[9,12], 국외 연구 결과처럼 다양한 균이 검출되지 않아 원인균에 대한 자세한 분석이 이루어지지 않았다는 한계가 있고, 특히 각막이식 후 발생한 세균안내염에 대한 국내 보고가 거의 없었기 때문에, 본 증례의 항생제 내성균에 의한 안내염의 임상적 경과보고가 의미가 있을 것으로 생각된다. 본 예에서 검출된 S. hominis는 MRCoNS로, 최근 20년간 인공삽입물 사용, 면역저하 환자 증가 등 병원 감염이 증가하는 경향의 주요 원인이다[13]. Kato and Hayasaka [14]에 의하면, 메티실린 내성균에 의한 안내염의 약 절반 이상(56%)이 피부상재균과 같이 수술 전부터 안구 결막에 무증상 감염된 상태로 존재한다. MRCoNS균은 methicillin-resistant Staphylococcus aureus와 마찬가지로 광범위한 항생제 사용 증가로 증가하며, 해당 균주들에 의한 안감염의 위험요인은 80세 이상 고령, 비강 내 또는 인후 동일 균주 존재, 누비관 폐쇄, 안구건조증, 최근 입원력 및 국소적 면역억제 등이었다[14]. 본 증례는 각막이식 후 아급성으로 발생하여 병원감염에 의한 안내염은 아닐 것으로 생각되며, 고령, 이식실패 과거력, 당뇨, 광범위 항생제 사용과 스테로이드 점안제 등의 위험요인에 의해 항생제 내성균이 감염된 경우로 생각된다. 따라서, 항생제 내성 감염의 다양한 위험요인이 있는 환자에서 각막이식 수술 후 항생제에 잘 반응하지 않는 각막감염 징후가 확인될 경우, 이식 후 감염에 대한 의심과 적극적인 균배양검사 및 빠른 경험적 항생제 치료를 염두에 두어야 한다. 또, 향후 노인 인구 비중이 높아질수록 이러한 항생제 내성균에 의한 감염 및 안내염이 호발하게 될 가능성이 있어 관련 연구가 추가 진행되어야 할 필요가 있다. 둘째, 고령과 당뇨 등 기저질환을 가진 면역 약화자에게는 피부 상재균의 단순 감염이라도 악화되어 안내염으로 발전할 여지가 있으므로 급성기가 지난 후에도 주의해야 한다는 점이다. 셋째, 안내염으로 발전했더라도 빠른 유리체절제술과 균주에 반응하는 적절한 항생제 치료가 조기에 병행될 경우, 안구 보존 및 이식각막 보존까지도 가능하다는 것이다. 각막이식 수술 후 발생한 안내염과 각막염에서 배양검사에 의한 조기 원인균 동정은 안내염의 최종 시력예후에 영향을 미치는 가장 중요한 인자이며, 감염 균주의 종류와 그에 따른 적절한 항생제 치료가 안내염 치료에 중요한 역할을 하는 것은 잘 알려져 있다[15]. 비록 유리체절제술이 안내염 환자의 최종시력에 영향을 끼치는지 여부에 대해서는 논란이 있지만[15,16], 초기 시력 광각 이하인 환자에서 조기 유리체절 제술이 효과적이라는 Endophthalmitis Vitrectomy Study [17]를 비롯한 이전 연구 결과를 볼 때[18], 전층각막이식수술 후에라도 안내염 발생 시 즉시 유리체절제술을 시행한 것이 안구 유지에 도움을 준 증례라는 의의가 있다.
Figure 1.
Anterior segment photograph and B-scan ultrasonography at the initial presentation. (A) Penetrating keratoplasty status, diffuse corneal opacity and eccentric small pupil were seen. No definite corneal suture was found. (B) Ultrasonography shows no definite vitreous opacity at initial presentation.
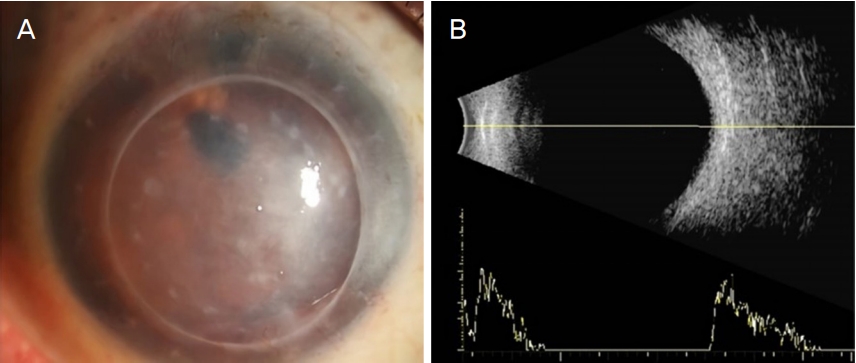
Figure 2.
Anterior segment photographs 25 days after penetrating keratoplasty re-operation. (A, B) Although corneal transparency was recovered 25 days after re-operation, corneal epithelial defect with stromal infiltration at 5 o'clock (about 1 × 1 mm2) was first seen.
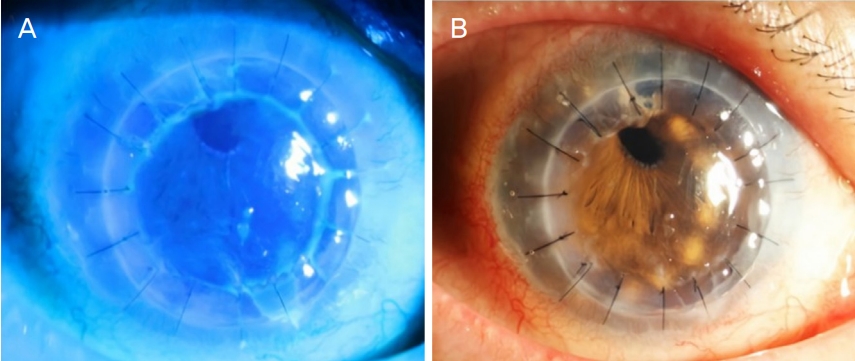
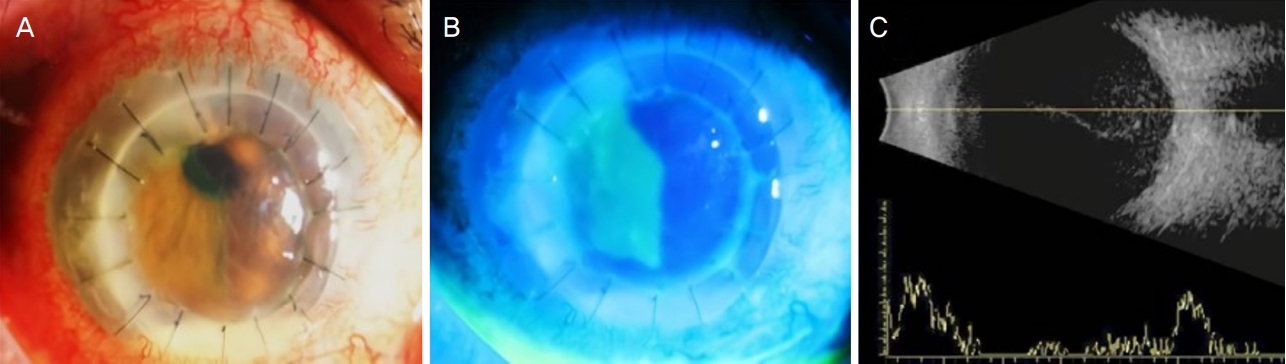
Figure 3.
Anterior segment photographs and B-scan ultrasonography 35 days after penetrating keratoplasty re-operation. (A) Hypopyon (about 1 mm) and corneal opacity throughout suture site were seen. (B) Diffuse corneal defect after staining were discovered. (C) Ultrasonography shows heterogeneous vitreous infiltration.
REFERENCES
1) Leveille AS, McMullan FD, Cavanagh HD. Endophthalmitis following penetrating keratoplasty. Ophthalmology 1983;90:38-9.


2) Eifrig CW, Flynn HW Jr, Scott IU, Newton J. Acute-onset postoperative endophthalmitis: review of incidence and visual outcomes (1995-2001). Ophthalmic Surg Lasers 2002;33:373-8.


3) Guss RB, Koenig S, De La Pena W, et al. Endophthalmitis after penetrating keratoplasty. Am J Ophthalmol 1983;95:651-8.


4) Kloess PM, Stulting RD, Waring GO 3rd, Wilson LA. Bacterial and fungal endophthalmitis after penetrating keratoplasty. Am J Ophthalmol 1993;115:309-16.


5) Tran KD, Yannuzzi NA, Si N, et al. Clinical features, antimicrobial susceptibilities, and treatment outcomes of patients with culture positive endophthalmitis after penetrating keratoplasty. Am J Ophthalmol Case Rep 2018;9:62-7.



6) Alharbi SS, Alrajhi A, Alkahtani E. Endophthalmitis following keratoplasty: incidence, microbial profile, visual and structural outcomes. Ocul Immunol Inflamm 2014;22:218-23.


7) Wagoner MD, Al-Swailem SA, Sutphin JE, Zimmerman MB. Bacterial keratitis after penetrating keratoplasty: incidence, microbiological profile, graft survival, and visual outcome. Ophthalmology 2007;114:1073-9.


8) Al-Hazzaa SA, Tabbara KF. Bacterial keratitis after penetrating keratoplasty. Ophthalmology 1988;95:1504-8.


9) Kwon HJ, Chung HS, Lee YM, et al. Patients at high risk for failure of penetrating keratoplasty. J Korean Ophthalmol Soc 2021;62:12-20.

10) Bouchami O, Ben Hassen A, de Lencastre H, Miragaia M. Molecular epidemiology of methicillin-resistant Staphylococcus hominis (MRSHo): low clonality and reservoirs of SCCmec structural elements. PLoS One 2011;6:e21940.



11) Wang N, Yang Q, Tan Y, et al. Bacterial spectrum and antibiotic resistance patterns of ocular infection: differences between external and intraocular diseases. J Ophthalmol 2015;2015:813979.



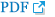
12) Sung MS, Choi W, You IC, Yoon KC. Factors affecting treatment outcome of graft infection following penetrating keratoplasty. Korean J Ophthalmol 2015;29:301-8.



13) Ormerod LD, Ho DD, Becker LE, et al. Endophthalmitis caused by the coagulase-negative staphylococci. 1. Disease spectrum and outcome. Ophthalmology 1993;100:715-23.


14) Kato T, Hayasaka S. Methicillin-resistant Staphylococcus aureus and methicillin-resistant coagulase-negative staphylococci from conjunctivas of preoperative patients. Jpn J Ophthalmol 1998;42:461-5.


15) Lee SB, Han JW, Chung SK, Baek NH. Factors associated with visual outcomes of postoperative endophthalmitis following cataract surgery. J Korean Ophthalmol Soc 2005;46:1618-23.
16) Pijl BJ, Theelen T, Tilanus MA, et al. Acute endophthalmitis after cataract surgery: 250 consecutive cases treated at a tertiary referral center in the Netherlands. Am J Ophthalmol 2010 149:482-7. e2.


17) Results of the Endophthalmitis Vitrectomy Study. A randomized trial of immediate vitrectomy and of intravenous antibiotics for the treatment of postoperative bacterial endophthalmitis. Endophthalmitis Vitrectomy Study Group. Arch Ophthalmol 1995;113:1479-96.


18) Kuhn F, Gini G. Complete and early vitrectomy for endophthalmitis (CEVE) as today’s alternative to the endophthalmitis vitrectomy study. In: Kirchhof B, Wong D, ed. Vitreo-retinal Surgery. Heidelberg: Springer, 2007;53-68.
-
METRICS

- Related articles
-
Streptococcus infantarius Endophthalmitis after XEN Gel Stent Implantation2021 October;62(10)
A Case of Staphylococcus lugdunensis Endophthalmitis after Cataract Surgery.2016 June;57(6)
A Case of Fungal Endophthalmitis Developed Early After Penetrating Keratoplasty.2008 July;49(7)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



