 |
 |
| J Korean Ophthalmol Soc > Volume 65(2); 2024 > Article |
|
국문초록
증례요약
2명의 환자가 습성 나이관련황반변성으로 유리체강 내 브롤루시주맙 주입술 1달 후 시력저하가 있었다. 증례1의 85세 남성은 좌안 스넬렌시력 0.2에서 안전수동으로 저하되었고, 증례2의 70세 여성은 우안 시력 0.4에서 안전수지 50 cm로 저하되었다. 두 환자 모두 내원 당시 전방 내 염증세포가 관찰되었고 형광안저촬영에서 망막동맥의 충만시간이 지연되어, 폐쇄성 망막혈관염 진단 하에 스테로이드 점안 및 정맥 주사 치료를 시행하였다. 증례1의 경우 인공수정체 후방의 염증막에 대한 유리체절제술을 추가로 시행하였다. 두 증례 모두 적극적인 치료에도 시력은 호전되지 않았다.
ABSTRACT
Purpose
To report two instances of retinal arterial occlusive vasculitis following intravitreal injection of brolucizumab.
Case summary
Two patients noted decreased visual acuity approximately one month after receiving intravitreal brolucizumab injections to treat wet age-related macular degeneration. In case 1, an 85-year-old male reported a reduction in visual acuity in his left eye, declining from a Snellen measurement of 0.2 to hand motion. In case 2, a 70-year-old female experienced a decline in visual acuity in her right eye from 0.4 to finger count at 50 cm. Both patients presented with anterior chamber reactions, and fluorescein angiography demonstrated delayed retinal artery filling time, leading to the diagnosis of retinal occlusive vasculitis. They were treated with both topical and systemic corticosteroids. For case 1, a subsequent vitrectomy was performed to remove the inflammatory membrane located behind the intraocular lens. However, despite aggressive interventions, neither patient showed visual improvement.
브롤루시주맙(Beovu®, Novartis, Basel, Switzerland)은 혈관내피세포성장인자(vascular endothelial growth factor, VEGF)-A와 결합함으로써 VEGF receptor (VEGFR)-1과 VEGFR-2와의 상호작용을 막아 VEGF를 억제한다. 단일 사슬 단편으로 타 anti-VEGF 제제에 비해 분자량이 26 kDa으로 작아 동일한 부피에 더 많은 분자를 주입할 수 있고, 작은 크기로 인해 안구 조직에 잘 침투하여 망막에 높은 농도로 도달할 수 있다.1
HAWK와 HARRIER 3상 임상 연구에서 습성 나이관련황반변성 치료 시 브롤루시주맙은 48주 동안 최대교정시력 변화에서 애플리버셉트(Eylea®, Regeneron, Tarrytown, NY, USA)와 비교 시 비열등성을 보였으며, 망막두께, 망막내액 및 망막하액의 감소와 관련된 해부학적 결과는 브롤루시주맙이 애플리버셉트보다 우세하였다.2 약 50%의 브롤루시주맙 치료 환자에서 48주까지 12주마다 투여 간격을 유지할 수 있었고, 8주마다 시행한 애플리버셉트 치료와 비교할 때 유사한 효과를 보였다.2
하지만 브롤루시주맙은 안구 내 염증과 관련된 이상 반응이 보고된 바 있다. 심한 경우 폐쇄성 망막혈관염(2.1%)이 생길 수 있으며 이로 인해 중등도 이상의 시력 감소(0.74%) 또한 보고되었다.3 유리체강 내 브롤루시주맙 치료 중 안구 내 염증이 발생한 환자는 망막혈관염 또는 망막혈관폐쇄로 발전할 위험이 있을 수 있으므로 면밀히 모니터링해야 한다.4 유리체강 내 브롤루시주맙 주입술 후 안구 내 염증을 동반한 폐쇄성 망막혈관염으로 심한 시력저하를 보였던 사례를 경험하였기에 저자들은 문헌 고찰과 함께 보고하고자 한다.
(증례 1) 85세 남자 환자가 1달 전 좌안의 습성 나이관련황반변성으로 유리체강 내 브롤루시주맙 주입술 후 시력저하를 주소로 내원하였다. 좌안의 최대교정 스넬렌시력은 주사 전 0.2에서 안전수동으로 저하되었다. 과거력상 당뇨가 있었고, 협심증으로 심장스텐트 시술 후 아스피린을 복용 중이었으며 이전 경동맥검사상 병변 반대측인 우측 근위부 내경동맥이 좁아져 있었다. 3년 전부터 양안의 습성 나이관련황반변성으로 양안 유리체강 내 라니비주맙 주입술 3회, 양안 유리체강 내 애플리버셉트 주입술을 4회 치료 받았었다. 브롤루시주맙 주사 2주 후 경과 관찰 시 주관적 시력저하를 호소하지 않았고, 교정시력은 0.2였다. 세극등검사상 전방 내 염증세포는 관찰되지 않았으며 빛간섭단층촬영에서 망막하액의 감소 소견이 관찰되었다. 주사 1달 후 내원 시, 환자 진술상 주사 20일 후부터 시력이 저하되었다고 하였으며, 세극등검사에서 전방 내 염증세포(2+)가 관찰되었고 인공수정체 후방으로 염증막 소견이 관찰되었다(Fig. 1). 빛간섭단층촬영검사상 치료 전 보였던 망막하액은 호전되었으나, 황반부위 망막내층 반사도의 증가 소견이 관찰되었다(Fig. 2A, B). 광각안저촬영상 망막은 창백하고 혼탁하였으며 시신경유두 주위 망막부종이 관찰되었다(Fig. 2C). 형광안저촬영에서 46초에 주변부 혈관누출 소견과 함께 망막동맥과 정맥의 형광충만장애가 관찰되었고, 7분 경과에서도 전반적인 혈류충만장애가 지속되는 심한 폐쇄성 망막혈관염 소견을 보였다(Fig. 2D, E). 중심망막동맥폐쇄 원인 감별을 위해 추가로 혈액검사, 경동맥검사를 시행하였다. 혈액검사는 온혈구검사, 프로트롬빈시간, 활성화부분트롬 보플라스틴시간, 혈중콜레스테롤, 혈중중성지방, 혈중고밀도지단백콜레스테롤과 혈중저밀도지단백콜레스테롤을 포함해 시행하였다. 혈액검사 결과에 이상 소견은 없었으며, 경동맥검사는 이전 검사와 차이가 없었다. 이를 종합하여 안구 내 염증을 동반한 폐쇄성 망막혈관염으로 진단하고 당일 테논낭하 triamcinolone acetonide (Triam®, Shinpoong Pharmaceuticals, Seoul, Korea) 주사를 시행하고 dexamethasone (Dexamethasone Yuhan Inj 5 mg/1 mL, Yuhan Corp., Seoul, Korea)을 3일간 하루 1회 12 mg 정맥 주사하였다. 국소 안약으로 1% prednisolone 점안액(Optipredy®, Reyon Pharm Co., Seoul, Korea), 0.1% bromfenac 점안액(Bronuck®, Taejoon, Seoul, Korea), brimonidine 점안액(Alphagan®, Allergan Inc., Irvine, CA, USA)을 각각 하루 3회 점안 지시하였고, 이후 외래에서 경구용 prednisolone (Solondo Tab, Yuhan Corp.) 30 mg을 하루 1회 7일간 투여 후, 2주 간격으로 5 mg씩 감량하였다. 약물 치료 도중 인공수정체 후방의 염증막으로 안저가 잘 관찰되지 않아 유리체절제술을 시행하였고 검체 배양 결과 균동정은 되지 않았다. 치료 3달 이후 최대교정시력은 안전수동으로 호전 없이 유지되었고 광각안저촬영 상 전반적으로 얇아진 망막혈관 및 망막출혈 소견이 보였다(Fig. 2F).
(증례 2) 70세 여자 환자가 양안 습성 나이관련황반변성으로 1달 전 우안 브롤루시주맙 주입술 후 시력저하 및 통증을 주소로 내원하였다. 우안의 최대교정 스넬렌시력은 0.4에서 안전수지 50 cm로 저하되었다. 과거력상 고혈압, 고지혈증, 파킨슨 증후군을 가지고 있었다. 4년 전부터 우안 유리체강 내 베바시주맙주입술 4회, 3년 전 우안 유리체강 내 애플리버셉트주입술 2회를 시행받았다. 브롤루시주맙 주사 2주 후 내원 시 교정시력 0.3으로 저하되었으나 주관적 시력저하를 호소하진 않았고, 세극등검사상 전방 내 염증세포는 관찰되지 않았으며 빛간섭단층촬영에서 망막하액은 감소하였다. 주사 1달 후 내원 시 환자 진술상 주사 26일 후부터 시력이 저하되었다고 하였으며 세극등검사상 전방 내 염증세포(0.5+)가 관찰되었고, 빛간섭단층촬영검사상 중심와곁 위쪽 부위에서 치료 전 보였던 망막하액은 호전되었다(Fig. 3A, B). 광각안저촬영상 유리체혼탁(1+)과 심한 망막동맥의 폐쇄가 관찰되었다(Fig. 3C). 형광안저촬영에서 주변부 혈관누출이 관찰되었고 34초가 지나서도 주변부의 망막동맥과 정맥의 폐쇄와 혈류저하가 있었고, 11분의 경과에서도 혈류충만장애가 지속되는 심한 폐쇄성 망막혈관염 소견을 보였다(Fig. 3D, E). 중심망막동맥폐쇄 감별을 위해 시행한 경동맥검사에서 정상 소견, 혈액검사 결과 이상 소견은 보이지 않았다. 안구 내 염증을 동반한 폐쇄성 망막혈관염으로 내원 당일부터 dexamethasone을 6일간 하루 1회 12 mg 정맥 주사하였다. 국소 안약으로 1% prednisolone 점안액을 하루 6회, 0.1% bromfenac 점안액을 하루 6회, brimonidine 점안액을 하루 3회 점안 지시하였고, 이후 외래에서 경구용 prednisolone 30 mg을 하루 1회 7일간 투여 후 1주 간격으로 5 mg씩 감량하였다. 치료 2달 이후 최대교정시력은 안전수지 30 cm로 저하되었고, 광각안저촬영 상 전반적인 망막혈관폐쇄과 함께 창백한 망막 소견을 보였다(Fig. 3F).
습성 나이관련황반변성에서 기존 anti-VEGF 약제에 저항성을 보이는 경우 브롤루시주맙으로 약제 변경 시 좋은 효과를 보일 수 있다. 보고에 따르면 기존 유리체강 내 anti-VEGF(애플리버셉트, 베바시주맙, 라니비주맙)을 사용하였으나 최대교정시력과 중심망막두께의 유의적인 개선이 없는 군에서 브롤루시주맙으로 전환 후 82.7%에서 최대교정시력 및 중심망막두께가 개선되었으며, 30.8%에서 12주 이상으로 유리체강 내 주입술 치료 간격을 연장할 수 있었다.5-7
하지만 브롤루시주맙은 일부 환자에서 안구 내 염증에 대한 안전성 문제가 대두되었다. 안전성검토위원회(Safety Review Committee)가 3상 HAWK 및 HARRIER 임상 시험에서 보고된 안구 내 염증, 망막혈관염, 망막혈관폐쇄에 대한 사례를 분석하였을 때, 안구 내 염증의 발생률은 4.6%, 안구 내 염증을 동반한 망막혈관염 발생률은 3.3%, 안구 내 염증과 망막혈관염을 동반한 망막혈관폐쇄 발생률은 2.1%였다.3 이 중 Early Treatment Diabetic Retinopathy Study (ETDRS) 15글자 이상의 감소가 있는 사례는 0.74%였으며 이 중 50%의 안구 내 염증이 첫 브롤루시주맙 주사 후 3개월 이내에 생겼다.3 반면 애플리버셉트 치료군에서는 안구 내 염증의 발생률은 1.1%였으며, 중등도의 시력 감소는 0.14%였다.3 Pakravan et al8 보고에서는 안구 내 염증의 발생이 평균 20일(1-56일)에 발생하였다.
미국망막전문의학회(American Society of Retina Specialists)의 보고에 따르면 브롤루시주맙 사용 후 망막혈관염은 총 26안에서 발견되었으며, 대부분의 사례(92%)에서는 안구 내 염증과 관련이 있었으며, 브롤루시주맙 주사 후 평균 25일(3-63일)에 발현되었다. 12안(46%)은 최종 경과 관찰 시 3줄 이상의 시력 감소를 경험하였으며, 최종 시력은 20/200 이하였다. 이 중 안저검사상 망막동맥(91%), 망막정맥(79%) 및 맥락막혈관(48%)에서 이상 소견이 확인되었다.9
두 증례 모두 고령의 환자로 중심망막동맥폐쇄의 위험을 높일 수 있는 기왕력이 있었다. 증례1은 당뇨, 협심증이 있었으며 증례2는 고혈압, 고지혈증, 파킨슨증후군이 있었다. 이에 추가로 경동맥검사와 혈액검사를 시행하였다. 경동맥 검사상 증례1에서는 이전부터 있었던 병변부 반대측의 협착만 있었고 증례2는 이상 소견은 없었다. 또한 두 증례 모두 온혈구검사, 프로트롬빈시간, 활성화부분트롬보플라스틴시간, 혈중콜레스테롤, 혈중중성지방, 혈중고밀도지단백콜레스테롤과 혈중저밀도지단백콜레스테롤을 포함한 혈액검사에서 이상이 없어 중심망막동맥폐쇄를 일으킬 만한 인자는 없다고 판단하였다. 두 증례 모두 브롤루시주맙 치료 후 1달 이내 안구 내 염증을 동반한 폐쇄성 망막혈관염이 생긴 점으로 보아 브롤루시주맙에 의한 이상 반응으로 생각해 볼 수 있겠다.
Kusuhara et al10은 형광안저혈관조형술에서 명백한 이상 소견이 없는 상태에서도 브롤루시주맙과 관련된 지연된 안구 내 염증와 망막혈관폐쇄가 발생한 증례를 보고하였다. 브롤루시주맙 유리체강 내 투여에 의한 강력하고 지속적인 VEGF 억제 작용으로 인해 망막혈관내피세포에 심각한 손상이 발생할 수 있으며 이후 망막혈관폐쇄를 유발하고 브롤루시주맙에 대한 면역 반응을 강화시킬 수 있다고 보고하였다.
브롤루시주맙 합병증 치료에 대한 권고사항으로 환자들은 브롤루시주맙 치료 후 부작용과 관련된 증상(시력의 갑작스러운 감소 또는 변화 등)을 신속히 보고하여 조기에 치료받을 수 있도록 교육되어야 한다. 또한 드물지만 망막혈관염 또는 망막혈관폐쇄와 같은 불가피한 비가역적 합병증이 발생할 수 있음을 미리 설명해야 한다. 일반적으로 브롤루시주맙 치료 후 2개월 이내에 다양한 중등도의 안구 내 염증, 망막혈관염 또는 망막혈관폐쇄가 나타나므로 시력감소, 흐려진 시야, 부유물의 증가, 눈의 발적 등의 증상이 나타나거나 안구 내 염증으로 진단된 환자들에게는 광각안저촬영, 형광안저혈관조영술, 빛간섭단층촬영들을 시행하여 동반된 망막혈관염 또는 망막혈관폐쇄에 대해 평가해야 한다.
일반적으로 망막혈관염 또는 망막혈관폐쇄가 확인되면 브롤루시주맙 치료는 중단하고 스테로이드 점안제, 전신 스테로이드 치료가 권장되고 중등도에 따라 유리체강 내 또는 테논낭하 스테로이드 주사 치료를 하는 경우도 있다.4 일부 보고에서 유리체절제술을 시행하였지만 추가적인 임상적 이점을 얻지 못하였다고 한다.8 하지만 아직 최적의 치료 전략은 알려지지 않았다. 증례의 환자들에서는 적극적인 치료에도 시력 개선이 되지 않고 안전수지 이하의 심한 시력저하가 발생하였다. 첫 번째 증례의 경우 3달 후, 두 번째 증례의 경우 2달 후 추적 관찰 탈락되어, 브롤루시주맙 치료 후 망막혈관폐쇄의 장기간 경과를 확인할 수 없어 초기 경과만을 보고하였다.
본 증례에서는 기존 anti-VEGF 치료에 반응이 좋지 않은 습성 나이관련황반변성 환자에서 브롤루시주맙 6 mg 1회 투여 1달 후 망막부종 및 망막하액은 호전되었으나 안구 내 염증을 동반한 심한 폐쇄성 망막혈관염이 발생하였고, 이에 대해 고용량 스테로이드 치료를 시행하였음에도 심한 시력저하를 보였다. 브롤루시주맙의 유리체강 내 주입술 후 폐쇄성 망막혈관염이 발생할 수 있으며 적극적인 치료에도 시력장애를 초래할 수 있기 때문에 주의를 요한다.
Figure 1.
After treatment with brolucizumab, a thick whitish inflammatory membrane was observed behind the intraocular lens.
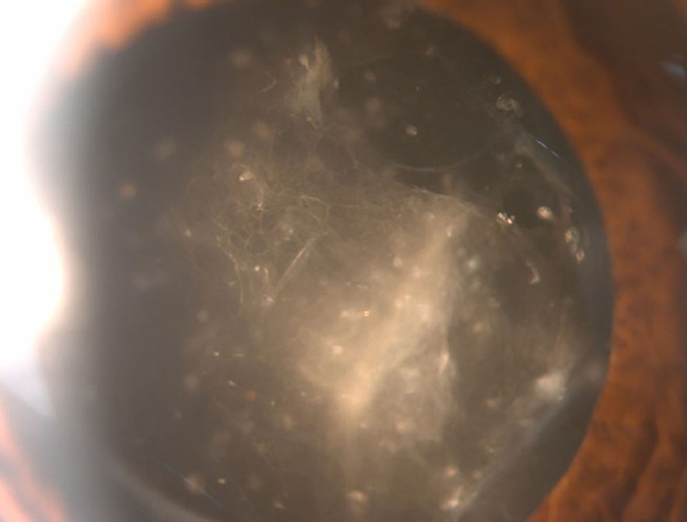
Figure 2.
Images of an 85-year-old male with wet age-related macular degeneration. (A) Before the first intravitreal brolucizumab injection, subretinal fluids were noticed in optical coherence tomography (OCT). (B) One month after the intravitreal brolucizumab injection, subretinal fluid decreased. Hyperreflectivity with edema of inner retinal layers at the nasal part of the macula was noticed in OCT. (C) The wide fundus photography showed pale and cloudy retinas with retinal edema around the optic nerve head. (D, E) Fluorescein angiography show marked arterial and venous filling defect, which persisted into the late phase. (F) Three months after the intravitreal brolucizumab injection, whitish retinal thickening around the optic nerve head and scattered retinal blot hemorrhages noticed in the wide fundus photography.
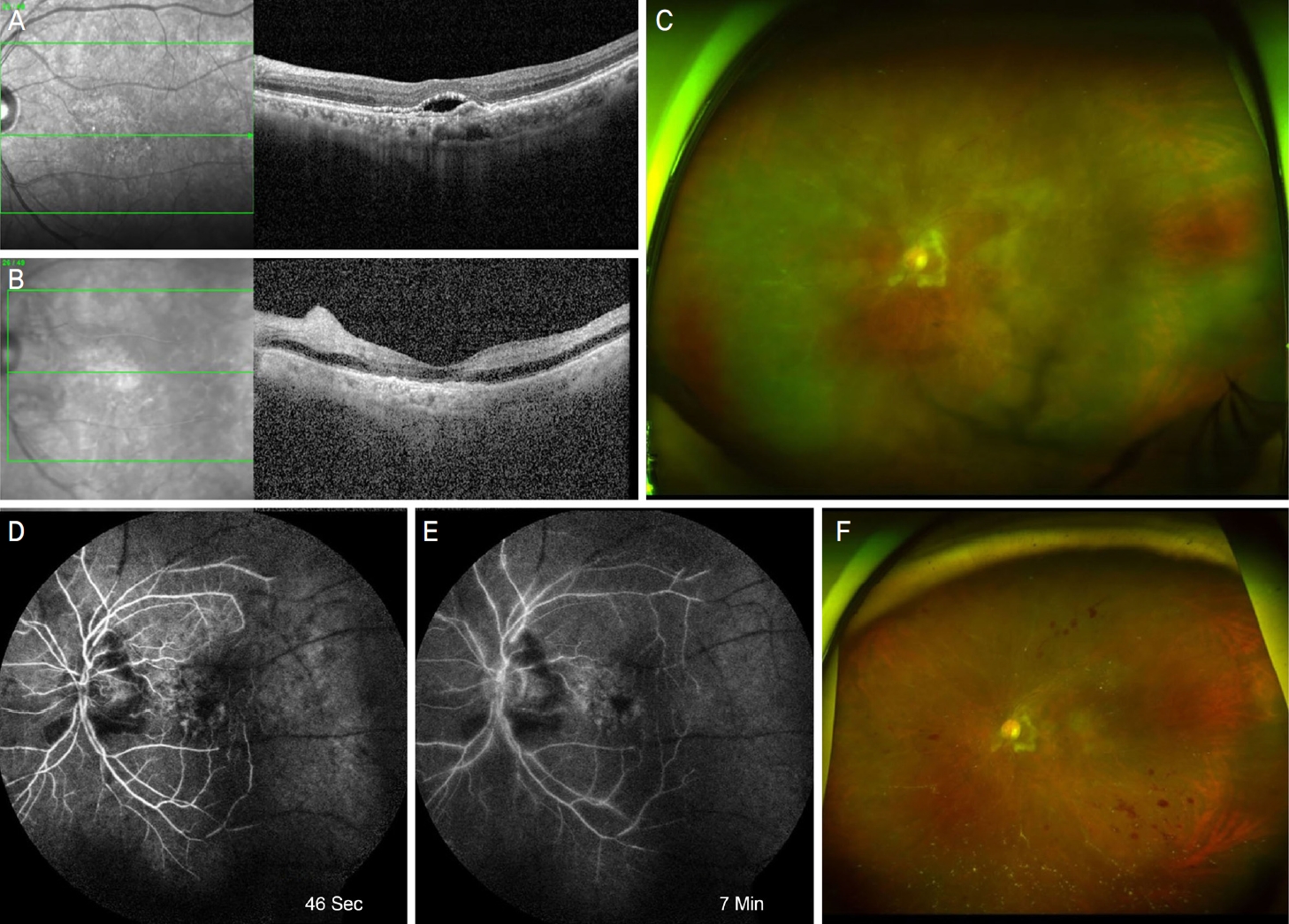
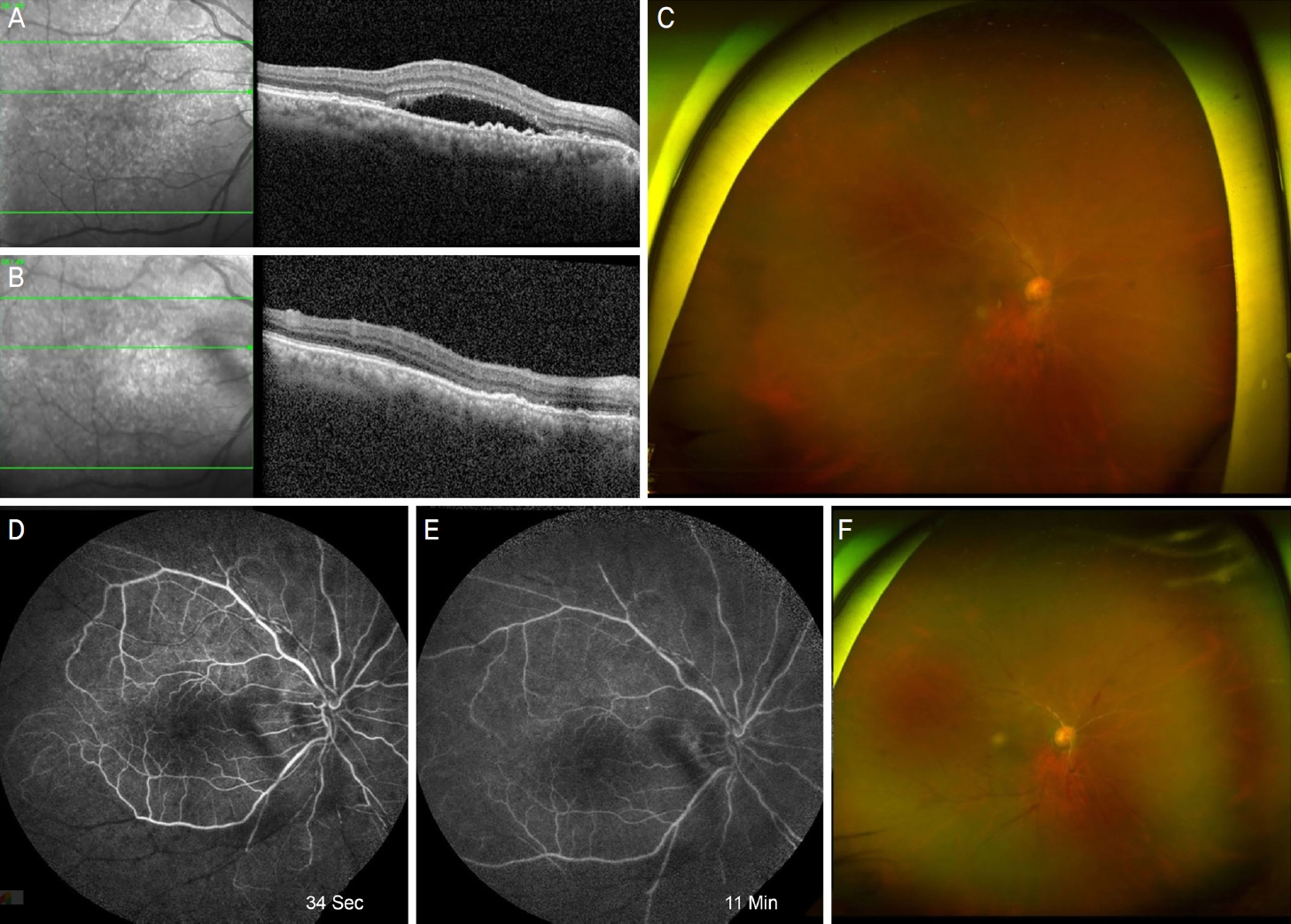
Figure 3.
Images of a 70-year-old female with wet age-related macular degeneration. (A) Before the first intravitreal brolucizumab injection, subretinal fluids were noticed in optical coherence tomography (OCT). (B) One month after the intravitreal brolucizumab injection, subretinal fluid decreased. (C) The wide fundus photography showed vitreous opacity 1+, and diffuse arterial attenuation. (D, E) Fluorescein angiography show marked arterial and venous filling defect, which persisted into the late phase. (F) Two months after the intravitreal brolucizumab injection, severe arterial attenuation was found in the wide fundus photography.
REFERENCES
1) Tietz J, Spohn G, Schmid G, et al. Affinity and potency of RTH258 (ESBA1008), a novel inhibitor of vascular endothelial growth factor a for the treatment of retinal disorders. Invest Ophthalmol Vis Sci 2015;56:1501.
2) Dugel PU, Koh A, Ogura Y, et al. HAWK and HARRIER: phase 3, multicenter, randomized, double-masked trials of brolucizumab for neovascular age-related macular degeneration. Ophthalmology 2020;127:72-84.


3) Monés J, Srivastava SK, Jaffe GJ, et al. Risk of inflammation, retinal vasculitis, and retinal occlusion-related events with brolucizumab: post hoc review of HAWK and HARRIER. Ophthalmology 2021;128:1050-9.

4) Baumal CR, Bodaghi B, Singer M, et al. Expert opinion on management of intraocular inflammation, retinal vasculitis, and vascular occlusion after brolucizumab treatment. Ophthalmol Retina 2021;5:519-27.


5) Chronopoulos A, Huynh E, Ashurov A, et al. Brolucizumab for recalcitrant macular neovascularization in age-related macular degeneration with pigment epithelial detachment. Eur J Ophthalmol 2023 Jul 18 doi: 10.1177/11206721231187663. [Epub ahead of print].

6) Van Cleemput L, Peeters F, Jacob J. Brolucizumab for neovascular age-related macular degeneration (BEL study). Clin Ophthalmol 2023;17:1077-85.


7) Yeom H, Kwon HJ, Kim YJ, et al. Real-world study to evaluate the efficacy and safety of intravitreal brolucizumab for refractory neovascular age-related macular degeneration. Sci Rep 2023;13:11400.



8) Pakravan P, Patel V, Lai J, et al. Intraocular inflammation incidence after intravitreal brolucizumab injection for exudative age-related macular degeneration. Retina 2023;43:1717-22.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 322 View
- 52 Download
- Related articles
-
Safety Evaluation of Bilateral Same-day Intravitreal Injections of Bevacizumab2020 October;61(10)
Noninfectious Endophthalmitis after Intravitreal Injection of Aflibercept.2016 June;57(6)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



