 |
 |
| J Korean Ophthalmol Soc > Volume 61(6); 2020 > Article |
|
국문초록
목적
마이봄선기능장애(MGD)환자에서 BlephExTM (Scope Ophthalmics, London, UK)를 이용한 안검미세각질제거 후의 임상적 효과를 객관적 수치를 통해 알아보고자 한다.
대상과 방법
2018년 10월부터 11월까지 세브란스병원에서 MGD로 진단받은 24명의 양안에 대하여 8-10분간 BlephExTM를 시행하였으며 이들의 안구표면질환지수(OSDI), 눈물막파괴검사, 쉬르머 검사, 각막염색지수, 눈꺼풀 경계 이상, 마이봄선기능장애정도와 Lipiview II 간섭계(TearScience Inc., Morrisville, NC, USA)를 통한 눈물지질층두께를 치료 전과 치료 후 1개월째에 조사하여 비교하였다.
결과
BlephExTM 사용 시 눈물층파괴시간은 치료 전 2.65 ± 1.16초에서 치료 1달 후 3.77 ± 1.80초로 유의미하게 증가하였다(p<0.001). 눈꺼풀 경계 이상은 치료 전 2.98 ± 1.16점에서 2.50 ± 1.01점으로 감소하였으며(p<0.001), 마이봄선기능장애정도 또한 치료 전 21.60 ± 6.95점에서 18.02 ± 6.68점으로 호전 정도가 유의미하였다(p=0.001). OSDI는 치료 전 38.83 ± 17.13점에서 치료 1달 후 18.67 ± 15.01점으로 유의미하게 감소하였다(p<0.001).
ABSTRACT
Purpose
To assess the clinical efficacy of microblepharoexfolication using BlephEx™ (Scope Ophthalmics, London, UK) in meibomian gland dysfunction (MGD) patients.
Methods
We performed a prospective study involving 48 eyes of 24 patients who were diagnosed with MGD. All patients were treated with BlephEx™ for 8-10 minutes, and the ocular surface disease index (OSDI), tear break-up time (TBUT), Schirmer’s I test, corneal staining score, lid margin abnormality, MGD score, and lipid thickness layer using the Lipiview II (TearScience, Morrisville, NC, USA) were assessed before treatment and after one month.
Results
Significant changes were observed after microblepharoexfoliation using BlephEx™. The TBUT improved from 2.65 ± 1.16 to 3.77 ± 1.80 after 1 month (p < 0.001) and the OSDI improved from 38.83 ± 17.13 to 18.67 ± 15.01 after 1 month (p < 0.001). Before and after 1 month of treatment, the lid margin abnormalities were 2.98 ± 1.16 and 2.50 ± 1.01 (p < 0.001) and the MGD scores were 21.60 ± 6.95 and 18.02 ± 6.68 (p = 0.001), respectively.
마이봄선기능장애(Meibomian gland dysfunction, MGD)란 마이봄선의 전반적이고 만성적인 이상을 의미하며 이는 주로 마이봄관 말단의 폐쇄 혹은 그와 동반되는 기름층의 양적인 혹은 질적인 변화를 특징으로 한다[1]. 이로 인해 눈물 지질층의 불안정성이 유발되며 눈의 자극감, 안구표면질환이 발생한다[1]. 이러한 기름층의 이상이 정상 세균총의 과증식을 유발하며[2] 안구표면의 염증을 증가시키고 추가적인 cytokine을 분비하여 우리가 흔히 말하는 건성안 증상이 발생한다고 알려져 있다[1,3].
Rynerson et al [4]은 이러한 기전의 중심에 눈꺼풀의 Biofilm을 주장한다. 정상적인 눈꺼풀경계에는 S. aureus, S. epidermidis로 대표되는 정상 세균총이 존재하는데 이들은 Polysaccharide/protein matrix로 된 Biofilm을 형성하게 된다[4-6]. Biofilm은 외부환경으로부터 세균을 보호하며 내부에 있는 영양분의 농도를 높여 세균이 살기 좋은 환경을 형성시켜준다[7]. 청결을 유지하기 힘든 위치인 눈꺼풀 경계에 형성된 Biofilm은 씻겨 내려가지 못하고 나이가 들수록 계속하여 쌓이게 된다. 이러한 Biofilm 안에서 세균이 내보내는 cytokine의 농도가 높아지고 서로를 인식할 수 있는 특정 농도에 도달하면 휴면기에 있던 유전자가 활성화되며 더 많은 해로운 인자들을 내보낸다[8-10]. 특정 농도에 도달해야 서로를 인식할 수 있게 되어 이를 Quorum sensing이라고 지칭하며 Biofilm 이라는 보호막이 이를 도와주는 것이다[8]. Quorum sensing 기전에 의해 발현되는 독소들은 눈꺼풀에서 그 정도와 범위에 따라 안검염, 마이봄선기능장애, 건성안 등을 일으키게 된다는 논리이다.
이러한 일원화된 문제의 시작점인 Biofilm을 효과적으로 제거하는 데에 있어 안검의 미세한 각질제거 및 청결이 필요하며 이에 적합한 장비로 BlephExTM (Scope ophthalmics, London, UK)가 주목받고 있다. BlephExTM는 손으로 조작할 수 있는 펜 사이즈의 기계로 기계 끝의 micro-sponge가 1,000 RPM의 속도로 회전하여 눈꺼풀 경계를 청소해주게 된다. 외래에서 안과 전문의가 8-10분간, 4-6개월 주기로 눈꺼풀 경계를 닦아주며 쌓여있던 미세한 각질과 Biofilm을 제거하는 형태의 치료로, 기존의 연구에서 demodex 안검염 치료로 BlephExTM가 입증된 바 있다[11]. 하지만 현재까지 한국에서는 BlephExTM의 사용이 대중화되지 않았으며, 이의 임상적인 치료 효과를 구체적이고 객관적인 수치로 분석해본 연구는 드물다. 이에 본 저자들은 마이봄선기능장애로 진단받은 환자에서 BlephExTM를 이용한 안검미세각질제거 치료의 임상적 효과를 평가해 보고자 한다.
2018년 10월 22일부터 2018년 11월 31일까지 세브란스병원 안과 외래에 건성안 증상으로 내원하여 마이봄선기능장애로 진료받은 19세 이상의 환자 24명을 대상으로 전향적 연구를 시행하였다. 본 연구는 본원 임상시험윤리위원회(Institutional Review Board, IRB)의 승인을 받았으며(승인 번호: 1-2018-0056), 의학연구윤리강령인 헬싱키선언을 준수하였다. 각 환자들은 자발적 참여 의사에 따라 대상자로 선정되었고, 연구에 대한 충분한 설명을 듣고 동의서를 작성하였다. 안과적 감염, 안과적 자가면역질환 및 전신질환이 있는 환자는 제외되었으며 환자들이 기존에 사용하던 안약의 종류 및 횟수는 그대로 유지하도록 하였다.
본 연구에 등록된 24명의 양안인 총 48안에 대하여 본 연구에 참여한 안과 전문의가 BlephExTM로 8-10분간 눈꺼풀을 닦아낸 후 1달 뒤 경과 관찰을 진행하였다. 연구 참여 시 모든 환자를 대상으로 눈물층파괴시간(Tear break-up time, TBUT), 제1형 쉬르머검사(Schirmer test type 1), 각막형광염색검사(Corneal staining score), 설문지를 통한 안구표면질환지수(Ocular Surface Disease Index, OSDI), Lipiview II (TearScience Inc., Morrisville, NC, USA) 간섭계를 통한 눈물지질층두께를 측정하였고, 세극등검사를 통해 눈꺼풀 경계 이상(lid margin abnormality)과 마이봄선기능장애정도(MGD score)를 평가하였다.
각막형광염색검사는 National Eye Institute corneal staining score를 사용하여 각막을 5개의 구역으로 나눠 염색 정도에 따라 grade 0부터 grade 3까지 점수를 준 후 합하여 총 0점에서 15점까지로 객관화하였다. 안구표면질환지수(OSDI)는 건성안 증상, 시야 이상에 따른 활동저하 정도, 환경 자극에 따른 증상으로 세분화하여 BlephExTM가 호전을 줄 수 있는 분야를 살펴보았다[12]. 눈꺼풀 경계 이상은 불규칙한 눈꺼풀 경계, 혈관의 울혈, 마이봄선 입구의 막힘, 눈꺼풀 점막피부 경계의 변화가 있을 때 각각 1점씩 부여하여 0-4점 범위로 수치화하였다[13]. 마이봄선기능장애정도는 Nichols et al [1]이 제시한 마이봄선 기능부전 진단 기준에 따라 Meibum quality (0-24점), expressibility (0-3점), digital pressure (0-3점) 각각을 점수화한 후 모두 더한 값으로 정의하였다.
통계학적 분석은 SPSS version 23.0 (IBM Corp., Armonk, NY, USA)을 이용하였으며 치료 전과 치료 후의 변화를 비교하기 위해 Wilcoxon signed rank test를 이용하였다. p값이 0.05 미만인 경우를 통계학적으로 유의한 수준으로 정의하였다.
연구 참여자 24명의 총 48안이 분석에 포함되었다. 환자군은 남자 4명, 여자 20명으로 평균 연령은 62.92 ± 8.80세였다(Table 1). 모든 환자들은 무방부제성 0.15% 히알루론산인공눈물(New hyaluni®, Taejoon Pharm. Co., Seoul, Korea)을 쓰고 있었으며, 0.1% 플루오로메톨론 스테로이드 안약(Ocumetholone 0.1%®, Samil Pharm. Co., Seoul, Korea)을 함께 쓰고 있던 안은 38안이었다. 이 중 3개월 이상의 기간 동안 스테로이드 안약을 쓰고 있던 안은 14안이었으며, 3개월 내의 기간으로 쓰고 있던 안은 24안이었다(Fig. 1).
눈물층파괴시간은 치료 전 2.65 ± 1.16초였으며 치료 1달 후 3.77 ± 1.80초로 유의미하게 증가하였다(p<0.001). 각막형광염색검사 및 제1형 쉬르머검사는 각각 치료 전 1.85 ± 2.98점, 9.25 ± 7.74 mm에서 치료 1달 후에 1.65 ± 3.32점(p=0.880), 9.31 ± 8.11 mm (p=0.292)로 호전되었으나 통계학적으로 유의미하지 않았다. 눈꺼풀 경계 이상은 치료 전 2.98 ± 1.16점에서 치료 1달 후에 2.50 ± 1.01점으로 유의한 감소를 보였다(p<0.001). 마이봄선기능장애정도 또한 치료 전 21.60 ± 6.95점에서 18.02 ± 6.68점으로 호전 정도가 유의미하였다(p=0.001). OSDI 전체 점수는 치료 전 38.83 ± 17.13점에서 치료 1달 후 18.67 ± 15.01점으로 유의미하게 감소하였다(p<0.001). OSDI의 평가 항목인 12가지를 세부 항목으로 나누어 분석해 보았을 때 건성안 증상 항목(3가지), 시야 관련 항목(6가지), 환경적인 자극 관련 항목(3가지) 모두에서 각각 유의미한 호전을 보였다(p<0.001) (Table 2).
Lipiview II를 통한 눈물지질층두께는 치료 전 88.27 ± 18.49 nm에서 치료 1달 후 87.19 ± 22.16 nm로 유의미한 차이는 아니었지만(p=0.732) 감소하는 결과를 보였다. 이에 초기 측정값이 최대값(100 nm)이 아닌 19안에 대해 추가 분석을 시행 시 치료 전 70.37 ± 18.23 nm에서 74.47 ± 28.37 nm로 증가하였으나 통계학적으로 유의미하지는 않았다(p=0.314) (Table 3).
안검미세각질제거의 효과에 있어 기존에 사용하던 스테로이드 안약의 영향을 보기 위해 인공눈물만 사용한 군(제1군, n=10), 인공눈물과 3개월 이상의 기간동안 스테로이드 안약을 사용한 군(제2군, n=14), 인공눈물과 3개월 내의 기간 동안 스테로이드 안약을 사용한 군(제3군, n=24)로 나누어 분석해 보았다. 제1군에서는 OSDI에서만 BlephExTM 치료 전 30.91 ± 14.42점에서 14.87 ± 7.41로 유의미한 감소가 있었으며(p=0.005) 눈물층파괴시간, 각막형광염색 정도, 눈꺼풀 경계 이상, 마이봄선기능장애정도는 호전을 보였으나 그 차이는 유의미하지 않았다(각각 p=0.059, p=0.206, p=0.180, p=0.408) (Table 4). 제2군에서는 치료 전에 비해 치료 후에 눈물층파괴시간은 3.29 ± 0.91에서 4.57 ± 1.79초로(p=0.022), 눈꺼풀 경계 이상은 3.29 ± 0.91점에서 2.57 ± 0.76점으로(p=0.019), OSDI에서는 34.40 ± 20.61점에서 13.91 ± 8.33점으로(p=0.004) 유의미한 호전을 보였다(Table 5). 마지막으로 제3군에서는 제2군에서 유의미하게 호전을 보인 항목에 추가적으로 마이봄샘기능장애정도가 치료 전 21.08 ± 7.92점에서 치료 1달 후에 16.96 ± 6.74점으로 유의한 호전을 보였다(p=0.001) (Table 6).
본 연구에서는 마이봄선기능장애로 진단받은 환자에서 BlephExTM를 이용한 안검미세각질제거 후 건성안 및 마이봄선기능장애 개선 정도를 객관적인 수치들로 분석해 보았다. BlephExTM는 2013년에 개발되었으나 우리나라에서는 최근 장비가 소개되었다. 안검염 치료에 주로 사용되고 있던 눈꺼풀청결은 안검염, 마이봄선기능장애, 건성안을 하나의 질환의 스펙트럼으로 고려하며 적용 범위가 넓어지고 있다. 본 연구에서는 특히 기구를 이용한 미세한 눈꺼풀의 각질, 즉 Biofilm 제거의 임상적 효과를 알아보았다는 점에서 의의를 갖는다.
본 연구에서 마이봄선기능장애 환자군의 눈물막파괴시간은 2.65 ± 1.16초에서 BlephExTM 치료 1달 후 3.77 ± 1.80초로 유의미하게 증가하였다(p<0.001). 이러한 결과는 BlephExTM를 통한 눈꺼풀 경계의 위생이 마이봄선기능장애를 감소시켜 지질의 질적인 분비의 변화로 눈물지질층의 불안정성이 호전된 것으로 생각된다. 혹은 눈꺼풀 경계 위생으로 안검 세균총에서 분비하는 Bacterial Lipase가 감소하여 지질층을 안정시켜 준 것으로 생각된다.
이는 또한 마이봄선기능장애의 연장선상에서 발생하게 되는 안구건조증을 완화시켜 환자가 호소하는 증상 및 기능적인 불편감을 낮춰주었다(치료 전 38.84 ± 17.13점, 치료 후 18.67 ± 15.01점, p<0.001, Table 2). OSDI는 다른 객관적인 수치들에 비해 큰 폭으로 감소하였는데, 이는 환자가 병원을 방문하게 되는 주 원인이 증상이라는 점을 고려했을 때 OSDI 수치의 개선을 통해 확인한 증상의 개선이 갖는 의의가 크다. 쉬르머검사와 각막염색지수는 유의한 차이를 보이지 않았으며 이를 통해 BlephExTM 치료는 눈물의 수성층에는 큰 역할을 하지 않을 것으로 사료된다.
마이봄선기능장애의 완화는 유의미한 눈꺼풀 경계 이상 및 마이봄선기능장애정도의 호전(p<0.001, p=0.001)으로 확인할 수 있으며, 이는 눈물지질층두께를 증가시킬 것으로 예상되나 대상이 되는 환자군의 초기 눈물지질층두께값이 BlephExTM 사용 전부터 최대값(100 nm)인 경우가 많아 오히려 감소하는 결과가 나왔다(Table 2). 이를 고려하여 추가 시행한 분석(Table 3)에서 그 값은 통계학적으로 의미가 있지는 않았으나 눈물지질층두께가 증가했다(치료 전 70.37 ± 18.23 nm, 치료 후 74.47 ± 28.37 nm, p=0.314). 이를 통해 마이봄선기능장애가 호전되어 눈물지질층두께의 증가로 이어지기까지는 1달 이상의 추적 관찰이 필요할 것으로 생각된다.
안구 표면의 염증은 만성 안검염 및 건성안의 원인이자 결과이며, 안구의 불편감, 자극감 등의 증상을 유발한다[14]. 많은 논문들에서 마이봄선기능장애를 가진 환자들의 눈물 내의 고농도 cytokine들을 보고한 바 있으며 그 종류에는 Serotonin, Interleukin (IL)-6, IL-8, IL-12, Matrix metalloproteinase-9 (MMP-9), Interferon-γ (IFN-γ), Tumor necrosis factor-α, IL-1, IL-17이 있다[15-19]. 이 중 특히 Serotonin의 경우 세균의 Quorum sensing을 유도하여[10] 독소를 내보내며 악순환을 일으킨다. 이에 따라 안구 표면의 염증을 줄이는 방안이 안검염 및 건성안의 치료 중 한 방향이 되었고, 염증을 조절하는 corticosteroid 안약 사용 시 건성안의 지표 및 증상이 호전됨을 보인 바 있다[20].
본 연구 결과에서도 인공눈물을 제외하고 BlephExTM만 사용한 군(group 1)에서는 OSDI를 통한 증상의 호전만이 유의미하였으나(Table 4), 스테로이드 안약을 같이 쓴 군(group 2, 3)에서는 증상뿐만 아니라 눈물막파괴시간, 눈꺼풀 경계 이상 수치에서도 유의미한 호전이 있었다(Table 5, 6). 이렇게 스테로이드 안약을 같이 썼을 시에 유의미하게 호전된 항목들은 스테로이드의 항염증 효과가 반영된 것으로 생각한다. 또한 BlephExTM를 통한 안검미세세척은 안구표면의 염증을 일으키는 cytokine과 이를 생성하는 근본인 안검의 세균 및 Biofilm을 제거하는 효과를 갖는다. 이러한 안검세균의 감소는 마이봄선기능장애에 영향을 주며[21] Conner et al [22]은 BlephExTM 치료 전과 비교하여 치료 4주 후 MMP-9가 감소했음을 보고한 바 있다. 본 연구에서도 BlephExTM만 사용한 군의 환자군이 적어 통계학적으로 유의미하지 못했지만 눈물층파괴시간, 각막형광염색정도, 눈꺼풀 경계 이상, 마이봄선기능장애정도가 줄어드는 것을 확인하였으며, 이에 따라 기존의 steroid 치료에 BlephExTM를 함께 적용 시 서로 상호적인 동반 효과로 인해 그 호전 정도가 극대화되었다고 볼 수 있다. 또한 스테로이드를 3개월 내로 쓴 group 3에서 3개월 이상 쓴 group 2에 비해 추가적으로 마이봄선기능장애정도의 호전을 보였으며 유의미한 항목들의 호전 정도(p-value)가 더 컸다. 이를 통해 스테로이드 안약의 효과는 사용 초기에 크며, 오래 사용할 시 그 호전 정도는 크지 않음을 알 수 있다. 이에 따라 마이봄선기능장애 치료 목적으로 스테로이드 안약 사용 시 장기적으로 사용하면 그 효과는 크지 않으나, 그 외 백내장, 안압상승 등의 합병증[23]을 우려할 수 있으므로 BlephExTM 사용 등의 보조적 치료로 바꾸는 것을 고려해 볼 수 있다.
안검 세척은 BlephExTM 이전에도 OcuSoft (Rosenberg, TX, USA), Eye Scrub (Novartis, Basel, Switzerland) 등의 약국에서 구입할 수 있는 자가 눈꺼풀청결제를 이용하여 시행하고 있던 치료 방법이다. 하지만 온찜질을 비롯한 눈꺼풀 세척이 일시적인 교육을 통해 환자에게 맡겨져 이뤄지고 있다 보니 그 순응도와 효율성이 좋지 않음은 예측 가능한 바이다. 과거 Alghamdi et al [24]의 연구에서 188명의 연구 참여자에게 하루 두 번 5분간의 온찜질과 따뜻한 물로 눈꺼풀 세척을 교육한 후 그 순응도를 조사했을 때에 104명인 55%에서 치료의 순응도를 보였다. 자가세척을 지키지 못한 사람들의 이유로 불편함, 건망증, 세척의 필요성을 느끼지 못하는 점이 있었다고 과거 논문에서는 분석하고 있다. 이러한 점에서 자가세척제와는 다르게 눈꺼풀 세척을 병원에서 기구를 이용해 전문가가 주기적으로 시행해주는 하나의 치료로 가져올 시에 실제 BlephExTM의 임상적 효과와 더불어 환자들이 갖는 만족감도 클 것이며 정확하고 미세하게 세척이 되어 효율적일 것이다.
본 연구는 BlephExTM 치료 1달 후 안구표면 지표들의 변화를 분석한 연구로 1달 이후의 추가적인 기간 동안 추적 관찰을 하지 못한 점에서 한계점을 갖는다. 더불어 치료군의 효과를 비교할 수 있는 대조군이 없다는 점도 있다. 마지막으로, 환자군 개개인에 맞춰 처방되어 사용하고 있던 안약을 통제하지 않아 BlephExTM만의 단독 효과라고 유추할 수 있는 군의 환자수가 적어 통계학적으로 유의미한 값을 얻지 못한 점도 한계점으로 남는다. 그러나 본 연구에서는 참여 시점부터 연구기간 동안 기존의 안약에서 변화 없이 BlephExTM가 추가된 것이기 때문에 그 효과를 보기에 충분하다. 뿐만 아니라 BlephExTM를 적용할 때 환자들이 기존의 건성안 혹은 마이봄선기능장애로 인공눈물, 스테로이드 제제 등의 안약을 사용하고 있을 가능성이 높아 본 연구의 환경이 실제 임상 환경과 가까워 더 유용하다고 할 수 있겠다.
결론적으로, 마이봄선기능장애 환자들에게 BlephExTM 사용 시 1달 후 눈물막파괴시간, OSDI, 눈꺼풀 경계이상 그리고 마이봄선기능장애가 유의미하게 호전되었으며 이는 스테로이드 안약과 함께 사용 시 효과가 컸다. 이를 통해 안검미세각질제거를 마이봄선기능장애 환자에서의 치료의 하나로 제시하는 바이다.
Figure 1.
Schematic diagram of subjects’ medication usage. Forty eight eyes of the 24 patients were enrolled. Thirty eight eyes had applied to steroid eyedrops. In order to take account of steroid effect, 10 eyes of the non-steroid users were grouped as group 1. Thirty eight eyes were devided as group 2 in which steroid eyedrop was used over 3 months and group 3 which has less than 3 months of steroid usage.
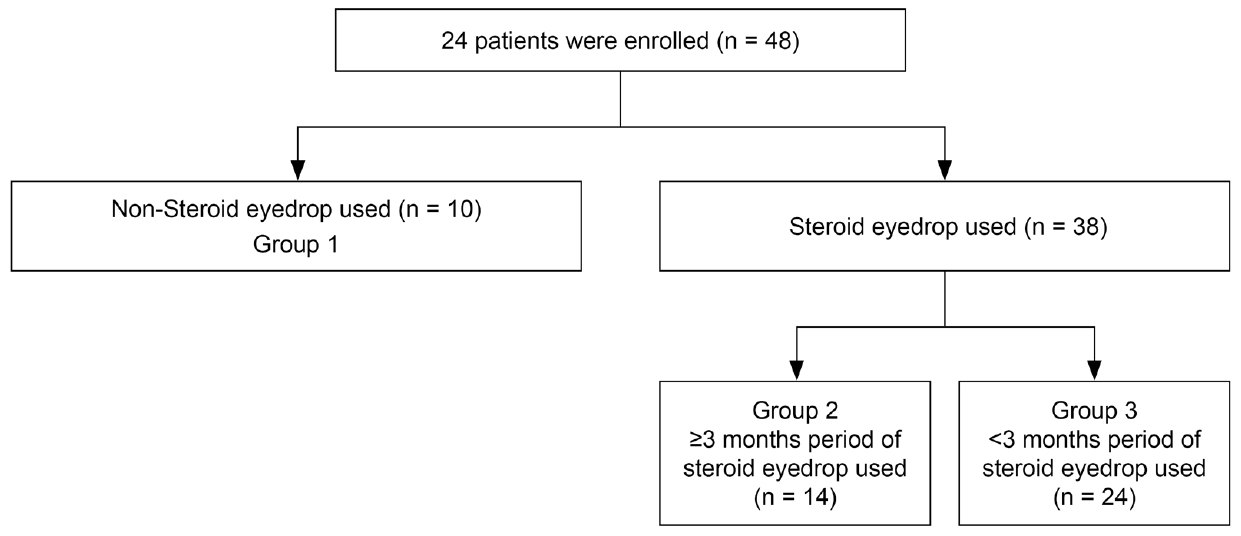
Table 1.
Clinical characteristics of the subjects
Table 2.
Changes of MGD related factors before and after treatment with BlephExTM (n = 48)
| Factor | Baseline | After 1 month | p-value* |
|---|---|---|---|
| Tear film break-up time (seconds) | 2.65 ± 1.16 | 3.77 ± 1.80 | <0.001 |
| Corneal staining score (0-15) | 1.85 ± 2.98 | 1.65 ± 2.32 | 0.292 |
| Schirmer’s I test (mm, 5 minutes) | 9.25 ± 7.74 | 9.31 ± 8.11 | 0.880 |
| Lid margin abnormality (0-4) | 2.98 ± 1.16 | 2.50 ± 1.01 | <0.001 |
| MGD score (0-30) | 21.60 ± 6.95 | 18.02 ± 6.68 | 0.001 |
| Lipid layer thickness (nm) | 88.27 ± 18.49 | 87.19 ± 22.16 | 0.732 |
| Overall OSDI score (0-100) | 38.84 ± 17.13 | 18.67 ± 15.01 | <0.001 |
| Ocular symptoms (3 items) | 11.15 ± 4.66 | 4.30 ± 3.50 | <0.001 |
| Vision-related function (6 items) | 15.84 ± 9.91 | 6.30 ± 8.26 | <0.001 |
| Environmental triggers (3 items) | 11.12 ± 5.64 | 7.34 ± 5.12 | <0.001 |
Table 3.
Changes of Lipid layer thickness before and after treatment with BlephExTM (n = 48)
| Factor | Value (n) | Baseline | After 1 month | p-value* |
|---|---|---|---|---|
| Lipid layer thickness (nm) | 48 | 88.27 ± 18.49 | 87.19 ± 22.16 | 0.732 |
| Except baseline 100 nm | 19 | 70.37 ± 18.23 | 74.47 ± 28.37 | 0.314 |
Table 4.
Changes of MGD related factors before and after treatment with BlephExTM in non-steroid used group (group 1, n = 10)
| Factor | Baseline | After 1 month | p-value* |
|---|---|---|---|
| Tear film break-up time (seconds) | 2.20 ± 0.79 | 2.70 ± 0.95 | 0.059 |
| Corneal staining score (0-15) | 1.50 ± 1.35 | 1.10 ± 0.99 | 0.206 |
| Schirmer’s I test (mm, 5 minutes) | 8.00 ± 6.68 | 6.90 ± 6.66 | 0.131 |
| Lid margin abnormality (0-4) | 3.00 ± 1.05 | 2.70 ± 0.48 | 0.180 |
| MGD score (0-30) | 21.90 ± 6.44 | 20.60 ± 5.50 | 0.408 |
| Lipid layer thickness (nm) | 84.10 ± 30.63 | 81.20 ± 32.32 | 0.068 |
| Overall OSDI score (0-100) | 30.91 ± 14.42 | 14.87 ± 7.41 | 0.005 |
Table 5.
Changes of MGD related factors before and after treatment with BlephExTM in ≥ 3 months period of steroid used group (group 2, n = 14)
| Factor | Baseline | After 1 month | p-value* |
|---|---|---|---|
| Tear film break-up time (seconds) | 3.29 ± 0.91 | 4.57 ± 1.79 | 0.022 |
| Corneal staining score (0-15) | 2.71 ± 4.33 | 2.14 ± 3.16 | 0.168 |
| Schirmer’s I test (mm, 5 minutes) | 8.57 ± 6.58 | 8.64 ± 6.95 | 0.943 |
| Lid margin abnormality (0-4) | 3.29 ± 0.91 | 2.57 ± 0.76 | 0.019 |
| MGD score (0-30) | 22.29 ± 5.80 | 18.00 ± 7.26 | 0.168 |
| Lipid layer thickness (nm) | 88.86 ± 15.07 | 92.93 ± 13.18 | 0.263 |
| Overall OSDI score (0-100) | 34.40 ± 20.61 | 13.91 ± 8.33 | 0.004 |
Table 6.
Changes of MGD related factors before and after treatment with BlephExTM in < 3 months period of steroid used group (group 3, n = 24)
| Factor | Baseline | After 1mon | p-value* |
|---|---|---|---|
| Tear film break-up time (seconds) | 2.46 ± 1.28 | 3.75 ± 1.89 | <0.001 |
| Corneal staining score (0-15) | 1.50 ± 2.47 | 1.58 ± 2.17 | 0.507 |
| Schirmer’s I test (mm, 5 minutes) | 10.17 ± 8.86 | 10.70 ± 9.21 | 0.218 |
| Lid margin abnormality (0-4) | 2.79 ± 1.32 | 2.38 ± 1.28 | 0.019 |
| MGD score (0-30) | 21.08 ± 7.92 | 16.96 ± 6.74 | 0.001 |
| Lipid layer thickness (nm) | 89.67 ± 13.90 | 86.33 ± 21.44 | 0.286 |
| Overall OSDI score (0-100) | 44.73 ± 14.22 | 23.03 ± 18.97 | <0.001 |
REFERENCES
1) Nichols KK, Foulks GN, Bron AJ, et al. The international workshop on meibomian gland dysfunction: executive summary. Invest Ophthalmol Vis Sci 2011;52:1922-9.



2) Liu R, Rong B, Tu P, et al. Analysis of cytokine levels in tears and clinical correlations after intense pulsed light treating meibomian gland dysfunction. Am J Ophthalmol 2017;183:81-90.


3) Wei Y, Asbell PA. The core mechanism of dry eye disease is inflammation. Eye Contact Lens 2014;40:248-56.



4) Rynerson JM, Perry HD. DEBS - a unification theory for dry eye and blepharitis. Clin Ophthalmol 2016;10:2455-67.


5) Weiser J, Henke HA, Hector N, et al. Sub-inhibitory tigecycline concentrations induce extracellular matrix binding protein Embp dependent Staphylococcus epidermidis biofilm formation and immune evasion. Int J Med Microbiol 2016;306:471-8.


6) Baldi F, Marchetto D, Battistel D, et al. Iron-binding characterization and polysaccharide production by Klebsiella oxytoca strain isolated from mine acid drainage. J Appl Microbiol 2009;107:1241-50.



7) Teles R, Teles F, Frias-Lopez J, et al. Lessons learned and unlearned in periodontal microbiology. Periodontol 2000 2013;62:95-162.



8) Wolf D, Rippa V, Mobarec JC, et al. The quorum-sensing regulator ComA from Bacillus subtilis activates transcription using topologically distinct DNA motifs. Nucleic Acids Res 2016;44:2160-72.


9) Hastings JW, Greenberg EP. Quorum sensing: the explanation of a curious phenomenon reveals a common characteristic of bacteria. J Bacteriol 1999;181:2667-8.



10) Knech LD, O’Connor G, Mittal R, et al. Serotonin activates bacterial quorum sensing and enhances the virulence of pseudomonas aeruginosa in the host. EBioMedicine 2016;9:161-9.



11) Murphy O, O’Dwyer V, Lloyd-McKernan A. The efficacy of tea tree face wash, 1, 2-Octanediol and microblepharoexfoliation in treating Demodex folliculorum blepharitis. Cont Lens Anterior Eye 2018;41:77-82.


12) Schiffman RM, Christianson MD, Jacobsen G, et al. Reliability and validity of the Ocular Surface Disease Index. Arch Ophthalmol 2000;118:615-21.


13) Arita R, Itoh K, Maeda S, et al. Proposed diagnostic criteria for obstructive meibomian gland dysfunction. Ophthalmology 2009 116:2058-63. e1.


15) Acera A, Rocha G, Vecino E, et al. Inflammatory markers in the tears of patients with ocular surface disease. Ophthalmic Res 2008;40:315-21.


16) Lam H, Blelden L, Palva CS, et al. Tear cytokine profiles in dysfunctional tear syndrome. Am J Ophthalmol 2009 147:198-205. e1.


17) Solomon A, Drusun D, Liu Z, et al. Pro- and anti-inflammatory forms of interleukin-1 in the tear fluid and conjunctiva of patients with dry-eye disease. Invest Ophthalmol Vis Sci 2001;42:2283-92.

18) Chhadva P, Lee T, Sarantopoulos CD, et al. Human tear serotonin levels correlate with symptoms and signs of dry eye. Ophthalmology 2015;122:1675-80.



19) Kang MH, Kim MK, Lee HJ, et al. Interleukin-17 in various ocular surface inflammatory diseases. J Korean Med Sci 2011;26:938-44.



20) Avunduk AM, Avunduk MC, Varnell ED, Kaufman HE. The comparison of efficacies of topical corticosteroids and nonsteroidal anti-inflammatory drops on dry eye patients: a clinical and immunocytochemical study. Am J Ophthalmol 2003;136:593-602.


21) Nattis A, Perry HD, Rosenberg ED, Donnenfeld ED. Influence of bacterial burden on meibomian gland dysfunction and ocular surface disease. Clin Ophthalmol 2019;13:1225-34.



22) Conner CG, Narayanan S, Miller W. Reduction in inflammatory marker matrix metalloproteinase-9 following lid debridement with BlephEx. Invest Ophthalmol Vis Sci 2017;58:498.




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




