 |
 |
| J Korean Ophthalmol Soc > Volume 61(11); 2020 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļ│Ė ņ”ØļĪĆļź╝ ĒåĄĒĢ┤ ņ▓£Ļ│ĄļÉ£ ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģ ĒÖśņ×ÉņŚÉņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ ņé¼ļ×ī Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņä▒Ļ│ĄņĀüņØĖ ņ╣śļŻī Ļ▓ĮĒŚśņØä ņĄ£ņ┤ł ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”ØļĪĆņÜöņĢĮ
ņÜ░ņĢłņØś ņäĀņ▓£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ░£ņāØĒĢ£ Ēøäņ▓£ņä▒ ņāüņĖĪļČĆ ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņ£╝ļĪ£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæņØ┤ļŹś 39ņäĖ ļé©ņ×É ĒÖśņ×ÉĻ░Ć ļé┤ņøÉ ļŗ╣ņØ╝ļČĆĒä░ ļ░£ņāØĒĢ£ ņÜ░ņĢłņØś ņČ£Ēśł, ĒåĄņ”Ø ļ░Å Ļ│╝ļÅäĒĢ£ ļłłļ¼╝ĒØśļ”╝ņØä ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆļŗż. Ļ▓Ćņ¦äņāü ņÜ░ņĢł ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņŚÉņä£ ņČ£ĒśłņØä ļÅÖļ░śĒĢ£ Seidel ņ¢æņä▒ņØś ņ▓£Ļ│ĄņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż. ņØ┤ņŚÉ ņĀäņŗĀļ¦łņĘ©ĒĢś ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģ ņŻ╝ņ£ä ņĪ░ņ¦üļ░Ģļ”¼, ņ▓£Ļ│Ą ļČĆņ£ä ņśüĻĄ¼ ņ¢æļ¦ēņØ┤ņŗØņłĀ, ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ē(Halo; Eversight Inc., Palo Alto, CA, USA)ņØ┤ņŗØņłĀ ļ░Å ĒśłĻ┤Ćņä▒ Ēģīļģ╝ļéŁņØś ņĀäņ¦äĒö╝ĒīÉņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ļ»ĖņÜ® Ļ░£ņäĀ ļ¬®ņĀüņ£╝ļĪ£ ņÜ░ņĢł Ļ░üļ¦ēļ¼ĖņŗĀņłĀņØä ļÅÖļ░ś ņŗ£Ē¢ēĒĢśņśĆļŗż. ņłśņłĀ Ēøä 4Ļ░£ņøö Ļ░ä ņ▓£Ļ│Ą ņ×¼ļ░£ ņŚåņØ┤ ņ£Āņ¦ĆļÉśņŚłņ£╝ļ®░ ņāüņĖĪļČĆ Ļ│Ąļ¦ēĒżļÅäņóģņØś ļÅīņČ£ ņĀĢļÅä ņŚŁņŗ£ ņłśņłĀ ņĀäņŚÉ ļ╣äĒĢ┤ Ļ░£ņäĀļÉśņŚłļŗż.
Ļ▓░ļĪĀ
ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņŚÉņä£ ņ▓£Ļ│ĄņØ┤ ļ░£ņāØ ņŗ£, ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņłśļ│ĄņĀü ņØ┤ņŗØņłĀņØĆ ļ┤ēĒĢ®ņØ┤ ņÜ®ņØ┤ĒĢśĻ│Ā ļÅīņČ£ ļČĆņ£äļź╝ ņĢĢļ░ĢĒĢśĻĖ░ņŚÉ ņČ®ļČäĒ׳ ļæÉĻ╗ŹĻ│Ā Ļ░üļ¦ēņØś ņĪ░ņ¦ü ĒŖ╣ņä▒ņāü ļÅÖņóģ Ļ│Ąļ¦ē ļīĆļ╣ä ņØ┤ņŗØĒÄĖņØś ļŖśņ¢┤ņ¦É ļ░Å ņ£ĄĒĢ┤ņØś ņ£äĒŚśņØ┤ ņĀüĻĖ░ ļĢīļ¼ĖņŚÉ ņóŗņØĆ ņ╣śļŻīņĀü ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳Ļ▓Āļŗż.
ABSTRACT
Purpose
To report a case of acquired perforated anterior scleral staphyloma treated successfully by lamellar grafting of the acellular preserved human cornea.
Case summary
A 39-year-old male patient with anterior scleral staphyloma at the superior scleral area near the corneal limbus of the right eye which occurred after congenital cataract surgery visited our hospital due to bleeding and excessive tearing in his right eye. Slit lamp bio-microscopic examination revealed a Seidel-positive perforation with bleeding at the anterior scleral staphyloma. Under general anesthesia, conjunctiva was dissected from the scleral staphyloma. Amniotic membrane (AM) was transplanted over the perforated area and an acellular preserved human cornea (Halo; Eversight Inc., Palo Alto, CA, USA) was grafted over the AM. To aid the vascularization over the grafts, an advancement flap of the adjacent TenonŌĆÖs capsule was constructed. Thereafter, the recipient cornea was tattooed for cosmetic purposes. At 4 months postoperatively, the wound had stabilized without perforation recurrence, and staphyloma protrusion had improved.
Conclusions
In a case of a perforated anterior scleral staphyloma, restorative transplantation using acellular preserved human corneal tissue may be a good therapeutic alternative, given that the cornea is easy to suture, is thick enough to compress the protruding area, and has a low risk of graft stretching or melting compared with the sclera.
ĒżļÅäņóģ(staphyloma)ņØĆ Ļ░üļ¦ē Ēś╣ņØĆ Ļ│Ąļ¦ēņØś Ļ▓░ņåÉļČĆļź╝ ĒåĄĒĢ┤ ņä£ ĒøäļČĆņØś ĒżļÅäļ¦ē ņĪ░ņ¦üņØ┤ļéś ļŗżļźĖ ņĢłļé┤ ņĪ░ņ¦üņØ┤ ĒāłņżäļÉśļŖö ņ¦łĒÖśņØ┤ļŗż[1]. ĒżļÅäņóģņØĆ ņ£äņ╣śņŚÉ ļö░ļØ╝ņä£ Ļ│ĀļÅäĻĘ╝ņŗ£ņÖĆ ņל ļÅÖļ░śļÉśļŖö ņŗ£ņŗĀĻ▓Į ņŻ╝ņ£äņØś ļÆż ĒżļÅäņóģĻ│╝ ņĀäņĢłļČĆņØś Ļ░üļ¦ē, Ļ│Ąļ¦ēņØä ņ╣©ļ▓öĒĢśļŖö ņĢ×ĒżļÅäņóģņ£╝ļĪ£ ļéśļē£ļŗż. ĻĘĖņżæ ņĢ×ĒżļÅäņóģņØĆ ļō£ļ¼╝Ļ▓ī ņäĀņ▓£ņĀüņ£╝ļĪ£ ļ░£ņāØ ņŗ£ ņŻ╝ļĪ£ ņĢłĻ▓ĆņŚ┤ ņé¼ņØ┤ņŚÉņä£ Ļ░üļ¦ēĒś╝Ēāü ļ░Å Ļ░üļ¦ēĒÖĢņןņ£╝ļĪ£ ļ░£ņāØĒĢśļ®░[2,3], Ēøäņ▓£ņĀüņ£╝ļĪ£ļŖö ļźśļ¦łĒŗ░ņŖż Ļ┤ĆņĀłņŚ╝ņŚÉ ļÅÖļ░śĒĢ£ Ļ│Ąļ¦ēņŚ╝, ņÖĖņāü ļ░Å ņä¼ņ£ĀņŻ╝ņĀłņĀ£ņłĀ, ļ░▒ļé┤ņןņłśņłĀ, ņØĄņāüĒÄĖņĀłņĀ£ņłĀ, ļ¦Øļ¦ēļ░Ģļ”¼ņłśņłĀ ļō▒ņØś ņĢłļé┤ ņłśņłĀ ļō▒ ņØ┤Ēøä Ļ│Ąļ¦ēņØś ņ¦Ćņ¦ĆļÅä ņĢĮĒÖöņŚÉ ņØśĒĢ┤ ņØ┤ņ░©ņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśĻ▓ī ļÉ£ļŗż[4].
ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņŚÉ ņ▓£Ļ│ĄņØ┤ ļ░£ņāØĒĢśņśĆņØä ļĢīņŚÉļŖö ņĢłĻĄ¼ļź╝ ļ│┤ņĀäĒĢśĻ│Ā ņĢłĻĄ¼ ĒśĢĒā£ļź╝ ņ£Āņ¦ĆĒĢśĻĖ░ ņ£äĒĢ┤ ņłśņłĀņĀü ņ╣śļŻīĻ░Ć ņÜöĻĄ¼ļÉśļŖöļŹ░, Ļ│╝Ļ▒░ ņ×ÉĻ░Ć Ēś╣ņØĆ ļÅÖņóģ Ļ│Ąļ¦ē[5-7] ļ░Å ļÅÖņóģ Ļ▓Įļ¦ē(dura mater)[4]ņØä ņØ┤ņÜ®ĒĢ£ ņłśļ│ĄņĀü ņØ┤ņŗØņØ┤ ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ņ£╝ļéś, ņ▓£Ļ│ĄļÉ£ Ļ│Ąļ¦ēļČĆņ£äņŚÉņä£ ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ņØ┤ņÜ®ĒĢ£ ņłśļ│ĄņłĀņØĆ Ēśäņ×¼Ļ╣īņ¦Ć ĻĄŁļé┤ņÖĖ ļ│┤Ļ│ĀļÉ£ ļ░ö ņŚåļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņ▓£Ļ│ĄļÉ£ Ēøäņ▓£ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņØä ļÅÖņóģņØś ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØ┤ņŗØ, ņ¢æļ¦ēņØ┤ņŗØ ļ░Å ņ×ÉĻ░Ć Ēģīļģ╝ļéŁĒö╝ĒīÉņłĀņØä ņØ┤ņÜ®ĒĢ£ ņĖĄĒīÉņØ┤ņŗØņłĀņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņä▒Ļ│ĄņĀüņ£╝ļĪ£ ņ╣śļŻīĒĢśņśĆĻĖ░ņŚÉ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
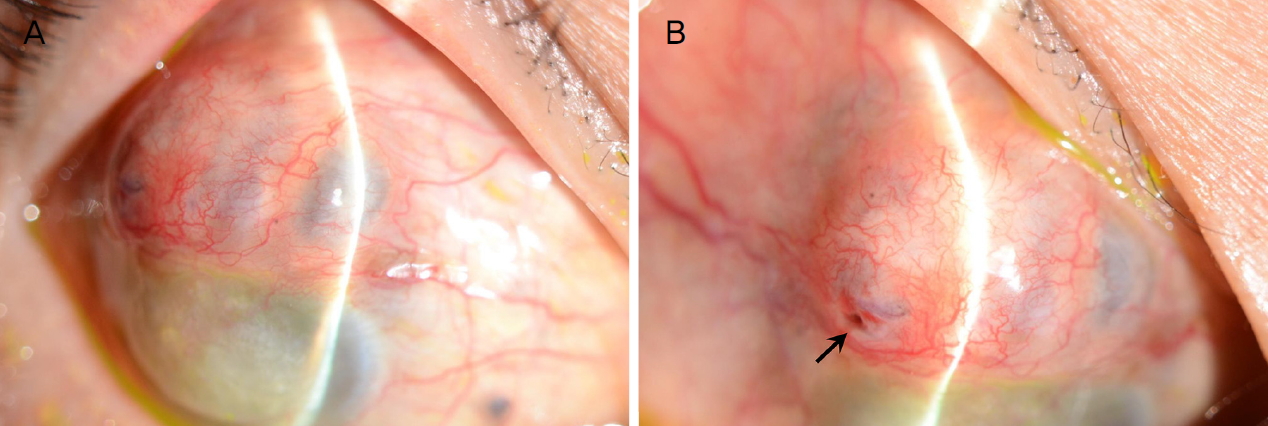
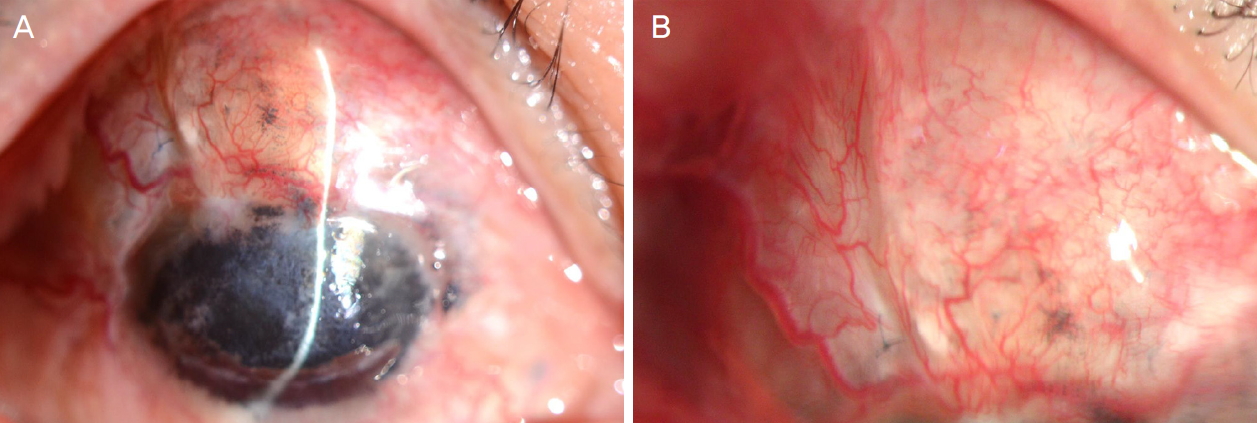
ņ¢æņĢł ņäĀņ▓£ļ░▒ļé┤ņן, ņåīņĢłĻĄ¼ņ”Ø, ņåīĻ░üļ¦ēņ”Ø(microcornea), ņĢłņ¦ä, 3ņäĖ ļĢī ņ¢æņĢł ļ░▒ļé┤ņןņłśņłĀļĀźņØ┤ ņ׳ņ£╝ļ®░, ņØ┤Ēøä 20ņäĖĻ▓Į ļ░£ņāØĒĢ£ ņÜ░ņĢłņØś ņāüņĖĪļČĆ Ļ│Ąļ¦ēņŚÉ 11.5 ├Ś 11.0 mm Ēü¼ĻĖ░ņØś ņĢ×ĒżļÅäņóģņØä ļÅÖļ░śĒĢ£ 39ņäĖ ļé©ņ×É ĒÖśņ×ÉĻ░Ć ņÖĖļל Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæ ļé┤ņøÉ ļŗ╣ņØ╝ļČĆĒä░ ļ░£ņāØĒĢ£ ņÜ░ņĢłņØś ņČ£Ēśł, ĒåĄņ”Ø ļ░Å ļłłļ¼╝ĒØśļ”╝ņØä ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆļŗż. ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņāü ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģ ļČĆņ£äņŚÉņä£ Ļ▓░ļ¦ēĻ▓░ņåÉ ļČĆņ£äļź╝ ĒåĄĒĢ┤ ņČ£Ēśł ļ░Å Seidel ņ¢æņä▒ņØś ĒżļÅäņóģ ņ▓£Ļ│ĄņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 1). ņØ┤ņŚÉ ņĀäņŗĀļ¦łņĘ©ĒĢś ņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░(Fig. 2A), ņÜ░ņäĀ ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņØś ņ£żĻ│ĮņØä Ēæ£ņŗ£ĒĢ£ Ēøä(Fig. 2B), ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģ ņŻ╝ņ£ä Ļ▓░ļ¦ē ļ░Å Ēģīļģ╝ļéŁ ņĪ░ņ¦ü ļ░Ģļ”¼(Fig. 2C), ņĪ░ņ¦üņĀæņ░®ņĀ£(Greenplast Q prefilled syringe kit; Greencross Medical Science Corp., Seoul, Korea)ļź╝ ņØ┤ņÜ®ĒĢ£ ņ▓£Ļ│ĄļČĆ ņ×äņŗ£ ĒÅÉņćä(Fig. 2D)ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņØ┤Ēøä ĒżļÅäņóģ ļČĆņ£äĻ░Ć ļŗż ļŹ«ņØ┤ļÅäļĪØ ļÅÖĻ▓░ ņ¢æļ¦ē(MS-Amnion; MSBIO, Inc., Seongnam, Korea)ņØ┤ ĻĖ░ņĀĆļ¦ēņØ┤ ņ£äļĪ£ ņśżĻ▓ī ĒĢśņŚ¼ ņśüĻĄ¼ ņ¢æļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż(Fig. 2E). Ļ│¦ņØ┤ņ¢┤ ņØ┤ņŗØĒĢ£ ņ¢æļ¦ē ņ£äļĪ£ 9.5 mm ņ¦üĻ▓ĮņØś ņøÉĒśĢņØś ļ¼┤ņäĖĒż ņé¼ļ×ī ļ│┤ņĪ┤ Ļ░üļ¦ē(sterile full-sized and split thickness cornea, Halo; Eversight, Ann Arbor, MI, USA)ņØä ņś¼ļĀżļåōĻ│Ā ĒżļÅäņóģ ņ▓£Ļ│ĄļČĆĻ░Ć Ļ░ĆĻĖēņĀü ļ│┤ņĪ┤ Ļ░üļ¦ēņØś ņżæņŗ¼ņČĢ ņäĀņāüņŚÉ ņśżļÅäļĪØ ĒĢ£ Ēøä ņĄ£ļīĆĒĢ£ ņĢłĻĄ¼ ĒøäļČĆ ņ¬Įņ£╝ļĪ£ ņéĮņ×ģĒĢ£ Ēøä, 10-0 ļéśņØ╝ļĪĀ ļ┤ēĒĢ®ņ£╝ļĪ£ Ļ│ĀņĀĢ ļ┤ēĒĢ®ĒĢśņŚ¼ ņłśļ│ĄņĀü ņĖĄĒīÉņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż(Fig. 2F). ņØ┤ņŗØĒĢ£ ļ│┤ņĪ┤ Ļ░üļ¦ēĻ│╝ ņ¢æļ¦ē ņ£äļĪ£ ņøÉĒÖ£ĒĢ£ ĒśłĻ┤Ć ņāØņ░®ņØä ņ£äĒĢ┤ ņŻ╝ņ£ä ņĀĢņāü Ļ▓░ļ¦ē ņĪ░ņ¦ü ĒĢś Ēģīļģ╝ļéŁņØä ļ░Ģļ”¼(Fig. 2G)ĒĢśĻ│Ā ņłśņŚ¼ņ×É Ļ░üļ¦ēņØś ņ£żļČĆļź╝ Ļ▓ĮĻ│äļĪ£ ņØ┤ļź╝ ņ╣©ļ▓öĒĢśļŖö ļČĆņ£äņØś ņ×öņŚ¼ ņØ┤ņŗØ Ļ░üļ¦ēĒÄĖņØä ņĀłņĀ£ĒĢ£ Ēøä(Fig. 2H), ņØ┤ņŗØĒĢ£ Ļ░üļ¦ēņĪ░ņ¦üņØ┤ ļ¬©ļæÉ ļŹ«ņØ┤ļÅäļĪØ ĒśłĻ┤Ćņä▒ Ēģīļģ╝ļéŁ ņĀäņ¦ä Ēö╝ĒīÉņłĀņØä ņŗ£Ē¢ēĒĢśĻ│Ā (Fig. 2I) ņāüņĖĪļČĆ Ļ▓░ļ¦ēņ£╝ļĪ£ ļŹ«ņ¢┤ņŻ╝ņŚłļŗż(Fig. 2J). ļśÉĒĢ£, ļ»ĖņÜ®Ļ░£ņäĀ ļ¬®ņĀüņ£╝ļĪ£ Ļ░üļ¦ē ļ¼ĖņŗĀņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż(Fig. 2K). ņÜ░ņäĀ Ļ░üļ¦ēņāüĒö╝ļź╝ 15ļ▓ł ņłśņłĀņÜ® ļĖöļĀłņØ┤ļō£ļĪ£ ļ▓ŚĻ▓©ļéĖ ļÆż, ņĀ£ĒŖĖ ļĖöļ×Ö ņāēņāüņØś ņŚ╝ļŻī(Jet black Micropigment, Bio-touch International Inc., City of Industry, CA, USA)ņÖĆ ļŗżĒü¼ ļĖīļØ╝ņÜ┤ ņāēņāüņØś ņŚ╝ļŻī(Dark brown Micropigment, Bio-touch International Inc.)ļź╝ ņĢĮ 10:1ņØś ļ╣äņ£©ļĪ£ Ēś╝ĒĢ®ĒĢśņŚ¼, ļ®ĖĻĘĀ ļ░öļŖśņØä ņŚ░Ļ▓░ĒĢ£ ņĀäņ×ÉļÅÖ ļ¼ĖņŗĀ ĻĖ░Ļ│ä(The Mosaic┬«; Bio-touch International Inc.)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ Ēś╝ĒĢ® ņŚ╝ļŻīļź╝ Ļ░üļ¦ēņŗżņ¦łņŚÉ ņŻ╝ņ×ģĒĢśņśĆļŗż. ņØ┤Ēøä ļČłĻĘ£ņ╣ÖĒĢ£ ĒÖśņ×ÉņØś Ļ░üļ¦ē Ēæ£ļ®┤ ņ£äļĪ£ ņāüĒö╝ ņ×¼ņāØņØä ļÅäļ¬©ĒĢśĻĖ░ ņ£äĒĢ┤ ĻĖ░ņĀĆļ¦ēņØ┤ ņĢäļלļĪ£ ņśżļÅäļĪØ ĒĢśņŚ¼ ņ×äņŗ£ ņ¢æļ¦ēļŹ¦ļīÉņłĀņØä ņŗ£Ē¢ēĒĢśĻ│Ā(Fig. 2L) ņłśņłĀņØä ņóģļŻīĒĢśņśĆļŗż. ņłśņłĀ Ēøä Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ ļ│ĄņÜ®, ĻĄŁņåīņŖżĒģīļĪ£ņØ┤ļō£ ļ░Å ĒĢŁņāØņĀ£ ņĀÉņĢł, 20% ņ×ÉĻ░ĆĒśłņ▓ŁņĢłņĢĮ ņĀÉņĢłĒĢśļ®┤ņä£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśņśĆņ£╝ļ®░ ņłśņłĀ 4Ļ░£ņøö Ēøä ņāüņ▓ś ļ▓īņ¢┤ņ¦É, ņ▓£Ļ│Ą ņ×¼ļ░£ ļ░Å ņłśņłĀ ļČĆņ£ä ņČöĻ░Ć ļÅīņČ£ ņŚåņØ┤ ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśņŚłļŗż(Fig. 3).
ĒżļÅäņóģņØĆ ļÅīņČ£ļÉ£ ĻĄ¼ņĪ░ļĪ£ ņØĖĒĢ┤ ņ×æņØĆ ņÖĖņāüņŚÉļÅä ņ▓£Ļ│Ą ļ░Å ņĢłļé┤ Ļ░ÉņŚ╝ņØ┤ ļ░£ņāØĒĢĀ ĒÖĢļźĀņØ┤ ļåÆļŗż. ĒŖ╣Ē׳, ņ▓£Ļ│ĄļÉ£ ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņØĆ ņĢłĻ│╝ņĀü ņØæĻĖē ņāüĒÖ®ņ£╝ļĪ£ņä£ ņĢłļé┤ Ļ░ÉņŚ╝ņØś ņśłļ░® ļ░Å ņĢłĻĄ¼ ĒśĢĒā£ņ£Āņ¦Ćļź╝ ņ£äĒĢ┤ ņŗ£ĻĖēĒĢ£ ņłśņłĀņĀü ņ▓śņ╣śĻ░Ć ņÜöĻĄ¼ļÉ£ļŗż. Ļ│╝Ļ▒░ Ļ│Ąļ¦ēņŚ░ĒÖöņ”Ø ļ░Å Ļ┤┤ņé¼ņä▒ Ļ│Ąļ¦ēņŚ╝ņŚÉņä£ ņé¼ņÜ®ļÉśļŖö ņĪ░ņ¦ü ņłśļ│Ąļ¼╝ņØś Ēøäļ│┤ņ×¼ļōżņØĆ ņ×ÉĻ░Ć Ļ▓░ļ¦ē Ēö╝ĒīÉ[8], ņ¢æļ¦ē[9], ļÅÖņóģ Ļ│Ąļ¦ē[10], ļÅÖņóģ Ļ░üļ¦ē[11], ļīĆĒć┤ ĻĘ╝ļ¦ē(fascia lata)[12] ļō▒ ļŗżņ¢æĒĢśĻ▓ī ņĢīļĀżņĀĖ ņÖöļŗż. ļ░śļ®┤, ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņŚÉņä£ļŖö Ēśäņ×¼Ļ╣īņ¦Ć ņØ┤ļōż Ēøäļ│┤ņ×¼ņØś ņØ┤ņŗØņØ┤ ļŗżņ¢æĒĢśĻ▓ī ņŗ£ļÅäļÉ£ ļ░ö ņŚåņŚłņ£╝ļ®░, ĒŖ╣Ē׳ ļ│Ė ņ”ØļĪĆņŚÉņä£ ņĀüņÜ®ĒĢ£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØ┤ņŗØņłĀņØĆ ņ▓£Ļ│ĄļÉ£ ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģ ĒÖśņ×ÉņŚÉņä£ ņØ┤ņĀ£Ļ╗Å ĻĄŁļé┤ņÖĖ ļ│┤Ļ│ĀļÉ£ ļ░ö ņŚåļŖö ņĄ£ņ┤ł ļ│┤Ļ│ĀņØ┤ļŗż.
ļ│Ė ņ”ØļĪĆņŚÉņä£ ņé¼ņÜ®ĒĢ£ ņé¼ļ×ī ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØĆ ĒĢ┤ļŗ╣ ņĢłņØĆĒ¢ēņØś ņäżļ¬ģ ņ×ÉļŻī ĻĘ╝Ļ▒░ĒĢś, ĻĖ░ņ”Ø Ļ░üļ¦ēņØä ņżæņŗ¼ļČĆ 9.5 mm ņ¦üĻ▓ĮņØś ņøÉĒśĢņ£╝ļĪ£ ņ×¼ļŗ©ĒĢśĻ│Ā ļæÉĻ╗śļŖö Ļ░üļ¦ēņØś ņøÉļל ļæÉĻ╗śņØś ņĀłļ░śņ£╝ļĪ£ ĻĘĀņØ╝ĒĢśĻ▓ī ļČäļ”¼ĒĢ£ ņøÉĒśĢņØś ņĀäņ▓┤ Ēü¼ĻĖ░/ņĀłļ░ś ļæÉĻ╗ś Ļ░üļ¦ē(full & split thickness cornea) ĒāĆņ×ģņØ┤ļŗż. ĒĢ┤ņÖĖņØś ņĢłņØĆĒ¢ēņŚÉņä£ Ļ┤Ćļ”¼ĒĢśļ®░ ļŗżļźĖ ĒāĆņ×ģņØś ļ│┤ņĪ┤ Ļ░üļ¦ēĻ│╝ņØś Ļ│ĄĒåĄ Ļ│╝ņĀĢņ£╝ļĪ£ņä£ ņÜ░ņäĀ BĒśĢ Ļ░äņŚ╝, CĒśĢ Ļ░äņŚ╝, ļ¦żļÅģ, ņŚÉņØ┤ņ”łņŚÉ ļīĆĒĢ£ ņé¼ņĀä ņäĀļ│äĻ▓Ćņé¼ļź╝ Ļ▒░ņ╣£ļŗż. ņØ┤Ēøä Ļ▓ÉĒāĆļ¦łņØ┤ņŗĀ(gentamicin)Ļ│╝ ņŖżĒŖĖļĀÖĒåĀļ¦łņØ┤ņŗĀ(streptomycin)ņØä ĒżĒĢ©ĒĢśļŖö Optisol GSņĢĪ(Bausch & Lomb, Rochester, NY, USA) Ēś╣ņØĆ Life4┬░C ņÜ®ņĢĪ(Numedis, Inc., Isanti, MN, USA)ņŚÉņä£ ņĪ░ņ¦ü ĒÜīļ│Ą Ļ│╝ņĀĢņØä Ļ▒░ņ╣£ Ēøä rice derived recombinant human serum albumin (rHSA) ņÜ®ņĢĪņØ┤ ļōĀ Ēżņן ļ╣äļŗÉ ņåŹņŚÉ ļ│┤Ļ┤ĆļÉśļ®░, 2-38┬░CņØś ņāüņś©ņŚÉņä£ ļ│┤Ļ┤ĆĒĢĀ ņłś ņ׳ļŗż. ļ│┤Ļ┤Ć ļ░Å Ēżņן Ļ│╝ņĀĢņŚÉņä£ ņØ╝ņ▓┤ņØś ļÅÖļ¼╝ Ēś╣ņØĆ ņØĖņ▓┤ ņ£Āļל ļ¼╝ņ¦łņØĆ ņØ┤ņÜ®ļÉśņ¦Ć ņĢŖļŖöļŗż. ņĄ£ņóģ ļ¼┤ņäĖĒż ļ░Å ļ®ĖĻĘĀĒÖö Ļ│╝ņĀĢņØä ņ£äĒĢ┤ ņĀäņ×ÉņäĀ ņĪ░ņé¼(electron beam irradiation, 15-21 KGy)ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ Ļ░üļ¦ēņØś ņāüĒö╝ņäĖĒż, Ļ░üļ¦ēņŗżņ¦łņäĖĒż, Ļ░üļ¦ēļé┤Ēö╝ņäĖĒż, ĒĢŁņøÉĒæ£ņ¦ĆņäĖĒż, ļ»ĖņāØļ¼╝ ļō▒ņØä ņĀ£Ļ▒░ĒĢ£ļŗż.
ņØ┤ļ¤¼ĒĢ£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØĆ ņŚ¼ļ¤¼ ņןņĀÉņØä Ļ░Ćņ¦ĆļŖöļŹ░, ņ▓½ņ¦Ė, ļ¼┤ņäĖĒż ņ▓śļ”¼ļÉśņ¢┤ ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ņŗØ Ēøä Ļ▒░ļČĆ ļ░śņØæņØś ņ£äĒŚśļÅäļź╝ ņāüļīĆņĀüņ£╝ļĪ£ ņżäņØ╝ ņłś ņ׳ļŗż. ļæśņ¦Ė, ņåīļ¤ēņØś rHSA ņÜ®ņĢĪ ņåŹņŚÉņä£ ņāüņś© ļ│┤Ļ┤ĆļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņłĀ ņ¦üņĀä ņČöĻ░ĆņĀüņØĖ ņĪ░ņ¦ü ņäĖņ▓Ö ļ░Å ĒĢ┤ļÅÖ Ļ│╝ņĀĢņØ┤ ĒĢäņÜö ņŚåņ¢┤ ņé¼ņÜ®ņØ┤ ĒÄĖļ”¼ĒĢśļŗżļŖö ņןņĀÉņØ┤ ņ׳ļŗż. ļéśņĢäĻ░Ć, ĒØöĒ׳ ņłśļ│ĄņĀü ņØ┤ņŗØņŚÉ ņé¼ņÜ®ļÉśļŖö Ļ│Ąļ¦ē ļīĆļ╣ä Ļ░üļ¦ēņØ┤ņŗØņØś ņןņĀÉņ£╝ļĪ£ņä£, Ļ│Ąļ¦ē ņĪ░ņ¦üņŚÉ ļ╣äĒĢ┤ ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņØś ļ░░ņŚ┤ņØ┤ ĻĘ£ņ╣ÖņĀüņØĖ Ļ░üļ¦ē Ļ│Āņ£ĀņØś ĒŖ╣ņä▒ņāü ļ┤ēĒĢ®ņØ┤ ļŹö ņēĮĻ│Ā, ļ┤ēĒĢ® Ēøä ņĪ░ņ¦üņØś ļŖśņ¢┤ņ¦É ļ░Å ņÜ®ĒĢ┤ņŚÉ Ļ░ĢĒĢśļ®░, Ļ░üļ¦ēņŚÉ ņĪ┤ņ×¼ĒĢśļŖö ĻĖ░ņĀĆļ¦ēņØ┤ ņŻ╝ņ£ä ņäĖĒżļōżļĪ£ ĒĢśņŚ¼ĻĖł ņ”ØņŗØĒĢśļŖö ļ░öļŗźņ£╝ļĪ£ ņ×æņÜ®ĒĢśĻ▓ī ĒĢśņŚ¼[13] ņØ┤ņŗØņ▓┤ņØś ļ│┤ļŗż ļ╣ĀļźĖ ņāØņ░®ņØä ļÅäļ¬©ĒĢĀ ņłś ņ׳ļŗż. ļśÉĒĢ£, Ļ░üļ¦ēņØĆ Ļ│Ąļ¦ēļ│┤ļŗż ļæÉĻ╗śĻ░Ć ĻĘĀņØ╝ĒĢśĻ│Ā ļæÉĒł╝ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ĒżļÅäņóģĻ│╝ Ļ░ÖņØ┤ ļÅīņČ£ņä▒ ļ│æļ│ĆņØä ņĢĢļ░ĢĒĢśļŖö ļŹ░ļ│┤ļŗż ņ£Āļ”¼ĒĢśļŗż.
ņĄ£ĻĘ╝ņŚÉļŖö ņé¼ļ×īņØś ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░ MĻ│╝ ļ®┤ņŚŁ ļ░śņØæņØä ņØ╝ņ£╝ĒéżļŖö ļÅ╝ņ¦ĆņØś Galactose-alpha-1,3-galactose (e.g. ╬▒Gal)ņØś Ļ┤ĆļĀ© ņ£ĀņĀäņ×Éļź╝ ļģ╣ņĢäņøā ņŗ£Ēé©(alpha-galactosyltransferase knockout) non-Gal ļÅ╝ņ¦Ć Ļ░üļ¦ēņØä ņøÉņłŁņØ┤ņŚÉ ņØ┤ņŗØĒĢ£ ĒÜ©Ļ│╝Ļ░Ć ņåīĻ░£ļÉśĻ│Ā[14], ĒĢ┤ņÖĖņŚÉņä£ļŖö ļ¼┤ņäĖĒżĒÖö ļÅ╝ņ¦Ć Ļ░üļ¦ēņØä ņé¼ļ×īņŚÉņä£ ņØ┤ņŗØĒĢ£ ļ░ö ņ׳ņ¢┤[15] Ēü░ Ļ┤Ćņŗ¼ņØä ļČłļ¤¼ņØ╝ņ£╝ĒéżĻ│Ā ņ׳ņ£╝ļéś, ĻĄŁļé┤ņŚÉņä£ļŖö ņĢäņ¦ü ņé¼ļ×īņŚÉĻ▓ī ņØ┤ņóģ Ļ░üļ¦ēņØ┤ņŗØņØ┤ ĒŚłņÜ®ļÉśņ¦Ć ņĢŖņĢä ņ×äņāüņĀü ņĀüņÜ®ņŚÉ ĒĢ£Ļ│äņĀÉņØ┤ ņ׳ļŗż.
ļ│Ė ņ”ØļĪĆņŚÉņä£ ļ│┤ņĪ┤ Ļ░üļ¦ēņØä ĒżļÅäņóģ ņ▓£Ļ│Ą ļČĆņ£äņŚÉ ļ░öļĪ£ ņØ┤ņŗØĒĢśņ¦Ć ņĢŖĻ│Ā ļ©╝ņĀĆ ņ¢æļ¦ēņØ┤ņŗØņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņØ┤ļŖö ĒżļÅäņóģņØś ņ▓£Ļ│Ą ļČĆņ£äĻ░Ć ļČłĻĘ£ņ╣ÖĒĢ£ Ēæ£ļ®┤ņØä ņ¦ĆļŗłĻ│Ā ņ׳ņ¢┤ ņ¢æļ¦ēņŚÉ ļ╣äĒĢ┤ ļæÉĒł╝ĒĢśĻ│Ā ņĀæĒלņØ┤ Ēø©ņö¼ ļŹ£ĒĢ£ Ļ░üļ¦ēņĪ░ņ¦üņØä ļ░öļĪ£ ņØ┤ņŗØĒĢśņśĆņØä ļĢī ņ▓£Ļ│Ą ļČĆņ£äņØś ļČłņÖäņĀäĒĢ£ ĒÅÉņćäļź╝ ņ┤łļלĒĢĀ ņłś ņ׳ļŖö ņÜ░ļĀżĻ░Ć ņ׳ņŚłĻ│Ā, ļśÉ ĒĢ£ĒÄĖņ£╝ļĪ£ļŖö ļ¦żņÜ░ ņ¢ćņĢäņĀĖ ņ׳ļŖö Ļ│Ąļ¦ēĒżļÅäņóģ ļČĆņ£äņØś ļģĖņČ£ļÉ£ ĒżļÅäļ¦ē Ēæ£ļ®┤ņØś ņāüĒö╝ņĖĄņØä ļ│┤Ļ░ĢĒĢśĻĖ░ ņ£äĒĢ£ ļ¬®ņĀüņØ┤ ņ׳ņŚłĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ņŗØĒĢĀ ļ│┤ņĪ┤Ļ░üļ¦ēĒÄĖ ņĢäļלņŚÉņä£ ņ¢æļ¦ēņØ┤ņŗØņØä ņÜ░ņäĀņĀüņ£╝ļĪ£ ņŗ£Ē¢ēĒĢśņśĆļŗż. ļ╣äļĪØ ļ│Ė ļŗ©ņØ╝ ņ”ØļĪĆļź╝ ĒåĄĒĢ┤ņä£ ņ▓£Ļ│Ą ņĢ×Ļ│Ąļ¦ēĒżļÅäļ¦ēņóģņŚÉņä£ ļ¼┤ņäĖĒż ļ│┤ņĪ┤ Ļ░üļ¦ēņØ┤ņŗØņłĀņØś ņןĻĖ░ņĀü ņĢłņĀäņä▒ņØä ĒÖĢļ”ĮĒĢĀ ņłśļŖö ņŚåņ¦Ćļ¦ī, ļ┤ēĒĢ®ņØ┤ ļ│┤ļŗż ņÜ®ņØ┤ĒĢśĻ│Ā ņØĖņן Ļ░ĢļÅäĻ░Ć ņÜ░ņłśĒĢśļ®░ ņ£ĄĒĢ┤ņŚÉ Ļ░ĢĒĢ£ Ļ░üļ¦ēņĪ░ņ¦üņØś ĒŖ╣ņä▒ņāü ņĢ×Ļ│Ąļ¦ēĒżļÅäņóģņŚÉņä£ ņĀüņÜ® ņŗ£ ļśÉ ļŗżļźĖ ņ╣śļŻīņĀü ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳Ļ▓Āļŗż.
Figure┬Ā1.
Slit-lamp photographs of 39-year-old man with the perforated anterior scleral staphyloma of his right eye before surgery. (A) The anterior protrusion at the scleral staphyloma is noted. (B) The temporal area at the staphyloma near the limbus is perforated (arrow).
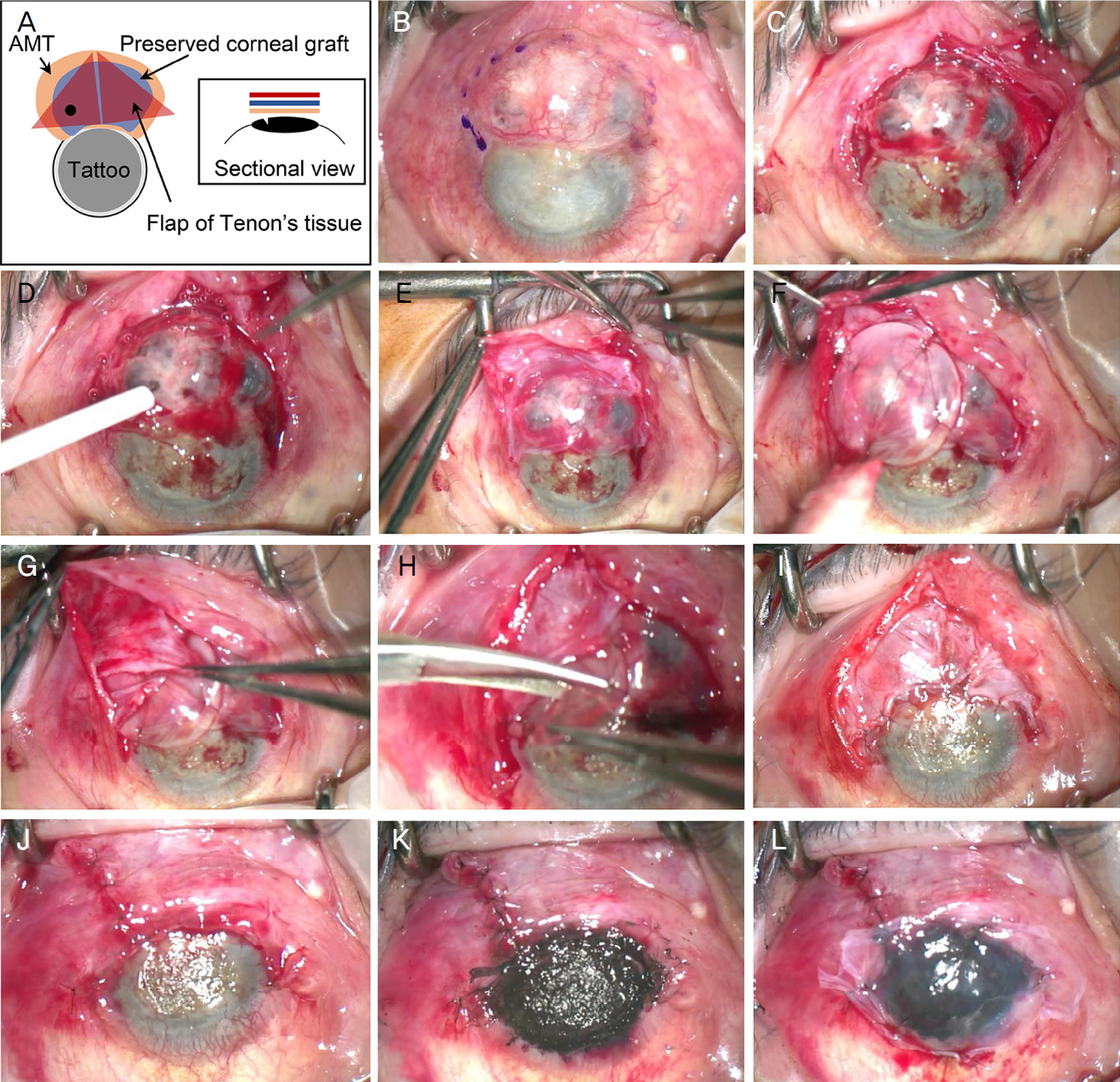
Figure┬Ā2.
Illustration of the surgical procedures and the intraoperative photos. (A) From bottom to up, amniotic membrane (AM), acellular preserved human cornea, and TenonŌĆÖs capsule flap were sutured over the perforated area. (B-L) After outlining the staphyloma (B), the overlying conjunctiva was dissected (C) and the perforation was temporarily sealed using fibrin glue (D). Then, the AM (E) and the acellular preserved human cornea (F) was transplanted. Thereafter, the adjacent TenonŌĆÖs tissue was dissected and advanced to be anchored over the corneal graft (G, I). The redundant corneal tissue was excised (H). The conjunctiva was closed (J), then the corneal was tattooed (K) and temporary AM patch was performed (L). AMT = amniotic membrane transplantation.
REFERENCES
1) Shields JA, Shields CL, Lavrich J. Congenital anterior scleral staphyloma in an otherwise normal eye. J Pediatr Ophthalmol Strabismus 2003;40:108-9.


2) Leff SR, Shields JA, Augsburger JJ, et al. Congenital corneal staphyloma: clinical, radiological, and pathological correlation. Br J Ophthalmol 1986;70:427-30.



3) Schanzlin DJ, Robin JB, Erickson G, et al. Histopathologic and ultrastructural analysis of congenital corneal staphyloma. Am J Ophthalmol 1983;95:506-14.


4) Yal├¦indag FN, Celik S, Ozdemir O. Repair of anterior staphyloma with dehydrated dura mater patch graft. Ophthalmic Surg Lasers Imaging 2008;39:346-7.


5) Gopal L, Badrinath SS. Autoscleral flap grafting: a technique of scleral repair. Ophthalmic Surg 1995;26:44-8.


6) Costa EF, Pinto LM, Campos MAG, et al. Partial regression of large anterior scleral staphyloma secondary to rhinosporidiosis after corneoscleral graft - a case report. BMC Ophthalmol 2018;18:61.



7) Nakazawa M, Tamai M, Kiyosawa M, Watanabe Y. Homograft of preserved sclera for post-traumatic scleral staphyloma in Ehlers-Danlos syndrome. Graefes Arch Clin Exp Ophthalmol 1986;224:247-50.


8) Kwon HJ, Nam SM, Lee SY, et al. Conjunctival flap surgery for calcified scleromalacia after cosmetic conjunctivectomy. Cornea 2013;32:821-5.


9) Ma DH, Wang SF, Su WY, et al. Amniotic membrane graft for the management of scleral melting and corneal perforation in recalcitrant infectious scleral and corneoscleral ulcers. Cornea 2002;21:275-83.


10) Oh JH, Kim JC. Repair of scleromalacia using preserved scleral graft with amniotic membrane transplantation. Cornea 2003;22:288-93.


11) Singh M, Chew PT, Tan D. Corneal patch graft repair of exposed glaucoma drainage implants. Cornea 2008;27:1171-3.


12) Torchia RT, Dunn RE, Pease PJ. Fascia lata grafting in scleromalacia perforans with lamellar corneal-scleral dissection. Am J Ophthalmol 1968;66:705-9.


13) Torricelli AA, Singh V, Santhiago MR, Wilson SE. The corneal epithelial basement membrane: structure, function, and disease. Invest Ophthalmol Vis Sci 2013;54:6390-400.



-
METRICS

-
- 0 Crossref
- 1 Scopus
- 2,471 View
- 73 Download
- Related articles




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



